必修I-氯气的生产原理
图片预览







文档简介
课件30张PPT。专题二
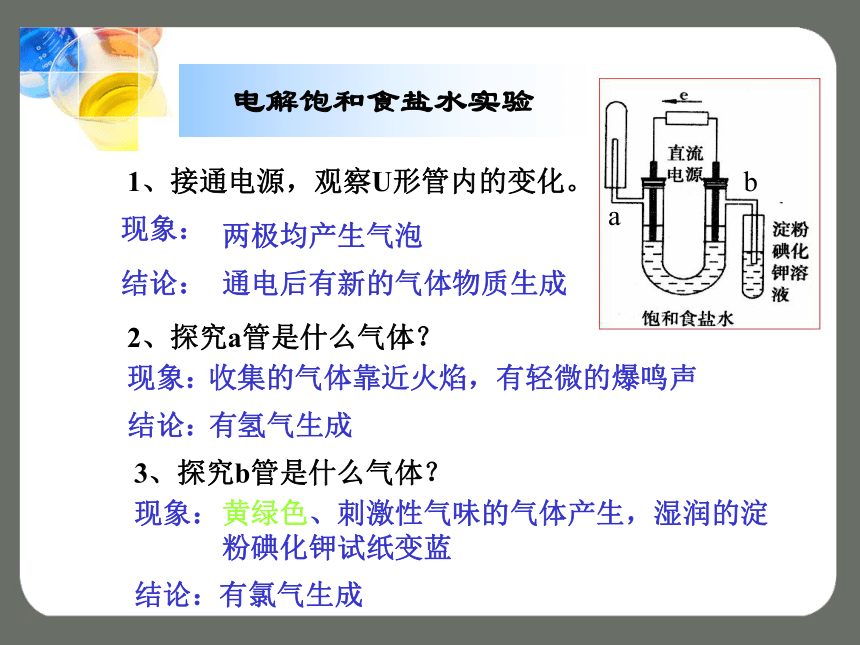
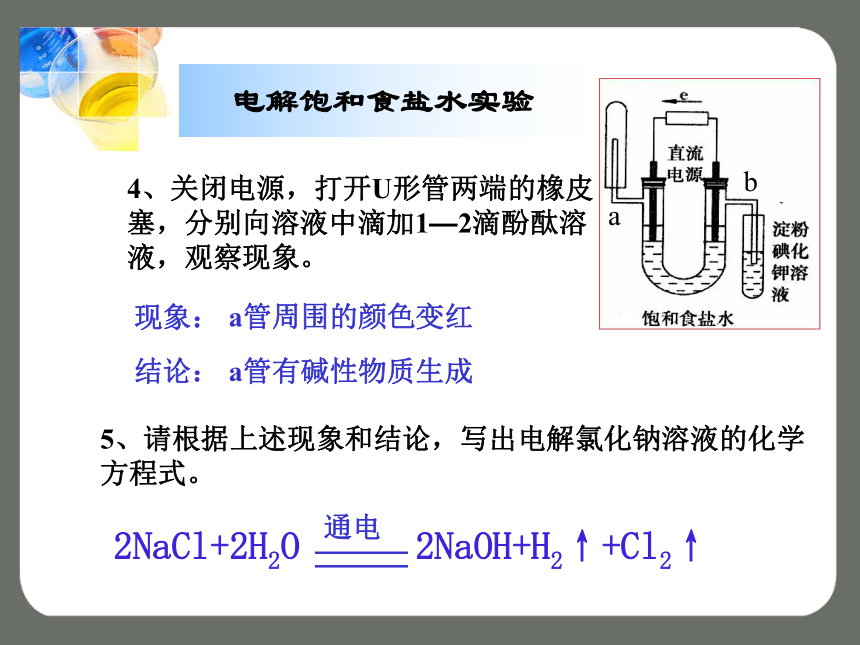
从海水中获得的化学物质海水晒盐 氯、溴、碘及其化合物第一单元氯气的生产原理一、工业制氯气二、实验室制氯气氯气的工业制法观察与思考电解饱和食盐水1、接通电源,观察U形管内的变化。 两极均产生气泡通电后有新的气体物质生成现象:结论:ab2、探究a管是什么气体?现象:结论:收集的气体靠近火焰,有轻微的爆鸣声有氢气生成3、探究b管是什么气体?现象:结论:黄绿色、刺激性气味的气体产生,湿润的淀粉碘化钾试纸变蓝有氯气生成电解饱和食盐水实验ab4、关闭电源,打开U形管两端的橡皮塞,分别向溶液中滴加1—2滴酚酞溶液,观察现象。 现象:结论:a管周围的颜色变红a管有碱性物质生成5、请根据上述现象和结论,写出电解氯化钠溶液的化学方程式。2NaCl+2H2O 2NaOH+H2↑+Cl2↑通电电解饱和食盐水实验两极均产生气泡有气体物质生成有轻微的爆鸣声有氢气生成湿润的淀粉碘化钾
试纸变蓝有氯气生成溶液变红有碱性物质生成小结 电解饱和食盐水制氯气的原理就是:通过氯化钠和水发生电解反应,在与电源正极相连的电极(阳极)上产生氯气,同时在与电源负极相连的电极(阴极)上产生氢气和氢氧化钠。
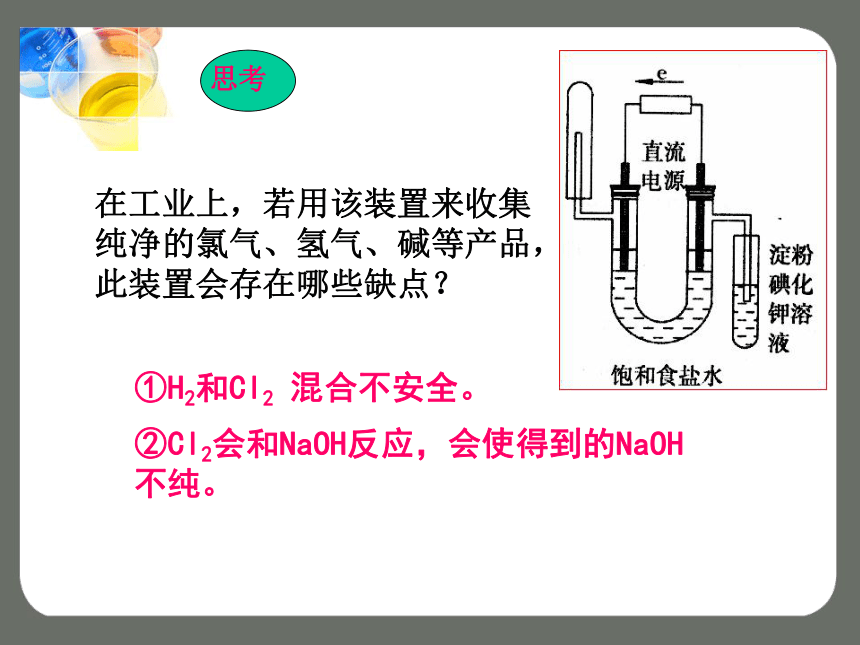
2NaCl+2H2O 2NaOH+H2↑+Cl2↑通电电源负极电源正极思考在工业上,若用该装置来收集纯净的氯气、氢气、碱等产品,此装置会存在哪些缺点?①H2和Cl2 混合不安全。
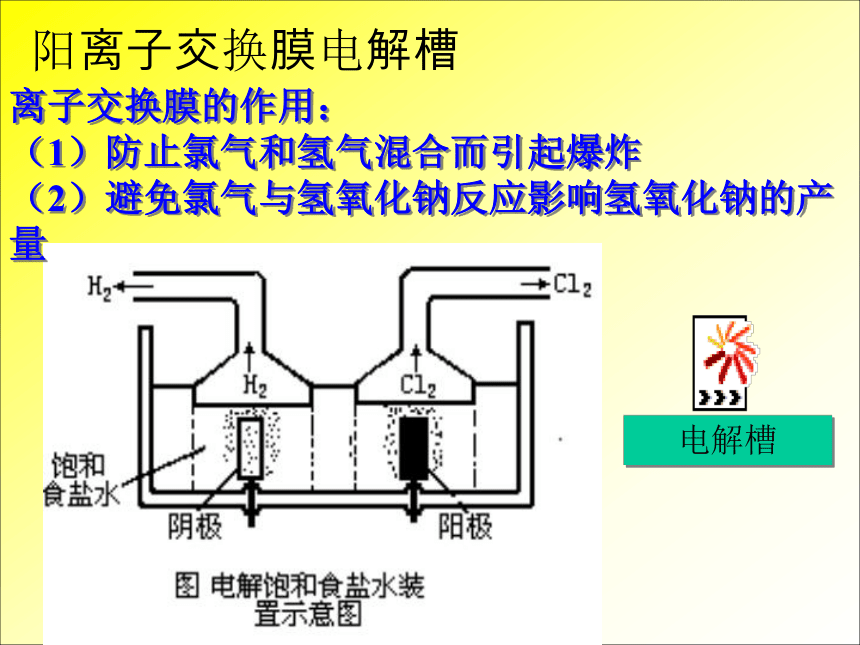
②Cl2会和NaOH反应,会使得到的NaOH不纯。阳离子交换膜电解槽电解槽离子交换膜的作用: (1)防止氯气和氢气混合而引起爆炸 (2)避免氯气与氢氧化钠反应影响氢氧化钠的产量 根据氯碱厂原料和产品的性质,你认为在生产过程中和贮运时应注意哪些问题?氯碱厂的厂址应如何选择? 调查研究 厂址的选择:现代化工生产要求有较大的生产规模;厂址选择涉及原料、水源、能源、土地供应、市场需求、交通运输、环境保护等因素,应对这些因素综合考虑,作出合理的抉择。由于氯气有毒,不便贮存和运输,因此要求厂址应避开人口稠密的居民区和环境保护要求高的地区,厂区必须与居民区有一定距离的安全隔离带。 工业上利用电解饱和食盐水的方法制取 、 和 。在电源正极上方收集到的气体能使湿润的 变蓝色,证明是 ;在电源负极上方收集到的气体是 ,在电极附近的水溶液中滴几滴酚酞溶液,则溶液 ,证明有 生成。若电解一段时间后,电源正极上方收集到的气体在标准状况下为4.48L,则在电源负极上方将收集到 g 气体,在溶液中产生 g 。停止通电后,待溶液混合均匀,溶液的pH会 。 练一练NaOHH2淀粉碘化钾试纸Cl2Cl2H2变红NaOH0.4H216NaOH升高化学式:Cl2观察与思考舍勒 (1742~1786)瑞典化学家。
1774年舍勒 发现氯气
他将这种元素命名为Chlorine,这个名称
来自希腊文,有“绿色”的意思。我国早
年译文将其译成“绿气”,后改为氯气。氯 气问题讨论用什么装置制氯气仪器及装置:酒精灯圆底烧瓶石棉网分液漏斗问题讨论制得的氯气可能含有什么杂质?HClH2O水?饱和食盐水浓硫酸除杂的顺序怎样?装置图!?仪器及装置:用什么方法收集氯气?a.向上排空气,b.排饱和食盐水法装置图仪器及装置:用什么吸收?饱和食盐水浓盐酸仪器及装置:饱和食盐水浓盐酸NaOH选择气体发生装置的原则是反应物的状态和反应条件项目装配发生装置的主要仪器收集气体方法发生装置类型Cl2O2H2向上排气法(或排饱和食盐水法)排水法(或向上排空气法固液加热固液不加热固固加热排水法(或向下排空气法2、氯气的实验室制法(1)实验原理:MnO2 + 4HCl(浓) = MnCl2 + Cl2 ↑ + 2H2O
(2)发生装置:
粉末状固体或液体+液体 气体(3)除杂装置:饱和食盐水(4)干燥装置:浓硫酸(5)收集装置:向上排空气法或排饱和食 盐水法(6)尾气处理:用氢氧化钠溶液吸收1、实验室制氯气时,二氧化锰的作用是 ( )
BDA.催化剂 B.氧化剂
C.还原剂 D.反应物练一练2、实验室制氯气时有如下操作,操作顺序正确的是 ( )
①连接好装置,检查气密性
②缓缓加热,加快反应,使气体均匀逸出 ③在烧瓶中加入二氧化锰粉末
④往分液漏斗中加入浓盐酸,再缓缓滴入烧瓶中 ⑤用向上排空气法收集氯气,尾气导入氢氧化钠溶液中
A.①②③④⑤ B.④③①②⑤
C.①③④②⑤ D.①④③②⑤C练一练再见!
试纸变蓝有氯气生成溶液变红有碱性物质生成小结 电解饱和食盐水制氯气的原理就是:通过氯化钠和水发生电解反应,在与电源正极相连的电极(阳极)上产生氯气,同时在与电源负极相连的电极(阴极)上产生氢气和氢氧化钠。
2NaCl+2H2O 2NaOH+H2↑+Cl2↑通电电源负极电源正极思考在工业上,若用该装置来收集纯净的氯气、氢气、碱等产品,此装置会存在哪些缺点?①H2和Cl2 混合不安全。
②Cl2会和NaOH反应,会使得到的NaOH不纯。阳离子交换膜电解槽电解槽离子交换膜的作用: (1)防止氯气和氢气混合而引起爆炸 (2)避免氯气与氢氧化钠反应影响氢氧化钠的产量 根据氯碱厂原料和产品的性质,你认为在生产过程中和贮运时应注意哪些问题?氯碱厂的厂址应如何选择? 调查研究 厂址的选择:现代化工生产要求有较大的生产规模;厂址选择涉及原料、水源、能源、土地供应、市场需求、交通运输、环境保护等因素,应对这些因素综合考虑,作出合理的抉择。由于氯气有毒,不便贮存和运输,因此要求厂址应避开人口稠密的居民区和环境保护要求高的地区,厂区必须与居民区有一定距离的安全隔离带。 工业上利用电解饱和食盐水的方法制取 、 和 。在电源正极上方收集到的气体能使湿润的 变蓝色,证明是 ;在电源负极上方收集到的气体是 ,在电极附近的水溶液中滴几滴酚酞溶液,则溶液 ,证明有 生成。若电解一段时间后,电源正极上方收集到的气体在标准状况下为4.48L,则在电源负极上方将收集到 g 气体,在溶液中产生 g 。停止通电后,待溶液混合均匀,溶液的pH会 。 练一练NaOHH2淀粉碘化钾试纸Cl2Cl2H2变红NaOH0.4H216NaOH升高化学式:Cl2观察与思考舍勒 (1742~1786)瑞典化学家。
1774年舍勒 发现氯气
他将这种元素命名为Chlorine,这个名称
来自希腊文,有“绿色”的意思。我国早
年译文将其译成“绿气”,后改为氯气。氯 气问题讨论用什么装置制氯气仪器及装置:酒精灯圆底烧瓶石棉网分液漏斗问题讨论制得的氯气可能含有什么杂质?HClH2O水?饱和食盐水浓硫酸除杂的顺序怎样?装置图!?仪器及装置:用什么方法收集氯气?a.向上排空气,b.排饱和食盐水法装置图仪器及装置:用什么吸收?饱和食盐水浓盐酸仪器及装置:饱和食盐水浓盐酸NaOH选择气体发生装置的原则是反应物的状态和反应条件项目装配发生装置的主要仪器收集气体方法发生装置类型Cl2O2H2向上排气法(或排饱和食盐水法)排水法(或向上排空气法固液加热固液不加热固固加热排水法(或向下排空气法2、氯气的实验室制法(1)实验原理:MnO2 + 4HCl(浓) = MnCl2 + Cl2 ↑ + 2H2O
(2)发生装置:
粉末状固体或液体+液体 气体(3)除杂装置:饱和食盐水(4)干燥装置:浓硫酸(5)收集装置:向上排空气法或排饱和食 盐水法(6)尾气处理:用氢氧化钠溶液吸收1、实验室制氯气时,二氧化锰的作用是 ( )
BDA.催化剂 B.氧化剂
C.还原剂 D.反应物练一练2、实验室制氯气时有如下操作,操作顺序正确的是 ( )
①连接好装置,检查气密性
②缓缓加热,加快反应,使气体均匀逸出 ③在烧瓶中加入二氧化锰粉末
④往分液漏斗中加入浓盐酸,再缓缓滴入烧瓶中 ⑤用向上排空气法收集氯气,尾气导入氢氧化钠溶液中
A.①②③④⑤ B.④③①②⑤
C.①③④②⑤ D.①④③②⑤C练一练再见!
