物质的聚集状态教学课件(福建省莆田市仙游县)
文档属性
| 名称 | 物质的聚集状态教学课件(福建省莆田市仙游县) |

|
|
| 格式 | rar | ||
| 文件大小 | 99.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2007-09-10 00:00:00 | ||
图片预览





文档简介
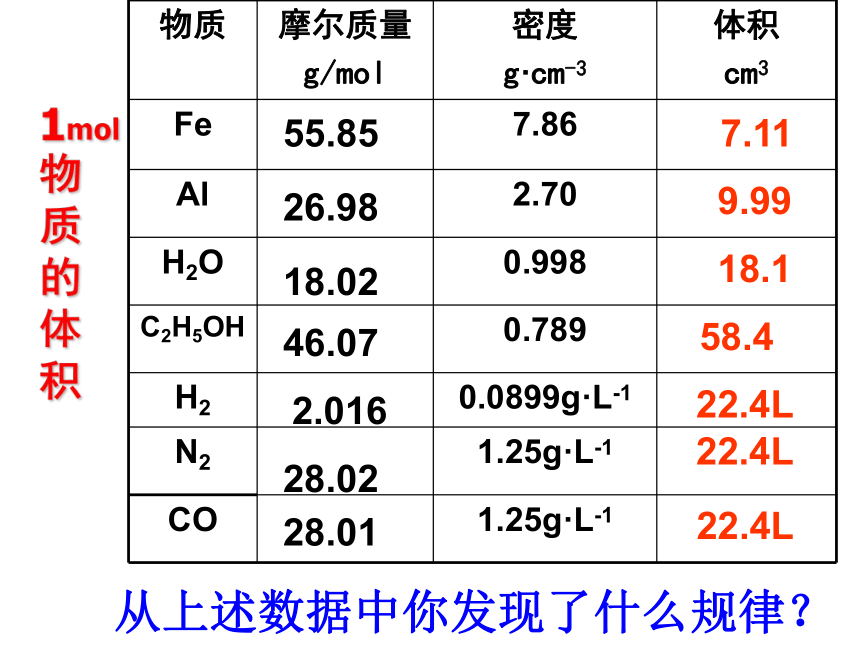
课件17张PPT。物质的聚集状态从上述数据中你发现了什么规律?1mol物质的体积讨论:
从微观上看,决定物质体积大小的因素有哪些?因素有:
⑴物质中所含的粒子数
⑵粒子间的距离
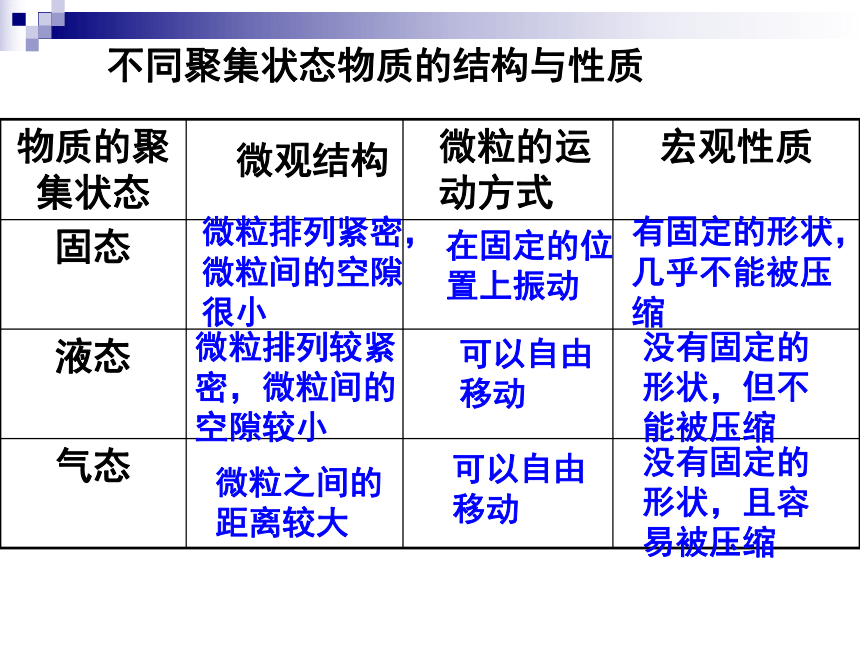
⑶粒子本身的体积大小不同聚集状态物质的结构与性质微观结构微粒的运动方式有固定的形状,几乎不能被压缩没有固定的形状,但不能被压缩没有固定的形状,且容易被压缩微粒排列紧密,微粒间的空隙很小微粒排列较紧密,微粒间的空隙较小微粒之间的距离较大在固定的位置上振动可以自由移动可以自由移动当粒子的数目相等时,你认为决定固态、液态、气态体积大小的主要因素是什么?固态、液态:体积主要由粒子大小决定气体:体积主要由粒子间距决定讨论:
气体分子间的距离与哪些因素有关?①乘坐热气球旅行已成为一种时尚运动,热气球升降的原理是什么?热气球的升与降与球体内气温有关,球体内气温高,气球浮力增大,气球就上升,球体内空气温度下降,球体产生的浮力小于球体自身重量和载重,气球就开始下降。飞行员在气球吊篮内,操纵着燃烧器的燃气开关,随时调整热气球囊体内气温,也就可以操纵热气球上升、平飞、或下降。 ②打开液化气钢瓶的阀门,就会有气体喷出来,喷出气体的体积是不是还和液化气钢瓶的体积相同? 在通常状况下,相同质量的气态物质要比它在固态或液态时的体积增大1000倍左右结 论: 一定质量的气体,当温度升高时,气体分子之间的距离 ,当温度降低时,气体分子之间的距离 ;当压强增大时,气体分子之间的距离 ,当压强减小时,气体分子之间的距离 。当气体的温度和压强相等时,气体分子之间的距离 。
因此,要比较一定质量气体的体积,就必须要在相同的温度和压强下进行才有意义。增大减小减小增大近似相等 在温度、压强一定时,1mol任何气体的体积基本相同。气体摩尔体积 思考:1mol气体在任何状况下所占的体积是不
是相等?是不是都约为22 .4L?1.定义:单位物质的量的气体所占的体积。
2.符号:Vm
3.单位:L/mol 或 m3/mol等
4.对象:任何气体(纯净或混合气体)
标准状况( 温度0 oC、压强 1.01×105 Pa)下 1mol气体体积:Vm约为22.4L练习一:下列说法正确吗?1、1mol任何气体的体积都是22.4L2、1mol任何物质在标准状况时所占的体积都约为22.4L3. 标准状况下,1molO2和N2混合气体的体积约为22.4L4、当温度高于0℃时,一定量任何气体的体积都大于22.4L1、在标准状况下(3)16gO2的体积是多少?
(4)44.8LN2中含有的N2分子数是多少?2、在某一温度和压强下
某气体的物质的量为1.5mol,其体积为30L,在该温度和压强下,气体的摩尔体积为多少?20L/mol练习二:(1)0.5molHCl占有的体积是多少?
(2)33.6LH2的物质的量是多少?11.2L1.5mol11.2L1.204×1024物质
质量物质
的量微粒
数÷M×M×NA÷NA×22.4L/mol÷22.4L/mol[小结](标准状况)体积气体在温度、压强一定时,任何具有相同微粒数的气体的体积 。在温度、压强一定时,相同体积的任何气体所含有的分子数 。大致相等大致相等阿伏加德罗定律 V1/V2=N1/N2=n1/n2阿伏加德罗定律推论:1、同温同压下,同体积的气体质量比等于
。 2、同温同压下,同质量气体的体积比等于
。 摩尔质量比摩尔质量的反比3、同温同压下,气体的摩尔质量比等于 。 4、恒温恒容下,气体的压强比等于
。 它们的物质的量之比密度比例题1、在一定温度和压强下,1体积X2(气)跟3
体积Y2(气)化合生成2体积气态化合物A,则化合物A的化学式是( )
A、XY3 B、XY C、X3Y D、X2Y3A例题2、在同温同压下,A容器中盛H2,B容器中
盛NH3,若原子数相等,则A、B的体积之比为( )
A 2:1 B 1:2 C 2:3 D 1:3A例:含16.0克氧化铁的铁矿石和足量的CO
反应,理论上最多可制得铁的物质的量为
多少?会产生多少体积(标准状况下)的
CO2气体?
从微观上看,决定物质体积大小的因素有哪些?因素有:
⑴物质中所含的粒子数
⑵粒子间的距离
⑶粒子本身的体积大小不同聚集状态物质的结构与性质微观结构微粒的运动方式有固定的形状,几乎不能被压缩没有固定的形状,但不能被压缩没有固定的形状,且容易被压缩微粒排列紧密,微粒间的空隙很小微粒排列较紧密,微粒间的空隙较小微粒之间的距离较大在固定的位置上振动可以自由移动可以自由移动当粒子的数目相等时,你认为决定固态、液态、气态体积大小的主要因素是什么?固态、液态:体积主要由粒子大小决定气体:体积主要由粒子间距决定讨论:
气体分子间的距离与哪些因素有关?①乘坐热气球旅行已成为一种时尚运动,热气球升降的原理是什么?热气球的升与降与球体内气温有关,球体内气温高,气球浮力增大,气球就上升,球体内空气温度下降,球体产生的浮力小于球体自身重量和载重,气球就开始下降。飞行员在气球吊篮内,操纵着燃烧器的燃气开关,随时调整热气球囊体内气温,也就可以操纵热气球上升、平飞、或下降。 ②打开液化气钢瓶的阀门,就会有气体喷出来,喷出气体的体积是不是还和液化气钢瓶的体积相同? 在通常状况下,相同质量的气态物质要比它在固态或液态时的体积增大1000倍左右结 论: 一定质量的气体,当温度升高时,气体分子之间的距离 ,当温度降低时,气体分子之间的距离 ;当压强增大时,气体分子之间的距离 ,当压强减小时,气体分子之间的距离 。当气体的温度和压强相等时,气体分子之间的距离 。
因此,要比较一定质量气体的体积,就必须要在相同的温度和压强下进行才有意义。增大减小减小增大近似相等 在温度、压强一定时,1mol任何气体的体积基本相同。气体摩尔体积 思考:1mol气体在任何状况下所占的体积是不
是相等?是不是都约为22 .4L?1.定义:单位物质的量的气体所占的体积。
2.符号:Vm
3.单位:L/mol 或 m3/mol等
4.对象:任何气体(纯净或混合气体)
标准状况( 温度0 oC、压强 1.01×105 Pa)下 1mol气体体积:Vm约为22.4L练习一:下列说法正确吗?1、1mol任何气体的体积都是22.4L2、1mol任何物质在标准状况时所占的体积都约为22.4L3. 标准状况下,1molO2和N2混合气体的体积约为22.4L4、当温度高于0℃时,一定量任何气体的体积都大于22.4L1、在标准状况下(3)16gO2的体积是多少?
(4)44.8LN2中含有的N2分子数是多少?2、在某一温度和压强下
某气体的物质的量为1.5mol,其体积为30L,在该温度和压强下,气体的摩尔体积为多少?20L/mol练习二:(1)0.5molHCl占有的体积是多少?
(2)33.6LH2的物质的量是多少?11.2L1.5mol11.2L1.204×1024物质
质量物质
的量微粒
数÷M×M×NA÷NA×22.4L/mol÷22.4L/mol[小结](标准状况)体积气体在温度、压强一定时,任何具有相同微粒数的气体的体积 。在温度、压强一定时,相同体积的任何气体所含有的分子数 。大致相等大致相等阿伏加德罗定律 V1/V2=N1/N2=n1/n2阿伏加德罗定律推论:1、同温同压下,同体积的气体质量比等于
。 2、同温同压下,同质量气体的体积比等于
。 摩尔质量比摩尔质量的反比3、同温同压下,气体的摩尔质量比等于 。 4、恒温恒容下,气体的压强比等于
。 它们的物质的量之比密度比例题1、在一定温度和压强下,1体积X2(气)跟3
体积Y2(气)化合生成2体积气态化合物A,则化合物A的化学式是( )
A、XY3 B、XY C、X3Y D、X2Y3A例题2、在同温同压下,A容器中盛H2,B容器中
盛NH3,若原子数相等,则A、B的体积之比为( )
A 2:1 B 1:2 C 2:3 D 1:3A例:含16.0克氧化铁的铁矿石和足量的CO
反应,理论上最多可制得铁的物质的量为
多少?会产生多少体积(标准状况下)的
CO2气体?
