氧气的实验室制法[上学期]
文档属性
| 名称 | 氧气的实验室制法[上学期] |

|
|
| 格式 | rar | ||
| 文件大小 | 516.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2005-12-01 00:00:00 | ||
图片预览







文档简介
课件27张PPT。复习检测:
1. 按体积计算空气中含量最多的气体是( )
氧气 B. 二氧化碳 C. 氮气 D. 稀有气体
2. 最早通过实验测定出空气是由氮气和氧气组成的科学家是( )
瑞典的舍勒 B. 英国的汤姆生
C. 法国的拉瓦锡 D. 英国的道尔顿
3. 人类生存需要清洁的空气,下列情况不会造成环境污染的是( )
A. 燃放烟花 B. 汽车尾气 C. 煤炭燃烧 D. 光合作用
4. 空气中氧气和氮气的比约是1:4,这是指它们的( )
A. 密度比 B. 质量比 C. 质量分数比 D. 体积比
情境创设: 猜一猜:
无影无形摸不着,火焰见它跳的高。
呼吸作用它参加,动物生长离不了。
(打一化学物质) 氧气的实验室制法城关中学理化生组今
天
探
究探究目标: 1、探究最适合实验室制取氧气的方法。
2、明确实验室制取氧气的发生装置和收集装置。
提出问题: 1、如何选择最适合实验室制取氧气的方法?依据是什么?
2、如何收集一瓶氧气?
3、如何检验一瓶氧气已收集满? 收集资料:1、回顾一下,写出你所知道的制氧气的一种方法。 2、自然界中氧气的主要来源 。
探 究 内 容实
验
药
品
仪
器
装
置
实
验
原
理
实
验
步
骤
收
集
方
法
注
意
事
项
反
馈
练
习
实验药品第一组:氯酸钾(白色固体)和二氧化锰(黑色固体)第二组:高锰酸钾(紫黑色固体)第三组:双氧水(无色液体)和二氧化锰(固体)拓展:各物质化学式:氯酸钾: 高锰酸钾:
二氧化锰: 双氧水:KClO3 KMnO4
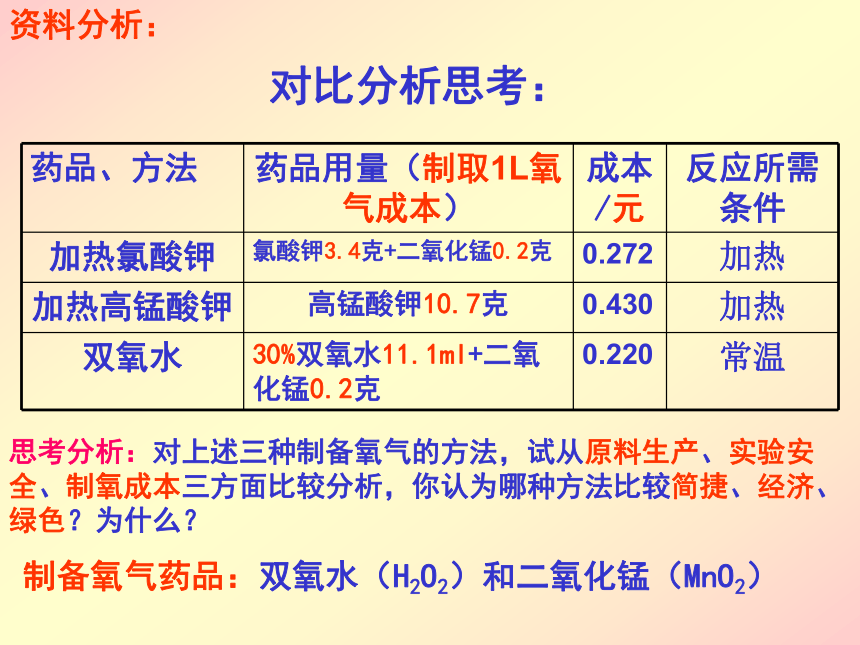
MnO2 H2O2 对比分析思考:资料分析:思考分析:对上述三种制备氧气的方法,试从原料生产、实验安全、制氧成本三方面比较分析,你认为哪种方法比较简捷、经济、绿色?为什么?制备氧气药品:双氧水(H2O2)和二氧化锰(MnO2)实验探究:实验原理用双氧水( H2O2 )和二氧化锰(MnO2):分解反应催化剂在化学反应中能改变其它物质的化学反应速率,而本身的质量和化学性质在化学反应前后没有变化的物质叫催化剂,它所起的作用叫催化作用。改变的两种含义:加快和减慢实验仪器装置B 、固体反应物(固固加热型)A 、固液反应物(固液不加热型)
气体发生装置的设计原则:根据反应物的状态和反应条件
长颈漏斗的下端浸入液面以下导气管刚进入橡皮塞即可反应不需要加热实验室制取氧气的装置特点:防止生成的气体从长颈漏斗中逸出便于气体的排出实验步骤连接仪器,检查装气密性(方法?)装:用药匙把固体二氧化锰药品装入大试管定:固定仪器查:收:收集气体。根据气体的物理性质,(水溶性,密度)注:从长颈漏斗中注入双氧水气体的收集方法想一想:氧气应如何收集?气体收集方法排水法:
气体不
易溶于
水排空气法向下排空气法:气体密度比空气小向上排空气法:气体密度比空气大排水法向上排空气法反馈练习:
1. 下列气体能使带火星的木条复燃的气体是( )
A. 氧气 B. 空气 C. 二氧化碳 D. 氮气
2. 常温下,当碘与镁化合时,速度很慢,若滴入几滴水,则剧烈反应生成碘化镁,还形成一股美丽的紫色烟雾,在此反应中水的作用是( )
A. 反应物 B. 氧化剂 C. 催化剂 D. 还原剂
3. 在实验室里,用分解过氧化氢溶液的方法制取氧气,加入二氧化锰的目的是( )
A. 使产生氧气的量增多 B. 提高氧气的纯度
C. 使其在常温下迅速分解放出氧气 D. 使生成的氧气更干燥4. 关于催化剂的说法正确的是( )
A. 催化剂只能加快化学反应速率
B. 催化剂在化学反应前后其质量和化学性质不变
C. 催化剂可增加生成物的量
D. MnO2可作任一反应的催化剂
5. 实验室用过氧化氢和二氧化锰来制取和收集氧气用到的一组仪器是( )
A. 集气瓶、导管、胶头滴管、药匙
B. 漏斗、量筒、铁架台、集气瓶
C. 铁架台、试管、导管、集气瓶
D. 试管、酒精灯、铁架台、集气瓶
6. 某气体既能用排水法收集,又能用向上排空气法收集,该气体具有的性质是( )
A. 易溶于水,比空气轻 B. 难溶于水,比空气轻
C. 易溶于水,比空气重 D. 难溶于水,比空气重
用过氧化氢溶液和二氧化锰制取氧气的装置。其中分液漏斗可以通过调节活塞控制液体的滴加速度。
根据上图回答下列问题:
(1)分液漏斗中放入的物质是 ,锥 形瓶中应放入的物质是 。
(2)写出该方法制取氧气的文字表达式 ,要收集一瓶纯净的氧气应选择的装置 。(填字母)
(3)已知: ,则用此法代替氯酸钾加热制取氧气优点是 (填编号)
(1)生成物只有氧气 (2)不需加热 (3)生成物是氧气和水,利于环保。
(4)装置A 中反应很剧烈,据此提出实验安全注意事项是 。
(1)控制液体的滴加速度 (2)用体积小的锥形瓶(3)加热反应物1. 通常情况下,氨气(NH3)是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,形成的溶液是氨水。实验室用加热氯化氨和消石灰的固体混合物制取氨气。下图是实验室常用的装置。请回答:(1)实验室制取氨气的发生装置,可选用 (填装置编号);
(2)收集氨气,应采用的装置为 (填装置编号);收集氨气的集气瓶必须十分干燥,这是因为 。 AE能力拓展训练:创意空间活动与探究 实验室里常用某些受热时易分解放出氧气的含氧物质来制取氧气,如常用二氧化锰作催化剂,加热氯酸钾制取氧气,发生如下表达式的反应:
研究表明,许多金属氧化物对氯酸钾的分解有催化作用。分别用下列金属氧化物作催化剂,氯酸钾开始发生分解反应和反应剧烈时的温度如下表所示:
(1)实验室用氯酸钾制取氧气,如果不用二氧化锰作催化剂,最好选用____(填序号)
A. 氧化铁 B. 氧化铝 C. 氧化铜 D. 氧化镁
(2)实验室用氯酸钾制取氧气时,_________(填“能”或“不能”)用实验室中用双氧水制取氧气的实验装置。
(3)实验室用氯酸钾制取氧气时若用二氧化锰作催化剂,反应前后二氧化锰的质量__________(填序号)
不变 B. 变大
C. 变小 D. 可能变大也可能变小
(4)实验室加热氯酸钾制氧气时,忘记加入二氧化锰,其结果是( )
A. 不能产生氧气 B. 生成氧气的速度慢
C. 产生氧气的总量减少 D. 没有氯化钾生成
祝同学们学习进步
1. 按体积计算空气中含量最多的气体是( )
氧气 B. 二氧化碳 C. 氮气 D. 稀有气体
2. 最早通过实验测定出空气是由氮气和氧气组成的科学家是( )
瑞典的舍勒 B. 英国的汤姆生
C. 法国的拉瓦锡 D. 英国的道尔顿
3. 人类生存需要清洁的空气,下列情况不会造成环境污染的是( )
A. 燃放烟花 B. 汽车尾气 C. 煤炭燃烧 D. 光合作用
4. 空气中氧气和氮气的比约是1:4,这是指它们的( )
A. 密度比 B. 质量比 C. 质量分数比 D. 体积比
情境创设: 猜一猜:
无影无形摸不着,火焰见它跳的高。
呼吸作用它参加,动物生长离不了。
(打一化学物质) 氧气的实验室制法城关中学理化生组今
天
探
究探究目标: 1、探究最适合实验室制取氧气的方法。
2、明确实验室制取氧气的发生装置和收集装置。
提出问题: 1、如何选择最适合实验室制取氧气的方法?依据是什么?
2、如何收集一瓶氧气?
3、如何检验一瓶氧气已收集满? 收集资料:1、回顾一下,写出你所知道的制氧气的一种方法。 2、自然界中氧气的主要来源 。
探 究 内 容实
验
药
品
仪
器
装
置
实
验
原
理
实
验
步
骤
收
集
方
法
注
意
事
项
反
馈
练
习
实验药品第一组:氯酸钾(白色固体)和二氧化锰(黑色固体)第二组:高锰酸钾(紫黑色固体)第三组:双氧水(无色液体)和二氧化锰(固体)拓展:各物质化学式:氯酸钾: 高锰酸钾:
二氧化锰: 双氧水:KClO3 KMnO4
MnO2 H2O2 对比分析思考:资料分析:思考分析:对上述三种制备氧气的方法,试从原料生产、实验安全、制氧成本三方面比较分析,你认为哪种方法比较简捷、经济、绿色?为什么?制备氧气药品:双氧水(H2O2)和二氧化锰(MnO2)实验探究:实验原理用双氧水( H2O2 )和二氧化锰(MnO2):分解反应催化剂在化学反应中能改变其它物质的化学反应速率,而本身的质量和化学性质在化学反应前后没有变化的物质叫催化剂,它所起的作用叫催化作用。改变的两种含义:加快和减慢实验仪器装置B 、固体反应物(固固加热型)A 、固液反应物(固液不加热型)
气体发生装置的设计原则:根据反应物的状态和反应条件
长颈漏斗的下端浸入液面以下导气管刚进入橡皮塞即可反应不需要加热实验室制取氧气的装置特点:防止生成的气体从长颈漏斗中逸出便于气体的排出实验步骤连接仪器,检查装气密性(方法?)装:用药匙把固体二氧化锰药品装入大试管定:固定仪器查:收:收集气体。根据气体的物理性质,(水溶性,密度)注:从长颈漏斗中注入双氧水气体的收集方法想一想:氧气应如何收集?气体收集方法排水法:
气体不
易溶于
水排空气法向下排空气法:气体密度比空气小向上排空气法:气体密度比空气大排水法向上排空气法反馈练习:
1. 下列气体能使带火星的木条复燃的气体是( )
A. 氧气 B. 空气 C. 二氧化碳 D. 氮气
2. 常温下,当碘与镁化合时,速度很慢,若滴入几滴水,则剧烈反应生成碘化镁,还形成一股美丽的紫色烟雾,在此反应中水的作用是( )
A. 反应物 B. 氧化剂 C. 催化剂 D. 还原剂
3. 在实验室里,用分解过氧化氢溶液的方法制取氧气,加入二氧化锰的目的是( )
A. 使产生氧气的量增多 B. 提高氧气的纯度
C. 使其在常温下迅速分解放出氧气 D. 使生成的氧气更干燥4. 关于催化剂的说法正确的是( )
A. 催化剂只能加快化学反应速率
B. 催化剂在化学反应前后其质量和化学性质不变
C. 催化剂可增加生成物的量
D. MnO2可作任一反应的催化剂
5. 实验室用过氧化氢和二氧化锰来制取和收集氧气用到的一组仪器是( )
A. 集气瓶、导管、胶头滴管、药匙
B. 漏斗、量筒、铁架台、集气瓶
C. 铁架台、试管、导管、集气瓶
D. 试管、酒精灯、铁架台、集气瓶
6. 某气体既能用排水法收集,又能用向上排空气法收集,该气体具有的性质是( )
A. 易溶于水,比空气轻 B. 难溶于水,比空气轻
C. 易溶于水,比空气重 D. 难溶于水,比空气重
用过氧化氢溶液和二氧化锰制取氧气的装置。其中分液漏斗可以通过调节活塞控制液体的滴加速度。
根据上图回答下列问题:
(1)分液漏斗中放入的物质是 ,锥 形瓶中应放入的物质是 。
(2)写出该方法制取氧气的文字表达式 ,要收集一瓶纯净的氧气应选择的装置 。(填字母)
(3)已知: ,则用此法代替氯酸钾加热制取氧气优点是 (填编号)
(1)生成物只有氧气 (2)不需加热 (3)生成物是氧气和水,利于环保。
(4)装置A 中反应很剧烈,据此提出实验安全注意事项是 。
(1)控制液体的滴加速度 (2)用体积小的锥形瓶(3)加热反应物1. 通常情况下,氨气(NH3)是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,形成的溶液是氨水。实验室用加热氯化氨和消石灰的固体混合物制取氨气。下图是实验室常用的装置。请回答:(1)实验室制取氨气的发生装置,可选用 (填装置编号);
(2)收集氨气,应采用的装置为 (填装置编号);收集氨气的集气瓶必须十分干燥,这是因为 。 AE能力拓展训练:创意空间活动与探究 实验室里常用某些受热时易分解放出氧气的含氧物质来制取氧气,如常用二氧化锰作催化剂,加热氯酸钾制取氧气,发生如下表达式的反应:
研究表明,许多金属氧化物对氯酸钾的分解有催化作用。分别用下列金属氧化物作催化剂,氯酸钾开始发生分解反应和反应剧烈时的温度如下表所示:
(1)实验室用氯酸钾制取氧气,如果不用二氧化锰作催化剂,最好选用____(填序号)
A. 氧化铁 B. 氧化铝 C. 氧化铜 D. 氧化镁
(2)实验室用氯酸钾制取氧气时,_________(填“能”或“不能”)用实验室中用双氧水制取氧气的实验装置。
(3)实验室用氯酸钾制取氧气时若用二氧化锰作催化剂,反应前后二氧化锰的质量__________(填序号)
不变 B. 变大
C. 变小 D. 可能变大也可能变小
(4)实验室加热氯酸钾制氧气时,忘记加入二氧化锰,其结果是( )
A. 不能产生氧气 B. 生成氧气的速度慢
C. 产生氧气的总量减少 D. 没有氯化钾生成
祝同学们学习进步
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 自然界中的水
- 第三节 水分子的变化
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 物质构成的奥秘
- 第一节 原子的构成
- 第二节 元素
- 第三节 物质组成的表示
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去 二氧化碳的实验室制取与性质
