常见气体的实验室制法[下学期]
图片预览

文档简介
课型: 复习课
课题: 气体的实验室制法
教学目标:
1.通过自学、回忆、分析、比较氧气、氢气、二氧化碳的实验室制法,讨论 、总结得出实验室制取气体的一般方法。
2.通过复习、自学、讨论、总结、记住实验室制取气体的操作步骤。
3.通过知识拓展、练习,学会运用实验室制取气体的一般方法解决新问题。
教学重点:制气装置,收集装置的选择方法。
教学过程:
引入新课:
[提问]实验室制取气体的方法和设计思路?
学生思考、讨论后回答:
出示课件
1、研究实验室制取气体的反应原理
2、研究实验室制取气体所采用的实验装置
3、研究如何检验所制得的气体
一:研究反应原理(课件)要求:回忆、看书、讨论,2分钟后回答下列问题
1:实验室制取氧气、氢气、二氧化碳通常选用的药品是什么?
2:反应条件是什么?
3:写出反应的方程式。
学生回忆、看书、对比、分析回答上述问题,并找学生在黑板写出反应方程式。
边让学生回答边出示课件,纠正学生答案。
二:研究实验装置
思考:实验室制取气体选用装置时应考虑哪些因素?从所给图中选出制氧气、氢气的装置,并解释原因。(要求:思考讨论、2分钟后回答)
1:气体发生装置的设计原则:
根据反应物质的状态和反应条件
2:气体发生装置的基本类型
A、固体反应物(加热)
B、C固液反应物(不加热)
学生自学讨论回答后,出示课件。
A、固体反应物(加热)
注意事项:
(1)试管口应略向下倾斜
(2)试管夹夹在试管的中上部;
(3)药品应平铺于试管底部
(4)导管不宜伸入试管过长
(5)实验开始时先检验装置的气密性
(6)加热时,先预热且应用外焰加热
(7)实验结束,先把导气管移出水槽,在熄灭酒精灯。
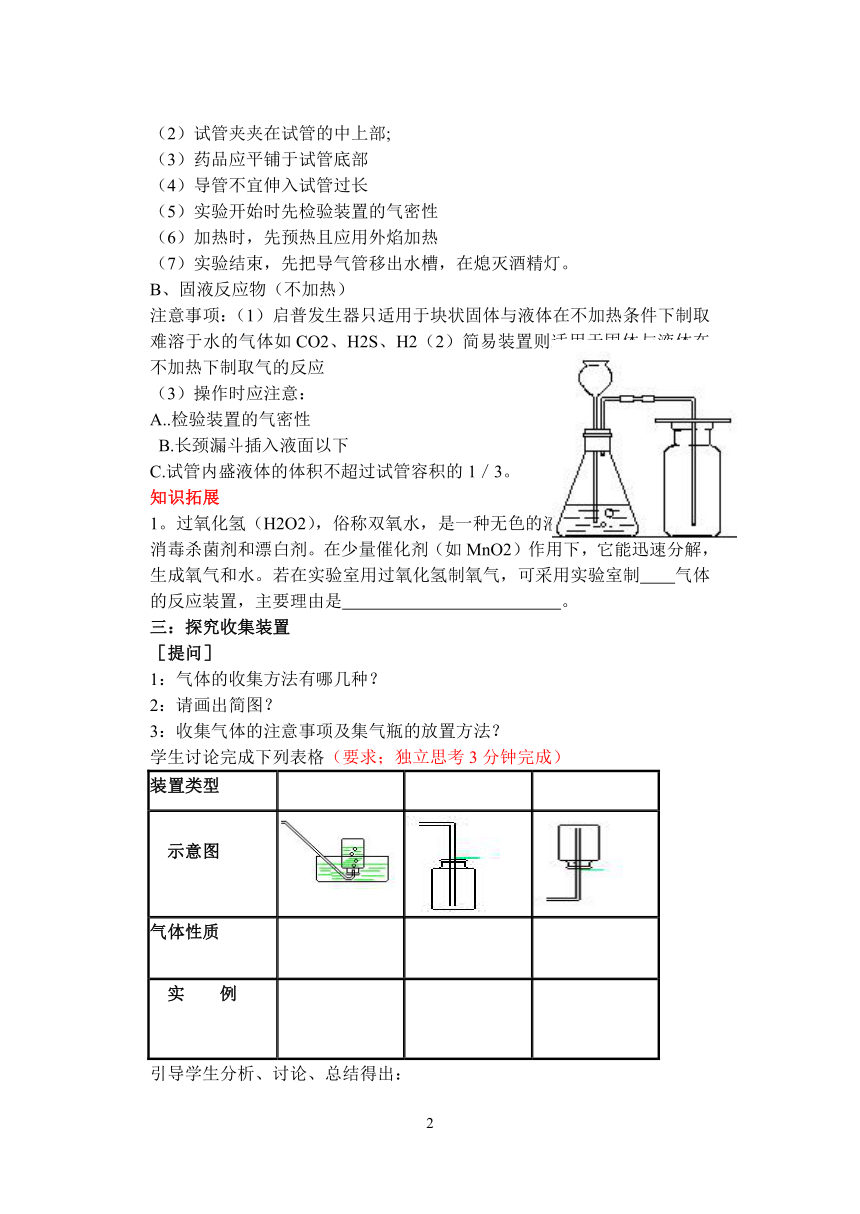
B、固液反应物(不加热)
注意事项:(1)启普发生器只适用于块状固体与液体在不加热条件下制取难溶于水的气体如CO2、H2S、H2(2)简易装置则适用于固体与液体在不加热下制取气的反应
(3)操作时应注意:
A..检验装置的气密性
B.长颈漏斗插入液面以下
C.试管内盛液体的体积不超过试管容积的1/3。
知识拓展
1。过氧化氢(H2O2),俗称双氧水,是一种无色的液体,常用作氧化剂、消毒杀菌剂和漂白剂。在少量催化剂(如MnO2)作用下,它能迅速分解,生成氧气和水。若在实验室用过氧化氢制氧气,可采用实验室制 气体的反应装置,主要理由是 。
三:探究收集装置
[提问]
1:气体的收集方法有哪几种?
2:请画出简图?
3:收集气体的注意事项及集气瓶的放置方法?
学生讨论完成下列表格(要求;独立思考3分钟完成)
装置类型
示意图
气体性质
实 例
引导学生分析、讨论、总结得出:
气体收集装置的设计原则
根据气体的 或 。
知识拓展
2.实验室常用加热醋酸钠和碱石灰的固体混合物来制取甲烷(CH4)气体,甲烷是一种无色无味、密度比空气小、极难溶于水的气体。制甲烷时,气体的发生装置与实验室制 气体的发生装置相同,气体的收集可选用 法。
四:检查制气装置的气密性
1如图所示,先把导管一端浸入水中,用双手捂住试管一会儿,导管口有气泡冒出;再把手拿开,过一会儿导管内又形成一段水柱,说明装置不漏气。
2启普发生器(或类似装置),将导气管上的活塞关闭,
向球形漏斗中注入一定量的水,使水面达到球形漏斗
的球体部位。停止加水后,水面能停留在
某一位置不再下降,说明不漏气。
五:气体验证与验满(思考回答)
1.如何验证O2、H2、CO2 ?
O2:用带火星的木条,伸入集气瓶内木条复燃。
CO2:通入澄清的石灰水,变混浊 。
H2:点燃火焰呈淡蓝色,产物只有水。
2.用排空空气法收集氧气、二氧化碳如何验满?
O2:用带火星的木条,伸入集气瓶口,木条复燃。
CO2:用然照的木条,伸入集气瓶口,木条熄灭。
六、制取气实验操作步骤(出示课件引导回答)
(一)固体加热型制取气体的实验步骤
1查:连接仪器,检查装气密性(方法?)
2装:用纸槽把固体药品装入大试管
3定:固定仪器
4点:点燃酒精灯(应用外焰加热)
5收:根据气体的物理性质,(水溶性,密度)
6移:把导管移出水面
7熄:熄灭酒精灯
(二)实验室制取氢气、二氧化碳(固、液不加热型)操作步骤
反馈练习
1检查桩的气密性,2先加固体再加液体药品,3固定装置,4收集气体。
2实验室用KClO3和MnO2来制取O2,要进行以下操作;①向试管加入药品;②加热试管;③检查装置的气密性;④用带有导管的橡皮塞塞紧试管;⑤将装置固定在铁架台上;⑥将导管口伸入水槽里装满水的倒立的集气瓶中⑦集气瓶装满水⑧移出导气管⑨熄灭酒精灯。其中正确的操作顺序是( )
A①④③⑤②⑥⑧⑦⑨ B ⑤④③①②⑥⑨⑧⑦
C④③①⑤⑦②⑥⑧⑨ D ④③①⑤⑦⑥②⑨⑧
引导学生小结:本节课你学到了什么?(出示课件)
实验室制取气体应从哪些方面考虑?
1原理:药品的选用,发生的化学反应及反应条件
2装置:根据反应物的状态及反应条件,选择制取气体的发生装置
3收集:根据生成气体方性质来确定收集的方法
4验证: 根据气体的性质来确定是要制备的气体
5验满:根据生成气体的性质来确定验满的方法
6操作步骤
7干燥:根据气体的性质确定所使用的干燥剂
8除杂:被净化的气体不参加反应,不能引进新的杂质
课堂练习
1下列制取二氧化碳的装置有哪些错误?
A.长颈漏斗下端管口没有插到液面以下。
B.广口瓶内导气管插到液面以下。
C.用向下排气法收集。
D.集气瓶内导管没有插到集气瓶底部。
E.集气瓶口没有放玻片
能力训练
2.硫化氢(H2S)是一种有毒气体,其密度比空气的密度大,且能溶于水形成氢硫酸。实验室通常用块状固体硫化亚铁(FeS)和稀硫酸混合,在常温下反应生成硫酸亚铁(FeSO4)硫化氢气体。试回答:
(l)实验室制取硫化氢的化学反应方程式为:
(2)根据装置图回答下列问题:
①制取硫化氢气体的发生装置可以选用
②若用C装置收集硫化氢气体,进气口应为 ,原因是
④D、E中盛有氢氧化钠溶液,用来吸收硫化氢气体,做上述实验时,为了防止多余的硫化氢逸出污染环境,可以将其通入装置_____吸收
3 通常情况下,氨气(NH3)是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,形成的溶液是氨水。实验室用加热氯化氨和消石灰的固体混合物制取氨气。下图是实验室常用的装置。请回答:
(1)实验室制取氨气的发生装置,可选用 (填装置编号);
(2)收集氨气,应采用的装置为 (填装置编号)
作业:1。基础训练
2点拨,常见气体的制法练习。
B
A
E
D
C
PAGE
1
课题: 气体的实验室制法
教学目标:
1.通过自学、回忆、分析、比较氧气、氢气、二氧化碳的实验室制法,讨论 、总结得出实验室制取气体的一般方法。
2.通过复习、自学、讨论、总结、记住实验室制取气体的操作步骤。
3.通过知识拓展、练习,学会运用实验室制取气体的一般方法解决新问题。
教学重点:制气装置,收集装置的选择方法。
教学过程:
引入新课:
[提问]实验室制取气体的方法和设计思路?
学生思考、讨论后回答:
出示课件
1、研究实验室制取气体的反应原理
2、研究实验室制取气体所采用的实验装置
3、研究如何检验所制得的气体
一:研究反应原理(课件)要求:回忆、看书、讨论,2分钟后回答下列问题
1:实验室制取氧气、氢气、二氧化碳通常选用的药品是什么?
2:反应条件是什么?
3:写出反应的方程式。
学生回忆、看书、对比、分析回答上述问题,并找学生在黑板写出反应方程式。
边让学生回答边出示课件,纠正学生答案。
二:研究实验装置
思考:实验室制取气体选用装置时应考虑哪些因素?从所给图中选出制氧气、氢气的装置,并解释原因。(要求:思考讨论、2分钟后回答)
1:气体发生装置的设计原则:
根据反应物质的状态和反应条件
2:气体发生装置的基本类型
A、固体反应物(加热)
B、C固液反应物(不加热)
学生自学讨论回答后,出示课件。
A、固体反应物(加热)
注意事项:
(1)试管口应略向下倾斜
(2)试管夹夹在试管的中上部;
(3)药品应平铺于试管底部
(4)导管不宜伸入试管过长
(5)实验开始时先检验装置的气密性
(6)加热时,先预热且应用外焰加热
(7)实验结束,先把导气管移出水槽,在熄灭酒精灯。
B、固液反应物(不加热)
注意事项:(1)启普发生器只适用于块状固体与液体在不加热条件下制取难溶于水的气体如CO2、H2S、H2(2)简易装置则适用于固体与液体在不加热下制取气的反应
(3)操作时应注意:
A..检验装置的气密性
B.长颈漏斗插入液面以下
C.试管内盛液体的体积不超过试管容积的1/3。
知识拓展
1。过氧化氢(H2O2),俗称双氧水,是一种无色的液体,常用作氧化剂、消毒杀菌剂和漂白剂。在少量催化剂(如MnO2)作用下,它能迅速分解,生成氧气和水。若在实验室用过氧化氢制氧气,可采用实验室制 气体的反应装置,主要理由是 。
三:探究收集装置
[提问]
1:气体的收集方法有哪几种?
2:请画出简图?
3:收集气体的注意事项及集气瓶的放置方法?
学生讨论完成下列表格(要求;独立思考3分钟完成)
装置类型
示意图
气体性质
实 例
引导学生分析、讨论、总结得出:
气体收集装置的设计原则
根据气体的 或 。
知识拓展
2.实验室常用加热醋酸钠和碱石灰的固体混合物来制取甲烷(CH4)气体,甲烷是一种无色无味、密度比空气小、极难溶于水的气体。制甲烷时,气体的发生装置与实验室制 气体的发生装置相同,气体的收集可选用 法。
四:检查制气装置的气密性
1如图所示,先把导管一端浸入水中,用双手捂住试管一会儿,导管口有气泡冒出;再把手拿开,过一会儿导管内又形成一段水柱,说明装置不漏气。
2启普发生器(或类似装置),将导气管上的活塞关闭,
向球形漏斗中注入一定量的水,使水面达到球形漏斗
的球体部位。停止加水后,水面能停留在
某一位置不再下降,说明不漏气。
五:气体验证与验满(思考回答)
1.如何验证O2、H2、CO2 ?
O2:用带火星的木条,伸入集气瓶内木条复燃。
CO2:通入澄清的石灰水,变混浊 。
H2:点燃火焰呈淡蓝色,产物只有水。
2.用排空空气法收集氧气、二氧化碳如何验满?
O2:用带火星的木条,伸入集气瓶口,木条复燃。
CO2:用然照的木条,伸入集气瓶口,木条熄灭。
六、制取气实验操作步骤(出示课件引导回答)
(一)固体加热型制取气体的实验步骤
1查:连接仪器,检查装气密性(方法?)
2装:用纸槽把固体药品装入大试管
3定:固定仪器
4点:点燃酒精灯(应用外焰加热)
5收:根据气体的物理性质,(水溶性,密度)
6移:把导管移出水面
7熄:熄灭酒精灯
(二)实验室制取氢气、二氧化碳(固、液不加热型)操作步骤
反馈练习
1检查桩的气密性,2先加固体再加液体药品,3固定装置,4收集气体。
2实验室用KClO3和MnO2来制取O2,要进行以下操作;①向试管加入药品;②加热试管;③检查装置的气密性;④用带有导管的橡皮塞塞紧试管;⑤将装置固定在铁架台上;⑥将导管口伸入水槽里装满水的倒立的集气瓶中⑦集气瓶装满水⑧移出导气管⑨熄灭酒精灯。其中正确的操作顺序是( )
A①④③⑤②⑥⑧⑦⑨ B ⑤④③①②⑥⑨⑧⑦
C④③①⑤⑦②⑥⑧⑨ D ④③①⑤⑦⑥②⑨⑧
引导学生小结:本节课你学到了什么?(出示课件)
实验室制取气体应从哪些方面考虑?
1原理:药品的选用,发生的化学反应及反应条件
2装置:根据反应物的状态及反应条件,选择制取气体的发生装置
3收集:根据生成气体方性质来确定收集的方法
4验证: 根据气体的性质来确定是要制备的气体
5验满:根据生成气体的性质来确定验满的方法
6操作步骤
7干燥:根据气体的性质确定所使用的干燥剂
8除杂:被净化的气体不参加反应,不能引进新的杂质
课堂练习
1下列制取二氧化碳的装置有哪些错误?
A.长颈漏斗下端管口没有插到液面以下。
B.广口瓶内导气管插到液面以下。
C.用向下排气法收集。
D.集气瓶内导管没有插到集气瓶底部。
E.集气瓶口没有放玻片
能力训练
2.硫化氢(H2S)是一种有毒气体,其密度比空气的密度大,且能溶于水形成氢硫酸。实验室通常用块状固体硫化亚铁(FeS)和稀硫酸混合,在常温下反应生成硫酸亚铁(FeSO4)硫化氢气体。试回答:
(l)实验室制取硫化氢的化学反应方程式为:
(2)根据装置图回答下列问题:
①制取硫化氢气体的发生装置可以选用
②若用C装置收集硫化氢气体,进气口应为 ,原因是
④D、E中盛有氢氧化钠溶液,用来吸收硫化氢气体,做上述实验时,为了防止多余的硫化氢逸出污染环境,可以将其通入装置_____吸收
3 通常情况下,氨气(NH3)是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水,形成的溶液是氨水。实验室用加热氯化氨和消石灰的固体混合物制取氨气。下图是实验室常用的装置。请回答:
(1)实验室制取氨气的发生装置,可选用 (填装置编号);
(2)收集氨气,应采用的装置为 (填装置编号)
作业:1。基础训练
2点拨,常见气体的制法练习。
B
A
E
D
C
PAGE
1
同课章节目录
