探究复分解反应的条件[下学期]
图片预览


文档简介
《探究复分解反应发生的条件》教学方案
明觉中学化学教研组 杨德项
课 题 探究复分解反应发生的条件
教学目标 目标表述 基础性目标: 1、初步掌握复分解反应的条件。2、能根据复分解反应发生的条件判断酸、碱、盐之间的反应能否发生。
发展性目标: 1、对学生进行实验技能的培养和训练,培养学生观察能力、探究能力和归纳实验现象的能力和习惯。2、通过对实验的探究、分析,培养学生严谨、认真、实事求是的科学态度。3使学生在实验探究、讨论中学会与别人交流、合作,增强协作精神。
制定依据 课标考纲 通过对复分解反应条件的探究来正确判断和书写复分解反应方程式。
教材分析 在第十单元我们已经学习了酸、碱的化学性质、复分解反应的概念,在此基础上,复分解反应条件的探究成为认知发展的必然要求。虽然前面学习了酸与盐、酸与金属氧化物、酸与碱、碱与盐之间的反应,但学生还没有形成这类物质之间进行反应的规律性的认知。本节课通过书写这类物质之间进行反应的化学方程式,分析得出复分解反应的形式,在此基础上,对“这些类型的物质是否都能发生复分解反应”进行质疑→通过实验探究复分解反应的条件→在得出复分解反应条件的基础上,再次探究盐与盐能否发生复分解反应→练习→归纳,使学生根据复分解反应的条件能正确判断复分解反应能否发生以及能正确的写出复分解反应的化学方程式。
学情分析 学生有什么 学生已经了解酸与盐、酸与金属氧化物、酸与碱、碱与盐反应及复分解反应的概念,并拥有继续深入学习化学的欲望和兴趣。
学生缺什么 零星的学习了有一些复分解的形式,还没有将它们归纳形成体系,缺乏规律性认识的能力。本节课将注意培养学生的分析归纳能力。
教学难点 难点表述 归纳复分解反应的条件。
原因分析 因复分解反应的条件是判断酸、碱、盐能否发生反应的根本条件,既是酸、碱、盐性质的重点又是酸、碱、盐性质的难点,该条件比较抽象又不易记得,我通过具体实验引出复分解反应的条件,再通过练习加以巩固,印象较深刻。
助学 方案: 创设情景→实验探究→得出结论→利用结论来判断
教学过程教学过程 教、学活动 具体内容 设计意图 耗时估算
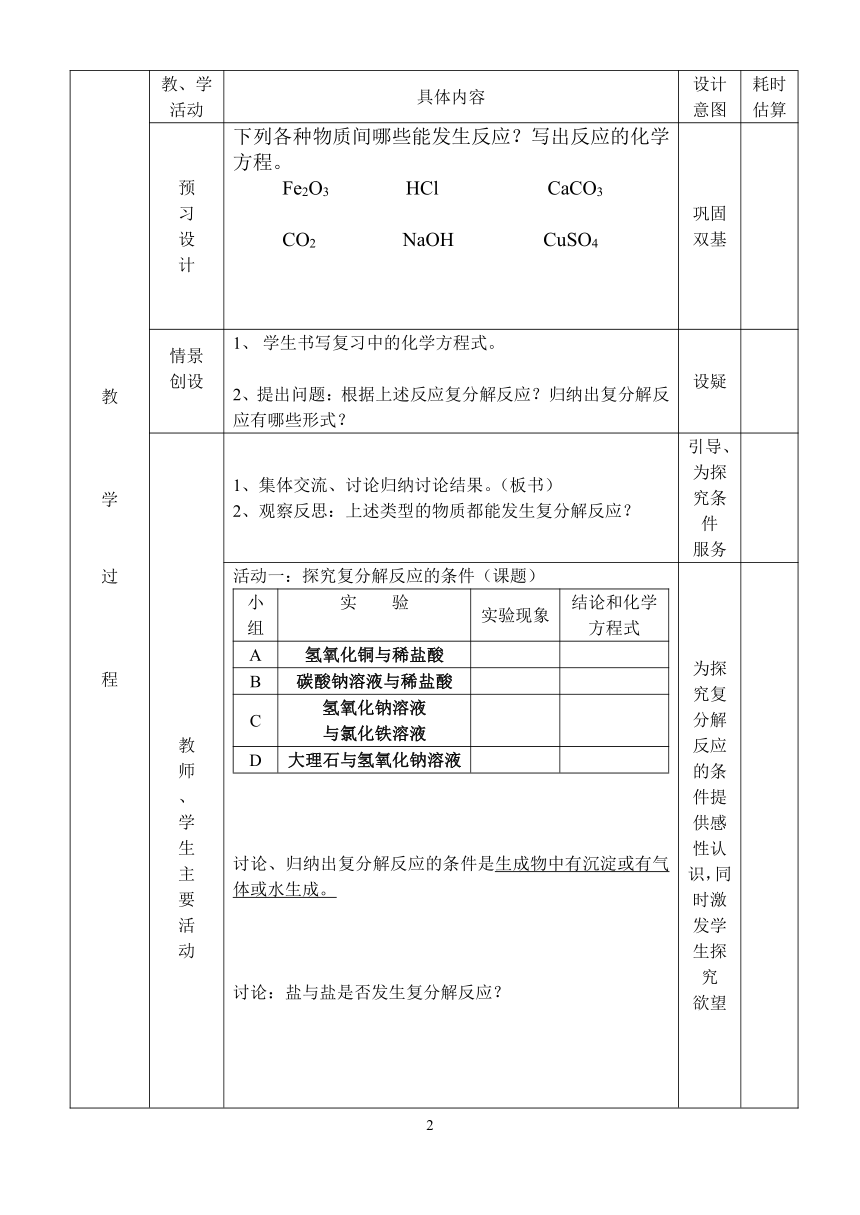
预习设计 下列各种物质间哪些能发生反应?写出反应的化学方程。Fe2O3 HCl CaCO3CO2 NaOH CuSO4 巩固双基
情景创设 学生书写复习中的化学方程式。2、提出问题:根据上述反应复分解反应?归纳出复分解反应有哪些形式? 设疑
教师、学生主要活动 1、集体交流、讨论归纳讨论结果。(板书)2、观察反思:上述类型的物质都能发生复分解反应? 引导、为探究条件服务
活动一:探究复分解反应的条件(课题)小组实 验实验现象结论和化学方程式A氢氧化铜与稀盐酸B碳酸钠溶液与稀盐酸C氢氧化钠溶液与氯化铁溶液D大理石与氢氧化钠溶液讨论、归纳出复分解反应的条件是生成物中有沉淀或有气体或水生成。讨论:盐与盐是否发生复分解反应? 为探究复分解反应的条件提供感性认识,同时激发学生探究欲望
活动二:探究盐与盐是否发生复分解反应实验现象结论硝酸银溶液与氯化钠溶液硫酸钠溶液与氯化钡溶液大理石与氯化钠溶液硫酸钠溶液与氯化铁溶液讨论、归纳:盐+盐=两种新盐(板书)复分解反应的形式: 酸+金属氧化物=盐+水酸+碱===盐+水酸+盐===新酸+新盐碱+盐===新碱+新盐盐+盐===两种新盐复分解反应的本质: 进一步通过实验验证复分解反应的条件
教学过程教学过程 教师、学生主要活动 活动三:学以致用下列物质之间能否发生复分解反应?若不能,说明理由;若能,写出它们的化学方程式:(1)H2SO4+ BaCl2(2)BaCO3+ Na2SO4(3)Mg(OH)2+HNO3(4)ZnO+H2SO4(5)Cu(OH)2+MgCl2(6)CuSO4+Ba(NO3)2小组讨论、交流得出正确答案。独立完成,比一比、赛一赛,看谁既快又准得得出正确答案:(1)H2SO4+ NaNO3(2)Na2CO3+ CaCl2(3)KOH+ZnSO4(4)K2CO3+Al(OH)3 运用复分解反应的条件,解决实际问题
反馈练习 1、下列反应类型属于复分解的是( )A、2NaOH+SO2===Na2SO3+H2O B、 Fe+ H2SO4===FeSO4+H2↑C、 CuO+ H2SO4=== CuSO4+ H2O D、Cu+ 2AgNO3===Cu(NO3)2+2Ag2.鉴别CO32-(或HCO3 -)常用的试剂是( )A、澄清石灰水 B、稀盐酸和氢氧化钠溶液C、稀盐酸 D、稀盐酸和澄清石灰水3、下列各组物质不能发生复分解反应的是( )A、AgNO3+ HCl B、BaCl2+ Ca CO3C、Ba(OH)2+ H2SO4 D、NaOH+ MgCl24、.鉴别三瓶无色溶液:H2SO4、CaCl2、NaCl可选用的试剂是( )A、Na2CO3 B、紫色石蕊试液液 C、BaCl2 D、AgNO35、现有下列物质:碳酸钠溶液、稀硫酸、氢氧化钠溶液、硫酸铜溶液、氢氧化镁。按下列要求写出不同形式的复分解反应:(1)有气体生成的复分解反应:(2)有沉淀生成的复分解反应:(3)有水生成的复分解反应: 教学目标达成检测及反馈
课堂小结 讨论:通过本节课的学习你有哪些收获?
板书设计 复分解反应的形式酸+金属氧化物=盐+水酸+碱===盐+水酸+盐===新酸+新盐碱+盐===新碱+新盐盐+盐===两种新盐二、复分解反应的条件: 生成物中有沉淀或有气体或有水生成。
课后作业 复习本课题的内容,预习下一课题的内容。完成学案中的课后作业和评价手册相关的内容。
反思与重建
《探究复分解反应发生的条件》学案
班级: 姓名: 合作者
复习:
下列各种物质间哪些能发生反应?写出反应的化学方程式。
Fe2O3 HCl CaCO3
CO2 NaOH CuSO4
讨论:根据上述反应判断哪些属于复分解反应?归纳出复分解反应有哪些形式?
活动一:探究复分解反应的条件
小组 实验 现象 结论或化学方程式
A 氢氧化铜与稀盐酸
B 碳酸钠溶液与稀盐酸
C 氢氧化钠溶液与氯化铁溶液
D 大理石与氢氧化钠溶液
复分解反应的条件是:
活动二:探究盐与盐是否发生复分解反应
实验 现 象 结 论
硝酸银溶液与氯化钠溶液
硫酸钠溶液与氯化钡溶液
大理石与氯化钠溶液
硫酸钠溶液与氯化铁溶液
讨论、归纳得出结论是:
活动三:学以致用
1、 下列物质之间能否发生复分解反应?若不能,说明理由;若能,写出它们的化学方程式:
(1)H2SO4+ BaCl2
(2)BaCO3+ Na2SO4
(3)Mg(OH)2+HNO3
(4)ZnO+H2SO4
(5)Cu(OH)2+MgCl2
(6)CuSO4+Ba(NO3)2
小组讨论、交流得出正确答案。
2、 独立完成,比一比、赛一赛,看谁既快又准的得出正确答案:
(1)H2SO4+ NaNO3
(2)Na2CO3+ CaCl2
(3)KOH+ZnSO4
(4)K2CO3+Al(OH)3
反馈练习:
1、下列反应类型属于复分解的是( )
A、2NaOH+SO2===Na2SO3+H2O B. Fe+ H2SO4====FeSO4+H2↑
C. CuO+ H2SO4==== CuSO4+ H2O D. Cu+ 2AgNO3====Cu(NO3)2+2Ag
2.鉴别CO32-(或HCO3 -)常用的试剂是( )
A、澄清石灰水 B、稀盐酸和氢氧化钠溶液
C、稀盐酸 D、稀盐酸和澄清石灰水
3、下列各组物质不能发生复分解反应的是( )
A、AgNO3+ HCl B、BaCl2+ Ca CO3
C、Ba(OH)2+ H2SO4 D、NaOH+ MgCl2
4、.鉴别三瓶无色溶液:H2SO4、CaCl2、NaCl可选用的试剂( )
A、Na2CO3 B、紫色石蕊试液 C、BaCl2 D、KNO3
5、现有下列物质:碳酸钠溶液、稀硫酸、氢氧化钠溶液、硫酸铜溶液、氢氧化镁。按下列要求写出不同形式的复分解反应:
(1)有气体生成的复分解反应:
(2)有沉淀生成的复分解反应:
(3)有水生成的复分解反应:
PAGE
1
明觉中学化学教研组 杨德项
课 题 探究复分解反应发生的条件
教学目标 目标表述 基础性目标: 1、初步掌握复分解反应的条件。2、能根据复分解反应发生的条件判断酸、碱、盐之间的反应能否发生。
发展性目标: 1、对学生进行实验技能的培养和训练,培养学生观察能力、探究能力和归纳实验现象的能力和习惯。2、通过对实验的探究、分析,培养学生严谨、认真、实事求是的科学态度。3使学生在实验探究、讨论中学会与别人交流、合作,增强协作精神。
制定依据 课标考纲 通过对复分解反应条件的探究来正确判断和书写复分解反应方程式。
教材分析 在第十单元我们已经学习了酸、碱的化学性质、复分解反应的概念,在此基础上,复分解反应条件的探究成为认知发展的必然要求。虽然前面学习了酸与盐、酸与金属氧化物、酸与碱、碱与盐之间的反应,但学生还没有形成这类物质之间进行反应的规律性的认知。本节课通过书写这类物质之间进行反应的化学方程式,分析得出复分解反应的形式,在此基础上,对“这些类型的物质是否都能发生复分解反应”进行质疑→通过实验探究复分解反应的条件→在得出复分解反应条件的基础上,再次探究盐与盐能否发生复分解反应→练习→归纳,使学生根据复分解反应的条件能正确判断复分解反应能否发生以及能正确的写出复分解反应的化学方程式。
学情分析 学生有什么 学生已经了解酸与盐、酸与金属氧化物、酸与碱、碱与盐反应及复分解反应的概念,并拥有继续深入学习化学的欲望和兴趣。
学生缺什么 零星的学习了有一些复分解的形式,还没有将它们归纳形成体系,缺乏规律性认识的能力。本节课将注意培养学生的分析归纳能力。
教学难点 难点表述 归纳复分解反应的条件。
原因分析 因复分解反应的条件是判断酸、碱、盐能否发生反应的根本条件,既是酸、碱、盐性质的重点又是酸、碱、盐性质的难点,该条件比较抽象又不易记得,我通过具体实验引出复分解反应的条件,再通过练习加以巩固,印象较深刻。
助学 方案: 创设情景→实验探究→得出结论→利用结论来判断
教学过程教学过程 教、学活动 具体内容 设计意图 耗时估算
预习设计 下列各种物质间哪些能发生反应?写出反应的化学方程。Fe2O3 HCl CaCO3CO2 NaOH CuSO4 巩固双基
情景创设 学生书写复习中的化学方程式。2、提出问题:根据上述反应复分解反应?归纳出复分解反应有哪些形式? 设疑
教师、学生主要活动 1、集体交流、讨论归纳讨论结果。(板书)2、观察反思:上述类型的物质都能发生复分解反应? 引导、为探究条件服务
活动一:探究复分解反应的条件(课题)小组实 验实验现象结论和化学方程式A氢氧化铜与稀盐酸B碳酸钠溶液与稀盐酸C氢氧化钠溶液与氯化铁溶液D大理石与氢氧化钠溶液讨论、归纳出复分解反应的条件是生成物中有沉淀或有气体或水生成。讨论:盐与盐是否发生复分解反应? 为探究复分解反应的条件提供感性认识,同时激发学生探究欲望
活动二:探究盐与盐是否发生复分解反应实验现象结论硝酸银溶液与氯化钠溶液硫酸钠溶液与氯化钡溶液大理石与氯化钠溶液硫酸钠溶液与氯化铁溶液讨论、归纳:盐+盐=两种新盐(板书)复分解反应的形式: 酸+金属氧化物=盐+水酸+碱===盐+水酸+盐===新酸+新盐碱+盐===新碱+新盐盐+盐===两种新盐复分解反应的本质: 进一步通过实验验证复分解反应的条件
教学过程教学过程 教师、学生主要活动 活动三:学以致用下列物质之间能否发生复分解反应?若不能,说明理由;若能,写出它们的化学方程式:(1)H2SO4+ BaCl2(2)BaCO3+ Na2SO4(3)Mg(OH)2+HNO3(4)ZnO+H2SO4(5)Cu(OH)2+MgCl2(6)CuSO4+Ba(NO3)2小组讨论、交流得出正确答案。独立完成,比一比、赛一赛,看谁既快又准得得出正确答案:(1)H2SO4+ NaNO3(2)Na2CO3+ CaCl2(3)KOH+ZnSO4(4)K2CO3+Al(OH)3 运用复分解反应的条件,解决实际问题
反馈练习 1、下列反应类型属于复分解的是( )A、2NaOH+SO2===Na2SO3+H2O B、 Fe+ H2SO4===FeSO4+H2↑C、 CuO+ H2SO4=== CuSO4+ H2O D、Cu+ 2AgNO3===Cu(NO3)2+2Ag2.鉴别CO32-(或HCO3 -)常用的试剂是( )A、澄清石灰水 B、稀盐酸和氢氧化钠溶液C、稀盐酸 D、稀盐酸和澄清石灰水3、下列各组物质不能发生复分解反应的是( )A、AgNO3+ HCl B、BaCl2+ Ca CO3C、Ba(OH)2+ H2SO4 D、NaOH+ MgCl24、.鉴别三瓶无色溶液:H2SO4、CaCl2、NaCl可选用的试剂是( )A、Na2CO3 B、紫色石蕊试液液 C、BaCl2 D、AgNO35、现有下列物质:碳酸钠溶液、稀硫酸、氢氧化钠溶液、硫酸铜溶液、氢氧化镁。按下列要求写出不同形式的复分解反应:(1)有气体生成的复分解反应:(2)有沉淀生成的复分解反应:(3)有水生成的复分解反应: 教学目标达成检测及反馈
课堂小结 讨论:通过本节课的学习你有哪些收获?
板书设计 复分解反应的形式酸+金属氧化物=盐+水酸+碱===盐+水酸+盐===新酸+新盐碱+盐===新碱+新盐盐+盐===两种新盐二、复分解反应的条件: 生成物中有沉淀或有气体或有水生成。
课后作业 复习本课题的内容,预习下一课题的内容。完成学案中的课后作业和评价手册相关的内容。
反思与重建
《探究复分解反应发生的条件》学案
班级: 姓名: 合作者
复习:
下列各种物质间哪些能发生反应?写出反应的化学方程式。
Fe2O3 HCl CaCO3
CO2 NaOH CuSO4
讨论:根据上述反应判断哪些属于复分解反应?归纳出复分解反应有哪些形式?
活动一:探究复分解反应的条件
小组 实验 现象 结论或化学方程式
A 氢氧化铜与稀盐酸
B 碳酸钠溶液与稀盐酸
C 氢氧化钠溶液与氯化铁溶液
D 大理石与氢氧化钠溶液
复分解反应的条件是:
活动二:探究盐与盐是否发生复分解反应
实验 现 象 结 论
硝酸银溶液与氯化钠溶液
硫酸钠溶液与氯化钡溶液
大理石与氯化钠溶液
硫酸钠溶液与氯化铁溶液
讨论、归纳得出结论是:
活动三:学以致用
1、 下列物质之间能否发生复分解反应?若不能,说明理由;若能,写出它们的化学方程式:
(1)H2SO4+ BaCl2
(2)BaCO3+ Na2SO4
(3)Mg(OH)2+HNO3
(4)ZnO+H2SO4
(5)Cu(OH)2+MgCl2
(6)CuSO4+Ba(NO3)2
小组讨论、交流得出正确答案。
2、 独立完成,比一比、赛一赛,看谁既快又准的得出正确答案:
(1)H2SO4+ NaNO3
(2)Na2CO3+ CaCl2
(3)KOH+ZnSO4
(4)K2CO3+Al(OH)3
反馈练习:
1、下列反应类型属于复分解的是( )
A、2NaOH+SO2===Na2SO3+H2O B. Fe+ H2SO4====FeSO4+H2↑
C. CuO+ H2SO4==== CuSO4+ H2O D. Cu+ 2AgNO3====Cu(NO3)2+2Ag
2.鉴别CO32-(或HCO3 -)常用的试剂是( )
A、澄清石灰水 B、稀盐酸和氢氧化钠溶液
C、稀盐酸 D、稀盐酸和澄清石灰水
3、下列各组物质不能发生复分解反应的是( )
A、AgNO3+ HCl B、BaCl2+ Ca CO3
C、Ba(OH)2+ H2SO4 D、NaOH+ MgCl2
4、.鉴别三瓶无色溶液:H2SO4、CaCl2、NaCl可选用的试剂( )
A、Na2CO3 B、紫色石蕊试液 C、BaCl2 D、KNO3
5、现有下列物质:碳酸钠溶液、稀硫酸、氢氧化钠溶液、硫酸铜溶液、氢氧化镁。按下列要求写出不同形式的复分解反应:
(1)有气体生成的复分解反应:
(2)有沉淀生成的复分解反应:
(3)有水生成的复分解反应:
PAGE
1
同课章节目录
