高三化学总复习多媒体教案晶体结构[下学期]
文档属性
| 名称 | 高三化学总复习多媒体教案晶体结构[下学期] |

|
|
| 格式 | rar | ||
| 文件大小 | 634.3KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2006-09-30 00:00:00 | ||
图片预览




文档简介
(共27张PPT)
高三化学总复习多媒体教案
晶 体 结 构
晶 体 结 构
高三化学总复习多媒体教案
主菜单
基础知识
晶体结构
课堂练习
课后作业
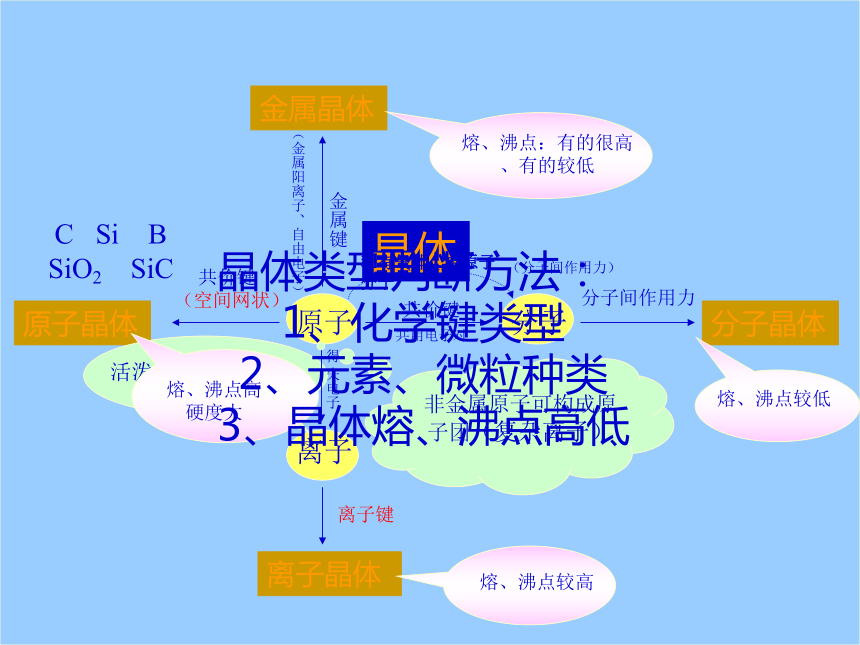
晶体、微粒、化学键
金属晶体
原子晶体
离子晶体
分子晶体
活泼金属、非金属
共价键
(空间网状)
共价键
得 失电子
分子间作用力
金属键
(金属阳离子、自由电子)
原子
分子
离子
共用电子对
晶体
稀有气体:单原子分子
非金属原子可构成原子团(复杂离子)
熔、沸点较高
熔、沸点较低
熔、沸点高硬度大
熔、沸点:有的很高、有的较低
C Si B
SiO2 SiC
离子键
(分子间作用力)
晶体类型判断方法:
1、化学键类型
2、元素、微粒种类
3、晶体熔、沸点高低
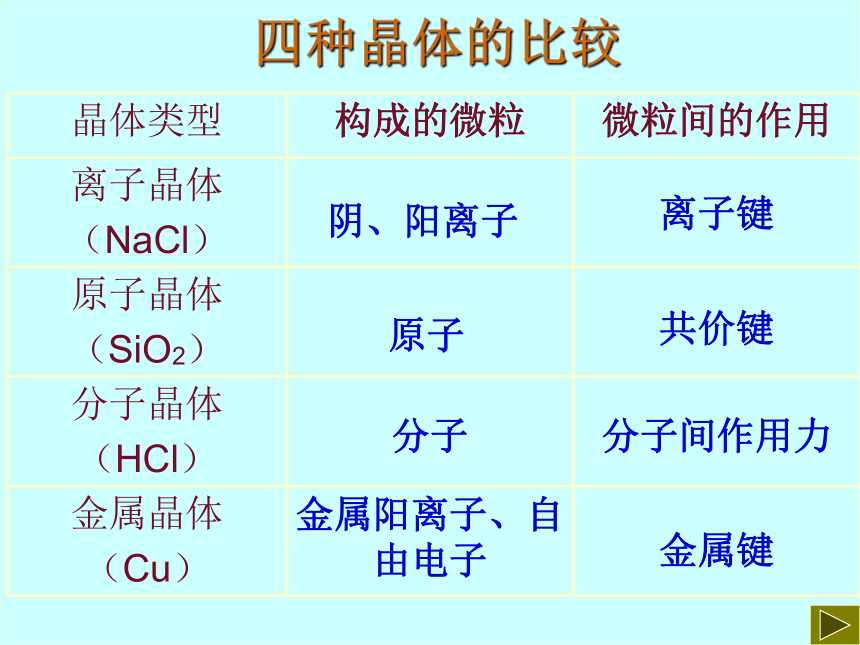
四种晶体的比较
晶体类型 构成的微粒 微粒间的作用
离子晶体
(NaCl)
原子晶体
(SiO2)
分子晶体
(HCl)
金属晶体
(Cu)
阴、阳离子
原子
分子
金属阳离子、自由电子
离子键
共价键
分子间作用力
金属键
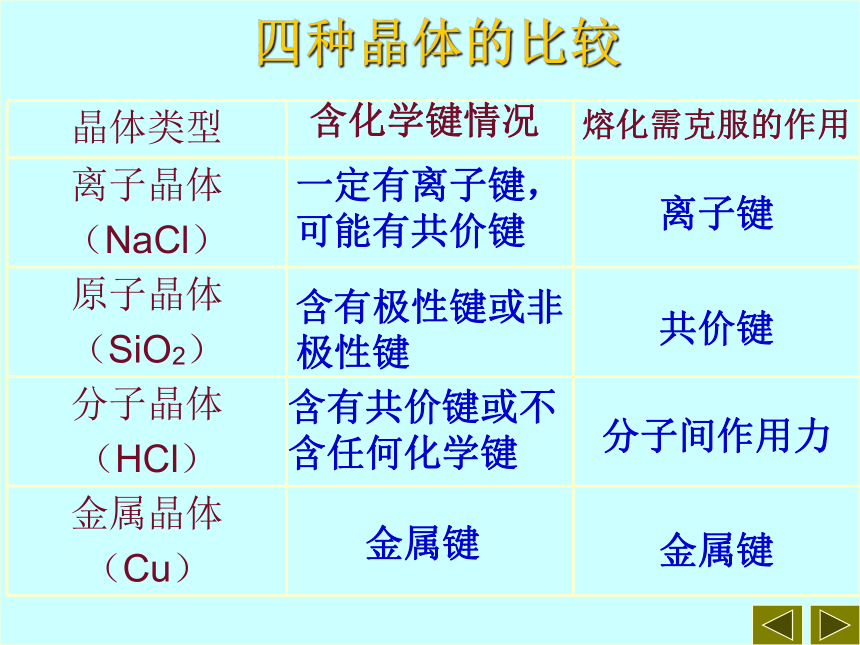
四种晶体的比较
晶体类型
离子晶体
(NaCl)
原子晶体
(SiO2)
分子晶体
(HCl)
金属晶体
(Cu)
一定有离子键,可能有共价键
含有极性键或非极性键
含有共价键或不含任何化学键
金属键
离子键
共价键
分子间作用力
金属键
含化学键情况
熔化需克服的作用
四种晶体的比较
晶体类型
离子晶体
(NaCl)
原子晶体
(SiO2)
分子晶体
(HCl)
金属晶体
(Cu)
不导电
导电
固体导电情况
熔化时导电情况
除半导体外不导电
不导电
导电
除半导体外不导电
不导电
导电
熔、沸点的比较
不同类型:
原子晶体〉离子晶体〉分子晶体
同种类型:
微粒间的作用越强,熔沸点越高
原子晶体:
原子半径越小,共价键越强,
熔沸点越高
离子晶体:
离子电荷数越多,离子半径越小,离子键 越强,熔沸点越高
金属晶体:
金属阳离子电荷数越多,离子半径越小,金属键越强,熔沸点越高
一般而言:
熔、沸点的比较
分子晶体:(一般来说)
A、相对分子质量越大,熔沸点越高
B、相对分子质量相同:
1、分子极性越大,熔沸点越高
如:CO 〉N2
2、支链越多,熔沸点越低
如:正戊烷〉异戊烷〉新戊烷
3、芳香族化合物:邻〉间〉对位化合物
返回主菜单
2、晶体举例:
NaCl的晶体结构:
6:6
常见晶体的微观结构
(1)NaCl晶体
(1)钠离子和氯离子的位置:
(1)钠离子和氯离子位于立方体的顶角上,并交错排列。(2)钠离子:体心和棱中点;氯离子:面心和顶点,或者反之。
(2)每个晶胞含钠离子、氯离子的个数
计算方法:
顶点占1/8;棱占1/4;面心占1/2;体心占1
氯离子: 钠离子:
(3)与Na+等距离且最近的Na+ 、Cl- 各有几个?
与Na+等距离且最近的Na+ 有:12个
与Na+等距离且最近的Cl- 有:6个
CsCl的晶体结构:
8:8
常见晶体的微观结构
(2)CsCl晶体
(1)铯离子和氯离子的位置:
铯离子:体心
氯离子:顶点;或者反之。
(2)每个晶胞含铯离子、氯离子的个数
铯离子:1个 ;氯离子:1个
(3)与铯离子等距离且最近的铯离子、氯离子各有几个?
铯离子:6个 ;氯离子:8个
常见晶体的微观结构
(3)干冰晶体
(1)二氧化碳分子的位置:
二氧化碳分子位于:体心和棱中点(面心和顶点)
(2)每个晶胞含二氧化碳分子的个数
二氧化碳分子的个数: 4 个
(3)与每个二氧化碳分子等距离且最近的二氧化
碳分子有几个?
12个
(4)金刚石(硅)与石墨
晶体 金刚石 石墨
构型
键角、键长
正四面体、空间网状原子晶体
平面正六边形、层状混合晶体
109 o 28′
120 o
键长:金刚石〉石墨
(4)金刚石(硅)与石墨
晶体 金刚石 石墨
最小碳环
C-C 键与C原子的个数比
六元环(不同面)
六元环(同面)
2 :1
3 :2
(4)金刚石(硅)与石墨
晶体 金刚石 石墨
熔点
硬度
金刚石〈 石墨
金刚石〉石墨
硬度的比较
(5)二氧化硅晶体
思考:
1、硅原子与跟它相连的4个氧原子的关系
2、硅原子与它周围4个硅原子的关系
3、Si-O键与Si原子的个数比为多少?
返回主菜单
课堂练习
练习1:下列说法中正确的是( )
A、离子晶体一定含有离子键,分子晶体一定含有共价键
B、NaCl、HCl、SiO2 的晶体中都不存在单个分子
C、HCl 和 乙醇晶体溶于水时克服微粒间作用力的类型相同
D、HCl 和 乙醇晶体熔化时克服微粒间作用力的类型相同
D
返回主菜单
课堂练习
练习2:据报道,科研人员应用电子计算机模拟出类似C60的物质N60, 试推测出该物质不可能具有的性质是( )
A、N60难溶于水
B、稳定性:N60〈 N2
C、熔点: N60 〉N2
D、它属于原子晶体
D
返回主菜单
课堂练习
练习3:下列说法中错误的是( )
A、12克石墨中含有1.5 mol C-C键
B、60克二氧化硅中含有4mol Si-O键
C、氯化钠晶体中,每个氯离子周围等距离且最近的氯离子有12个
D、在石墨晶体中,每个最小环平均含有6个碳原子
D
返回主菜单
课堂练习
返回主菜单
练习4:某晶体的晶胞结构如图,试确定其化学式
A:1/4×4=1 B:1/8 ×8=1 C:1 ×1=1
A、B、C的个数比为:1:1:1
化学式为:ABC
课堂练习
返回主菜单
练习5:晶体硼的基本结构单元是由硼原子组成的正二十面体,其中有20个等边三角形的面和一定数目的顶点,每个顶点各有一个硼原子,则此基本结构单元是由( )个硼原子构成的,其中B-B键的键角为( ),共含有( )个B-B键。
12
60o
30
晶体的熔点
金刚石
食盐
干冰
返回原处
晶体的硬度
金刚石
石 墨
返回原处
高三化学总复习多媒体教案
晶 体 结 构
晶 体 结 构
高三化学总复习多媒体教案
主菜单
基础知识
晶体结构
课堂练习
课后作业
晶体、微粒、化学键
金属晶体
原子晶体
离子晶体
分子晶体
活泼金属、非金属
共价键
(空间网状)
共价键
得 失电子
分子间作用力
金属键
(金属阳离子、自由电子)
原子
分子
离子
共用电子对
晶体
稀有气体:单原子分子
非金属原子可构成原子团(复杂离子)
熔、沸点较高
熔、沸点较低
熔、沸点高硬度大
熔、沸点:有的很高、有的较低
C Si B
SiO2 SiC
离子键
(分子间作用力)
晶体类型判断方法:
1、化学键类型
2、元素、微粒种类
3、晶体熔、沸点高低
四种晶体的比较
晶体类型 构成的微粒 微粒间的作用
离子晶体
(NaCl)
原子晶体
(SiO2)
分子晶体
(HCl)
金属晶体
(Cu)
阴、阳离子
原子
分子
金属阳离子、自由电子
离子键
共价键
分子间作用力
金属键
四种晶体的比较
晶体类型
离子晶体
(NaCl)
原子晶体
(SiO2)
分子晶体
(HCl)
金属晶体
(Cu)
一定有离子键,可能有共价键
含有极性键或非极性键
含有共价键或不含任何化学键
金属键
离子键
共价键
分子间作用力
金属键
含化学键情况
熔化需克服的作用
四种晶体的比较
晶体类型
离子晶体
(NaCl)
原子晶体
(SiO2)
分子晶体
(HCl)
金属晶体
(Cu)
不导电
导电
固体导电情况
熔化时导电情况
除半导体外不导电
不导电
导电
除半导体外不导电
不导电
导电
熔、沸点的比较
不同类型:
原子晶体〉离子晶体〉分子晶体
同种类型:
微粒间的作用越强,熔沸点越高
原子晶体:
原子半径越小,共价键越强,
熔沸点越高
离子晶体:
离子电荷数越多,离子半径越小,离子键 越强,熔沸点越高
金属晶体:
金属阳离子电荷数越多,离子半径越小,金属键越强,熔沸点越高
一般而言:
熔、沸点的比较
分子晶体:(一般来说)
A、相对分子质量越大,熔沸点越高
B、相对分子质量相同:
1、分子极性越大,熔沸点越高
如:CO 〉N2
2、支链越多,熔沸点越低
如:正戊烷〉异戊烷〉新戊烷
3、芳香族化合物:邻〉间〉对位化合物
返回主菜单
2、晶体举例:
NaCl的晶体结构:
6:6
常见晶体的微观结构
(1)NaCl晶体
(1)钠离子和氯离子的位置:
(1)钠离子和氯离子位于立方体的顶角上,并交错排列。(2)钠离子:体心和棱中点;氯离子:面心和顶点,或者反之。
(2)每个晶胞含钠离子、氯离子的个数
计算方法:
顶点占1/8;棱占1/4;面心占1/2;体心占1
氯离子: 钠离子:
(3)与Na+等距离且最近的Na+ 、Cl- 各有几个?
与Na+等距离且最近的Na+ 有:12个
与Na+等距离且最近的Cl- 有:6个
CsCl的晶体结构:
8:8
常见晶体的微观结构
(2)CsCl晶体
(1)铯离子和氯离子的位置:
铯离子:体心
氯离子:顶点;或者反之。
(2)每个晶胞含铯离子、氯离子的个数
铯离子:1个 ;氯离子:1个
(3)与铯离子等距离且最近的铯离子、氯离子各有几个?
铯离子:6个 ;氯离子:8个
常见晶体的微观结构
(3)干冰晶体
(1)二氧化碳分子的位置:
二氧化碳分子位于:体心和棱中点(面心和顶点)
(2)每个晶胞含二氧化碳分子的个数
二氧化碳分子的个数: 4 个
(3)与每个二氧化碳分子等距离且最近的二氧化
碳分子有几个?
12个
(4)金刚石(硅)与石墨
晶体 金刚石 石墨
构型
键角、键长
正四面体、空间网状原子晶体
平面正六边形、层状混合晶体
109 o 28′
120 o
键长:金刚石〉石墨
(4)金刚石(硅)与石墨
晶体 金刚石 石墨
最小碳环
C-C 键与C原子的个数比
六元环(不同面)
六元环(同面)
2 :1
3 :2
(4)金刚石(硅)与石墨
晶体 金刚石 石墨
熔点
硬度
金刚石〈 石墨
金刚石〉石墨
硬度的比较
(5)二氧化硅晶体
思考:
1、硅原子与跟它相连的4个氧原子的关系
2、硅原子与它周围4个硅原子的关系
3、Si-O键与Si原子的个数比为多少?
返回主菜单
课堂练习
练习1:下列说法中正确的是( )
A、离子晶体一定含有离子键,分子晶体一定含有共价键
B、NaCl、HCl、SiO2 的晶体中都不存在单个分子
C、HCl 和 乙醇晶体溶于水时克服微粒间作用力的类型相同
D、HCl 和 乙醇晶体熔化时克服微粒间作用力的类型相同
D
返回主菜单
课堂练习
练习2:据报道,科研人员应用电子计算机模拟出类似C60的物质N60, 试推测出该物质不可能具有的性质是( )
A、N60难溶于水
B、稳定性:N60〈 N2
C、熔点: N60 〉N2
D、它属于原子晶体
D
返回主菜单
课堂练习
练习3:下列说法中错误的是( )
A、12克石墨中含有1.5 mol C-C键
B、60克二氧化硅中含有4mol Si-O键
C、氯化钠晶体中,每个氯离子周围等距离且最近的氯离子有12个
D、在石墨晶体中,每个最小环平均含有6个碳原子
D
返回主菜单
课堂练习
返回主菜单
练习4:某晶体的晶胞结构如图,试确定其化学式
A:1/4×4=1 B:1/8 ×8=1 C:1 ×1=1
A、B、C的个数比为:1:1:1
化学式为:ABC
课堂练习
返回主菜单
练习5:晶体硼的基本结构单元是由硼原子组成的正二十面体,其中有20个等边三角形的面和一定数目的顶点,每个顶点各有一个硼原子,则此基本结构单元是由( )个硼原子构成的,其中B-B键的键角为( ),共含有( )个B-B键。
12
60o
30
晶体的熔点
金刚石
食盐
干冰
返回原处
晶体的硬度
金刚石
石 墨
返回原处
同课章节目录
