专题二 第一单元氧化还原反应(浙江省舟山市)
文档属性
| 名称 | 专题二 第一单元氧化还原反应(浙江省舟山市) |

|
|
| 格式 | rar | ||
| 文件大小 | 79.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2007-10-04 00:00:00 | ||
图片预览





文档简介
课件21张PPT。氧化还原反应新课标化学1 第2专题第1单元(四)判断是否氧化还原反应 (特征)有元素化合价升降的化学反应就
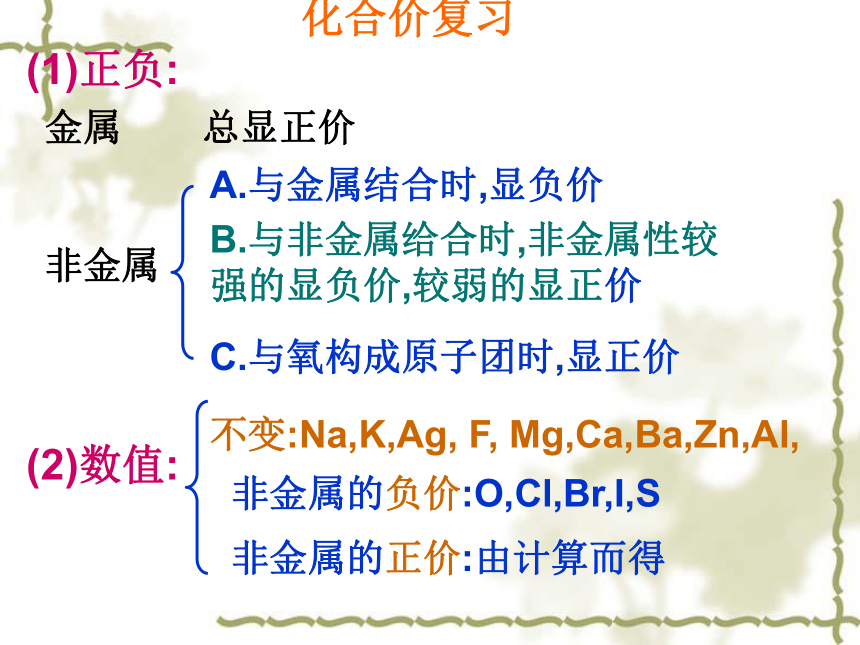
是氧化还原反应。? 化合价复习 (1)正负: (2)数值:总显正价
B.与非金属给合时,非金属性较强的显负价,较弱的显正价
不变:Na,K,Ag, F, Mg,Ca,Ba,Zn,Al,
A.与金属结合时,显负价C.与氧构成原子团时,显正价金属
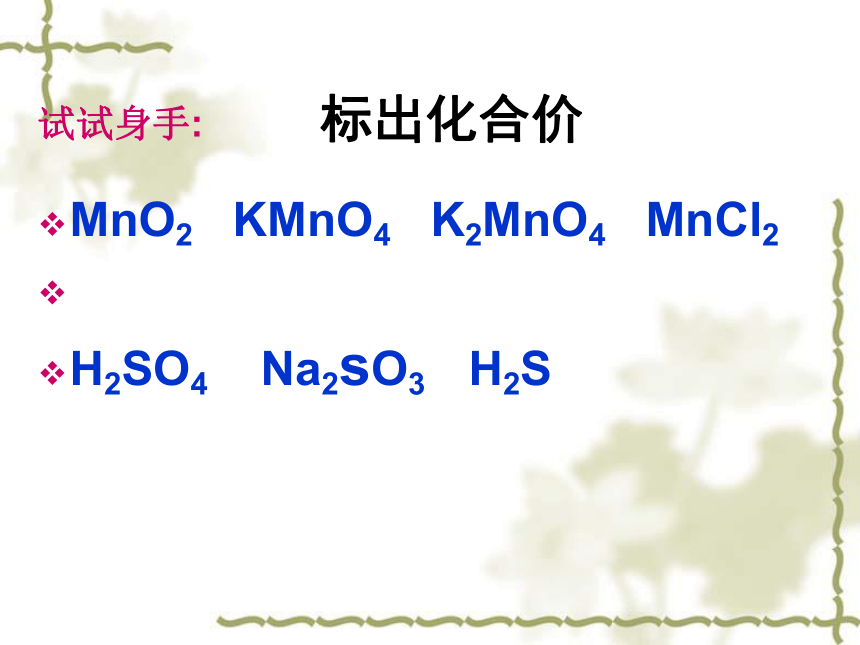
非金属非金属的负价:O,Cl,Br,I,S非金属的正价:由计算而得试试身手: 标出化合价MnO2 KMnO4 K2MnO4 MnCl2
H2SO4 Na2sO3 H2S
① CO2 + C 2CO
② Na2CO3 + CaCl2 = CaCO3↓+ 2NaCl
③ 3NO2+H2O = 2HNO3+NO
④ Cl2 + 2KBr = 2KCl + Br2
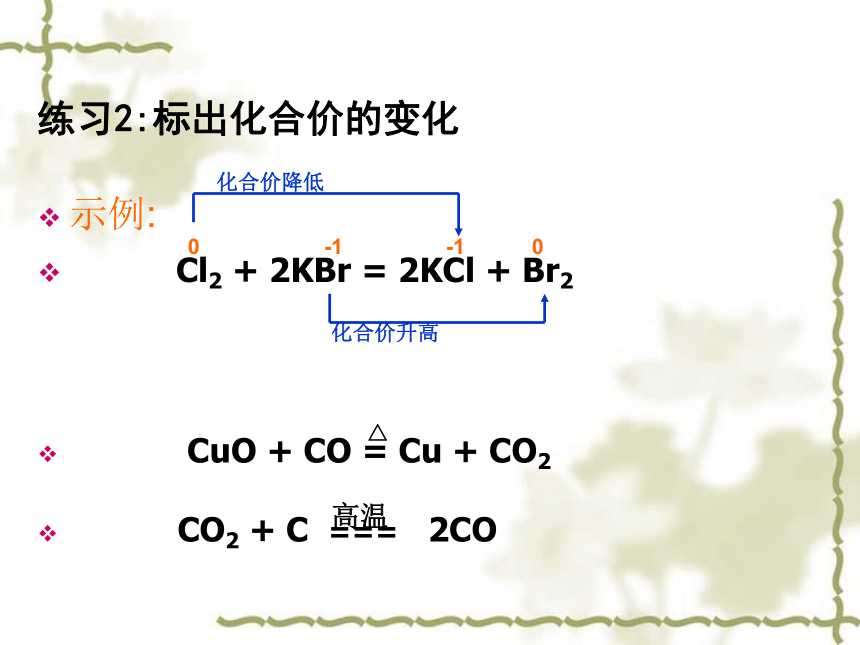
高温练习1:下列反应中属于氧化还原反应的有__ 氧化还原反应:①③④练习2:标出化合价的变化示例:
Cl2 + 2KBr = 2KCl + Br2
CuO + CO = Cu + CO2
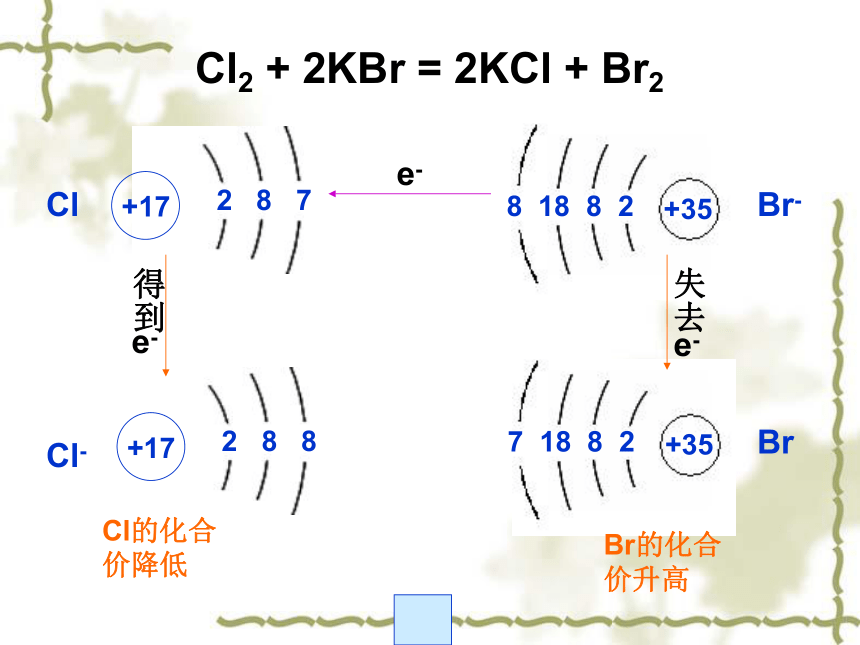
CO2 + C === 2CO0-1-10化合价降低化合价升高△高温化合价为什么会变化呢?为达到电子层的稳定结构,反应中原子间发生了电子的转移。失去电子时,元素化合价升高,得到电子时,元素化合价降低。ClCl-Br-Bre-Cl2 + 2KBr = 2KCl + Br2Cl的化合价降低Br的化合价升高氧化还原反应:有电子转移的化学反 应称为氧化还原反应。 (本质) ?什么是氧化还原反应? 氧化反应:物质失去电子(化合价升高)的变化叫氧化反应还原反应:物质得到电子(化合价降低)的变化叫还原反应ClCl-Br-Bre-Cl2 + 2KBr = 2KCl + Br2还原反应氧化反应Cl2发生还原反应,是氧化剂,KBr发生氧化反应,是还原剂。Cl的化合价降低Br的化合价升高氧化剂、还原剂氧化剂:Cl2,O2等物质在反应中常表现为得电子。反应中得到电子的物质叫氧化剂。氧化剂发生还原反应。
还原剂:Na,Mg,H2等在反应中常表现为失电子。反应中失去电子的物质叫还原剂。还原剂发生氧化反应氧化还原诸概念间的关系化合价升高---失电子---氧化反应---还原剂
化合价降低---得电子---还原反应---氧化剂口诀: 升 , 失 ,氧; ---还原剂
降, 得 , 还。 ---氧化剂
失去电子的物质是 剂,氧化还原氧化 得到电子的物质是 剂,
氧化还原还原反应中其元素化合价 ,发生_________反应(即被 )。反应中其元素化合价 ,发生 ______反应(即被 )。升高降低练习3: 在氧化还原反应中:练习4:指出电子的得失和氧化还原关系示例:
Cl2 + 2KBr = 2KCl + Br2
CuO + CO = Cu + CO2
CO2 + C === 2CO0-1-10化合价降低化合价升高△高温,得到电子,被还原,失去电子,被氧化 Cl2是氧化剂,KBr是还原剂小结 氧化还原反应一、氧化还原反应的特征:
-------------元素化合价有变化
二、氧化还原反应的本质------电子转移
1.氧化剂:得到电子的物质
还原剂:失去电子的物质
2.氧化反应:失去电子的反应
还原反应:得到电子的反应
概念间的联系:还原剂:升,失,被氧;
氧化剂:降 得 被还 ;氧化性还原性强弱的比较 处于最高价态的元素
处于最低价态的元素
处于中间价态的元素——仅有氧化性
——仅有还原性
——两者皆有用双线桥法分析氧化还原反应的步骤一、正确书写化学反应方程式二、标出有变化元素的化合价三、画出双线桥四、在双线桥上标出电子转移的总数Zn + 2HCl = ZnCl2 + H2↑ 0+2+10失去2e-得到2×e-还原剂氧化剂【问题解决】
请指出下列氧化还原反应中化合价发生变化的元素,分析电子转移的方向和数目,并指出氧化剂、还原剂。
(1)Cl2 + 2KBr = 2KCl + Br2
(2)Zn + CuSO4 = ZnSO4 + Cu
(3)MnO2 + 4HCl(浓)= MnCl2 + Cl2↑+ 2H2O
(4)Fe2O3 + 3CO 2Fe + 3CO2
△高温练习5:
水(H2O)在很多化学反应中起极其重要的作用。请研究下列有水参与的氧化还原反应:
① 2Na + 2H2O === 2NaOH + H2↑
② 3NO2 + H2O === 2HNO3 + NO
③ 2H2O === 2H2↑+ O2↑
④ 2F2 + 2H2O === 4HF + O2
(1)水只做氧化剂的是 ,水只做还原剂的是 ,水既做氧化剂又还原剂的是 ,水既不是氧化剂又不是还原剂的是 。
电解① ④③ ②用单线桥法分析氧化还原反应的步骤一、正确书写化学反应方程式Zn + 2HCl = ZnCl2 + H2↑二、标出有变化元素的化合价0+2+10三、画出单线桥四、在单线桥上标出电子转移的总数2e-练习6:
氯的原子结构示意图为 ,氯元素有多种化合价,其最高正价为+7价,最低化合价为 。在微粒Cl2、Cl-、ClO-、ClO3-、ClO4-中,氯元素的化合价依次是 ,从氯元素的化合价分析,上述微粒中有还原性而无氧化性的是 ,有氧化性而无还原性的是 。-1价0价、-1价、+1价、+5价、+7价Cl-ClO4-
是氧化还原反应。? 化合价复习 (1)正负: (2)数值:总显正价
B.与非金属给合时,非金属性较强的显负价,较弱的显正价
不变:Na,K,Ag, F, Mg,Ca,Ba,Zn,Al,
A.与金属结合时,显负价C.与氧构成原子团时,显正价金属
非金属非金属的负价:O,Cl,Br,I,S非金属的正价:由计算而得试试身手: 标出化合价MnO2 KMnO4 K2MnO4 MnCl2
H2SO4 Na2sO3 H2S
① CO2 + C 2CO
② Na2CO3 + CaCl2 = CaCO3↓+ 2NaCl
③ 3NO2+H2O = 2HNO3+NO
④ Cl2 + 2KBr = 2KCl + Br2
高温练习1:下列反应中属于氧化还原反应的有__ 氧化还原反应:①③④练习2:标出化合价的变化示例:
Cl2 + 2KBr = 2KCl + Br2
CuO + CO = Cu + CO2
CO2 + C === 2CO0-1-10化合价降低化合价升高△高温化合价为什么会变化呢?为达到电子层的稳定结构,反应中原子间发生了电子的转移。失去电子时,元素化合价升高,得到电子时,元素化合价降低。ClCl-Br-Bre-Cl2 + 2KBr = 2KCl + Br2Cl的化合价降低Br的化合价升高氧化还原反应:有电子转移的化学反 应称为氧化还原反应。 (本质) ?什么是氧化还原反应? 氧化反应:物质失去电子(化合价升高)的变化叫氧化反应还原反应:物质得到电子(化合价降低)的变化叫还原反应ClCl-Br-Bre-Cl2 + 2KBr = 2KCl + Br2还原反应氧化反应Cl2发生还原反应,是氧化剂,KBr发生氧化反应,是还原剂。Cl的化合价降低Br的化合价升高氧化剂、还原剂氧化剂:Cl2,O2等物质在反应中常表现为得电子。反应中得到电子的物质叫氧化剂。氧化剂发生还原反应。
还原剂:Na,Mg,H2等在反应中常表现为失电子。反应中失去电子的物质叫还原剂。还原剂发生氧化反应氧化还原诸概念间的关系化合价升高---失电子---氧化反应---还原剂
化合价降低---得电子---还原反应---氧化剂口诀: 升 , 失 ,氧; ---还原剂
降, 得 , 还。 ---氧化剂
失去电子的物质是 剂,氧化还原氧化 得到电子的物质是 剂,
氧化还原还原反应中其元素化合价 ,发生_________反应(即被 )。反应中其元素化合价 ,发生 ______反应(即被 )。升高降低练习3: 在氧化还原反应中:练习4:指出电子的得失和氧化还原关系示例:
Cl2 + 2KBr = 2KCl + Br2
CuO + CO = Cu + CO2
CO2 + C === 2CO0-1-10化合价降低化合价升高△高温,得到电子,被还原,失去电子,被氧化 Cl2是氧化剂,KBr是还原剂小结 氧化还原反应一、氧化还原反应的特征:
-------------元素化合价有变化
二、氧化还原反应的本质------电子转移
1.氧化剂:得到电子的物质
还原剂:失去电子的物质
2.氧化反应:失去电子的反应
还原反应:得到电子的反应
概念间的联系:还原剂:升,失,被氧;
氧化剂:降 得 被还 ;氧化性还原性强弱的比较 处于最高价态的元素
处于最低价态的元素
处于中间价态的元素——仅有氧化性
——仅有还原性
——两者皆有用双线桥法分析氧化还原反应的步骤一、正确书写化学反应方程式二、标出有变化元素的化合价三、画出双线桥四、在双线桥上标出电子转移的总数Zn + 2HCl = ZnCl2 + H2↑ 0+2+10失去2e-得到2×e-还原剂氧化剂【问题解决】
请指出下列氧化还原反应中化合价发生变化的元素,分析电子转移的方向和数目,并指出氧化剂、还原剂。
(1)Cl2 + 2KBr = 2KCl + Br2
(2)Zn + CuSO4 = ZnSO4 + Cu
(3)MnO2 + 4HCl(浓)= MnCl2 + Cl2↑+ 2H2O
(4)Fe2O3 + 3CO 2Fe + 3CO2
△高温练习5:
水(H2O)在很多化学反应中起极其重要的作用。请研究下列有水参与的氧化还原反应:
① 2Na + 2H2O === 2NaOH + H2↑
② 3NO2 + H2O === 2HNO3 + NO
③ 2H2O === 2H2↑+ O2↑
④ 2F2 + 2H2O === 4HF + O2
(1)水只做氧化剂的是 ,水只做还原剂的是 ,水既做氧化剂又还原剂的是 ,水既不是氧化剂又不是还原剂的是 。
电解① ④③ ②用单线桥法分析氧化还原反应的步骤一、正确书写化学反应方程式Zn + 2HCl = ZnCl2 + H2↑二、标出有变化元素的化合价0+2+10三、画出单线桥四、在单线桥上标出电子转移的总数2e-练习6:
氯的原子结构示意图为 ,氯元素有多种化合价,其最高正价为+7价,最低化合价为 。在微粒Cl2、Cl-、ClO-、ClO3-、ClO4-中,氯元素的化合价依次是 ,从氯元素的化合价分析,上述微粒中有还原性而无氧化性的是 ,有氧化性而无还原性的是 。-1价0价、-1价、+1价、+5价、+7价Cl-ClO4-
