物质的分离与提纯(包括三课时)
图片预览









文档简介
课件44张PPT。化学实验是研究化学的重要方法。化学实验是学生化学探究的重要途径。 我们在初中化学里也学过一些简单的实验方法,可用于混合物的分离和提纯,请同学们回忆一下,你了解哪些分离、提纯的方法?过滤、结晶、蒸馏等目 录分离与提纯的原则一、 概 念 分离是混合物中的各物质通过物理或化学方法一一分开,获得纯净组分的过程。 提纯是将混合物中的杂质(不需要或有害的物质)通过物理或化学方法除掉而得到所需物质的过程,(其中杂质不必恢复为原来的物质)。
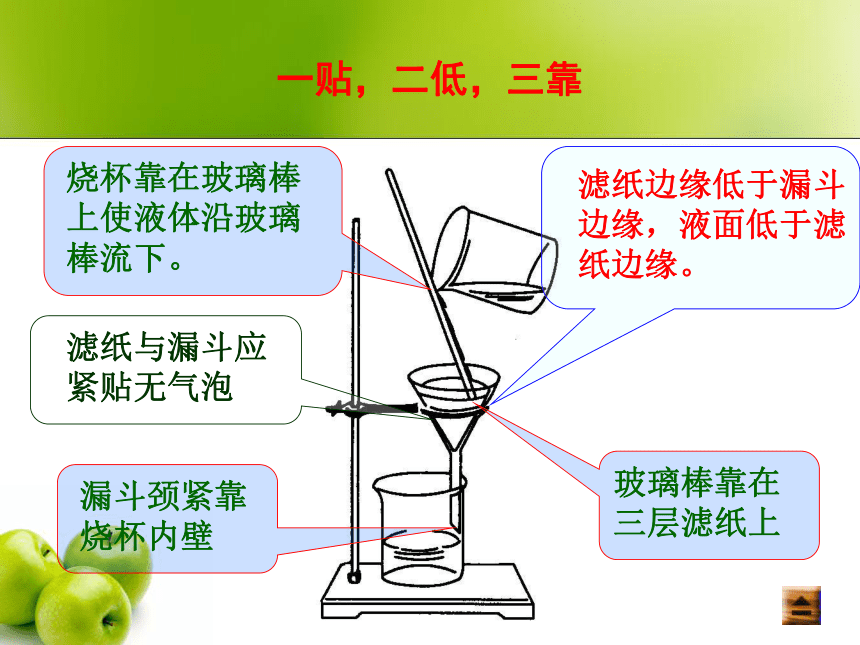
分离和提纯有什么不同? 分离 是通过适当的方法,把混合物中的几种物质分开,每一组分都要保留下来,且如原来是固体,最后还是固体。 提纯 指保留混合物中的某一主要组分,把其余杂质通过一定方法都除去。混合物的性质与分离方法之间有什么关系? 不同的分离方法都有一定的适用范围,因此要根据不同混合物的性质来选择合适的分离方法进行分离。二、 操作原则“四原则”和“三必须”1“四原则”是:2“三必须”是:(1) 除杂试剂必须过量(2) 过量试剂必须除尽(因为过量试剂带入新的杂质)(3) 除杂途径必须选最佳基本实验方法1 原理: 利用物质的溶解性差异,将液体和不溶于液体的固体分离开来的方法。例如用过滤法除去粗盐中的泥沙 。2 实验仪器:3 操作要点:“一贴,二低,三靠”漏斗,滤纸,烧杯,玻璃棒,铁架台(铁圈)过滤一定要洗涤滤纸与漏斗应
紧贴无气泡 滤纸边缘低于漏斗边缘,液面低于滤纸边缘。 玻璃棒靠在
三层滤纸上 漏斗颈紧靠
烧杯内壁 烧杯靠在玻璃棒上使液体沿玻璃棒流下。一贴,二低,三靠二 结晶1 原理: 利用溶剂对被提纯物质及杂质的溶解度不同,可以使被提纯物质从过饱和溶液中析出。而让杂质全部或大部分仍留在溶液中,从而达到提纯的目的。2 实验仪器:蒸发皿,酒精灯,玻璃棒,铁架台(铁圈),烧杯3 结晶方法:蒸发结晶冷却结晶蒸发结晶具体操作: 通过蒸发或气化,减少一部分溶剂使溶液达到饱和而析出晶体。适用物质: 此法主要用于溶解度随温度改变而变化不大的物质。(如氯化钠)蒸发结晶冷却结晶具体操作: 通过降低温度,使溶液冷却达到饱和而析出晶体。重结晶指的是重复冷却结晶。适用物质: 此法主要用于溶解度随温度下降而明显减小的物质。(如硝酸钾)4、操作要点及注意事项:蒸发结晶法:蒸发过程中要不断用玻璃棒搅拌蒸发皿内溶液不能超过其容量的2/3防止局部温度过高而使液体飞溅。当出现大量固体时,应停止加热用余热蒸干。不能把热的蒸发皿直接放在实验台上,应垫上石棉网。冷却结晶法: 若冷却时无晶体的析出,可用玻璃棒在容器内壁摩擦几下,或在溶液中投入几粒该晶体(俗称晶种),就会析出晶体。5 思考:
根据书上图1-11所示,KNO3中混有少量的 KCl,如何提纯KNO3思考:
根据书上图1-11所示,KNO3粉末中混有少量的 KCl,如何提纯KNO3
根据书上图1-11所示,KNO3粉末中混有少量的 KCl,如何提纯KNO3氯化钾和硝酸钾混合物的分离方法1、将两者的混合物置于烧杯中,加少量100摄氏度热水,在加热的情况下不断少量加入热水并搅拌,直至混合物完全溶解
2、停止加热,冷却(可以用冰水水浴),当温度降 至30摄氏度时硝酸钾晶体析出。
3、过滤混合溶液得到较为纯净硝酸钾晶体
4、蒸发滤液,得到较为纯净的氯化钾晶体溶解(除泥沙和Mg(OH)2沉淀)NaOH(稍过量)(使Mg2+沉淀)过滤(除HCl 获得食盐晶体)稀HCl(中和过量的OH-)蒸发现有含少量氯化镁和泥沙等杂质的粗食盐,请设计实验方案,由粗食盐提纯氯化钠。实验探究:溶解过滤(除泥沙等)Na2CO3NaOH(除去过量的Ba2+)(除去SO42-)(除去Mg2+)BaCl2过滤(除沉淀)稀HCl(除去CO32-和OH-)蒸发现有含硫酸钠、氯化镁和泥沙等杂质的粗食
盐,请设计实验方案,由粗食盐提纯氯化钠。实验探究:②Na2SO4+BaCl2 = BaSO4↓+2NaCl③BaCl2 + Na2CO3 = BaCO3↓+2NaCl④MgCl2+ 2NaOH = Mg(OH)2↓+2NaCl⑤Na2CO3+2HCl = H2O+CO2↑+2NaCl
NaOH + HCl = H2O+NaCl有关反应的化学方程式为: 上述加入试剂的先后顺序还可设计为:BaCl2 → NaOH → Na2CO3 → HCl关键是Na2CO3溶液要在BaCl2溶液之后,而稀HCl必须在最后加。思路NaOH → BaCl2 → Na2CO3 → HCl实验方案:(具体实验步骤)1、将粗食盐加水使之溶解。(溶解)2、将步骤(1)所得混合物进行过滤。(过滤)3、向(2)所得滤液加入过量BaCl2溶液到沉淀不再增加为止,静置沉降。(除SO42-)4、向(3)所得的上层清液加入过量Na2CO3溶液,直至沉淀不再生成为止,静置沉降。(除Ba2+)5、向(4)所得上层清液加入过量的NaOH溶液,直至沉淀不再生成,静置沉降。(除Mg2+)6、将(5)所得混合物过滤,往滤液中加入稍过量的稀HCl至不再产生气泡。(除OH-、CO32-)7、将(6)所得溶液加热蒸发。(除HCl)巩固练习:1、为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作:①过滤 ②加过量NaOH ③加盐酸 ④加过量Na2CO3 ⑤加过量BaCl2溶液。正确的操作顺序是( )
A.⑤②④①③ B.④①②⑤③
C.②⑤④①③ D.①④②⑤③ 2、能依次按溶解、过滤、蒸发三个步骤分离方法是( )
A KNO3和HCl B H2O和酒精
C 铁和铜 D 碳酸钙和氯化钠ACD【实验探究】 某些地区的自来水中含有Fe3+,那么如何从含有Fe3+的自来水中获得少量纯净的水(蒸馏水)?蒸馏三 蒸馏1 原理: 利用互溶的液体混合物中各组分的沸点不同,给液体混合物加热,使其中的某一组分变成蒸气再冷凝成液体,从而达到分离提纯的目的。蒸馏一般用于分离沸点相差较大的液体混合物。(例如蒸馏含有Fe3+的水提纯其中水份,蒸馏石油提纯不同沸点的有机组分) 2 实验仪器: 圆底烧瓶,水冷凝管,酒精灯,锥形瓶(接收器),牛角管,温度计,铁架台(铁圈、铁夹),石棉网等 蒸馏烧瓶冷凝管牛角管过程:将液态物质加热至沸点,使之汽化,然后将蒸气重新冷凝为液体的操作过程称为蒸馏。温度计水银球的顶端与支管下沿处于同一水平线蒸馏烧瓶中液体的量是烧瓶容量的1/3~2/3 在圆底烧瓶内放有沸石,防止暴沸冷凝管横放时头高尾
低保证冷凝液自然下
流,冷却水进水通入
与被冷凝蒸气流向相反给圆底烧瓶加热要垫石棉网牛角管圆底烧瓶水冷凝管海水蒸馏原理示意图操作注意:
1、先通水,再加热
2、刚开始收集到的馏分
应该弃去
3、严格控制温度4 思考:(1) 为什么冷却水通入方向与被冷凝蒸气流向相反(2)为什么温度计水银球的顶端要与圆底烧瓶支管下沿处于同一水平线为了使蒸馏出的蒸气与冷却水长时间充分接触,带走尽可能多的热量。对于蒸馏来说,只有精确控制蒸馏的温度才能达到分离提纯的目的,而蒸馏烧瓶支管口的温度正是被蒸馏变为气体某组分的温度,故温度计水银球顶端要与圆底烧瓶支管下沿处于同一水平线。四 萃取和分液1 原理:2 实验仪器:萃取:利用某溶质在互不相溶的溶剂中的溶解度不同, 一种溶剂把溶质从它与另一种溶剂组成的溶液中提取出来,再利用分液的原理和方法将它们分离开来。分液:把两种互不相溶的液体(且密度不同)分开的操作分液漏斗,铁架台(铁圈),烧杯步骤:检漏装液振荡静置分液分液漏斗、
铁架台、
烧杯实验萃取(1)用量筒量取10ml碘的饱和水溶液,倒入分液漏斗,
然后再注入4ml四氯化碳(CCl4),盖好玻璃塞。装液
(2)用右手压住分液漏斗口部,左手握住活塞部分,
分液漏斗转过来用力振荡。振荡
(3)把分液漏斗放在铁架台上,静置。静置
(4)待液体分层后,将分液漏斗上的玻璃塞打开,或使
塞上的凹槽(或小孔)对准漏斗上的小孔,再将分液
漏斗下面的活塞打开,使下层液体漫漫流出。分液
(分液时,下层液体从漏斗管流出,上层液体从上口流)
3 操作要点:萃取:(1)选择的萃取剂,应对被提取物
有较大的溶解能力,而对杂质不溶
或微溶;跟原溶液的溶剂要互不相溶。(2)操作时先检验分液漏斗是否漏液。萃取溶液和萃取剂总量不要超过漏斗容积的1/2。(4)静置后,当液体分成清晰的两层时分液。(3)振荡时,用右手掌压紧盖子,左手用
拇指、食指和中指握住活塞。把漏斗倒转过来振荡,如图。并不时旋开活塞,放出易挥发物质的蒸气。这样反复操作几次,当产生的气体很少时,再剧烈振荡几次,把漏斗放在漏斗架上静置。分液:静置到液体分成清晰的两层时开始分液。先把玻璃盖子取下,以便与大气相通。然后旋开活塞,使下层液体慢慢流入烧杯里,当下层液体恰好流尽时,迅速关上活塞。从漏斗口倒出上层液体。分液漏斗的液体量最多可达分液漏斗容量的3/4。 现 象结 论
3、振荡前:上层是橙色
下层是无色
振荡后: 上层是无色
下层是红棕色溴在CCl4中的溶解度远大于在水中的溶解度。水和CCl4互不相溶2、溴水在上层
CCl4在下层1、 分 层CCl4的密度比水大在两支试管中各加入2~3ml溴水,再向其中的一支试管中滴加1mlCCl4,振荡、静置。【实验探究】实验步骤:在两支试管中各加入2~3ml溴水,再向其中的一支试管中滴加1mlCCl4,振荡、静置。现象:溴水呈橙色,溶液分层,上层几乎无色,下层呈橙红色。实验步骤:在两支试管中各加入2~3ml溴水,再向其中的一支试管中滴加1ml汽油(或苯),振荡、静置。现象:溴水呈橙色,溶液分层,下层几乎无色,上层呈橙红色。一、物质分离和提纯的常用物理方法1、过滤分离固体和液体混合物2、结晶或
重结晶分离溶解度随温度变化差异大的物质3、蒸馏分离沸点不同的互溶的液态混合物4、升华分离某些具有升华特性的固体和受热不分解的固体组成的混合物 小 结5、分液分离互不相溶的液体混合物6、萃取利用一种溶剂把溶质从另一种溶剂中提取出来7、渗析用半透膜分离溶液和胶体一、物质分离和提纯的常用物理方法二、物质分离和提纯的常用化学方法练习与实践现需要分离下列物质,请用直线将分离实例、分离方法和选择分离方法的依据连接起来。 实 例 分离方法 选择的依据
除去氯化钠溶液中的泥沙 蒸馏 溶解度随温度变化的差异
用CCl4提取溴水中溴单质 过滤 在不同溶剂中溶解度的差异
分离醋酸(沸点118℃)与乙醇(沸点78.5℃) 分液 沸点的差异较大
分离汽油和水 结晶 两溶剂互不相溶
从含有氯化钠的硝酸钾溶液中提取硝酸钾 萃取 物质在水中溶解度的不同
分离和提纯有什么不同? 分离 是通过适当的方法,把混合物中的几种物质分开,每一组分都要保留下来,且如原来是固体,最后还是固体。 提纯 指保留混合物中的某一主要组分,把其余杂质通过一定方法都除去。混合物的性质与分离方法之间有什么关系? 不同的分离方法都有一定的适用范围,因此要根据不同混合物的性质来选择合适的分离方法进行分离。二、 操作原则“四原则”和“三必须”1“四原则”是:2“三必须”是:(1) 除杂试剂必须过量(2) 过量试剂必须除尽(因为过量试剂带入新的杂质)(3) 除杂途径必须选最佳基本实验方法1 原理: 利用物质的溶解性差异,将液体和不溶于液体的固体分离开来的方法。例如用过滤法除去粗盐中的泥沙 。2 实验仪器:3 操作要点:“一贴,二低,三靠”漏斗,滤纸,烧杯,玻璃棒,铁架台(铁圈)过滤一定要洗涤滤纸与漏斗应
紧贴无气泡 滤纸边缘低于漏斗边缘,液面低于滤纸边缘。 玻璃棒靠在
三层滤纸上 漏斗颈紧靠
烧杯内壁 烧杯靠在玻璃棒上使液体沿玻璃棒流下。一贴,二低,三靠二 结晶1 原理: 利用溶剂对被提纯物质及杂质的溶解度不同,可以使被提纯物质从过饱和溶液中析出。而让杂质全部或大部分仍留在溶液中,从而达到提纯的目的。2 实验仪器:蒸发皿,酒精灯,玻璃棒,铁架台(铁圈),烧杯3 结晶方法:蒸发结晶冷却结晶蒸发结晶具体操作: 通过蒸发或气化,减少一部分溶剂使溶液达到饱和而析出晶体。适用物质: 此法主要用于溶解度随温度改变而变化不大的物质。(如氯化钠)蒸发结晶冷却结晶具体操作: 通过降低温度,使溶液冷却达到饱和而析出晶体。重结晶指的是重复冷却结晶。适用物质: 此法主要用于溶解度随温度下降而明显减小的物质。(如硝酸钾)4、操作要点及注意事项:蒸发结晶法:蒸发过程中要不断用玻璃棒搅拌蒸发皿内溶液不能超过其容量的2/3防止局部温度过高而使液体飞溅。当出现大量固体时,应停止加热用余热蒸干。不能把热的蒸发皿直接放在实验台上,应垫上石棉网。冷却结晶法: 若冷却时无晶体的析出,可用玻璃棒在容器内壁摩擦几下,或在溶液中投入几粒该晶体(俗称晶种),就会析出晶体。5 思考:
根据书上图1-11所示,KNO3中混有少量的 KCl,如何提纯KNO3思考:
根据书上图1-11所示,KNO3粉末中混有少量的 KCl,如何提纯KNO3
根据书上图1-11所示,KNO3粉末中混有少量的 KCl,如何提纯KNO3氯化钾和硝酸钾混合物的分离方法1、将两者的混合物置于烧杯中,加少量100摄氏度热水,在加热的情况下不断少量加入热水并搅拌,直至混合物完全溶解
2、停止加热,冷却(可以用冰水水浴),当温度降 至30摄氏度时硝酸钾晶体析出。
3、过滤混合溶液得到较为纯净硝酸钾晶体
4、蒸发滤液,得到较为纯净的氯化钾晶体溶解(除泥沙和Mg(OH)2沉淀)NaOH(稍过量)(使Mg2+沉淀)过滤(除HCl 获得食盐晶体)稀HCl(中和过量的OH-)蒸发现有含少量氯化镁和泥沙等杂质的粗食盐,请设计实验方案,由粗食盐提纯氯化钠。实验探究:溶解过滤(除泥沙等)Na2CO3NaOH(除去过量的Ba2+)(除去SO42-)(除去Mg2+)BaCl2过滤(除沉淀)稀HCl(除去CO32-和OH-)蒸发现有含硫酸钠、氯化镁和泥沙等杂质的粗食
盐,请设计实验方案,由粗食盐提纯氯化钠。实验探究:②Na2SO4+BaCl2 = BaSO4↓+2NaCl③BaCl2 + Na2CO3 = BaCO3↓+2NaCl④MgCl2+ 2NaOH = Mg(OH)2↓+2NaCl⑤Na2CO3+2HCl = H2O+CO2↑+2NaCl
NaOH + HCl = H2O+NaCl有关反应的化学方程式为: 上述加入试剂的先后顺序还可设计为:BaCl2 → NaOH → Na2CO3 → HCl关键是Na2CO3溶液要在BaCl2溶液之后,而稀HCl必须在最后加。思路NaOH → BaCl2 → Na2CO3 → HCl实验方案:(具体实验步骤)1、将粗食盐加水使之溶解。(溶解)2、将步骤(1)所得混合物进行过滤。(过滤)3、向(2)所得滤液加入过量BaCl2溶液到沉淀不再增加为止,静置沉降。(除SO42-)4、向(3)所得的上层清液加入过量Na2CO3溶液,直至沉淀不再生成为止,静置沉降。(除Ba2+)5、向(4)所得上层清液加入过量的NaOH溶液,直至沉淀不再生成,静置沉降。(除Mg2+)6、将(5)所得混合物过滤,往滤液中加入稍过量的稀HCl至不再产生气泡。(除OH-、CO32-)7、将(6)所得溶液加热蒸发。(除HCl)巩固练习:1、为了除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作:①过滤 ②加过量NaOH ③加盐酸 ④加过量Na2CO3 ⑤加过量BaCl2溶液。正确的操作顺序是( )
A.⑤②④①③ B.④①②⑤③
C.②⑤④①③ D.①④②⑤③ 2、能依次按溶解、过滤、蒸发三个步骤分离方法是( )
A KNO3和HCl B H2O和酒精
C 铁和铜 D 碳酸钙和氯化钠ACD【实验探究】 某些地区的自来水中含有Fe3+,那么如何从含有Fe3+的自来水中获得少量纯净的水(蒸馏水)?蒸馏三 蒸馏1 原理: 利用互溶的液体混合物中各组分的沸点不同,给液体混合物加热,使其中的某一组分变成蒸气再冷凝成液体,从而达到分离提纯的目的。蒸馏一般用于分离沸点相差较大的液体混合物。(例如蒸馏含有Fe3+的水提纯其中水份,蒸馏石油提纯不同沸点的有机组分) 2 实验仪器: 圆底烧瓶,水冷凝管,酒精灯,锥形瓶(接收器),牛角管,温度计,铁架台(铁圈、铁夹),石棉网等 蒸馏烧瓶冷凝管牛角管过程:将液态物质加热至沸点,使之汽化,然后将蒸气重新冷凝为液体的操作过程称为蒸馏。温度计水银球的顶端与支管下沿处于同一水平线蒸馏烧瓶中液体的量是烧瓶容量的1/3~2/3 在圆底烧瓶内放有沸石,防止暴沸冷凝管横放时头高尾
低保证冷凝液自然下
流,冷却水进水通入
与被冷凝蒸气流向相反给圆底烧瓶加热要垫石棉网牛角管圆底烧瓶水冷凝管海水蒸馏原理示意图操作注意:
1、先通水,再加热
2、刚开始收集到的馏分
应该弃去
3、严格控制温度4 思考:(1) 为什么冷却水通入方向与被冷凝蒸气流向相反(2)为什么温度计水银球的顶端要与圆底烧瓶支管下沿处于同一水平线为了使蒸馏出的蒸气与冷却水长时间充分接触,带走尽可能多的热量。对于蒸馏来说,只有精确控制蒸馏的温度才能达到分离提纯的目的,而蒸馏烧瓶支管口的温度正是被蒸馏变为气体某组分的温度,故温度计水银球顶端要与圆底烧瓶支管下沿处于同一水平线。四 萃取和分液1 原理:2 实验仪器:萃取:利用某溶质在互不相溶的溶剂中的溶解度不同, 一种溶剂把溶质从它与另一种溶剂组成的溶液中提取出来,再利用分液的原理和方法将它们分离开来。分液:把两种互不相溶的液体(且密度不同)分开的操作分液漏斗,铁架台(铁圈),烧杯步骤:检漏装液振荡静置分液分液漏斗、
铁架台、
烧杯实验萃取(1)用量筒量取10ml碘的饱和水溶液,倒入分液漏斗,
然后再注入4ml四氯化碳(CCl4),盖好玻璃塞。装液
(2)用右手压住分液漏斗口部,左手握住活塞部分,
分液漏斗转过来用力振荡。振荡
(3)把分液漏斗放在铁架台上,静置。静置
(4)待液体分层后,将分液漏斗上的玻璃塞打开,或使
塞上的凹槽(或小孔)对准漏斗上的小孔,再将分液
漏斗下面的活塞打开,使下层液体漫漫流出。分液
(分液时,下层液体从漏斗管流出,上层液体从上口流)
3 操作要点:萃取:(1)选择的萃取剂,应对被提取物
有较大的溶解能力,而对杂质不溶
或微溶;跟原溶液的溶剂要互不相溶。(2)操作时先检验分液漏斗是否漏液。萃取溶液和萃取剂总量不要超过漏斗容积的1/2。(4)静置后,当液体分成清晰的两层时分液。(3)振荡时,用右手掌压紧盖子,左手用
拇指、食指和中指握住活塞。把漏斗倒转过来振荡,如图。并不时旋开活塞,放出易挥发物质的蒸气。这样反复操作几次,当产生的气体很少时,再剧烈振荡几次,把漏斗放在漏斗架上静置。分液:静置到液体分成清晰的两层时开始分液。先把玻璃盖子取下,以便与大气相通。然后旋开活塞,使下层液体慢慢流入烧杯里,当下层液体恰好流尽时,迅速关上活塞。从漏斗口倒出上层液体。分液漏斗的液体量最多可达分液漏斗容量的3/4。 现 象结 论
3、振荡前:上层是橙色
下层是无色
振荡后: 上层是无色
下层是红棕色溴在CCl4中的溶解度远大于在水中的溶解度。水和CCl4互不相溶2、溴水在上层
CCl4在下层1、 分 层CCl4的密度比水大在两支试管中各加入2~3ml溴水,再向其中的一支试管中滴加1mlCCl4,振荡、静置。【实验探究】实验步骤:在两支试管中各加入2~3ml溴水,再向其中的一支试管中滴加1mlCCl4,振荡、静置。现象:溴水呈橙色,溶液分层,上层几乎无色,下层呈橙红色。实验步骤:在两支试管中各加入2~3ml溴水,再向其中的一支试管中滴加1ml汽油(或苯),振荡、静置。现象:溴水呈橙色,溶液分层,下层几乎无色,上层呈橙红色。一、物质分离和提纯的常用物理方法1、过滤分离固体和液体混合物2、结晶或
重结晶分离溶解度随温度变化差异大的物质3、蒸馏分离沸点不同的互溶的液态混合物4、升华分离某些具有升华特性的固体和受热不分解的固体组成的混合物 小 结5、分液分离互不相溶的液体混合物6、萃取利用一种溶剂把溶质从另一种溶剂中提取出来7、渗析用半透膜分离溶液和胶体一、物质分离和提纯的常用物理方法二、物质分离和提纯的常用化学方法练习与实践现需要分离下列物质,请用直线将分离实例、分离方法和选择分离方法的依据连接起来。 实 例 分离方法 选择的依据
除去氯化钠溶液中的泥沙 蒸馏 溶解度随温度变化的差异
用CCl4提取溴水中溴单质 过滤 在不同溶剂中溶解度的差异
分离醋酸(沸点118℃)与乙醇(沸点78.5℃) 分液 沸点的差异较大
分离汽油和水 结晶 两溶剂互不相溶
从含有氯化钠的硝酸钾溶液中提取硝酸钾 萃取 物质在水中溶解度的不同
