第一单元 含硫化合物的性质和应用二氧化硫性质和作用
文档属性
| 名称 | 第一单元 含硫化合物的性质和应用二氧化硫性质和作用 |

|
|
| 格式 | rar | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2007-11-03 00:00:00 | ||
图片预览







文档简介
课件28张PPT。专题4 硫、氮和可持续发展第一单元 含硫化合物的性质和应用二氧化硫的性质和作用一、物理性质 状态:
颜色:
气味:
毒性:
密度:
溶解度: 气体无色刺激性有毒比空气大易溶于水,常温、常压下,1体积水溶解40体积SO2第二节 二氧化硫一、二氧化硫的性质
(一)、物理性质
无色,有刺激性气味的有毒气体,密度比空气大,易液化(沸点是-10 oC),易溶于水(常温常压下一体积水能溶解40个体积的二氧化硫).
答: 实验室制SO2应注意防止空气污染!用向上排空气法收集,不能用排水法收集。【思考】
1、 实验室制SO2 气体,应注意什么?该如何收集? SO2有哪些化学性质?提示:
1、从物质分类角度
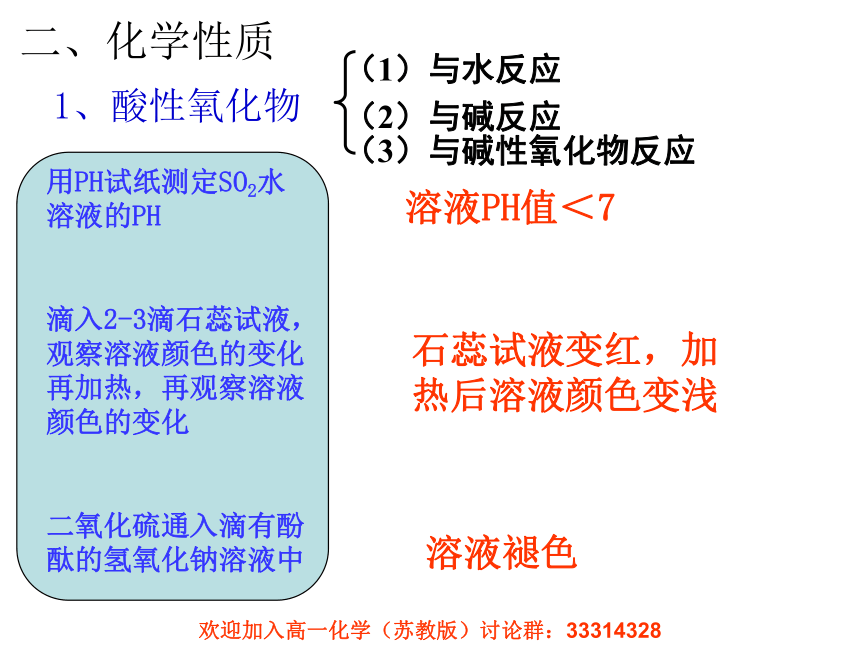
2、从氧化还原角度二、化学性质1、酸性氧化物用PH试纸测定SO2水溶液的PH
滴入2-3滴石蕊试液,观察溶液颜色的变化再加热,再观察溶液颜色的变化
二氧化硫通入滴有酚酞的氢氧化钠溶液中溶液PH值<7石蕊试液变红,加热后溶液颜色变浅溶液褪色*亚硫酸是一种不稳定的弱酸,但它的酸性比碳酸强:
(二):化学性质
1:具有酸性氧化物的通性
(1)、与H2O反应: SO2+H2O H2SO3(亚硫酸) (2)、与碱反应
SO2+2NaOH=Na2SO3+H2O (碱过量)
SO2+NaOH=NaHSO3 (碱少量)
(3)、与碱性氧化物反应:
SO2+Na2O=Na2SO3 SO2 +CaO==CaSO3
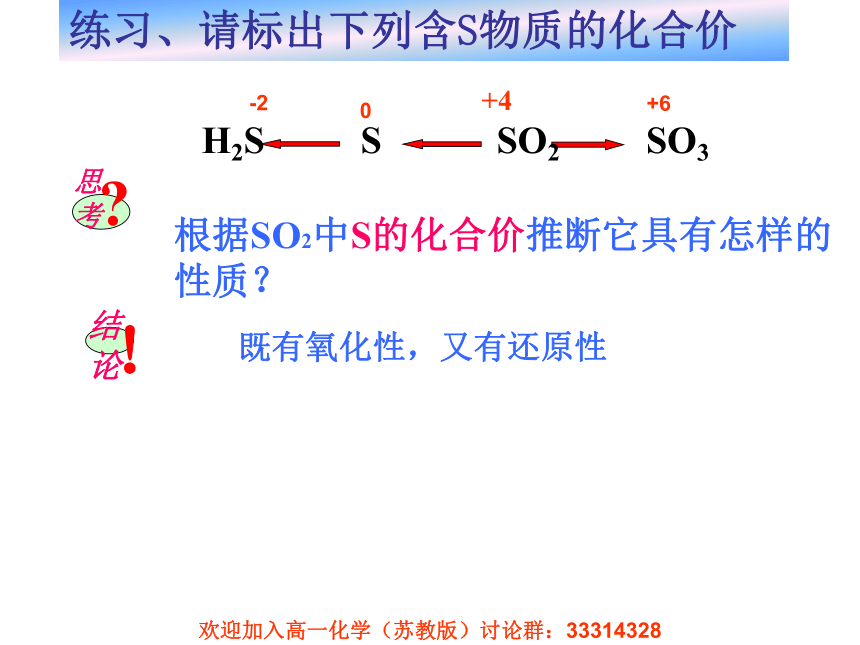
实验室制取SO2,可选择碱液吸收尾气,防止空气污 染。+4根据SO2中S的化合价推断它具有怎样的性质?既有氧化性,又有还原性练习、请标出下列含S物质的化合价-20+6H2S S SO2 SO3现象:结论:反应:滴加BaCl2没有明显现象
滴加H2O2有白色沉淀生成
加盐酸后白色沉淀不消失 H2SO3容易被H2O2氧化生成硫酸SO2+ H2O2 = H2SO4
H2SO4 + BaCl2 =BaSO4 +2HCl 实 验:
向一支试管中加入5ml SO2水溶液,滴加BaCl2溶液,再滴加0.5ml3%的H2O2溶液,振荡放置片刻后滴加稀盐酸观察实验现象。2 . SO2较强的还原性3. SO2的氧化性SO2+2H2S = 3S + 2H2O4. SO2的漂白性 实 验
向试管中加入5ml SO2水溶液,滴加品红溶液,振荡,然后加热试管,比较前后溶液颜色的变化。
现象:品红溶液褪色,
加热后溶液变回红色漂白机理:SO2 与某些有色物质化合生成无色 物质,但是这些无色物质不稳定,容易分解而恢复原来的颜色 。注意:SO2能使品红褪色,是SO2的特征反应,
常被用来鉴别SO2。
SO2也具有的特殊化学性质:漂白性
它能与有色色素结合成不稳定的
无色物质而具有漂白性.
它可以用来漂白纸浆、毛、丝、
草编制品等。二、化学性质4、漂白性SO2通入品红溶液,然后加热品红褪色,加热后又变红注意:SO2能使品红褪色,是SO2的特征反应,常被用来鉴别SO2。思考一下 为什么长时间放置的
报纸和草帽会变黄?漂白剂的种类吸附性漂白:活性炭;
2. 氧化性漂白:HClO、O3、H2O2等;
3. 非氧化性漂白:SO2特点:化合反应,可逆,漂白不稳定。特点:物理变化特点:氧化还原反应,不可逆,漂白稳定。 三、二氧化硫的污染 空气中的二氧化硫主要来自于化石燃料(如煤与石油)的燃烧、含硫金属的冶炼以及制造硫酸、磷肥等产生的废气。酸雨的形成石油 煤 酸雨燃 烧CO2 SO2 SO3 雨水.霜.雹.露等三、酸雨的形成及防治SO3 + H2O = H2SO42H2SO3 + O2 = 2H2SO4硫酸型酸雨的形成酸雨的危害实例录:
1.50年前,故宫太和殿台阶的栏杆上雕刻着各式各样精美浮雕花纹还清晰可见,而现在却大多是模糊不清,部分已成光板……如何控制酸雨?1、改善燃料种类,积极开发新能源;
2、对煤(其中含硫为0.3%-5%)进行处理,如
选洗加工、综合开发、在煤中加入适量的生
石灰、对排放的烟进行处理以回收SO2.
3、种植能够吸收SO2的有关树木(如臭椿、
垂柳、柳杉)等;总结SO2与H2O反应与碱反应氧化性还原性重视环境保护,防止酸雨危害环境!与碱性氧化物思考1、试比较SO2与CO2的性质有哪些相似性的和不同点?2、如何鉴别SO2与CO2?3、如何鉴别一混合气体是SO2与CO2的混合气体?课堂习题下列可以用来鉴别SO2 和CO2 的方法是[ ]
A、通入紫色石蕊试液 B、闻气味
C、通入澄清石灰水 D、通入品红溶液中
都是酸性氧化物,都可以使石蕊变红SO2有刺激性气味,而CO2没有都可以使澄清石灰水变浑浊SO2可使品红褪色,而CO2不能 B D小结 SO21、物理性质2、化学性质酸性氧化物的通性还原性氧化性漂白性 *SO2的污染三、酸雨的形成及防治氨水法石灰石-石膏法1、下列关于SO2的说法中错误的是( )
A.SO2是一种无色,有刺激性气味的有
毒气体
B.SO2能使紫色的石蕊变红色
C.SO2是硫酸的酸酐,称为硫酐
D.SO2能与CaO反应生成CaSO3C2、下列物质做干燥剂可干燥SO2的是( )
A.生石灰 B.NaOH固体
C.碱石灰 D.浓硫酸D3、 二氧化硫和氯气都有漂白性,现把二者以等物质的量混合,让混合气体通入品红溶液,则其漂白性将 ( )
A 、和氯气单独通过时相同
B、和二氧化硫单独通过时相同
C、是二者作用效果之和
D、失去漂白性D
颜色:
气味:
毒性:
密度:
溶解度: 气体无色刺激性有毒比空气大易溶于水,常温、常压下,1体积水溶解40体积SO2第二节 二氧化硫一、二氧化硫的性质
(一)、物理性质
无色,有刺激性气味的有毒气体,密度比空气大,易液化(沸点是-10 oC),易溶于水(常温常压下一体积水能溶解40个体积的二氧化硫).
答: 实验室制SO2应注意防止空气污染!用向上排空气法收集,不能用排水法收集。【思考】
1、 实验室制SO2 气体,应注意什么?该如何收集? SO2有哪些化学性质?提示:
1、从物质分类角度
2、从氧化还原角度二、化学性质1、酸性氧化物用PH试纸测定SO2水溶液的PH
滴入2-3滴石蕊试液,观察溶液颜色的变化再加热,再观察溶液颜色的变化
二氧化硫通入滴有酚酞的氢氧化钠溶液中溶液PH值<7石蕊试液变红,加热后溶液颜色变浅溶液褪色*亚硫酸是一种不稳定的弱酸,但它的酸性比碳酸强:
(二):化学性质
1:具有酸性氧化物的通性
(1)、与H2O反应: SO2+H2O H2SO3(亚硫酸) (2)、与碱反应
SO2+2NaOH=Na2SO3+H2O (碱过量)
SO2+NaOH=NaHSO3 (碱少量)
(3)、与碱性氧化物反应:
SO2+Na2O=Na2SO3 SO2 +CaO==CaSO3
实验室制取SO2,可选择碱液吸收尾气,防止空气污 染。+4根据SO2中S的化合价推断它具有怎样的性质?既有氧化性,又有还原性练习、请标出下列含S物质的化合价-20+6H2S S SO2 SO3现象:结论:反应:滴加BaCl2没有明显现象
滴加H2O2有白色沉淀生成
加盐酸后白色沉淀不消失 H2SO3容易被H2O2氧化生成硫酸SO2+ H2O2 = H2SO4
H2SO4 + BaCl2 =BaSO4 +2HCl 实 验:
向一支试管中加入5ml SO2水溶液,滴加BaCl2溶液,再滴加0.5ml3%的H2O2溶液,振荡放置片刻后滴加稀盐酸观察实验现象。2 . SO2较强的还原性3. SO2的氧化性SO2+2H2S = 3S + 2H2O4. SO2的漂白性 实 验
向试管中加入5ml SO2水溶液,滴加品红溶液,振荡,然后加热试管,比较前后溶液颜色的变化。
现象:品红溶液褪色,
加热后溶液变回红色漂白机理:SO2 与某些有色物质化合生成无色 物质,但是这些无色物质不稳定,容易分解而恢复原来的颜色 。注意:SO2能使品红褪色,是SO2的特征反应,
常被用来鉴别SO2。
SO2也具有的特殊化学性质:漂白性
它能与有色色素结合成不稳定的
无色物质而具有漂白性.
它可以用来漂白纸浆、毛、丝、
草编制品等。二、化学性质4、漂白性SO2通入品红溶液,然后加热品红褪色,加热后又变红注意:SO2能使品红褪色,是SO2的特征反应,常被用来鉴别SO2。思考一下 为什么长时间放置的
报纸和草帽会变黄?漂白剂的种类吸附性漂白:活性炭;
2. 氧化性漂白:HClO、O3、H2O2等;
3. 非氧化性漂白:SO2特点:化合反应,可逆,漂白不稳定。特点:物理变化特点:氧化还原反应,不可逆,漂白稳定。 三、二氧化硫的污染 空气中的二氧化硫主要来自于化石燃料(如煤与石油)的燃烧、含硫金属的冶炼以及制造硫酸、磷肥等产生的废气。酸雨的形成石油 煤 酸雨燃 烧CO2 SO2 SO3 雨水.霜.雹.露等三、酸雨的形成及防治SO3 + H2O = H2SO42H2SO3 + O2 = 2H2SO4硫酸型酸雨的形成酸雨的危害实例录:
1.50年前,故宫太和殿台阶的栏杆上雕刻着各式各样精美浮雕花纹还清晰可见,而现在却大多是模糊不清,部分已成光板……如何控制酸雨?1、改善燃料种类,积极开发新能源;
2、对煤(其中含硫为0.3%-5%)进行处理,如
选洗加工、综合开发、在煤中加入适量的生
石灰、对排放的烟进行处理以回收SO2.
3、种植能够吸收SO2的有关树木(如臭椿、
垂柳、柳杉)等;总结SO2与H2O反应与碱反应氧化性还原性重视环境保护,防止酸雨危害环境!与碱性氧化物思考1、试比较SO2与CO2的性质有哪些相似性的和不同点?2、如何鉴别SO2与CO2?3、如何鉴别一混合气体是SO2与CO2的混合气体?课堂习题下列可以用来鉴别SO2 和CO2 的方法是[ ]
A、通入紫色石蕊试液 B、闻气味
C、通入澄清石灰水 D、通入品红溶液中
都是酸性氧化物,都可以使石蕊变红SO2有刺激性气味,而CO2没有都可以使澄清石灰水变浑浊SO2可使品红褪色,而CO2不能 B D小结 SO21、物理性质2、化学性质酸性氧化物的通性还原性氧化性漂白性 *SO2的污染三、酸雨的形成及防治氨水法石灰石-石膏法1、下列关于SO2的说法中错误的是( )
A.SO2是一种无色,有刺激性气味的有
毒气体
B.SO2能使紫色的石蕊变红色
C.SO2是硫酸的酸酐,称为硫酐
D.SO2能与CaO反应生成CaSO3C2、下列物质做干燥剂可干燥SO2的是( )
A.生石灰 B.NaOH固体
C.碱石灰 D.浓硫酸D3、 二氧化硫和氯气都有漂白性,现把二者以等物质的量混合,让混合气体通入品红溶液,则其漂白性将 ( )
A 、和氯气单独通过时相同
B、和二氧化硫单独通过时相同
C、是二者作用效果之和
D、失去漂白性D
