第二节 氯气的性质 第2课时(浙江省绍兴市)
文档属性
| 名称 | 第二节 氯气的性质 第2课时(浙江省绍兴市) |

|
|
| 格式 | rar | ||
| 文件大小 | 309.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2007-11-03 00:00:00 | ||
图片预览








文档简介
课件21张PPT。复习:氯气的化学性质:1.与金属反应(铁和铜) (变价金属,生成高价)
氯气与非金属的反应(H2和磷)
3.氯气与水的反应
氯气与碱的反应氯气跟碱的反应 氯气与碱溶液反应生成次氯酸盐、金属氯化物和水
CaCl2和Ca(ClO)2Ca(ClO)2Cl2+2NaOH==NaCl+NaClO+H2O 试写出氯气与氢氧化钙溶液反应的化学方程式?
(漂白粉的制取原理) 漂白粉的主要成分? 漂白粉的有效成分?Ca(ClO) 2+H2O+CO2==CaCO3 +2HClO
漂白粉的失效原理:Ca(ClO) 2+H2O+CO2==CaCO3 +2HClO漂白粉的漂白原理:
2HClO==2HCl+O2
光照Ca(ClO) 2+2HCl==CaCl2+2HClO氯气与水的反应Cl2+H2O可逆反应次氯酸的氧化性很强,能杀死水中的细菌,也能使染料等有机色素褪色,在光照下易分解放出氧气。
Cl2通入水制得的溶液称为氯水。HCl+HClO次氯酸探究a 新制氯水中含有哪些微粒?b 如何证明这些微粒的存在?
a 新制氯水成分探究实验2实验3结 论氯水既有酸性又有漂白性,盐酸显酸性,没有漂白性(HClO)实验1实验现象:次氯酸有漂白性(HClO)氯水中含有氯气,可以将I2置换出来氯水中含有Cl-实验4有白色沉淀生成
湿润的淀粉KI试纸变蓝
品红褪色滴氯水的pH试纸先变红后变白,滴盐酸的pH试纸显红色氯水成分次氯酸(HClO)氯气(Cl2)盐酸(HCl)水(H2O)Cl-H+ClO-离子:分子:H2OCl2HClO氯水中含有哪些微粒?思考少量OH-综合上述4个实验你能得出什么结论?
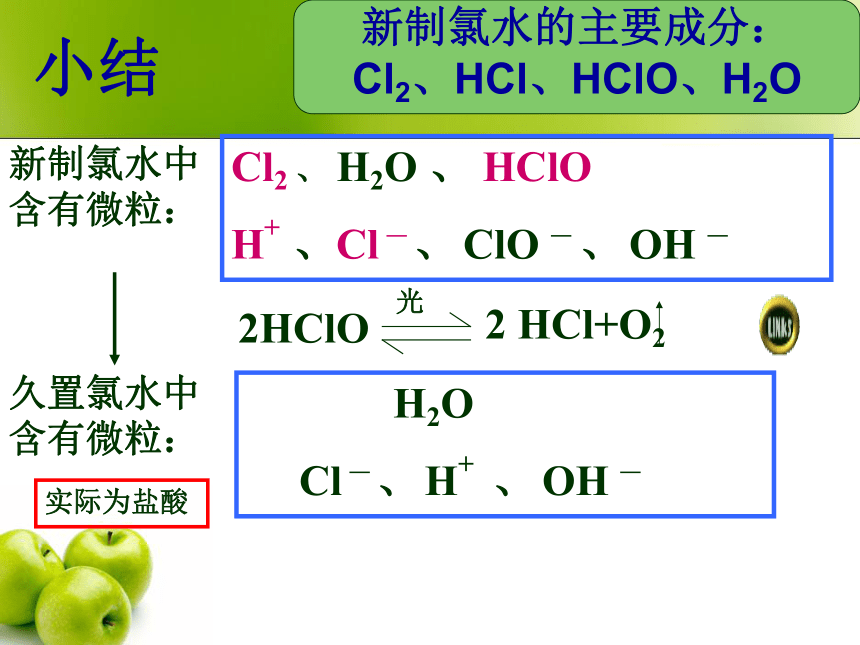
新制氯水中
含有微粒:久置氯水中
含有微粒:Cl2 、 H2O 、 HClO
H+ 、Cl ― 、 ClO ― 、 OH ― H2O
Cl ― 、 H+ 、 OH ―实际为盐酸新制氯水的主要成分:
Cl2、HCl、HClO、H2O小结氯离子的检验用硝酸酸化的AgNO3溶液如出现白色沉淀,则说明有氯离子NaCl+AgNO3==NaNO3+AgCl↓(白色)
氯气的用途 氯气是一种重要的化工原料(聚氯乙烯、染料):在生产和生活中应用十分广泛。自来水的消毒、农药的生产、药物的合成、冶金等都需要用到氯气。
二氧化氯 二氧化氯(ClO2)是一种有刺激性气味的
黄绿色气体,沸点11℃,易溶于水,在水
中不分解。它在水中的杀菌、消毒能力强、
持效长,受水体PH变化的影响小。
二氧化氯的应用十分广泛,除用于一般
的杀菌、消毒外,还广泛地用于环保、灭
藻、漂白、保鲜、除臭等方面。二氧化氯
现已被世界卫生组织(WHO)列为A1级
高效安全灭菌消毒剂。知识拓展总 结1 氯气是一种黄绿色,有刺激性气味的有毒气体;密度比空气大;能溶于水,1体积水能溶2体积氯气;氯气易液化。2 氯气的化学性质极为活泼,氯气可以和绝大多 数的金属反应,也可以和许多非金属反应,还能和水,碱等化合物发生反应.3 新制氯水成分HClO 、HCl、 H2O 、 Cl24 久制氯水成分稀盐酸练 习 由于氯气与水反应生成次氯酸,而次氯酸见光易分解,Cl2 HClO HCl 这个过程不断进行,使氯水中的氯气,以及次氯酸最终全转化为HCl,所以在阳光下久置后的氯水的主要成分应是HCl。1 若一瓶氯水在阳光下放置很久,那么此时氯水的成分是什么?与新制氯水有何区别?2 用滴管往盛有少量新制氯水的试管中慢慢滴加石蕊试液,请推测将看到的实验现象。 由于氯水中含有氢离子,所以石蕊试液会先变红,然后由于次氯酸的漂白作用,又会使石蕊试液褪色。
3.下列有关氯的说法正确的是 ( )
A.液氯与氯水是同一种物质
B.标况下氯气的密度是3.17g/L
C.液氯是非电解质,氯水导电是电解质
D.氯水应保存在棕色的广口瓶中 B 4.氰气的化学式为(CN)2,其性质和
卤素相似,称为“类卤素”。以下关于
(CN)2的叙述中不正确的是 ( )
A (CN)2化学性质活泼
B (CN)2不能和氢氧化钠反应
C (CN)2参加反应时常做氧化剂
D (CN)2可以和H2反应
B5.用氯气消毒的自来水配制下列溶液时,会使配制的溶液变质的是( )
①NaOH ②AgNO3 ③Na2CO3 ④FeCl2
A、只有② ③ B、只有① ④
C、只有① ② ④ D、全部
D实验现象:滴上氯水的pH试纸中间 变白,外围变红。(开始变红,后来变白)
滴上盐酸的pH试纸显红色
结论:氯水既有酸性又有漂白性 分别用滴管吸取少量新制氯水和稀盐酸,滴在pH试纸上,将pH试纸放置片刻,比较放置前后试纸颜色的变化。
实验1实验现象:品红褪色 在洁净的试管中加入2mL新制氯水,再向试管中滴加2滴品红溶液,观察现象。实验2结论:氯水有漂白性(HClO)次氯酸的性质:1.强氧化性2.弱酸性3.不稳定性杀菌、消毒、漂白实验现象:产生白色沉淀结论:氯水中含有Cl- 在洁净的试管中加入2mL新制氯水,再向试管中加入几滴硝酸银溶液和几滴稀硝酸,观察现象。实验3方法(1):观察新制氯水的颜色
实验4实验现象:氯水显淡黄绿色,且有刺激性气味.
结论: 氯水中含有Cl2氯水中Cl2分子的检验方法方法(2):在洁净的试管中加入2mLKI溶液,滴加新制氯水,再加少量CCl4,振荡,观察实验现象。
实验现象:下层有紫红色物质出现方法(3):使淀粉碘化钾试纸变蓝2KI+Cl2=2KCl+I2
氯气与非金属的反应(H2和磷)
3.氯气与水的反应
氯气与碱的反应氯气跟碱的反应 氯气与碱溶液反应生成次氯酸盐、金属氯化物和水
CaCl2和Ca(ClO)2Ca(ClO)2Cl2+2NaOH==NaCl+NaClO+H2O 试写出氯气与氢氧化钙溶液反应的化学方程式?
(漂白粉的制取原理) 漂白粉的主要成分? 漂白粉的有效成分?Ca(ClO) 2+H2O+CO2==CaCO3 +2HClO
漂白粉的失效原理:Ca(ClO) 2+H2O+CO2==CaCO3 +2HClO漂白粉的漂白原理:
2HClO==2HCl+O2
光照Ca(ClO) 2+2HCl==CaCl2+2HClO氯气与水的反应Cl2+H2O可逆反应次氯酸的氧化性很强,能杀死水中的细菌,也能使染料等有机色素褪色,在光照下易分解放出氧气。
Cl2通入水制得的溶液称为氯水。HCl+HClO次氯酸探究a 新制氯水中含有哪些微粒?b 如何证明这些微粒的存在?
a 新制氯水成分探究实验2实验3结 论氯水既有酸性又有漂白性,盐酸显酸性,没有漂白性(HClO)实验1实验现象:次氯酸有漂白性(HClO)氯水中含有氯气,可以将I2置换出来氯水中含有Cl-实验4有白色沉淀生成
湿润的淀粉KI试纸变蓝
品红褪色滴氯水的pH试纸先变红后变白,滴盐酸的pH试纸显红色氯水成分次氯酸(HClO)氯气(Cl2)盐酸(HCl)水(H2O)Cl-H+ClO-离子:分子:H2OCl2HClO氯水中含有哪些微粒?思考少量OH-综合上述4个实验你能得出什么结论?
新制氯水中
含有微粒:久置氯水中
含有微粒:Cl2 、 H2O 、 HClO
H+ 、Cl ― 、 ClO ― 、 OH ― H2O
Cl ― 、 H+ 、 OH ―实际为盐酸新制氯水的主要成分:
Cl2、HCl、HClO、H2O小结氯离子的检验用硝酸酸化的AgNO3溶液如出现白色沉淀,则说明有氯离子NaCl+AgNO3==NaNO3+AgCl↓(白色)
氯气的用途 氯气是一种重要的化工原料(聚氯乙烯、染料):在生产和生活中应用十分广泛。自来水的消毒、农药的生产、药物的合成、冶金等都需要用到氯气。
二氧化氯 二氧化氯(ClO2)是一种有刺激性气味的
黄绿色气体,沸点11℃,易溶于水,在水
中不分解。它在水中的杀菌、消毒能力强、
持效长,受水体PH变化的影响小。
二氧化氯的应用十分广泛,除用于一般
的杀菌、消毒外,还广泛地用于环保、灭
藻、漂白、保鲜、除臭等方面。二氧化氯
现已被世界卫生组织(WHO)列为A1级
高效安全灭菌消毒剂。知识拓展总 结1 氯气是一种黄绿色,有刺激性气味的有毒气体;密度比空气大;能溶于水,1体积水能溶2体积氯气;氯气易液化。2 氯气的化学性质极为活泼,氯气可以和绝大多 数的金属反应,也可以和许多非金属反应,还能和水,碱等化合物发生反应.3 新制氯水成分HClO 、HCl、 H2O 、 Cl24 久制氯水成分稀盐酸练 习 由于氯气与水反应生成次氯酸,而次氯酸见光易分解,Cl2 HClO HCl 这个过程不断进行,使氯水中的氯气,以及次氯酸最终全转化为HCl,所以在阳光下久置后的氯水的主要成分应是HCl。1 若一瓶氯水在阳光下放置很久,那么此时氯水的成分是什么?与新制氯水有何区别?2 用滴管往盛有少量新制氯水的试管中慢慢滴加石蕊试液,请推测将看到的实验现象。 由于氯水中含有氢离子,所以石蕊试液会先变红,然后由于次氯酸的漂白作用,又会使石蕊试液褪色。
3.下列有关氯的说法正确的是 ( )
A.液氯与氯水是同一种物质
B.标况下氯气的密度是3.17g/L
C.液氯是非电解质,氯水导电是电解质
D.氯水应保存在棕色的广口瓶中 B 4.氰气的化学式为(CN)2,其性质和
卤素相似,称为“类卤素”。以下关于
(CN)2的叙述中不正确的是 ( )
A (CN)2化学性质活泼
B (CN)2不能和氢氧化钠反应
C (CN)2参加反应时常做氧化剂
D (CN)2可以和H2反应
B5.用氯气消毒的自来水配制下列溶液时,会使配制的溶液变质的是( )
①NaOH ②AgNO3 ③Na2CO3 ④FeCl2
A、只有② ③ B、只有① ④
C、只有① ② ④ D、全部
D实验现象:滴上氯水的pH试纸中间 变白,外围变红。(开始变红,后来变白)
滴上盐酸的pH试纸显红色
结论:氯水既有酸性又有漂白性 分别用滴管吸取少量新制氯水和稀盐酸,滴在pH试纸上,将pH试纸放置片刻,比较放置前后试纸颜色的变化。
实验1实验现象:品红褪色 在洁净的试管中加入2mL新制氯水,再向试管中滴加2滴品红溶液,观察现象。实验2结论:氯水有漂白性(HClO)次氯酸的性质:1.强氧化性2.弱酸性3.不稳定性杀菌、消毒、漂白实验现象:产生白色沉淀结论:氯水中含有Cl- 在洁净的试管中加入2mL新制氯水,再向试管中加入几滴硝酸银溶液和几滴稀硝酸,观察现象。实验3方法(1):观察新制氯水的颜色
实验4实验现象:氯水显淡黄绿色,且有刺激性气味.
结论: 氯水中含有Cl2氯水中Cl2分子的检验方法方法(2):在洁净的试管中加入2mLKI溶液,滴加新制氯水,再加少量CCl4,振荡,观察实验现象。
实验现象:下层有紫红色物质出现方法(3):使淀粉碘化钾试纸变蓝2KI+Cl2=2KCl+I2
