铁、铜及其化合物(第二课时)
图片预览




文档简介
课件14张PPT。铁、铜及其化合物的应用从矿物到基础材料(第二课时)三门中学化学组 陈爱娇资料 铁与动植物 铁是人体健康、植物生长所必需的元素之一
一个成年人的身体里约含3g~5g铁元素,其中70%以上在血红蛋白里。人体必须保证足够的铁的摄入,如果每天膳食中的含铁量太低,长时间供铁不足,就会患缺铁性贫血。这类病人往往面色苍白,并有头昏、无力、心悸、气急等症状。因此,应多吃一些含铁丰富的食物。含铁较多的食物有动物的肝脏,苋菜、芹菜、番茄等。
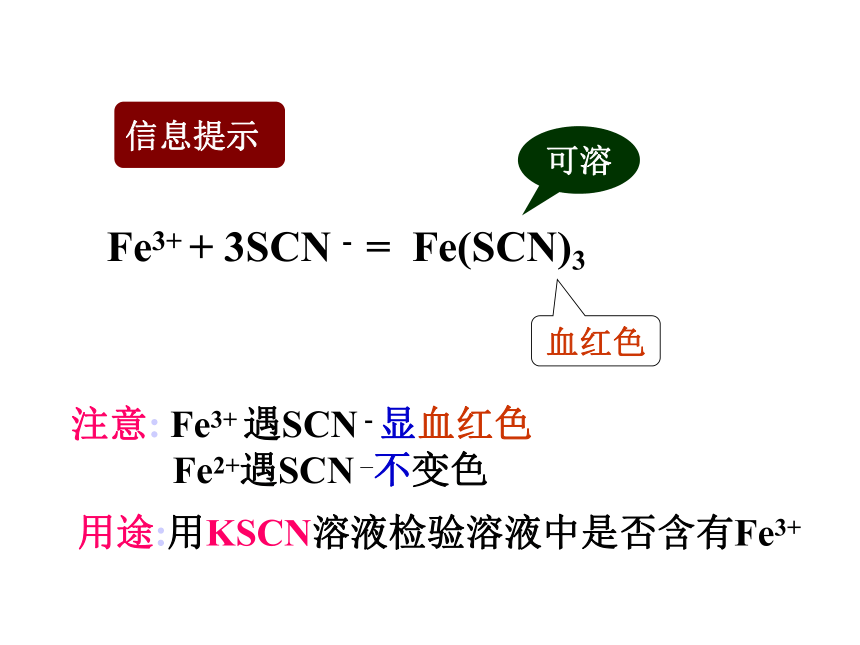
植物生长也离不开铁,铁是植物制造叶绿素时不可缺少的催化剂。如果一盆花很快失去艳丽的颜色和芳香的气味,叶子发黄枯萎,这就是土壤中缺铁的特征,就应施加如硫酸亚铁等予以补充。铁锈红装饰品磁性材料含铁化合物的净水剂发病的水稻需喷洒波尔多液Fe3+ + 3SCN - = Fe(SCN)3可溶血红色注意: Fe3+ 遇SCN - 显血红色
Fe2+遇SCN –不变色用途:用KSCN溶液检验溶液中是否含有Fe3+
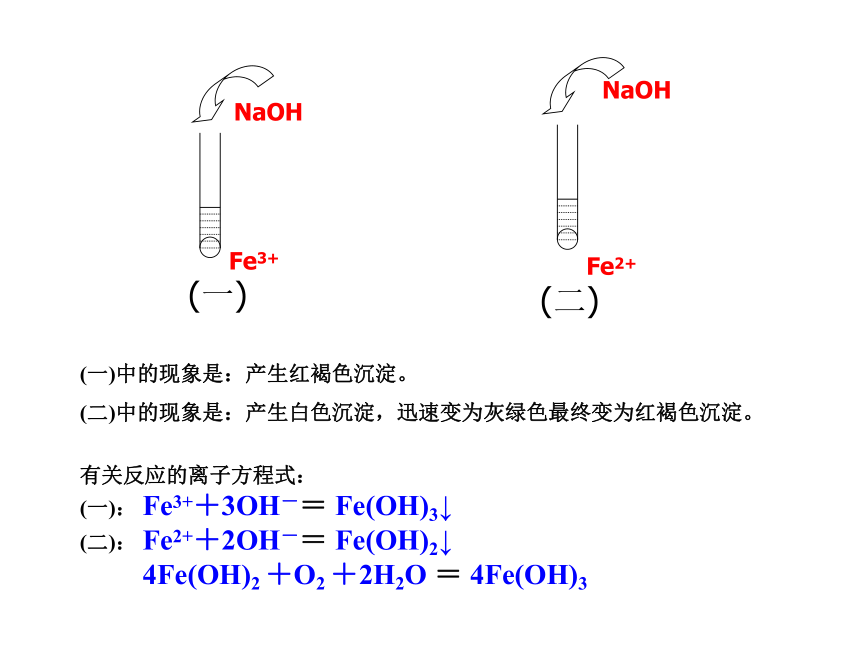
(一)中的现象是:产生红褐色沉淀。
(二)中的现象是:产生白色沉淀,迅速变为灰绿色最终变为红褐色沉淀。有关反应的离子方程式:
(一): Fe3++3OH-= Fe(OH)3↓
(二): Fe2++2OH-= Fe(OH)2↓
4Fe(OH)2 +O2 +2H2O = 4Fe(OH)3
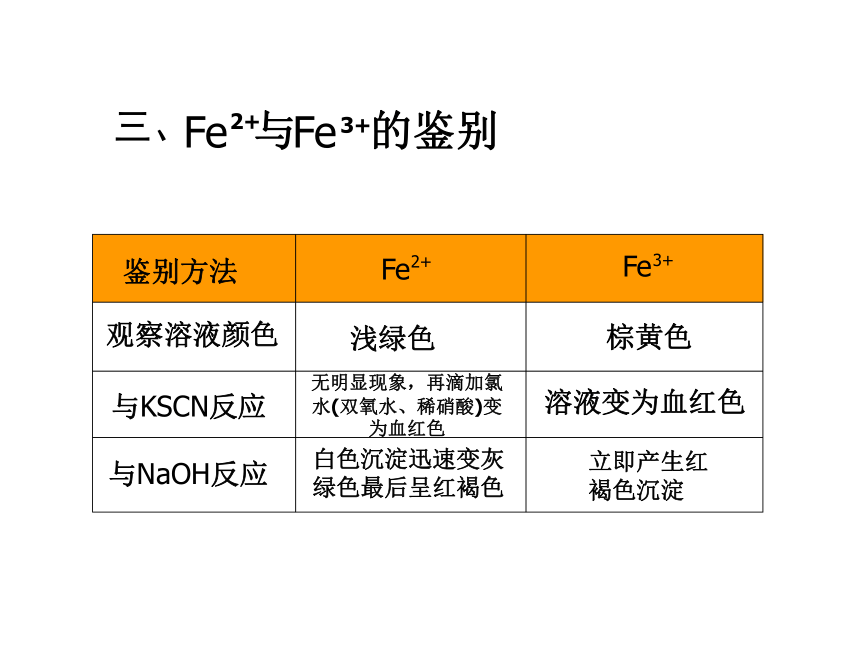
观察溶液颜色与KSCN反应与NaOH反应浅绿色棕黄色无明显现象,再滴加氯水(双氧水、稀硝酸)变为血红色溶液变为血红色白色沉淀迅速变灰
绿色最后呈红褐色立即产生红
褐色沉淀三、思 考不同价态的铁元素之间
是否可以相互转化呢??化合价 , 升高需加入氧化剂。还原剂。降低
KSCN一、无明显变化二、加入KSCN
溶液后溶液呈
血红色(一)溶液变成血红色(二)加铁粉后
溶液由黄色变成
浅绿色加KSCN
溶液后无明显变化化合价 , 升高需加入氧化剂。还原剂。降低氧化剂:氯水、溴水、双氧水、硝酸、高锰酸钾溶液等。还原剂:S2-、SO32-、I-、金属单质(Zn、Fe、Cu)等。小 结:氧化性较强的氧化剂如Cl2、硝酸等Fe氧化性较强的氧化剂如Cl2、硝酸等Zn 、Al、 Mg等等Zn、Al、Mg五、铁及铜的化合物的应用1、铁的化合物①Fe2O3作颜料②氯化铁、硫酸亚铁可作净水剂③作磁性材料④维持生命的微量元素2、铜的化合物:铜盐可杀菌,CuSO4溶液杀灭寄生虫,治疗皮肤病。完成下列的离子方程式Fe2++Cl2=
Fe2++Br2=
Fe3++S2- =
Fe3++SO32-+H2O =
Fe3++I- =
Fe3++Cu=
Fe3++Fe =
Fe3++Zn=
一个成年人的身体里约含3g~5g铁元素,其中70%以上在血红蛋白里。人体必须保证足够的铁的摄入,如果每天膳食中的含铁量太低,长时间供铁不足,就会患缺铁性贫血。这类病人往往面色苍白,并有头昏、无力、心悸、气急等症状。因此,应多吃一些含铁丰富的食物。含铁较多的食物有动物的肝脏,苋菜、芹菜、番茄等。
植物生长也离不开铁,铁是植物制造叶绿素时不可缺少的催化剂。如果一盆花很快失去艳丽的颜色和芳香的气味,叶子发黄枯萎,这就是土壤中缺铁的特征,就应施加如硫酸亚铁等予以补充。铁锈红装饰品磁性材料含铁化合物的净水剂发病的水稻需喷洒波尔多液Fe3+ + 3SCN - = Fe(SCN)3可溶血红色注意: Fe3+ 遇SCN - 显血红色
Fe2+遇SCN –不变色用途:用KSCN溶液检验溶液中是否含有Fe3+
(一)中的现象是:产生红褐色沉淀。
(二)中的现象是:产生白色沉淀,迅速变为灰绿色最终变为红褐色沉淀。有关反应的离子方程式:
(一): Fe3++3OH-= Fe(OH)3↓
(二): Fe2++2OH-= Fe(OH)2↓
4Fe(OH)2 +O2 +2H2O = 4Fe(OH)3
观察溶液颜色与KSCN反应与NaOH反应浅绿色棕黄色无明显现象,再滴加氯水(双氧水、稀硝酸)变为血红色溶液变为血红色白色沉淀迅速变灰
绿色最后呈红褐色立即产生红
褐色沉淀三、思 考不同价态的铁元素之间
是否可以相互转化呢??化合价 , 升高需加入氧化剂。还原剂。降低
KSCN一、无明显变化二、加入KSCN
溶液后溶液呈
血红色(一)溶液变成血红色(二)加铁粉后
溶液由黄色变成
浅绿色加KSCN
溶液后无明显变化化合价 , 升高需加入氧化剂。还原剂。降低氧化剂:氯水、溴水、双氧水、硝酸、高锰酸钾溶液等。还原剂:S2-、SO32-、I-、金属单质(Zn、Fe、Cu)等。小 结:氧化性较强的氧化剂如Cl2、硝酸等Fe氧化性较强的氧化剂如Cl2、硝酸等Zn 、Al、 Mg等等Zn、Al、Mg五、铁及铜的化合物的应用1、铁的化合物①Fe2O3作颜料②氯化铁、硫酸亚铁可作净水剂③作磁性材料④维持生命的微量元素2、铜的化合物:铜盐可杀菌,CuSO4溶液杀灭寄生虫,治疗皮肤病。完成下列的离子方程式Fe2++Cl2=
Fe2++Br2=
Fe3++S2- =
Fe3++SO32-+H2O =
Fe3++I- =
Fe3++Cu=
Fe3++Fe =
Fe3++Zn=
