鲁教版初中化学九年级上册第四单元《我们周围的空气》单元测试题(解析版)
文档属性
| 名称 | 鲁教版初中化学九年级上册第四单元《我们周围的空气》单元测试题(解析版) |  | |
| 格式 | zip | ||
| 文件大小 | 163.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2018-12-22 15:44:12 | ||
图片预览




文档简介
第四单元《我们周围的空气》单元测试题
一、单选题(每小题只有一个正确答案)
1.人体呼出的气体可以使( )
A.带火星木条复燃 B.澄清石灰水变浑浊C.燃着木条更旺 D.以上三个都对
2.属于有机物的是( )
A. 碳酸钙 B. 酒精 C. 二氧化碳 D. 碳酸
3.空气的成分按体积计算,约占0.03%的是( )
A. 氧气 B. 氮气 C. 二氧化碳 D. 稀有气体
4.下列有关物质燃烧现象的描述,正确的是( )
A. 氢气在空气中燃烧产生大量白烟 B. 铁丝在氧气中燃烧发出明亮的火焰
C. 镁条在空气中燃烧发出耀眼的强光 D. 硫在氧气中燃烧发出淡蓝色的火焰
5.空气中含量最多的气体是( )
A.Ne B.N2 C.CO2 D. O2
6.下列反应是化合反应但不是氧化反应的是( )
A. 蜡烛+氧气----二氧化碳+水 B. 氧化钙+水---氢氧化钙
C. 铜+氧气---氧化铜 D. 碳酸氢钙---氨气+二氧化碳+水
7.下列实验现象描述正确的是 ( )
A.镁条在空气中燃烧,发出耀眼的白光,生成白色固体
B.硫在氧气中燃烧,产生淡蓝色火焰,生成有刺激性气味的气体
C.细铁丝在空气中剧烈燃烧,火星四射,生成四氧化三铁
D.硝酸铵晶体溶解于水,形成的溶液温度明显升高
8.2015年10月,中国女药学家屠呦呦因创制新型抗疟药——青蒿素和双氢青蒿素的贡献,与另外两位科学家共享2015年度诺贝尔生理学或医学奖。青蒿素的化学式为C15H22O5。下列说法中不正确的是( )
A.青蒿素由碳、氢、氧三种元素组成
B.一个青蒿素分子由15个碳原子、22个氢原子和5个氧原子构成
C.青蒿素分子中碳、氢、氧元素的原子个数比为15:22:5
D.青蒿素中氢元素的质量分数最大
9.掌握化学用语是学好化学的关键。下列化学用语与所表述的意义相符合的是( )
A. ①④⑤⑦ B. ②③④⑥ C. ①②⑤⑦ D. ②⑤⑥⑦
10.国务院决定自2018年5月1日起,将抗癌药品的进口关税降为零。氮芥(C5H11Cl2N)是最早用于临床并取得突出疗效的抗肿瘤药物。下列关于氮芥的说法正确的是( )
A. 氮芥由19个原子构成
B. 氮芥的相对分子质量为156 g
C. 氮芥中氯元素的质量分数为45.5%
D. 氮芥中碳、氢、氯、氮元素的质量比为5∶11∶2∶1
11.一种高效食品保鲜剂、环保型消毒剂由–2价氧元素和+4价氯元素组成,其化学式为( )
A. Cl2O7 B. ClO2 C. O2Cl D. Cl2O
12.不能达到实验目的的方案是( )
A. 用稀硫酸鉴别炭粉和氧化铜
B. 用锌粒鉴别食盐水和稀盐酸
C. 用硝酸银溶液鉴别稀盐酸和稀硫酸
D. 用燃着的木条鉴别氢气、氧气和二氧化碳
13.以下是小明同学书写的部分化学用语,其中正确的是 ( )
①氖气—Ne ②四氧化三铁—O4Fe3 ③氯化铁—FeCl2 ④钠元素显+1价—Na+1
⑤两个铝离子—2Al3+
A. ①⑤ B. ③⑤ C. ①④ D. ②③④
14. 氧化锆(ZrO2)是一种高级耐火原料,其中锆元素(Zr)的化合价为( )
A.+4 B.+3 C.+2 D.+1
15.硅(Si)是太阳能电池和电脑芯片不可缺少的材料.利用石英砂(主要成分为SiO2)生产高纯硅(Si)的流程图如下(整个制备过程必须达到无水、无氧气).
(提示:Si+3HClSiHCl3+H2↑)
根据以上信息判断,下列相关说法错误的是( )
A. 三氯硅烷(SiHCl3)是由三种元素组成的物质
B. 在H2和SiHCl3反应的过程中若混入O2,可能引起爆炸
C. 以上生成高纯硅的流程中,可循环使用的物质只有HCl
D. Si+3HClSiHCl3+H2↑反应中硅元素的化合价发生改变
二、填空题
16.归纳总结是学习化学的有效方法。以下是小东同学关于实验方面的某些归纳总结,请你帮助完成:
(1)实验室中有些药品需密封保存的原因:A.药品能吸收空气中的水蒸气;B.药品能与空气中的某些成分发生化学反应。
①该同学的归纳不完整,你还能补充的一种情况是 。
②写出一个符合情况A的物质的名称 。
(2)许多因素会影响化学反应速率。请分析下列实验或事实,分别说明在其他条件不变时,这些因素是如何影响化学反应速率的。示例:硫在纯氧中燃烧比在空气中进行得更快,更剧烈。答:增大反应物浓度,可以加快化学反应速率。
①同种食品在夏天比冬天更容易变质。
②在相同质量的锌粉和锌粒中分别加入足量l0%的稀盐酸,前者先反应完
17.“TNT”学名是三硝荃甲苯,化学式为C7H5(NO2)3,该物质由_______元素组成,相对分子质量为__________,一个分子中共含有__________个原子,其中碳元素和氧元素的质量比为
18.在宏观、微观和符号之间建立联系是化学学科的特点。
(1)氯化钠、铁、过氧化氢三种物质中,由离子构成是__________。
(2)下列微观示意图1中,能表示化合物的是_____(填字母序号,下同),能表示3个分子的是_______。
(3)A、B、C、D表示四种物质中,在高温条件下,A和B反应生成C和D,微观示意图如图2所示,反应后,生成C和D两种粒子的个数比应为________________。
19.用化学用语填空:
(1)氖
(2)2个二氧化硫分子
(3)地壳中含量最多的金属元素
(4)表示 的结构示意图
(5)核电荷数为14的元素
20.“84”消毒液的有效成分NaClO中氯元素的化合价为________价。
三、实验题
21.化学课外小组的同学以“氢氧化钠变质程度”为课题,进行科学探究活动,请根据己学知识完成下列探究问题.
提出问题:氢氧化钠变质程度是怎样的?
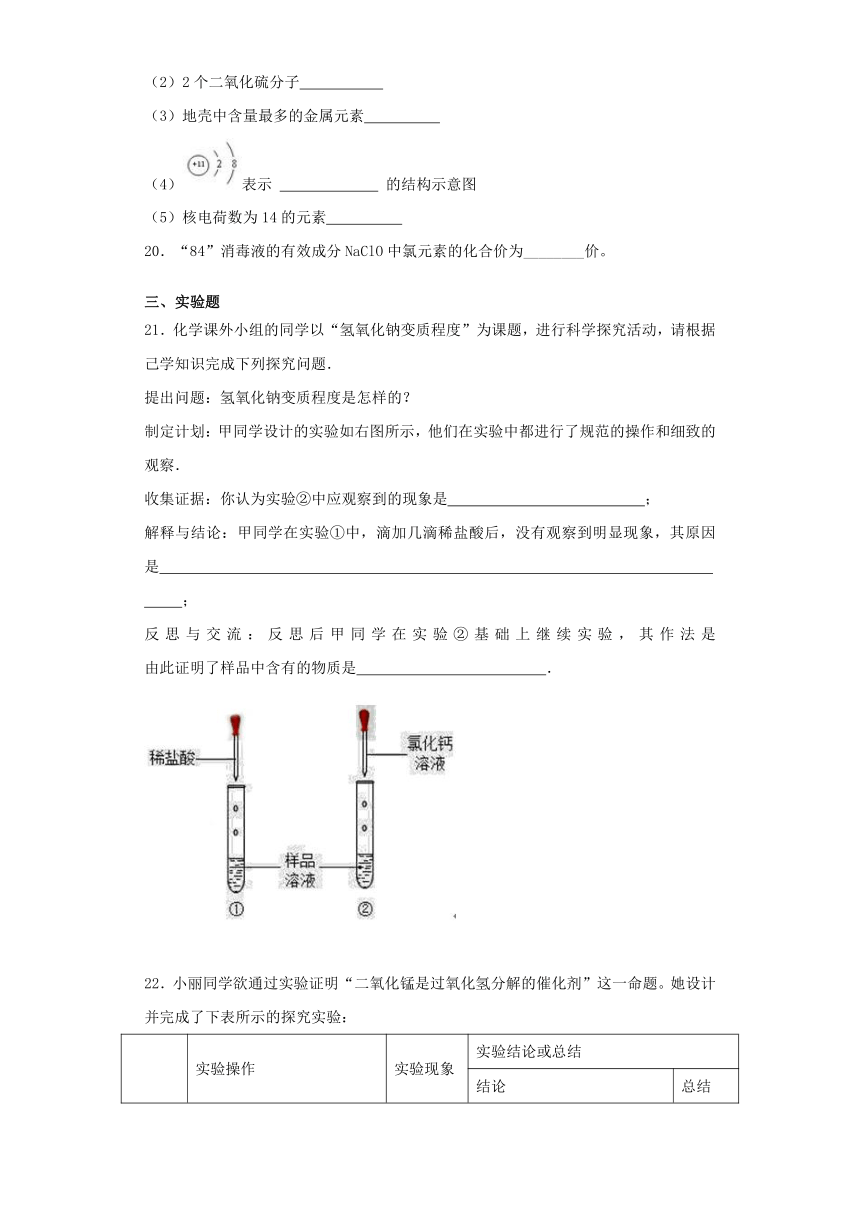
制定计划:甲同学设计的实验如右图所示,他们在实验中都进行了规范的操作和细致的观察.
收集证据:你认为实验②中应观察到的现象是 ;
解释与结论:甲同学在实验①中,滴加几滴稀盐酸后,没有观察到明显现象,其原因是 ;
反思与交流:反思后甲同学在实验②基础上继续实验,其作法是 由此证明了样品中含有的物质是 .
22.小丽同学欲通过实验证明“二氧化锰是过氧化氢分解的催化剂”这一命题。她设计并完成了下表所示的探究实验:
实验操作 实验现象 实验结论或总结
结论 总结
实验一 取5mL5%的过氧化氢溶液于试管中,伸入带火星的木条 有气泡产生,木条不复燃 过氧化氢分解产生氧气,但是 ③ 。 二氧化锰是过氧化氢分解的催化剂
实验二 向盛水的试管中加入二氧化锰,伸入带火星的木条 没有明显现象 水中加入二氧化锰,不产生氧气
实验三 ① ② 二氧化锰能加快过氧化氢的分解
(1)请你帮小丽同学填写上表中未填完的空格。
(2)在小丽的探究实验中,“实验一”和“实验二”起对照作用
(3)小英同学认为仅由上述实验还不能完全得出表内的“总结”,她补充设计了两个方面的探究实验,最终完成了对“命题”的实验证明。
第一方面的实验操作中包含了两次称量,其目的是: ;
第二方面的实验是利用“实验三”反应后试管内的剩余物继续实验。接下来的实验操作、现象是: ;
四、推断题
23.A、B、C、E、F都是九年级化学常见的物质.A是一种暗紫色固体,医疗上常用作消毒剂;C、F是黑色固体,E是黑色粉末,C常用作加热氯酸钾制取氧气的催化剂。它们间有如下转化关系:
①A C+ D+ B↑,② B+ E F。(提示:“↑”表示气体)
(1)写出A的名称:____________。
(2)写出物质B的一种用途:___________。
(3)叙述E在B中反应的现象:__________。
(4)写出木炭在B中燃烧的文字表达式:________。
五、计算题
24.我国《食品安全法》于2009年6月1日正式实施.曾有不法分子将严重危害人体健康的三聚氰胺(化学式为C3N6H6)添加到奶制品中以提高产品含氮量。
(1)三聚氰胺分子中碳原子和氢原子的个数比为___________;
(2)三聚氰胺中氢元素和碳元素的质量比为_____。
25.青少年正处于生长发育时期,每天需要摄取足量的蛋白质,蛋白质的代谢产物中含有尿素【化学式为CO(NH2)2】。请根据尿素的化学式计算:
(1)尿素中碳元素和氮元素的质量比为_______________;
(2)尿素中氮元素的质量分数为______________;
(3)120g尿素与___________g硝酸铵(NH4NO3)所含氮元素的质量相等?
参考答案
1.B
【解析】
试题分析:人体呼出的气体中含有大量的二氧化碳,二氧化碳不能支持燃烧,但能使澄清的石灰水变浑浊。故选B。
考点:人体呼出气体的成分
2.B
【解析】A. 碳酸钙属于无机化合物中的盐,错误;B. 酒精属于有机物,正确;C. 二氧化碳属于无机化合物中的氧化物,错误;D. 碳酸属于无机化合物中的酸,错误。故选B。
3.C
【解析】
【详解】
空气的成分按体积分数计算,大约是氮气为78%、氧气为21%、稀有气体为0.94%、二氧化碳为0.03%、其它气体和杂质为0.03%。故选C。
4.C
【解析】
【详解】
A、氢气在空气中燃烧产生淡蓝色火焰,故A错误;B、铁丝在氧气中燃烧火星四射,故B错误;C、镁条在空气中燃烧发出耀眼的强光,故C正确;D、硫在空气中燃烧发出淡蓝色火焰,在氧气中发出蓝紫色火焰,故D错误。故选C。
5.B
【解析】考点:空气的成分及各成分的体积分数.
专题:空气与水.
分析:根据空气中各成分及体积分数来回答本题,并能灵活运用它们解释一些生活中常见的现象.
解答:解:空气中各成分及体积分数为:氮气:78%、氧气:21%、稀有气体:0.94%、二氧化碳0.03%、水蒸气和杂质:0.03%.
故选B.
点评:熟记空气中各成分及体积分数,知道空气中的主要气体,哪种气体最多,哪种气体最少.
6.B
【解析】由两种或两种以上物质生成一种物质的反应叫化合反应;由一种物质生成两种或两种以上物质的反应叫分解反应;物质与氧气的反应属于氧化反应。A. 蜡烛+氧气----二氧化碳+水,两种反应物,两种生成物,既不是化合反应也不是分解反应,但反应物中有氧气,是氧化反应; B. 氧化钙+水---氢氧化钙,由两种物质生成一种物质,是化合反应,但不是氧化反应,不符合题意;C. 铜+氧气---氧化铜 , 由两种物质生成一种物质,是化合反应,也是氧化反应,不符合题意; D. 碳酸氢钙---碳酸钙+二氧化碳+水,是由一种物质生成三种物质,是分解反应;选B
7.A
【解析】
试题分析:A、镁条在空气中燃烧,发出耀眼的白光,生成白色固体,正确,B、硫在氧气中燃烧,产生明亮蓝紫色火焰,生成有刺激性气味的气体,错误,C、细铁丝在空气中不会燃烧,错误,D、硝酸铵晶体溶解于水,形成的溶液温度明显降低,错误,故选A
考点:物质燃烧现象的描述,物质溶解时的热现象
8.D
【解析】
试题分析:由青蒿素的化学式可知青蒿素由碳、氢、氧三种元素组成,A正确;一个青蒿素分子由15个碳原子、22个氢原子和5个氧原子构成,B正确;青蒿素分子中碳、氢、氧元素的原子个数比
=15:22:5 ,C正确;青蒿素中氢元素原子的相对原子质量之和最香,故它的质量分数最小,D错误。故选D。
考点:化学式的意义
9.C
【解析】①由化合物的书写规则和化合价原则,氯化亚铁可表示为:FeCl2,正确;②离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。就在其元素符号前加上相应的数字,故2个钙离子可表示为:2Ca2+,正确;③原子的表示方法就是用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字。所以2个氢原子,就可表示为:2H,错误;④元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,所以表示+1价的钠元素,错误;⑤分子的表示方法:正确书写物质的化学式,若表示多个该分子,就在其化学式前加上相应的数字,所以2个水分子可表示为:2H2O,正确;⑥原子的表示方法就是用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字。所以2H表示2个氢原子,错误;⑦元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后, 所以可表示氮气中氮元素的化合价为零,正确。故选C。
点睛:化学符号周围的数字表示不同的意义:符号前面的数字,表示原子或分子或离子个数;右上角的数字表示一个离子所带的单位电荷数;右下角的数字表示几个原子构成一个分子,标在元素符号正上方的数字表示该元素化合价的数值。
10.C
【解析】氮芥由氮芥分子构成,1个氮芥分子由19个原子构成,A项错误;相对分子质量没有单位,氮芥的相对分子质量为156,B项错误;氮芥中氯元素的质量分数为(71/156)×100%=45.5%,C项正确;氮芥中碳、氢、氯、氮原子的个数比为5∶11∶2∶1,氮芥中碳、氢、氯、氮元素的质量比为12×5∶1×11∶35.5×2∶14×1=60∶11∶71∶14,D项错误。
11.B
【解析】环保型消毒剂由-2价的氧元素和+4价的氯元素组成,按照“左正右负”的原则,即正价元素或原子团写在左边,负价元素或原子团写在右边,再利用化合价数值交叉法书写化学式为Cl2O4,原子个数得约分,化学式为ClO2。故选B。
12.C
【解析】A. 稀硫酸不与炭粉反应,无现象,与氧化铜反应,液体由无色变为蓝色,正确;B. 锌粒与食盐水不反应,无现象,与稀盐酸反应,有气泡产生,正确;C. 硝酸银溶液与稀盐酸、稀硫酸反应均产生白色沉淀,错误;D. 使燃着的木条熄灭的是二氧化碳,燃烧更旺的是氧气,气体燃烧起来的是氢气,正确。故选C。
13.A
【解析】①、氖气是稀有气体单质,化学式为Ne,正确;②、书写化合物时,一般正价前负价后,四氧化三铁的化学式为Fe3O4,故错误;③、氯化铁中铁为+3价,化学式为FeCl3,故错误;④、标化合价时化合价应标在元素符号的正上方,钠元素显+1价应为,故错误;⑤、两个铝离子—2Al3+,表示正确。故选A。
14.A
【解析】
试题分析:根据在化合物中正负化合价代数和为零。在化合物中氧元素常显-2价,设锆元素(Zr)的化合价为X,则X+(-2)*2=0,解得:X=+4,故选A。
考点:化合价与化学式
15.C
【解析】A、由三氯硅烷(SiHCl3)的化学式可知它是由Si、H、Cl三种元素组成的,正确;B、氢气具有可燃性,不纯可能会发生爆炸,正确;C、三氯硅烷与氢气反应生成高纯硅和HCl, HCl可循环利用,Si+3HClSiHCl3+H2↑,根据流程图可知,氢气也可循环利用,错误;D、反应物中的硅是单质,单质中元素的化合价为0,生成物三氯硅烷中硅元素为+4价,化合价发生了改变,正确。故选C。
点睛:氢气、一氧化碳、甲烷都属可燃性气体,可燃性气体点燃前要验纯,否则可能会发生爆炸。
16.(1)①药品易挥发;②浓硫酸;
(2)①升高温度,可以加快化学反应速率; ②增大反应物接触面积,可以加快化学反应速率。
【解析】
试题分析:(1)实验室中有些药品需密封保存的原因:A.药品能吸收空气中的水蒸气;B.药品能与空气中的某些成分发生化学反应。①该同学的归纳不完整,还能补充的一种情况是药品易挥发;②符合情况A的物质的名称为浓硫酸、氢氧化钠等;(2)许多因素会影响化学反应速率①同种食品在夏天比冬天更容易变质升高温度,可以加快化学反应速率;②在相同质量的锌粉和锌粒中分别加入足量l0%的稀盐酸,前者先反应完,是因为增大反应物接触面积,可以加快化学反应速率。
考点:物质的变质、化学反应的应先因素
17.C、N、H、O 227 21 7:8
【解析】
试题分析:“TNT”学名是三硝荃甲苯,化学式为C7H5(NO2)3,该物质由C、N、H、O元素组成;相对分子质量=12×7+1×5+(14+16×2)×3=227;化学式中元素符号右下角的数字表示一个分子中所含的原子个数,一个分子中共含有原子个数=7+5+(1+2)×3=21;其中碳元素和氧元素的质量比=12×7:16×6=7:8
考点:根据化学式进行的计算
18.(1)氯化钠(1分);(2)乙(1分);甲乙(2分,写对1个给1分);(3)1:3(2分).
【解析】
试题分析:(1)氯化钠由钠离子和氯离子构成,铁由铁原子构成,过氧化氢由过氧化氢分子构成;(2)由示意图可知,甲只由氧分子构成,只含有氧元素,属于单质,乙由氨分子构成,含有氮元素和氢元素,属于化合物,丙中有氧分子和水分子,属于混合物,丁只有氮原子;甲中有三个氧分子,乙中有三个氨分子;(3)由质量守恒定律可知,变化前后每种元素的原子个数不变,故C和D的分子个数比为1:3
考点:分子、原子、离子、元素与物质之间的关系;单质和化合物的判别;微粒观点及模型图的应用;化学符号及其周围数字的意义
19.(1)Ne (2)2SO2 (3)Al (4)Na+ (5)Si
【解析】
试题分析:根据化学符号的书写原则可知,(1)氖用元素符号表示其化学式为 Ne。(2)2个二氧化硫分子表示为2SO2; (3)地壳中含量最多的金属元素为铝元素,其元素符号为Al (4)微粒结构示意图中质子数为11,核外电子数为10,故表示Na+ 的结构示意图;(5)核电荷数为14的元素为硅元素,化学符号为Si
考点:化学符号的书写
20.+1
【解析】在NaClO中,钠元素的化合价是+1,氧元素的化合价是-2,设:氯元素的化合价是x,则有(+1)+x+(-2)=0,解得x=+1。
21.收集证据:出现白色沉淀.
解释与结论:稀盐酸不足,只能够和氢氧化钠反应.
反思与交流:继续滴加氯化钡溶液,直至不再产生白色沉淀;取上层清液,加入试管中,滴加酚酞试液,酚酞试液变红色;氢氧化钠和碳酸钠.
【解析】
试题分析:收集证据:变质的氢氧化钠中含有碳酸钠,加入氯化钙溶液时会出现白色沉淀,因为碳酸钠能和氯化钙反应生成碳酸钙沉淀和氯化钠.故填:出现白色沉淀。
解释与结论:甲同学在实验①中,滴加几滴稀盐酸后,没有观察到明显现象,其原因是:稀盐酸不足,只能够和氢氧化钠反应
反思与交流:在实验②基础上继续实验,其作法是:继续滴加氯化钡溶液,直至不再产生白色沉淀;取上层清液,加入试管中,滴加酚酞试液,酚酞试液变红色,由此证明了样品中含有的物质是氢氧化钠和碳酸钠
考点:碱的化学性质;证明碳酸盐.
22.(1)①向盛5mL5%的过氧化氢溶液的试管中加入二氧化锰,伸入带火星的木条②有大量气泡产生,木条复燃③ 反应很缓慢(3)证明反应前后二氧化锰的质量不变 过滤,向其中滴加浓盐酸,有黄绿色气体生成,证明二氧化锰化学性质不变。
【解析】
试题分析∶由题中信息知,(1)实验操作∶[取5mL5%的过氧化氢溶液于试管中,伸入带火星的木条。实验现象∶有气泡产生,木条不复燃。结论∶过氧化氢分解产生氧气,但是③反应很缓慢。实验操作∶向盛水的试管中加入二氧化锰,伸入带火星的木条。实验现象∶没有明显现象。结论∶水中加入二氧化锰,不产生氧气。实验操作∶①向盛5mL5%的过氧化氢溶液的试管中加入二氧化锰,伸入带火星的木条。实验现象∶②有大量气泡产生,木条复燃。结论∶二氧化锰能加快过氧化氢的分解。
总结∶二氧化锰是过氧化氢分解的催化剂。(2)在小丽的探究实验中,“实验一”和“实验二”起对照作用。(3)小英同学认为仅由上述实验还不能完全得出表内的“总结”,她补充设计了两个方面的探究实验,最终完成了对“命题”的实验证明。第一方面的实验操作中包含了两次称量,其目的是:证明反应前后二氧化锰的质量不变。第二方面的实验是利用“实验三”反应后试管内的剩余物继续实验。接下来的实验操作、现象是:过滤,向其中滴加浓盐酸,有黄绿色气体生成,证明二氧化锰化学性质不变。
考点∶考查实验探究的基本思路和方法。
23.高锰酸钾 供给呼吸(合理即可) 剧烈燃烧,火星四射,放出大量的热,生成黑色固体 木炭+氧气二氧化碳
【解析】
【详解】
(1)A是一种暗紫色固体,医疗上常用作消毒剂,符合高锰酸钾的性质,故A为高锰酸钾;由反应①可知,高锰酸钾受热分解为锰酸钾、二氧化锰和氧气,故B为氧气,C为黑色固体且C常用作加热氯酸钾制取氧气的催化剂,故C为二氧化锰;E是黑色粉末,且在氧气中燃烧生成黑色固体F,该反应符合铁粉在氧气中燃烧生成四氧化三铁,故E为铁粉(纯铁块儿状为银白色金属,粉末为黑色),F为四氧化三铁;
(2)由(1)分析可知,B为氧气,可供给呼吸;
(3)由(1)分析可知,E在B中发生的化学反应为铁粉在氧气中燃烧的反应,现象是剧烈燃烧,火星四射,放出大量的热,生成黑色固体;
(4)B为氧气,故木炭在氧气中燃烧生成二氧化碳,文字表达式为木炭+氧气二氧化碳。
24. 3:6(或1:2) 6:36(或1:6)
【解析】(1)三聚氰胺(化学式为C3N6H6)中碳原子和氢原子的个数比为3:6=1:2;
(2)三聚氰胺中氢元素和碳元素的质量比6:(12)=1:6;
25. 3:7 46.7% 160g
【解析】尿素【化学式为CO(NH2)2】。(1)尿素中碳元素和氮元素的质量比为∶12∶14×2=3:7;(2)尿素中氮元素的质量分数为∶ ×100%=46.7%;
(3)解∶设120g尿素与xg硝酸铵(NH4NO3)所含氮元素的质量相等
120g×46.7%=x× ,x=160g.
答∶(1)尿素中碳元素和氮元素的质量比为3:7;(2)尿素中氮元素的质量分数为46.7%;
(3)120g尿素与160g硝酸铵(NH4NO3)所含氮元素的质量相等。
点睛∶化学式意义∶①宏观意义a.表示一种物质;b.表示该物质的元素组成;②微观意义a.表示该物质的一个分子;b.表示该物质的分子构成;③量的意义a.表示物质的一个分子中各原子个数比;b.表示组成物质的各元素质量比。
一、单选题(每小题只有一个正确答案)
1.人体呼出的气体可以使( )
A.带火星木条复燃 B.澄清石灰水变浑浊C.燃着木条更旺 D.以上三个都对
2.属于有机物的是( )
A. 碳酸钙 B. 酒精 C. 二氧化碳 D. 碳酸
3.空气的成分按体积计算,约占0.03%的是( )
A. 氧气 B. 氮气 C. 二氧化碳 D. 稀有气体
4.下列有关物质燃烧现象的描述,正确的是( )
A. 氢气在空气中燃烧产生大量白烟 B. 铁丝在氧气中燃烧发出明亮的火焰
C. 镁条在空气中燃烧发出耀眼的强光 D. 硫在氧气中燃烧发出淡蓝色的火焰
5.空气中含量最多的气体是( )
A.Ne B.N2 C.CO2 D. O2
6.下列反应是化合反应但不是氧化反应的是( )
A. 蜡烛+氧气----二氧化碳+水 B. 氧化钙+水---氢氧化钙
C. 铜+氧气---氧化铜 D. 碳酸氢钙---氨气+二氧化碳+水
7.下列实验现象描述正确的是 ( )
A.镁条在空气中燃烧,发出耀眼的白光,生成白色固体
B.硫在氧气中燃烧,产生淡蓝色火焰,生成有刺激性气味的气体
C.细铁丝在空气中剧烈燃烧,火星四射,生成四氧化三铁
D.硝酸铵晶体溶解于水,形成的溶液温度明显升高
8.2015年10月,中国女药学家屠呦呦因创制新型抗疟药——青蒿素和双氢青蒿素的贡献,与另外两位科学家共享2015年度诺贝尔生理学或医学奖。青蒿素的化学式为C15H22O5。下列说法中不正确的是( )
A.青蒿素由碳、氢、氧三种元素组成
B.一个青蒿素分子由15个碳原子、22个氢原子和5个氧原子构成
C.青蒿素分子中碳、氢、氧元素的原子个数比为15:22:5
D.青蒿素中氢元素的质量分数最大
9.掌握化学用语是学好化学的关键。下列化学用语与所表述的意义相符合的是( )
A. ①④⑤⑦ B. ②③④⑥ C. ①②⑤⑦ D. ②⑤⑥⑦
10.国务院决定自2018年5月1日起,将抗癌药品的进口关税降为零。氮芥(C5H11Cl2N)是最早用于临床并取得突出疗效的抗肿瘤药物。下列关于氮芥的说法正确的是( )
A. 氮芥由19个原子构成
B. 氮芥的相对分子质量为156 g
C. 氮芥中氯元素的质量分数为45.5%
D. 氮芥中碳、氢、氯、氮元素的质量比为5∶11∶2∶1
11.一种高效食品保鲜剂、环保型消毒剂由–2价氧元素和+4价氯元素组成,其化学式为( )
A. Cl2O7 B. ClO2 C. O2Cl D. Cl2O
12.不能达到实验目的的方案是( )
A. 用稀硫酸鉴别炭粉和氧化铜
B. 用锌粒鉴别食盐水和稀盐酸
C. 用硝酸银溶液鉴别稀盐酸和稀硫酸
D. 用燃着的木条鉴别氢气、氧气和二氧化碳
13.以下是小明同学书写的部分化学用语,其中正确的是 ( )
①氖气—Ne ②四氧化三铁—O4Fe3 ③氯化铁—FeCl2 ④钠元素显+1价—Na+1
⑤两个铝离子—2Al3+
A. ①⑤ B. ③⑤ C. ①④ D. ②③④
14. 氧化锆(ZrO2)是一种高级耐火原料,其中锆元素(Zr)的化合价为( )
A.+4 B.+3 C.+2 D.+1
15.硅(Si)是太阳能电池和电脑芯片不可缺少的材料.利用石英砂(主要成分为SiO2)生产高纯硅(Si)的流程图如下(整个制备过程必须达到无水、无氧气).
(提示:Si+3HClSiHCl3+H2↑)
根据以上信息判断,下列相关说法错误的是( )
A. 三氯硅烷(SiHCl3)是由三种元素组成的物质
B. 在H2和SiHCl3反应的过程中若混入O2,可能引起爆炸
C. 以上生成高纯硅的流程中,可循环使用的物质只有HCl
D. Si+3HClSiHCl3+H2↑反应中硅元素的化合价发生改变
二、填空题
16.归纳总结是学习化学的有效方法。以下是小东同学关于实验方面的某些归纳总结,请你帮助完成:
(1)实验室中有些药品需密封保存的原因:A.药品能吸收空气中的水蒸气;B.药品能与空气中的某些成分发生化学反应。
①该同学的归纳不完整,你还能补充的一种情况是 。
②写出一个符合情况A的物质的名称 。
(2)许多因素会影响化学反应速率。请分析下列实验或事实,分别说明在其他条件不变时,这些因素是如何影响化学反应速率的。示例:硫在纯氧中燃烧比在空气中进行得更快,更剧烈。答:增大反应物浓度,可以加快化学反应速率。
①同种食品在夏天比冬天更容易变质。
②在相同质量的锌粉和锌粒中分别加入足量l0%的稀盐酸,前者先反应完
17.“TNT”学名是三硝荃甲苯,化学式为C7H5(NO2)3,该物质由_______元素组成,相对分子质量为__________,一个分子中共含有__________个原子,其中碳元素和氧元素的质量比为
18.在宏观、微观和符号之间建立联系是化学学科的特点。
(1)氯化钠、铁、过氧化氢三种物质中,由离子构成是__________。
(2)下列微观示意图1中,能表示化合物的是_____(填字母序号,下同),能表示3个分子的是_______。
(3)A、B、C、D表示四种物质中,在高温条件下,A和B反应生成C和D,微观示意图如图2所示,反应后,生成C和D两种粒子的个数比应为________________。
19.用化学用语填空:
(1)氖
(2)2个二氧化硫分子
(3)地壳中含量最多的金属元素
(4)表示 的结构示意图
(5)核电荷数为14的元素
20.“84”消毒液的有效成分NaClO中氯元素的化合价为________价。
三、实验题
21.化学课外小组的同学以“氢氧化钠变质程度”为课题,进行科学探究活动,请根据己学知识完成下列探究问题.
提出问题:氢氧化钠变质程度是怎样的?
制定计划:甲同学设计的实验如右图所示,他们在实验中都进行了规范的操作和细致的观察.
收集证据:你认为实验②中应观察到的现象是 ;
解释与结论:甲同学在实验①中,滴加几滴稀盐酸后,没有观察到明显现象,其原因是 ;
反思与交流:反思后甲同学在实验②基础上继续实验,其作法是 由此证明了样品中含有的物质是 .
22.小丽同学欲通过实验证明“二氧化锰是过氧化氢分解的催化剂”这一命题。她设计并完成了下表所示的探究实验:
实验操作 实验现象 实验结论或总结
结论 总结
实验一 取5mL5%的过氧化氢溶液于试管中,伸入带火星的木条 有气泡产生,木条不复燃 过氧化氢分解产生氧气,但是 ③ 。 二氧化锰是过氧化氢分解的催化剂
实验二 向盛水的试管中加入二氧化锰,伸入带火星的木条 没有明显现象 水中加入二氧化锰,不产生氧气
实验三 ① ② 二氧化锰能加快过氧化氢的分解
(1)请你帮小丽同学填写上表中未填完的空格。
(2)在小丽的探究实验中,“实验一”和“实验二”起对照作用
(3)小英同学认为仅由上述实验还不能完全得出表内的“总结”,她补充设计了两个方面的探究实验,最终完成了对“命题”的实验证明。
第一方面的实验操作中包含了两次称量,其目的是: ;
第二方面的实验是利用“实验三”反应后试管内的剩余物继续实验。接下来的实验操作、现象是: ;
四、推断题
23.A、B、C、E、F都是九年级化学常见的物质.A是一种暗紫色固体,医疗上常用作消毒剂;C、F是黑色固体,E是黑色粉末,C常用作加热氯酸钾制取氧气的催化剂。它们间有如下转化关系:
①A C+ D+ B↑,② B+ E F。(提示:“↑”表示气体)
(1)写出A的名称:____________。
(2)写出物质B的一种用途:___________。
(3)叙述E在B中反应的现象:__________。
(4)写出木炭在B中燃烧的文字表达式:________。
五、计算题
24.我国《食品安全法》于2009年6月1日正式实施.曾有不法分子将严重危害人体健康的三聚氰胺(化学式为C3N6H6)添加到奶制品中以提高产品含氮量。
(1)三聚氰胺分子中碳原子和氢原子的个数比为___________;
(2)三聚氰胺中氢元素和碳元素的质量比为_____。
25.青少年正处于生长发育时期,每天需要摄取足量的蛋白质,蛋白质的代谢产物中含有尿素【化学式为CO(NH2)2】。请根据尿素的化学式计算:
(1)尿素中碳元素和氮元素的质量比为_______________;
(2)尿素中氮元素的质量分数为______________;
(3)120g尿素与___________g硝酸铵(NH4NO3)所含氮元素的质量相等?
参考答案
1.B
【解析】
试题分析:人体呼出的气体中含有大量的二氧化碳,二氧化碳不能支持燃烧,但能使澄清的石灰水变浑浊。故选B。
考点:人体呼出气体的成分
2.B
【解析】A. 碳酸钙属于无机化合物中的盐,错误;B. 酒精属于有机物,正确;C. 二氧化碳属于无机化合物中的氧化物,错误;D. 碳酸属于无机化合物中的酸,错误。故选B。
3.C
【解析】
【详解】
空气的成分按体积分数计算,大约是氮气为78%、氧气为21%、稀有气体为0.94%、二氧化碳为0.03%、其它气体和杂质为0.03%。故选C。
4.C
【解析】
【详解】
A、氢气在空气中燃烧产生淡蓝色火焰,故A错误;B、铁丝在氧气中燃烧火星四射,故B错误;C、镁条在空气中燃烧发出耀眼的强光,故C正确;D、硫在空气中燃烧发出淡蓝色火焰,在氧气中发出蓝紫色火焰,故D错误。故选C。
5.B
【解析】考点:空气的成分及各成分的体积分数.
专题:空气与水.
分析:根据空气中各成分及体积分数来回答本题,并能灵活运用它们解释一些生活中常见的现象.
解答:解:空气中各成分及体积分数为:氮气:78%、氧气:21%、稀有气体:0.94%、二氧化碳0.03%、水蒸气和杂质:0.03%.
故选B.
点评:熟记空气中各成分及体积分数,知道空气中的主要气体,哪种气体最多,哪种气体最少.
6.B
【解析】由两种或两种以上物质生成一种物质的反应叫化合反应;由一种物质生成两种或两种以上物质的反应叫分解反应;物质与氧气的反应属于氧化反应。A. 蜡烛+氧气----二氧化碳+水,两种反应物,两种生成物,既不是化合反应也不是分解反应,但反应物中有氧气,是氧化反应; B. 氧化钙+水---氢氧化钙,由两种物质生成一种物质,是化合反应,但不是氧化反应,不符合题意;C. 铜+氧气---氧化铜 , 由两种物质生成一种物质,是化合反应,也是氧化反应,不符合题意; D. 碳酸氢钙---碳酸钙+二氧化碳+水,是由一种物质生成三种物质,是分解反应;选B
7.A
【解析】
试题分析:A、镁条在空气中燃烧,发出耀眼的白光,生成白色固体,正确,B、硫在氧气中燃烧,产生明亮蓝紫色火焰,生成有刺激性气味的气体,错误,C、细铁丝在空气中不会燃烧,错误,D、硝酸铵晶体溶解于水,形成的溶液温度明显降低,错误,故选A
考点:物质燃烧现象的描述,物质溶解时的热现象
8.D
【解析】
试题分析:由青蒿素的化学式可知青蒿素由碳、氢、氧三种元素组成,A正确;一个青蒿素分子由15个碳原子、22个氢原子和5个氧原子构成,B正确;青蒿素分子中碳、氢、氧元素的原子个数比
=15:22:5 ,C正确;青蒿素中氢元素原子的相对原子质量之和最香,故它的质量分数最小,D错误。故选D。
考点:化学式的意义
9.C
【解析】①由化合物的书写规则和化合价原则,氯化亚铁可表示为:FeCl2,正确;②离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略。就在其元素符号前加上相应的数字,故2个钙离子可表示为:2Ca2+,正确;③原子的表示方法就是用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字。所以2个氢原子,就可表示为:2H,错误;④元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,所以表示+1价的钠元素,错误;⑤分子的表示方法:正确书写物质的化学式,若表示多个该分子,就在其化学式前加上相应的数字,所以2个水分子可表示为:2H2O,正确;⑥原子的表示方法就是用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字。所以2H表示2个氢原子,错误;⑦元素化合价的表示方法:确定出化合物中所要标出的元素的化合价,然后在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后, 所以可表示氮气中氮元素的化合价为零,正确。故选C。
点睛:化学符号周围的数字表示不同的意义:符号前面的数字,表示原子或分子或离子个数;右上角的数字表示一个离子所带的单位电荷数;右下角的数字表示几个原子构成一个分子,标在元素符号正上方的数字表示该元素化合价的数值。
10.C
【解析】氮芥由氮芥分子构成,1个氮芥分子由19个原子构成,A项错误;相对分子质量没有单位,氮芥的相对分子质量为156,B项错误;氮芥中氯元素的质量分数为(71/156)×100%=45.5%,C项正确;氮芥中碳、氢、氯、氮原子的个数比为5∶11∶2∶1,氮芥中碳、氢、氯、氮元素的质量比为12×5∶1×11∶35.5×2∶14×1=60∶11∶71∶14,D项错误。
11.B
【解析】环保型消毒剂由-2价的氧元素和+4价的氯元素组成,按照“左正右负”的原则,即正价元素或原子团写在左边,负价元素或原子团写在右边,再利用化合价数值交叉法书写化学式为Cl2O4,原子个数得约分,化学式为ClO2。故选B。
12.C
【解析】A. 稀硫酸不与炭粉反应,无现象,与氧化铜反应,液体由无色变为蓝色,正确;B. 锌粒与食盐水不反应,无现象,与稀盐酸反应,有气泡产生,正确;C. 硝酸银溶液与稀盐酸、稀硫酸反应均产生白色沉淀,错误;D. 使燃着的木条熄灭的是二氧化碳,燃烧更旺的是氧气,气体燃烧起来的是氢气,正确。故选C。
13.A
【解析】①、氖气是稀有气体单质,化学式为Ne,正确;②、书写化合物时,一般正价前负价后,四氧化三铁的化学式为Fe3O4,故错误;③、氯化铁中铁为+3价,化学式为FeCl3,故错误;④、标化合价时化合价应标在元素符号的正上方,钠元素显+1价应为,故错误;⑤、两个铝离子—2Al3+,表示正确。故选A。
14.A
【解析】
试题分析:根据在化合物中正负化合价代数和为零。在化合物中氧元素常显-2价,设锆元素(Zr)的化合价为X,则X+(-2)*2=0,解得:X=+4,故选A。
考点:化合价与化学式
15.C
【解析】A、由三氯硅烷(SiHCl3)的化学式可知它是由Si、H、Cl三种元素组成的,正确;B、氢气具有可燃性,不纯可能会发生爆炸,正确;C、三氯硅烷与氢气反应生成高纯硅和HCl, HCl可循环利用,Si+3HClSiHCl3+H2↑,根据流程图可知,氢气也可循环利用,错误;D、反应物中的硅是单质,单质中元素的化合价为0,生成物三氯硅烷中硅元素为+4价,化合价发生了改变,正确。故选C。
点睛:氢气、一氧化碳、甲烷都属可燃性气体,可燃性气体点燃前要验纯,否则可能会发生爆炸。
16.(1)①药品易挥发;②浓硫酸;
(2)①升高温度,可以加快化学反应速率; ②增大反应物接触面积,可以加快化学反应速率。
【解析】
试题分析:(1)实验室中有些药品需密封保存的原因:A.药品能吸收空气中的水蒸气;B.药品能与空气中的某些成分发生化学反应。①该同学的归纳不完整,还能补充的一种情况是药品易挥发;②符合情况A的物质的名称为浓硫酸、氢氧化钠等;(2)许多因素会影响化学反应速率①同种食品在夏天比冬天更容易变质升高温度,可以加快化学反应速率;②在相同质量的锌粉和锌粒中分别加入足量l0%的稀盐酸,前者先反应完,是因为增大反应物接触面积,可以加快化学反应速率。
考点:物质的变质、化学反应的应先因素
17.C、N、H、O 227 21 7:8
【解析】
试题分析:“TNT”学名是三硝荃甲苯,化学式为C7H5(NO2)3,该物质由C、N、H、O元素组成;相对分子质量=12×7+1×5+(14+16×2)×3=227;化学式中元素符号右下角的数字表示一个分子中所含的原子个数,一个分子中共含有原子个数=7+5+(1+2)×3=21;其中碳元素和氧元素的质量比=12×7:16×6=7:8
考点:根据化学式进行的计算
18.(1)氯化钠(1分);(2)乙(1分);甲乙(2分,写对1个给1分);(3)1:3(2分).
【解析】
试题分析:(1)氯化钠由钠离子和氯离子构成,铁由铁原子构成,过氧化氢由过氧化氢分子构成;(2)由示意图可知,甲只由氧分子构成,只含有氧元素,属于单质,乙由氨分子构成,含有氮元素和氢元素,属于化合物,丙中有氧分子和水分子,属于混合物,丁只有氮原子;甲中有三个氧分子,乙中有三个氨分子;(3)由质量守恒定律可知,变化前后每种元素的原子个数不变,故C和D的分子个数比为1:3
考点:分子、原子、离子、元素与物质之间的关系;单质和化合物的判别;微粒观点及模型图的应用;化学符号及其周围数字的意义
19.(1)Ne (2)2SO2 (3)Al (4)Na+ (5)Si
【解析】
试题分析:根据化学符号的书写原则可知,(1)氖用元素符号表示其化学式为 Ne。(2)2个二氧化硫分子表示为2SO2; (3)地壳中含量最多的金属元素为铝元素,其元素符号为Al (4)微粒结构示意图中质子数为11,核外电子数为10,故表示Na+ 的结构示意图;(5)核电荷数为14的元素为硅元素,化学符号为Si
考点:化学符号的书写
20.+1
【解析】在NaClO中,钠元素的化合价是+1,氧元素的化合价是-2,设:氯元素的化合价是x,则有(+1)+x+(-2)=0,解得x=+1。
21.收集证据:出现白色沉淀.
解释与结论:稀盐酸不足,只能够和氢氧化钠反应.
反思与交流:继续滴加氯化钡溶液,直至不再产生白色沉淀;取上层清液,加入试管中,滴加酚酞试液,酚酞试液变红色;氢氧化钠和碳酸钠.
【解析】
试题分析:收集证据:变质的氢氧化钠中含有碳酸钠,加入氯化钙溶液时会出现白色沉淀,因为碳酸钠能和氯化钙反应生成碳酸钙沉淀和氯化钠.故填:出现白色沉淀。
解释与结论:甲同学在实验①中,滴加几滴稀盐酸后,没有观察到明显现象,其原因是:稀盐酸不足,只能够和氢氧化钠反应
反思与交流:在实验②基础上继续实验,其作法是:继续滴加氯化钡溶液,直至不再产生白色沉淀;取上层清液,加入试管中,滴加酚酞试液,酚酞试液变红色,由此证明了样品中含有的物质是氢氧化钠和碳酸钠
考点:碱的化学性质;证明碳酸盐.
22.(1)①向盛5mL5%的过氧化氢溶液的试管中加入二氧化锰,伸入带火星的木条②有大量气泡产生,木条复燃③ 反应很缓慢(3)证明反应前后二氧化锰的质量不变 过滤,向其中滴加浓盐酸,有黄绿色气体生成,证明二氧化锰化学性质不变。
【解析】
试题分析∶由题中信息知,(1)实验操作∶[取5mL5%的过氧化氢溶液于试管中,伸入带火星的木条。实验现象∶有气泡产生,木条不复燃。结论∶过氧化氢分解产生氧气,但是③反应很缓慢。实验操作∶向盛水的试管中加入二氧化锰,伸入带火星的木条。实验现象∶没有明显现象。结论∶水中加入二氧化锰,不产生氧气。实验操作∶①向盛5mL5%的过氧化氢溶液的试管中加入二氧化锰,伸入带火星的木条。实验现象∶②有大量气泡产生,木条复燃。结论∶二氧化锰能加快过氧化氢的分解。
总结∶二氧化锰是过氧化氢分解的催化剂。(2)在小丽的探究实验中,“实验一”和“实验二”起对照作用。(3)小英同学认为仅由上述实验还不能完全得出表内的“总结”,她补充设计了两个方面的探究实验,最终完成了对“命题”的实验证明。第一方面的实验操作中包含了两次称量,其目的是:证明反应前后二氧化锰的质量不变。第二方面的实验是利用“实验三”反应后试管内的剩余物继续实验。接下来的实验操作、现象是:过滤,向其中滴加浓盐酸,有黄绿色气体生成,证明二氧化锰化学性质不变。
考点∶考查实验探究的基本思路和方法。
23.高锰酸钾 供给呼吸(合理即可) 剧烈燃烧,火星四射,放出大量的热,生成黑色固体 木炭+氧气二氧化碳
【解析】
【详解】
(1)A是一种暗紫色固体,医疗上常用作消毒剂,符合高锰酸钾的性质,故A为高锰酸钾;由反应①可知,高锰酸钾受热分解为锰酸钾、二氧化锰和氧气,故B为氧气,C为黑色固体且C常用作加热氯酸钾制取氧气的催化剂,故C为二氧化锰;E是黑色粉末,且在氧气中燃烧生成黑色固体F,该反应符合铁粉在氧气中燃烧生成四氧化三铁,故E为铁粉(纯铁块儿状为银白色金属,粉末为黑色),F为四氧化三铁;
(2)由(1)分析可知,B为氧气,可供给呼吸;
(3)由(1)分析可知,E在B中发生的化学反应为铁粉在氧气中燃烧的反应,现象是剧烈燃烧,火星四射,放出大量的热,生成黑色固体;
(4)B为氧气,故木炭在氧气中燃烧生成二氧化碳,文字表达式为木炭+氧气二氧化碳。
24. 3:6(或1:2) 6:36(或1:6)
【解析】(1)三聚氰胺(化学式为C3N6H6)中碳原子和氢原子的个数比为3:6=1:2;
(2)三聚氰胺中氢元素和碳元素的质量比6:(12)=1:6;
25. 3:7 46.7% 160g
【解析】尿素【化学式为CO(NH2)2】。(1)尿素中碳元素和氮元素的质量比为∶12∶14×2=3:7;(2)尿素中氮元素的质量分数为∶ ×100%=46.7%;
(3)解∶设120g尿素与xg硝酸铵(NH4NO3)所含氮元素的质量相等
120g×46.7%=x× ,x=160g.
答∶(1)尿素中碳元素和氮元素的质量比为3:7;(2)尿素中氮元素的质量分数为46.7%;
(3)120g尿素与160g硝酸铵(NH4NO3)所含氮元素的质量相等。
点睛∶化学式意义∶①宏观意义a.表示一种物质;b.表示该物质的元素组成;②微观意义a.表示该物质的一个分子;b.表示该物质的分子构成;③量的意义a.表示物质的一个分子中各原子个数比;b.表示组成物质的各元素质量比。
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
