专题一 化学家眼中的物质世界综合复习
图片预览







文档简介
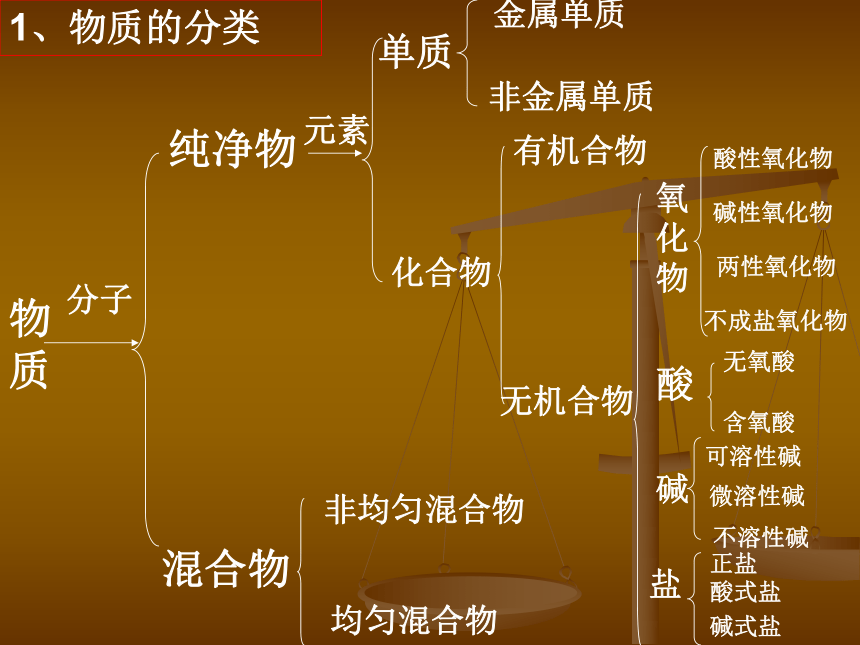
课件24张PPT。专题1复习余杭中学化学组 2007.6化学① [必修]复习系列 专题1: 化学家眼中的物质世界 单元一: 丰富多彩的化学物质 单元二: 研究物质的 实验方法 单元三: 人类对原子结构的认识 物质分子混合物纯净物元素单质化合物金属单质非金属单质有机合物无机合物氧化物酸碱盐酸性氧化物碱性氧化物两性氧化物不成盐氧化物无氧酸含氧酸微溶性碱可溶性碱不溶性碱正盐酸式盐碱式盐非均匀混合物均匀混合物1、物质的分类单元一: 丰富多彩的化学物质应知 1 : 物质的分类方法应会: 根据物质的组成对物质进行分类 (任何分类都要有依据)练习1:下列各物质的分类、名称(或俗名)、化学式都正确的是---( )
A.碱性氧化物 七氧化二锰 Mn2O7
B.酸性氧化物 干冰 C0
C.酸 硫酸 H2O
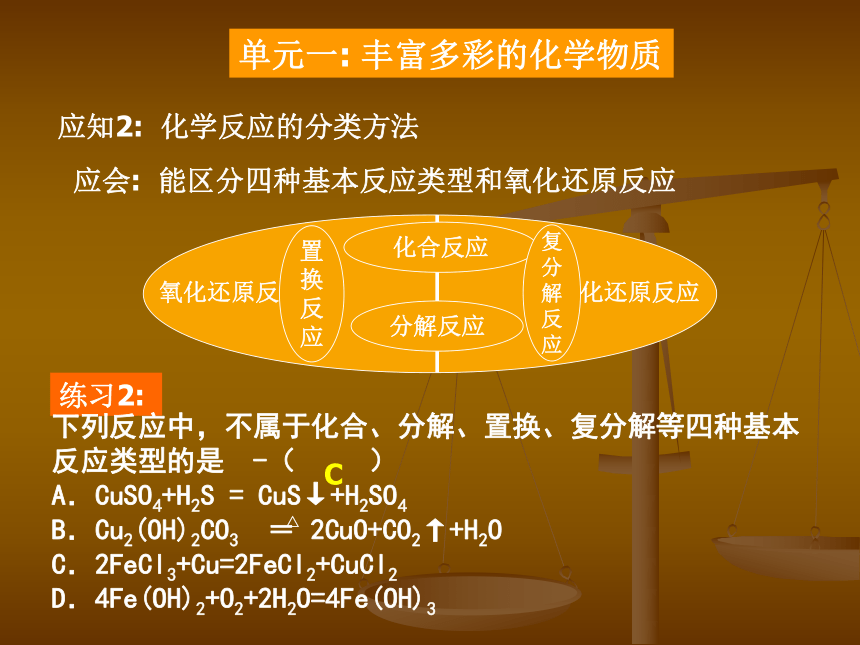
D.盐 纯碱 Na2CO3D应知2: 化学反应的分类方法 单元一: 丰富多彩的化学物质应会: 能区分四种基本反应类型和氧化还原反应 练习2: C 氧化还原反应 非氧化还原反应 化合反应分解反应置
换
反
应复
分
解
反
应单元一: 丰富多彩的化学物质应知3: 化学物质的计量方法
和物理量的单位 ( 物质的量 mol ) 应会: 涉及物质的量的各种换算方法 (1) 关于质量的换算 _________ (2) 关于粒子数目的换算 _______ (3) 关于气体体积的换算 _______(4) 关于物质的量浓度的计算 ______物理量的单位: n - mol m - g M - g/mol N - 个 NA - mol-1V - L 单元一: 丰富多彩的化学物质练习3: 下列溶液中的Cl-浓度与50 mL 1 mol·L-1的AlCl3溶液中Cl-的浓度相等的是 ----------------------------------------------------( )
A.150 mL 1mol·L-1的NaCl? B.75 mL 2 mol·L-1的NH4Cl
C.150 mL 3 mol·L-1的KCl? D.75 mL 1 mol·L-1的CaCl2C 22.2 g某二价金属氯化物(ACl2)中含有0.4 mol Cl-,则ACl2的摩尔质量是______________;A的相对原子质量是__________;ACl2的化学式是___________。111g/mol40 CaCl2电解质电解质 强电解质: 弱电解质: (电离是一个可逆过程)在水溶液或融化状态下能导电的化合物。在水溶液和融化状态下都不能导电的化合物电解质 :非电解质强酸、强碱、盐 弱酸、 NH3.H2O、 H2O单元一: 丰富多彩的化学物质应知4: 分散系有______、_____和______ 3 种. 溶液浊液胶体电解质和非电解质的概念 应会: 会区别分散系的类型、会区别电解质和非电解质. 练习4: 用特殊的方法把固体加工到纳米级(1~100nm, 1nm=10-9m)的超细粉末粒子,然后制得纳米材料。下列分散系中的分散质的粒子直径和这种粒子具有相同的数量级的是 ----------------------------------------------------------------( )
A. 溶液 B. 悬浮液 C. 胶体 D. 乳浊液C 下列物质: ①氢氧化钠固体 ②水银 ③氯化氢气体 ④稀硫酸 ⑤二氧化碳气体 ⑥氨水 ⑦碳酸钠粉末 ⑧蔗糖晶体 ⑨熔融氯化钠 ⑩CuSO4·5H2O晶体
⑴上述状态下能导电的是:_____________
⑵属于电解质的是:________________
⑶属于非电解质的是:______________②④⑥⑨①③⑦⑨⑩⑤⑧返回主页 单元一: 丰富多彩的化学物质应知 : 根据物质的组成对物质进行分类应会:1. 物质的分类方法 2. 化学反应的分类方法能区分四种基本反应类型
和氧化还原反应3 化学物质的计量方法
和物理量的单位 涉及物质的量的各种换算方法 4: 分散系有溶液、浊液
和胶体 3 种电解质和非电解质的概念会区别分散系的类型会区别电解质和非电解质.7、物质的分离和提纯单元二: 研究物质的 实验方法应知1: 物质的分离和提纯的方法有: ______、______、
______、______、______、______ 6种.层析 过滤结晶萃取分液蒸馏应会: 对不同的混合物能采用不同的分离方法 常用仪器的使用 下列实验操作中错误的是 ------------------------------------- ( )
A.蒸发操作时,应将溶液中的水分完全蒸干后,才能停止加热
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从
上口倒出.
D.萃取操作时,萃取剂与溶液中的溶剂不能互溶.练习1: A 下面物质的分离方法不正确的是 ---------------- ( )
AC 单元二: 研究物质的 实验方法8、几种常见离子的检验应知2: 几种常见离子的检验方法 单元二: 研究物质的 实验方法应会: Cl- 、SO42-、CO32-、NH4+、Na+、K+离子的检验 现有一种化合物Z,它的阳离子可能是Na+、K+、NH4+、Cu2+、Ag+,阴离子可能是NO3—、SO42—、Cl—、CO32—,进行以下实验(填离子符号)
⑴做焰色反应,有黄色火焰,透过蓝色的钴玻璃观察,无紫色火焰. 肯定有 离子。
⑵取少量固体Z放入水中,得到无色溶液肯定无 离子。
⑶向Z溶液中加入酸化的AgNO3溶液,无明显变化,肯定无 __离子
⑷另取Z溶液,加入酸化的BaCl2溶液,无明显变化。肯定无 _离子
⑸另取Z溶液,加入NaOH溶液共热,无明显变化。肯定无 离子。
由上述实验事实,可推断化合物Z是 。练习2:Na+Cu2+Cl— CO32—SO42— Ag+NH4+NaNO3 物质的量浓度应知3: 物质的量浓度溶液 ,单位__________ . 单元二: 研究物质的 实验方法mol/L 或 mol·L-1 应会: 物质的量浓度溶液的配制方法 下面是配制500mL 0.2 mol/L KCl溶液的操作,请按要求填空:
(1)所需KCl的质量为 。
(2)称量过程中主要用到的仪器是 。
(3)将烧杯中的溶液沿 引流到 中,并用蒸馏水洗涤 烧杯2~3次,洗涤液要 ,并摇匀。
(4)加水至距刻度线 处,改用 加水,使液面的凹 液面正好与刻度线相切。
(5)在容量瓶中进行定容时,仰视刻度线,所配的溶液浓度将 (偏高、偏低、无影响)_________。练习3: 7.45 g天平 玻璃棒 500mL容量瓶 转移到容量瓶中 2~3 cm 胶头滴管 偏低 返回主页 单元二: 研究物质的 实验方法应知 应会 1: 物质的分离和提纯的方法 对不同的混合物能采用
不同的分离方法 2: 几种常见离子的检验方法 Cl- 、SO42-、CO32-、NH4+、
Na+、K+离子的检验3: 物质的量浓度溶液 物质的量浓度溶液
的配制方法10、原子结构A、Z、c、d、e各代表什么? A——代表质量数;
Z——代表核电荷数(质子数)
c——代表离子所带的电荷数
d——代表化合价
e——代表原子个数请指出Al、Al3+中所含的质子数和电子数。单元三: 人类对原子结构的认识 应知1: 构成原子的粒子有_____、_____、_____ .电子 质子 中子应会: 原子内各种粒子间的数量关系的计算 练习1 和Na+具有相同质子数和电子数的微粒是------------( )
A.NH4+ B. F- C. H2O D. NH3 A 某元素R的阳离子Rn+核外有x个电子,该元素的质量数为A,则该元素原子核内的中子数----------------------------( )
A. A-x-n B. A-x+n C. A+x-n D. A+x+nA 符号的每个字母的含义 原子结构示意图和离子结构示意图(另有专题) 单元三: 人类对原子结构的认识 应知2: B 练习2 单元三: 人类对原子结构的认识 应知 应会 1: 构成原子的粒子有
质子、中子和电子。 原子内各种粒子间的
数量关系的计算2: 符号的每个字母的含义原子结构示意图和
离子结构示意图(另有专题) 返回主页 作业 课后的讲义
A.碱性氧化物 七氧化二锰 Mn2O7
B.酸性氧化物 干冰 C0
C.酸 硫酸 H2O
D.盐 纯碱 Na2CO3D应知2: 化学反应的分类方法 单元一: 丰富多彩的化学物质应会: 能区分四种基本反应类型和氧化还原反应 练习2: C 氧化还原反应 非氧化还原反应 化合反应分解反应置
换
反
应复
分
解
反
应单元一: 丰富多彩的化学物质应知3: 化学物质的计量方法
和物理量的单位 ( 物质的量 mol ) 应会: 涉及物质的量的各种换算方法 (1) 关于质量的换算 _________ (2) 关于粒子数目的换算 _______ (3) 关于气体体积的换算 _______(4) 关于物质的量浓度的计算 ______物理量的单位: n - mol m - g M - g/mol N - 个 NA - mol-1V - L 单元一: 丰富多彩的化学物质练习3: 下列溶液中的Cl-浓度与50 mL 1 mol·L-1的AlCl3溶液中Cl-的浓度相等的是 ----------------------------------------------------( )
A.150 mL 1mol·L-1的NaCl? B.75 mL 2 mol·L-1的NH4Cl
C.150 mL 3 mol·L-1的KCl? D.75 mL 1 mol·L-1的CaCl2C 22.2 g某二价金属氯化物(ACl2)中含有0.4 mol Cl-,则ACl2的摩尔质量是______________;A的相对原子质量是__________;ACl2的化学式是___________。111g/mol40 CaCl2电解质电解质 强电解质: 弱电解质: (电离是一个可逆过程)在水溶液或融化状态下能导电的化合物。在水溶液和融化状态下都不能导电的化合物电解质 :非电解质强酸、强碱、盐 弱酸、 NH3.H2O、 H2O单元一: 丰富多彩的化学物质应知4: 分散系有______、_____和______ 3 种. 溶液浊液胶体电解质和非电解质的概念 应会: 会区别分散系的类型、会区别电解质和非电解质. 练习4: 用特殊的方法把固体加工到纳米级(1~100nm, 1nm=10-9m)的超细粉末粒子,然后制得纳米材料。下列分散系中的分散质的粒子直径和这种粒子具有相同的数量级的是 ----------------------------------------------------------------( )
A. 溶液 B. 悬浮液 C. 胶体 D. 乳浊液C 下列物质: ①氢氧化钠固体 ②水银 ③氯化氢气体 ④稀硫酸 ⑤二氧化碳气体 ⑥氨水 ⑦碳酸钠粉末 ⑧蔗糖晶体 ⑨熔融氯化钠 ⑩CuSO4·5H2O晶体
⑴上述状态下能导电的是:_____________
⑵属于电解质的是:________________
⑶属于非电解质的是:______________②④⑥⑨①③⑦⑨⑩⑤⑧返回主页 单元一: 丰富多彩的化学物质应知 : 根据物质的组成对物质进行分类应会:1. 物质的分类方法 2. 化学反应的分类方法能区分四种基本反应类型
和氧化还原反应3 化学物质的计量方法
和物理量的单位 涉及物质的量的各种换算方法 4: 分散系有溶液、浊液
和胶体 3 种电解质和非电解质的概念会区别分散系的类型会区别电解质和非电解质.7、物质的分离和提纯单元二: 研究物质的 实验方法应知1: 物质的分离和提纯的方法有: ______、______、
______、______、______、______ 6种.层析 过滤结晶萃取分液蒸馏应会: 对不同的混合物能采用不同的分离方法 常用仪器的使用 下列实验操作中错误的是 ------------------------------------- ( )
A.蒸发操作时,应将溶液中的水分完全蒸干后,才能停止加热
B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从
上口倒出.
D.萃取操作时,萃取剂与溶液中的溶剂不能互溶.练习1: A 下面物质的分离方法不正确的是 ---------------- ( )
AC 单元二: 研究物质的 实验方法8、几种常见离子的检验应知2: 几种常见离子的检验方法 单元二: 研究物质的 实验方法应会: Cl- 、SO42-、CO32-、NH4+、Na+、K+离子的检验 现有一种化合物Z,它的阳离子可能是Na+、K+、NH4+、Cu2+、Ag+,阴离子可能是NO3—、SO42—、Cl—、CO32—,进行以下实验(填离子符号)
⑴做焰色反应,有黄色火焰,透过蓝色的钴玻璃观察,无紫色火焰. 肯定有 离子。
⑵取少量固体Z放入水中,得到无色溶液肯定无 离子。
⑶向Z溶液中加入酸化的AgNO3溶液,无明显变化,肯定无 __离子
⑷另取Z溶液,加入酸化的BaCl2溶液,无明显变化。肯定无 _离子
⑸另取Z溶液,加入NaOH溶液共热,无明显变化。肯定无 离子。
由上述实验事实,可推断化合物Z是 。练习2:Na+Cu2+Cl— CO32—SO42— Ag+NH4+NaNO3 物质的量浓度应知3: 物质的量浓度溶液 ,单位__________ . 单元二: 研究物质的 实验方法mol/L 或 mol·L-1 应会: 物质的量浓度溶液的配制方法 下面是配制500mL 0.2 mol/L KCl溶液的操作,请按要求填空:
(1)所需KCl的质量为 。
(2)称量过程中主要用到的仪器是 。
(3)将烧杯中的溶液沿 引流到 中,并用蒸馏水洗涤 烧杯2~3次,洗涤液要 ,并摇匀。
(4)加水至距刻度线 处,改用 加水,使液面的凹 液面正好与刻度线相切。
(5)在容量瓶中进行定容时,仰视刻度线,所配的溶液浓度将 (偏高、偏低、无影响)_________。练习3: 7.45 g天平 玻璃棒 500mL容量瓶 转移到容量瓶中 2~3 cm 胶头滴管 偏低 返回主页 单元二: 研究物质的 实验方法应知 应会 1: 物质的分离和提纯的方法 对不同的混合物能采用
不同的分离方法 2: 几种常见离子的检验方法 Cl- 、SO42-、CO32-、NH4+、
Na+、K+离子的检验3: 物质的量浓度溶液 物质的量浓度溶液
的配制方法10、原子结构A、Z、c、d、e各代表什么? A——代表质量数;
Z——代表核电荷数(质子数)
c——代表离子所带的电荷数
d——代表化合价
e——代表原子个数请指出Al、Al3+中所含的质子数和电子数。单元三: 人类对原子结构的认识 应知1: 构成原子的粒子有_____、_____、_____ .电子 质子 中子应会: 原子内各种粒子间的数量关系的计算 练习1 和Na+具有相同质子数和电子数的微粒是------------( )
A.NH4+ B. F- C. H2O D. NH3 A 某元素R的阳离子Rn+核外有x个电子,该元素的质量数为A,则该元素原子核内的中子数----------------------------( )
A. A-x-n B. A-x+n C. A+x-n D. A+x+nA 符号的每个字母的含义 原子结构示意图和离子结构示意图(另有专题) 单元三: 人类对原子结构的认识 应知2: B 练习2 单元三: 人类对原子结构的认识 应知 应会 1: 构成原子的粒子有
质子、中子和电子。 原子内各种粒子间的
数量关系的计算2: 符号的每个字母的含义原子结构示意图和
离子结构示意图(另有专题) 返回主页 作业 课后的讲义
