硝酸的性质
图片预览



文档简介
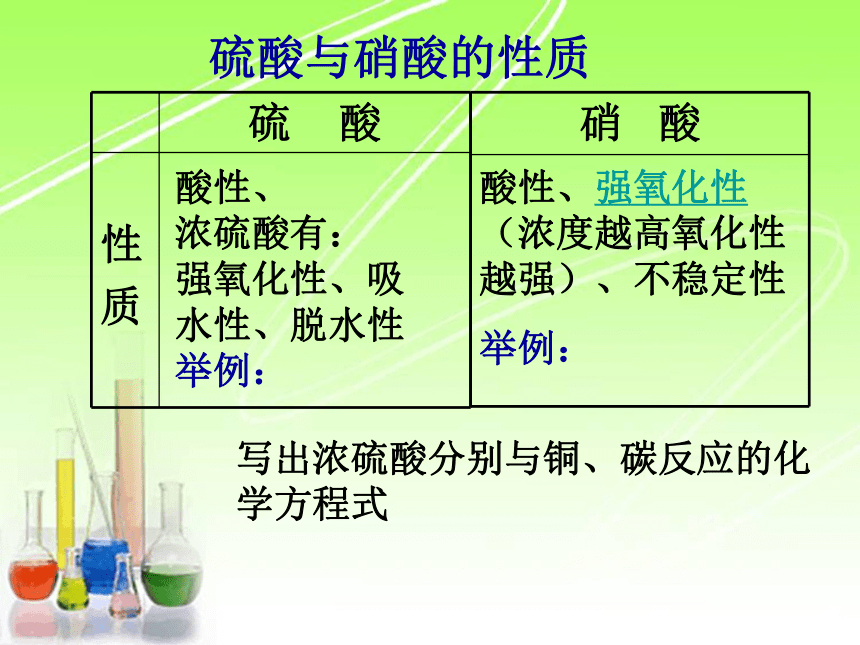
课件10张PPT。硝酸的性质酸性、
浓硫酸有:
强氧化性、吸水性、脱水性
举例:硫酸与硝酸的性质 酸性、强氧化性(浓度越高氧化性越强)、不稳定性
举例:写出浓硫酸分别与铜、碳反应的化学方程式1、铜与硝酸反应,硝酸表现出哪些性质?
2、得到相同的硝酸铜,二者消耗的硝酸的
物质的量之比是多少?被还原的硝酸的
物质的量之比是多少?
3、浓硝酸为什么会略显黄色?如何保存
硝酸? HNO3棕色瓶
避光
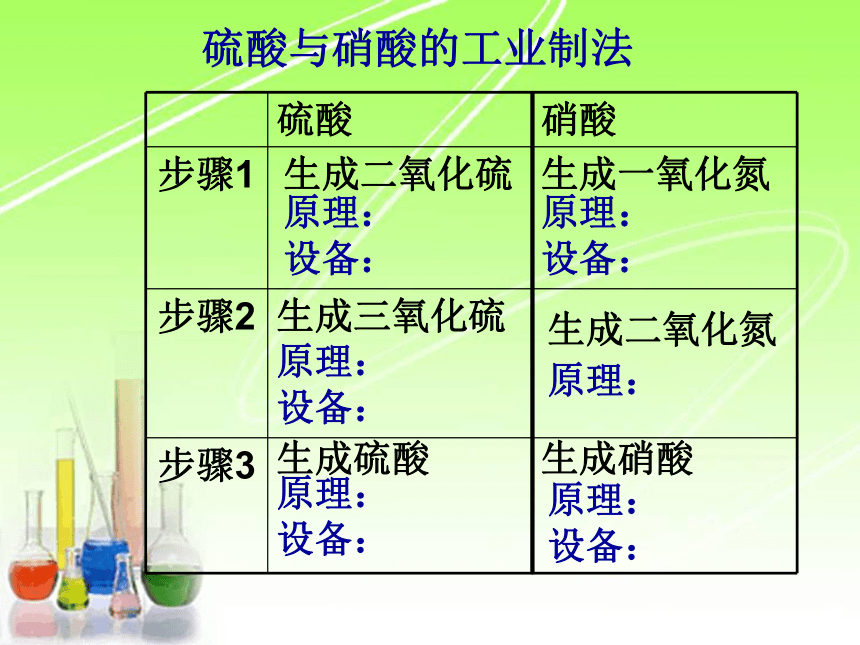
低温硫酸与硝酸的工业制法 生成二氧化硫生成三氧化硫生成硫酸原理:
设备:原理:
设备:原理:
设备:生成一氧化氮生成二氧化氮生成硝酸原理:
设备:原理:
设备:原理:练习:计算5.1吨液氨,理论上可氧化制得多少吨63%的成品硝酸? 氧化还原反应方程式的配平 原则:化合价升降法配平 练习:配平以下氧化还原反应的方程式
CO + Fe2O3 === Fe + CO2
Fe(OH)3 + ClO-+ OH- ===
FeO42-+ Cl-+ H2O小结:氮及其化合物的转化1、下列物质的溶液在长期放置的过程中因
被氧化而成黄色的是 ( )
A.浓硝酸 B.工业盐酸 C.氯化亚铁
D.浓溴水 E.KI溶液思考:CE2.某溶液能与Al作用产生H2,则该溶液可
能大量共存的离子组合是( )
A.Na+、NO3-、Fe2+、K+
B.Cl-、Na+、Fe2+、K+
C.K+、I-、NO3-、H+
D. NO3-、 Na+、NH4+、HCO3-B3、取三张蓝色石蕊试纸,放在玻璃片上,然后依次分别滴加85%的HNO3、98.3%的H2SO4和新制的饱和氯水,三张试纸最后呈现的颜色是( )
(A)白、红、白 (B)白、黑、红
(C)红、红、红 (D)白、黑、白D4、向盛有Fe(NO3)2溶液的试管中加入适量的稀盐酸,有什么现象?为什么?5、铜粉放入稀硫酸中,加热后无明显现象,但加入某盐一段时间后,发现铜粉质量减少,溶液呈蓝色,则该盐可能是( ) (A)FeCl3 (B)Na2CO3 (C)KNO3 (D)FeSO4 AC
浓硫酸有:
强氧化性、吸水性、脱水性
举例:硫酸与硝酸的性质 酸性、强氧化性(浓度越高氧化性越强)、不稳定性
举例:写出浓硫酸分别与铜、碳反应的化学方程式1、铜与硝酸反应,硝酸表现出哪些性质?
2、得到相同的硝酸铜,二者消耗的硝酸的
物质的量之比是多少?被还原的硝酸的
物质的量之比是多少?
3、浓硝酸为什么会略显黄色?如何保存
硝酸? HNO3棕色瓶
避光
低温硫酸与硝酸的工业制法 生成二氧化硫生成三氧化硫生成硫酸原理:
设备:原理:
设备:原理:
设备:生成一氧化氮生成二氧化氮生成硝酸原理:
设备:原理:
设备:原理:练习:计算5.1吨液氨,理论上可氧化制得多少吨63%的成品硝酸? 氧化还原反应方程式的配平 原则:化合价升降法配平 练习:配平以下氧化还原反应的方程式
CO + Fe2O3 === Fe + CO2
Fe(OH)3 + ClO-+ OH- ===
FeO42-+ Cl-+ H2O小结:氮及其化合物的转化1、下列物质的溶液在长期放置的过程中因
被氧化而成黄色的是 ( )
A.浓硝酸 B.工业盐酸 C.氯化亚铁
D.浓溴水 E.KI溶液思考:CE2.某溶液能与Al作用产生H2,则该溶液可
能大量共存的离子组合是( )
A.Na+、NO3-、Fe2+、K+
B.Cl-、Na+、Fe2+、K+
C.K+、I-、NO3-、H+
D. NO3-、 Na+、NH4+、HCO3-B3、取三张蓝色石蕊试纸,放在玻璃片上,然后依次分别滴加85%的HNO3、98.3%的H2SO4和新制的饱和氯水,三张试纸最后呈现的颜色是( )
(A)白、红、白 (B)白、黑、红
(C)红、红、红 (D)白、黑、白D4、向盛有Fe(NO3)2溶液的试管中加入适量的稀盐酸,有什么现象?为什么?5、铜粉放入稀硫酸中,加热后无明显现象,但加入某盐一段时间后,发现铜粉质量减少,溶液呈蓝色,则该盐可能是( ) (A)FeCl3 (B)Na2CO3 (C)KNO3 (D)FeSO4 AC
