硅
图片预览




文档简介
课件19张PPT。硅和二氧化硅问题:
1. 硅元素以什么形式存在于自然界中?硅元素主要存在于什么物质中?
2. 硅有几种同素异形体?分别是什么?
3. 为什么晶体硅的熔沸点高, 硬度大?
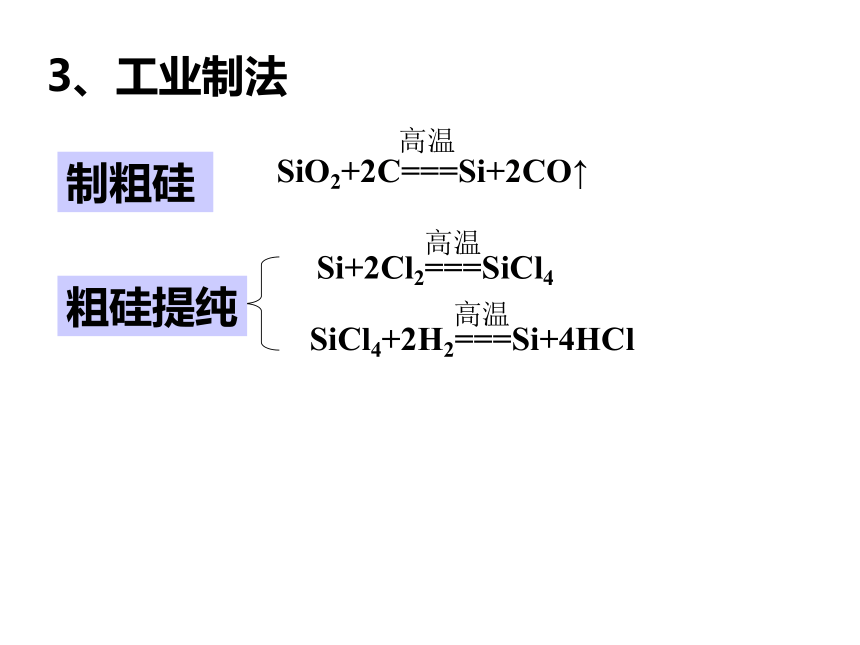
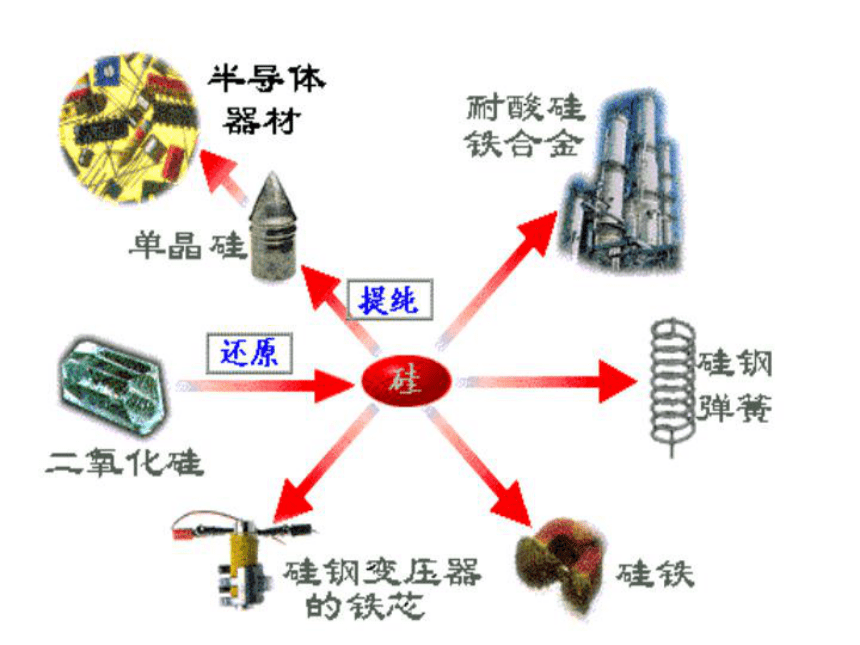
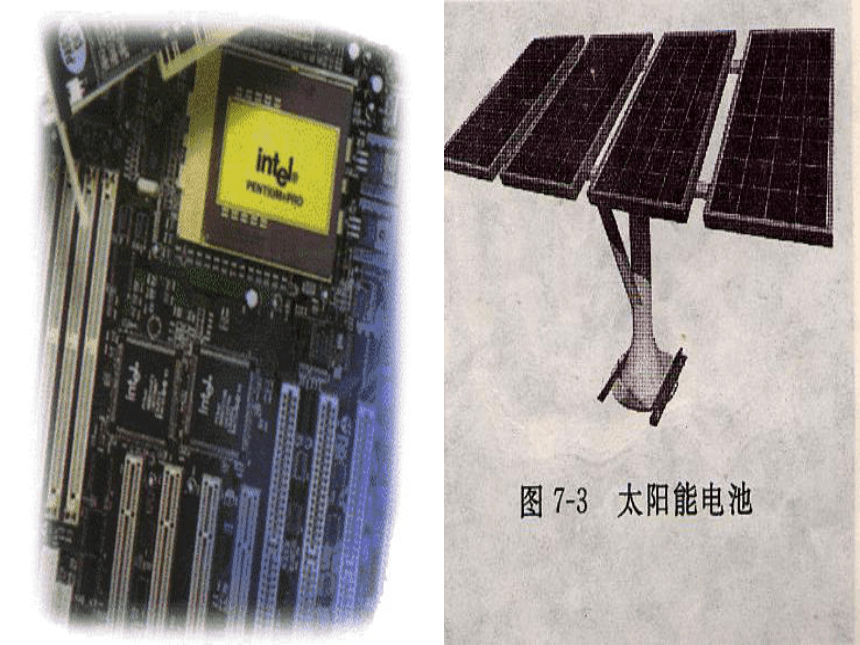
4. 硅的导电性怎么样?硅一、硅1、存在和状态(1)只有化合态,无游离态;在地壳中含量居第二位。(2)两种同素异形体:晶体硅和无定形硅。2、物理性质3、工业制法SiO2+2C===Si+2CO↑高温Si+2Cl2===SiCl4高温SiCl4+2H2===Si+4HCl高温制粗硅粗硅提纯4、用途高纯硅:半导体材料合金变压器铁芯(含硅4%的钢有导磁性)耐酸设备(含硅15%左右的钢有耐酸性)二、二氧化硅
2、物理性质:坚硬难熔的固体
天然二氧化硅叫硅石、石英砂。晶体二氧化硅叫石英、水晶,
1、存在和状态 3、化学性质:不活泼(1)酸性氧化物:不溶于水,也不与水反应(2)常温与氢氟酸、强碱反应2NaOH+SiO2==Na2SiO3+H2O不能用磨口玻璃塞盛碱性溶液,如NaOH、KOH、Na2CO3、Na2SiO3等溶液。用氢氟酸雕刻玻璃(3)高温时:SiO2+CaO===CaSiO3高温Na2CO3+SiO2===Na2SiO3+CO2↑高温CaCO3+SiO2====CaSiO3+CO2↑高温干态下物质间的反应规律: 高沸点物质(SiO2)制低沸点物质(CO2) SiO2+2C===Si+2CO↑高温Na+KCl===NaCl+K↑高温注意:工业上制玻璃4、用途
光导纤维
光学仪器
电子仪器
工艺品(水晶、玛瑙)
石英玻璃、玻璃原料
建筑材料注意:硅肺病(矽肺病),长期吸入SiO2粉尘。三、硅酸及硅酸盐不溶于水,白色粉末状固体,酸性比碳酸弱,不能使指示剂变色.Na2SiO3+CO2+2H2O===Na2CO3+H4SiO4↓H4SiO4===H2SiO3+H2O(易)(1)硅酸:白色胶状沉淀用可溶性硅酸盐与酸反应制硅酸①多数不溶于水(Na2SiO3易溶)②表示方法---------金属氧化物形式:高岭石Al2(Si2O5)(OH)4求KAlSi3Ox中X的值并将其写成金属氧化物的形式X=8K2O·Al2O3·6SiO2水玻璃:无色粘稠的溶液,是一种矿物胶,做粘合剂、防腐剂。Na2SiO3的水溶液(2)硅酸盐:MO·6SiO2·H2OAl2O3·2SiO2·2H2O硅酸钠 Na2SiO3Na2O·SiO2再见各种各样的水晶水晶千手观音和七星阵玛瑙制品玛瑙鼻烟壶石英砂,水晶和玛瑙
1. 硅元素以什么形式存在于自然界中?硅元素主要存在于什么物质中?
2. 硅有几种同素异形体?分别是什么?
3. 为什么晶体硅的熔沸点高, 硬度大?
4. 硅的导电性怎么样?硅一、硅1、存在和状态(1)只有化合态,无游离态;在地壳中含量居第二位。(2)两种同素异形体:晶体硅和无定形硅。2、物理性质3、工业制法SiO2+2C===Si+2CO↑高温Si+2Cl2===SiCl4高温SiCl4+2H2===Si+4HCl高温制粗硅粗硅提纯4、用途高纯硅:半导体材料合金变压器铁芯(含硅4%的钢有导磁性)耐酸设备(含硅15%左右的钢有耐酸性)二、二氧化硅
2、物理性质:坚硬难熔的固体
天然二氧化硅叫硅石、石英砂。晶体二氧化硅叫石英、水晶,
1、存在和状态 3、化学性质:不活泼(1)酸性氧化物:不溶于水,也不与水反应(2)常温与氢氟酸、强碱反应2NaOH+SiO2==Na2SiO3+H2O不能用磨口玻璃塞盛碱性溶液,如NaOH、KOH、Na2CO3、Na2SiO3等溶液。用氢氟酸雕刻玻璃(3)高温时:SiO2+CaO===CaSiO3高温Na2CO3+SiO2===Na2SiO3+CO2↑高温CaCO3+SiO2====CaSiO3+CO2↑高温干态下物质间的反应规律: 高沸点物质(SiO2)制低沸点物质(CO2) SiO2+2C===Si+2CO↑高温Na+KCl===NaCl+K↑高温注意:工业上制玻璃4、用途
光导纤维
光学仪器
电子仪器
工艺品(水晶、玛瑙)
石英玻璃、玻璃原料
建筑材料注意:硅肺病(矽肺病),长期吸入SiO2粉尘。三、硅酸及硅酸盐不溶于水,白色粉末状固体,酸性比碳酸弱,不能使指示剂变色.Na2SiO3+CO2+2H2O===Na2CO3+H4SiO4↓H4SiO4===H2SiO3+H2O(易)(1)硅酸:白色胶状沉淀用可溶性硅酸盐与酸反应制硅酸①多数不溶于水(Na2SiO3易溶)②表示方法---------金属氧化物形式:高岭石Al2(Si2O5)(OH)4求KAlSi3Ox中X的值并将其写成金属氧化物的形式X=8K2O·Al2O3·6SiO2水玻璃:无色粘稠的溶液,是一种矿物胶,做粘合剂、防腐剂。Na2SiO3的水溶液(2)硅酸盐:MO·6SiO2·H2OAl2O3·2SiO2·2H2O硅酸钠 Na2SiO3Na2O·SiO2再见各种各样的水晶水晶千手观音和七星阵玛瑙制品玛瑙鼻烟壶石英砂,水晶和玛瑙
