徐州市2007--2008学年度第一学期期末考试高二化学试题(选修)(江苏省徐州市)
文档属性
| 名称 | 徐州市2007--2008学年度第一学期期末考试高二化学试题(选修)(江苏省徐州市) |  | |
| 格式 | rar | ||
| 文件大小 | 202.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2008-02-02 17:46:00 | ||
图片预览



文档简介
徐州市2007——2008学年度第一学期期末考试
高二化学试题(选修)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 F 19 Na 23 Si 28 S 32 Cl 35.5 K 39 Fe 56 Cu 64 Ag 108
一、单项选择题:本题包括8小题,每小题3分,共计24分。每小题只有一个选项符合题意。
1.下列有机物的命名正确的是
A.CH3CH2C(CH3)2CH(C2H5)CH3:2—乙基—3,3—二甲基戊烷
B.HC≡C—CH2CH(CH3)—CH3:2—甲基—5—戊炔
C.CH3CHClCH2CHClCH2CH2Cl:2,4,6—三氯己烷
D.CH3CHOHCH2CHOHCHOHCH3:2,3,5—己三醇
2.下列叙述中不正确的是
A.牛油、纤维素、蛋白质都是高分子化合物
B.淀粉水解的最终产物是葡萄糖
C.棉花和人造丝的主要成分都是纤维素
D.浓硝酸和蛋白质发生反应可使皮肤呈黄色
3.下列说法中正确的是
A.乙烯的结构简式可以表示为CH2CH2
B.石油裂解可以得到氯乙烯
C.丙烯转化为聚丙烯符合绿色化学原子经济性要求
D.油脂都不能使溴的四氯化碳溶液褪色
4.某卤代烃C5H11Cl发生消去反应时,可以得到两种烯烃,则该卤代烃的结构简式可能为
5.下列说法中正确的是
A.甲苯、二甲苯都属于苯的同系物,依据是这两种物质分子中均含有甲基
B.醇类的官能团是跟烃分子中饱和碳原子直接相连的羟基
C.醇类和酚类具有相同的官能团,因而具有相同的化学性质
D.甲醇、乙二醇、甘油都属于醇,依据是这三种物质分子中均含有饱和烃基
6.分子式为C8H16O2的有机物A,它能在酸性条件下水解生成B和C,在一定条件下B能转化成C。下列说法正确的是
A.有机物B的红外线谱图出现C=O键的振动吸收
B.有机物C的核磁共振氢谱有可能是三个吸收峰
C.有机物A的结构可能有4种
D.有机物C可以发生缩聚反应
7.半导体工业用石英砂做原料通过以下三个主要反应生产纯硅:
则生产56.00 g纯硅的反应热为
A.600.20 kJ·mol—1 B.+1200. 40 kJ·mol—1
C.-1965.08 kJ·mol—1 D.-1200. 40 kJ·mol—1
8.下列叙述正确的是
A.已知2H2(g) + O2(g)=2H2O(l) △H =-571.6 kJ·mol—1,则氢气的燃烧热为285.8 kJ·mol—1
B.已知C(石墨,s)=C(金刚石,s) △H>0,则金刚石比石墨稳定
C.已知含20.0 g NaOH的稀NaOH溶液与稀盐酸完全中和可放热28.7 kJ,则该反应的热化学方程式为:NaOH(l) + HCl (l)=NaCl (l) + H2O(l) △H=-57.4 kJ·mol—1
D.己知2C(s) + 2O2(g) =2CO2(g) △H1,2C(s) + O2(g) =2CO(g) △H2,则△H1>△H2
二、不定项选择题:本题包括6小题,每小题4分,共24分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个,该小题就为0分。
9.下列说法正确的是
A.所有烷烃分子中均含有碳碳单键
B.苯及其同系物、醇类和羧酸都能发生取代反应
C.大气臭氧层的破坏主要与氟氯烃的氟原子有关
D.氨基酸与酸、碱都能发生反应生成盐
10.设NA为阿伏加德罗常数,下列叙述不正确的是
A.标准状况下,1 L庚烷完全燃烧所生成的气态分子数不是
B.28 g丙烯中含有的共用电子对数为6NA
C.0.5 mol 1, 3—丁二烯分子中含有C=C双键数为NA
D.1 mol碳正离子(CH3+)所含的电子总数为9NA
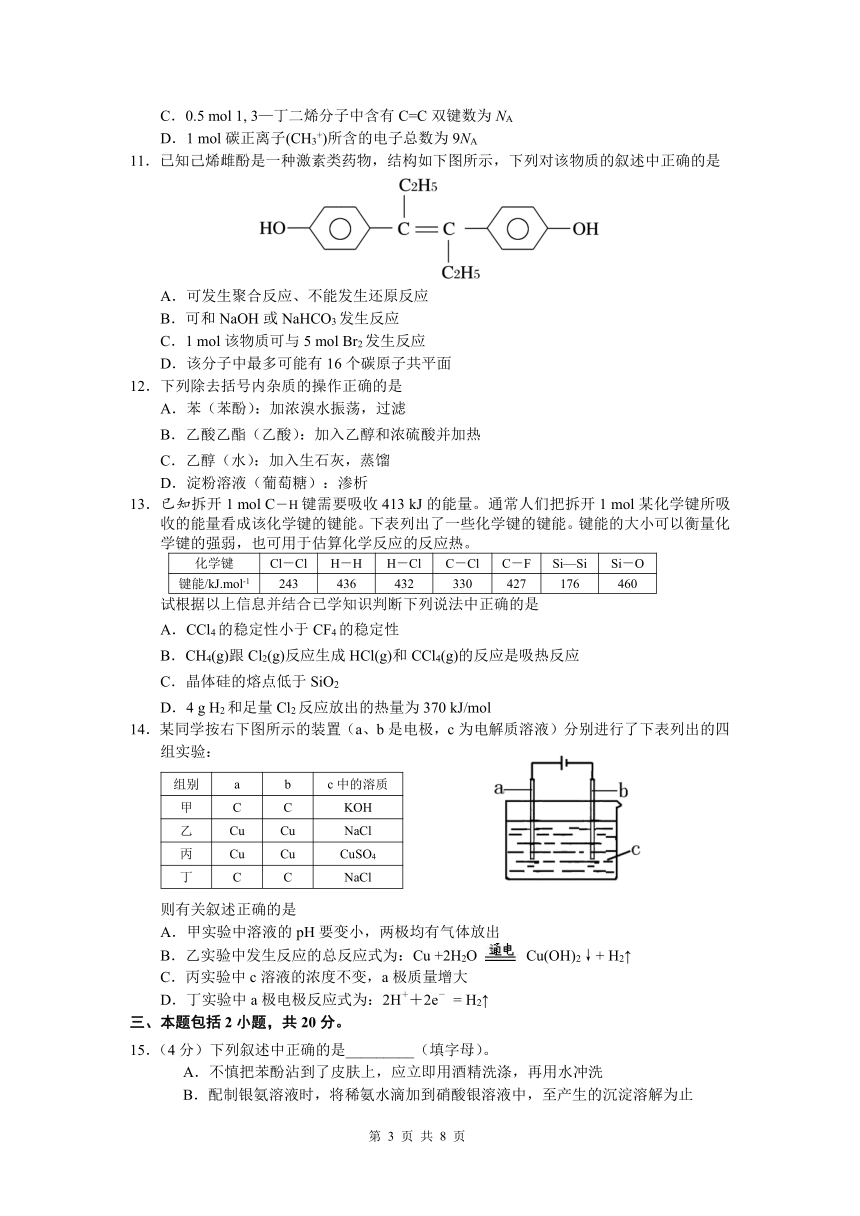
11.已知己烯雌酚是一种激素类药物,结构如下图所示,下列对该物质的叙述中正确的是
A.可发生聚合反应、不能发生还原反应
B.可和NaOH或NaHCO3发生反应
C.1 mol该物质可与5 mol Br2发生反应
D.该分子中最多可能有16个碳原子共平面
12.下列除去括号内杂质的操作正确的是
A.苯(苯酚):加浓溴水振荡,过滤
B.乙酸乙酯(乙酸):加入乙醇和浓硫酸并加热
C.乙醇(水):加入生石灰,蒸馏
D.淀粉溶液(葡萄糖):渗析
13.已知拆开1 mol C-H键需要吸收413 kJ的能量。通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。下表列出了一些化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热。
化学键
Cl-Cl
H-H
H-Cl
C-Cl
C-F
Si—Si
Si-O
键能/kJ.mol-1
243
436
432
330
427
176
460
试根据以上信息并结合已学知识判断下列说法中正确的是
A.CCl4的稳定性小于CF4的稳定性
B.CH4(g)跟Cl2(g)反应生成HCl(g)和CCl4(g)的反应是吸热反应
C.晶体硅的熔点低于SiO2
D.4 g H2和足量Cl2反应放出的热量为370 kJ/mol
14.某同学按右下图所示的装置(a、b是电极,c为电解质溶液)分别进行了下表列出的四组实验:
组别
a
b
c中的溶质
甲
C
C
KOH
乙
Cu
Cu
NaCl
丙
Cu
Cu
CuSO4
丁
C
C
NaCl
则有关叙述正确的是
A.甲实验中溶液的pH要变小,两极均有气体放出
B.乙实验中发生反应的总反应式为:Cu +2H2O Cu(OH)2↓+ H2↑
C.丙实验中c溶液的浓度不变,a极质量增大
D.丁实验中a极电极反应式为:2H++2e- = H2↑
三、本题包括2小题,共20分。
15.(4分)下列叙述中正确的是_________(填字母)。
A.不慎把苯酚沾到了皮肤上,应立即用酒精洗涤,再用水冲洗
B.配制银氨溶液时,将稀氨水滴加到硝酸银溶液中,至产生的沉淀溶解为止
C.淀粉水解后,直接滴加新制氢氧化铜悬浊液并加热检验水解产物中的葡萄糖
D.在苯和液溴的混合物中加少量铁粉即可得到溴苯
E.向溴乙烷跟烧碱反应后的混合液中滴加硝酸银溶液,可以检验水解生成的溴离子
F.实验室进行石油的蒸馏、乙酸乙酯的水解、中和反应反应热的测定实验时均需要使用温度计
16.(16分)为探究乙烯的制取及乙烯和溴水反应的有关问题,甲、乙、丙三同学进行了如下实验活动,请你参与他们的活动并回答相关问题。
(1)甲设计了如右下图所示的实验装置,并进行实验。当温度升至170℃左右时,有大量气体产生,溴水的颜色迅速褪去。甲认为达到了实验目的。请写出甲实验中两个主要反应的化学方程式: 。烧瓶中除加入浓硫酸和无水乙醇外,还需要加入 。装置中氢氧化钠溶液的作用是 。
(2)乙考察了甲的实验过程,发现下
列两个问题:
①当温度升到160℃左右时混合液
呈黑色,在超过170℃后生成气体
的速率明显加快并有刺激性气味
的气体生成。则乙同学观察到的黑
色物质是_ ___________,刺激性
气味的气体是_________。
②当一定量的溴水中的溴全部褪色时,所消耗乙醇和浓硫酸混合液的量比正常情况下超过许多。如果装置的气密性没有问题,则其可能的原因是_________。
(3)丙为验证生成的气体与溴水的反应是加成而不是取代,提出甲的装置必须先作“在A、B之间增加一个装有烧碱溶液的洗气装置后再开始加热”的改进,然后用pH试纸来测试反应后B中溶液的酸性即可验证,则丙提出的增加一个洗气装置的理由是 ,此时用pH试纸来进行实验能够达到实验目的的原因是 。丙认为按甲的装置进行实验,烧瓶内混合液在实验过程中可能还有另外两种气体产生,这两种气体是 。
四、本题包括2小题,共14分。
17.(6分)已知尼泊金酸的结构简式为: ,其酸性比乙酸强。
据此请回答:
(1)尼泊金酸的分子式为__________。
(2)写出在一定条件下尼泊金酸与金属钠反应的化学方程式________;将此反应生成的有机物溶于适量的水中形成溶液,向该溶液中通入足量的二氧化碳,则这时又可生成的有机物的结构简式为_____ __。
18.(8分)已知在一定条件下,醇A跟羧酸B发生酯化反应可以得到酯C,氧化A可得到B。又知C的分子式为C14H12O2,且C不能使溴的四氯化碳溶液褪色。请回答:
(1)C的烃基中是否含有碳碳双键或碳碳叁键?答: 。(填“含有”或“不含有”)
(2)B的结构简式为 。
(3)A的同分异构体有多种,请按下列要求各写出其一种有关同分异构体的结构简式:
①可以跟氢氧化钠反应的同分异构体 。
②分子结构中没有羟基的同分异构体 。
五、本题包括1小题,共12分。
19.(12分)右图是一种化学能与电能相互转化的装置。
已知:①甲池的总反应式为:
2CH3OH +3O2 + 4KOH 2K2CO3 + 6H2O
②甲池中盛有200 mL 0.2 mol/L的氢氧化钾溶液,
两电极均为铂电极。
请回答下列问题:
(1)甲池是 装置,通入O2的电极上的电
极反应式是 。
(2)乙池是 装置,铁电极上的电极反应式
是 。乙池中反应的化学方程式为 。
(3)当乙池中铁电极的质量增加9.72 g时,则甲池溶液中的OH 的物质的量浓度为 __ ___。(设甲中溶液的体积没有变化)
六、本题包括1小题,共14分。
20.(14分)已知:
Ⅰ. (X表示卤素原子,下同)
Ⅱ.
Ⅲ.当一取代苯继续发生取代反应时,再引进的取代基受到原取代基的影响而取代邻位、对位或间位。可以使再引进的取代基进入它的邻位、对位的常见取代基有:-CH3、
-NH2、-X等;可以使再引进的取代基进入它的间位的常见取代基有:-COOH、
-NO2等。
又知有机物F的商品名称为“敌稗(Propanil)”,是一种优良的水稻除草剂,E呈酸性,现通过下列合成路线制备F:
请结合以上信息,回答下列问题:
(1)A的结构简式为 。反应②条件为 。
(2)反应⑤的化学方程式为 ;该反应的反应类型为 。
(3)若只考虑苯环上的位置异构,则C的异构体有 种。
(4)请你设计D→E(C3H6O2)的合成反应流程图(有机物写结构简式)。
要求:①合成过程中无机试剂任选、有机原料的碳原子不超过2个;②合成反应流程图表示方法示例如下:
七、本题包括1小题,共12分。
21.(12分)由碳、氢、氧三种元素组成的某有机物分子中共含有13个原子,其原子核外共有40个电子,l mol该有机物在氧气中完全燃烧时需消耗5.5 mol O2。请回答:
(1)试求出该有机物的分子式。
(2)若该有机物可使溴水褪色,且分子中不含有甲基,也不能发生银镜反应,取0.1 mol该有机物与足量钠反应,能产生1.12 L H2(标准状况),则该有机物的结构简式可能是 ;该有机物在一定条件下发生聚合反应的化学方程式是 。
(3)若该有机物能发生银镜反应,且分子中只含有一个甲基,则其结构简式是 。
(4)若该有机物的结构呈环状,且既不含甲基又不含羟基,则其键线式是 。
徐州市2007——2008学年度第一学期期末考试
高二化学试题(选修)参考答案和评分标准
说明:学生解答主观性试题时,使用与本答案不同的其它合理答案的也给分。
一、共24分。每小题3分。每小题只有一个选项符合题意。
1.D 2.A 3.C 4.C 5.B 6.B 7.D 8.A
二、共24分。每小题4分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个,该小题就为0分。
9.BD 10.D 11.C 12.CD 13.AC 14.B
三、共20分。第15题4分。第16题16分,第(1)、(3)题各6分,第(2)题4分。
15.ADF
16.(1)CH3CH2OH CH2=CH2↑ + H2O
CH2=CH2 + Br2 Br-CH2CH2-Br
碎瓷片(或沸石) 吸收尾气,防止污染
(2)①C SO2
②一是实验中乙醇和浓硫酸的混合液没迅速达到170℃(或控温不当),二是乙烯发生(或通过溴水)速率过快,三是乙烯中混有一定量的SO2等
(3)除去SO2等酸性气体 如起取代反应则有HBr生成,溶液酸性增强
CO、CO2等
四、共14分。第17题6分,每空各2分。第18题8分,每空各2分。
17.(1)C7H6O3
(2)
18.(1)不含有
(2)
(3)①
②
五、共12分。第19题12分,每空各2分。
19.(1)原电池 O2 + 4e- + 2H2O = 4OH―
(2)电解池 Ag+ + e— = Ag
4AgNO4 +2H2O 4Ag + O2↑+ 4HNO3
(3)0.05 mol/L
六、共14分。第20题14分,第(1)、(2)、(4)题各4分,第(3)题2分。
20.(1)
(2)
(3)6
(4)
七、共12分。第21题12分,第(1)题4分,其余每空2分。
21.(1)C4H8O
(2)CH2=CHCH2CH2OH
(3)CH3CH2CH2CHO
(4)
高二化学试题(选修)
可能用到的相对原子质量:H 1 C 12 N 14 O 16 F 19 Na 23 Si 28 S 32 Cl 35.5 K 39 Fe 56 Cu 64 Ag 108
一、单项选择题:本题包括8小题,每小题3分,共计24分。每小题只有一个选项符合题意。
1.下列有机物的命名正确的是
A.CH3CH2C(CH3)2CH(C2H5)CH3:2—乙基—3,3—二甲基戊烷
B.HC≡C—CH2CH(CH3)—CH3:2—甲基—5—戊炔
C.CH3CHClCH2CHClCH2CH2Cl:2,4,6—三氯己烷
D.CH3CHOHCH2CHOHCHOHCH3:2,3,5—己三醇
2.下列叙述中不正确的是
A.牛油、纤维素、蛋白质都是高分子化合物
B.淀粉水解的最终产物是葡萄糖
C.棉花和人造丝的主要成分都是纤维素
D.浓硝酸和蛋白质发生反应可使皮肤呈黄色
3.下列说法中正确的是
A.乙烯的结构简式可以表示为CH2CH2
B.石油裂解可以得到氯乙烯
C.丙烯转化为聚丙烯符合绿色化学原子经济性要求
D.油脂都不能使溴的四氯化碳溶液褪色
4.某卤代烃C5H11Cl发生消去反应时,可以得到两种烯烃,则该卤代烃的结构简式可能为
5.下列说法中正确的是
A.甲苯、二甲苯都属于苯的同系物,依据是这两种物质分子中均含有甲基
B.醇类的官能团是跟烃分子中饱和碳原子直接相连的羟基
C.醇类和酚类具有相同的官能团,因而具有相同的化学性质
D.甲醇、乙二醇、甘油都属于醇,依据是这三种物质分子中均含有饱和烃基
6.分子式为C8H16O2的有机物A,它能在酸性条件下水解生成B和C,在一定条件下B能转化成C。下列说法正确的是
A.有机物B的红外线谱图出现C=O键的振动吸收
B.有机物C的核磁共振氢谱有可能是三个吸收峰
C.有机物A的结构可能有4种
D.有机物C可以发生缩聚反应
7.半导体工业用石英砂做原料通过以下三个主要反应生产纯硅:
则生产56.00 g纯硅的反应热为
A.600.20 kJ·mol—1 B.+1200. 40 kJ·mol—1
C.-1965.08 kJ·mol—1 D.-1200. 40 kJ·mol—1
8.下列叙述正确的是
A.已知2H2(g) + O2(g)=2H2O(l) △H =-571.6 kJ·mol—1,则氢气的燃烧热为285.8 kJ·mol—1
B.已知C(石墨,s)=C(金刚石,s) △H>0,则金刚石比石墨稳定
C.已知含20.0 g NaOH的稀NaOH溶液与稀盐酸完全中和可放热28.7 kJ,则该反应的热化学方程式为:NaOH(l) + HCl (l)=NaCl (l) + H2O(l) △H=-57.4 kJ·mol—1
D.己知2C(s) + 2O2(g) =2CO2(g) △H1,2C(s) + O2(g) =2CO(g) △H2,则△H1>△H2
二、不定项选择题:本题包括6小题,每小题4分,共24分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个,该小题就为0分。
9.下列说法正确的是
A.所有烷烃分子中均含有碳碳单键
B.苯及其同系物、醇类和羧酸都能发生取代反应
C.大气臭氧层的破坏主要与氟氯烃的氟原子有关
D.氨基酸与酸、碱都能发生反应生成盐
10.设NA为阿伏加德罗常数,下列叙述不正确的是
A.标准状况下,1 L庚烷完全燃烧所生成的气态分子数不是
B.28 g丙烯中含有的共用电子对数为6NA
C.0.5 mol 1, 3—丁二烯分子中含有C=C双键数为NA
D.1 mol碳正离子(CH3+)所含的电子总数为9NA
11.已知己烯雌酚是一种激素类药物,结构如下图所示,下列对该物质的叙述中正确的是
A.可发生聚合反应、不能发生还原反应
B.可和NaOH或NaHCO3发生反应
C.1 mol该物质可与5 mol Br2发生反应
D.该分子中最多可能有16个碳原子共平面
12.下列除去括号内杂质的操作正确的是
A.苯(苯酚):加浓溴水振荡,过滤
B.乙酸乙酯(乙酸):加入乙醇和浓硫酸并加热
C.乙醇(水):加入生石灰,蒸馏
D.淀粉溶液(葡萄糖):渗析
13.已知拆开1 mol C-H键需要吸收413 kJ的能量。通常人们把拆开1 mol某化学键所吸收的能量看成该化学键的键能。下表列出了一些化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热。
化学键
Cl-Cl
H-H
H-Cl
C-Cl
C-F
Si—Si
Si-O
键能/kJ.mol-1
243
436
432
330
427
176
460
试根据以上信息并结合已学知识判断下列说法中正确的是
A.CCl4的稳定性小于CF4的稳定性
B.CH4(g)跟Cl2(g)反应生成HCl(g)和CCl4(g)的反应是吸热反应
C.晶体硅的熔点低于SiO2
D.4 g H2和足量Cl2反应放出的热量为370 kJ/mol
14.某同学按右下图所示的装置(a、b是电极,c为电解质溶液)分别进行了下表列出的四组实验:
组别
a
b
c中的溶质
甲
C
C
KOH
乙
Cu
Cu
NaCl
丙
Cu
Cu
CuSO4
丁
C
C
NaCl
则有关叙述正确的是
A.甲实验中溶液的pH要变小,两极均有气体放出
B.乙实验中发生反应的总反应式为:Cu +2H2O Cu(OH)2↓+ H2↑
C.丙实验中c溶液的浓度不变,a极质量增大
D.丁实验中a极电极反应式为:2H++2e- = H2↑
三、本题包括2小题,共20分。
15.(4分)下列叙述中正确的是_________(填字母)。
A.不慎把苯酚沾到了皮肤上,应立即用酒精洗涤,再用水冲洗
B.配制银氨溶液时,将稀氨水滴加到硝酸银溶液中,至产生的沉淀溶解为止
C.淀粉水解后,直接滴加新制氢氧化铜悬浊液并加热检验水解产物中的葡萄糖
D.在苯和液溴的混合物中加少量铁粉即可得到溴苯
E.向溴乙烷跟烧碱反应后的混合液中滴加硝酸银溶液,可以检验水解生成的溴离子
F.实验室进行石油的蒸馏、乙酸乙酯的水解、中和反应反应热的测定实验时均需要使用温度计
16.(16分)为探究乙烯的制取及乙烯和溴水反应的有关问题,甲、乙、丙三同学进行了如下实验活动,请你参与他们的活动并回答相关问题。
(1)甲设计了如右下图所示的实验装置,并进行实验。当温度升至170℃左右时,有大量气体产生,溴水的颜色迅速褪去。甲认为达到了实验目的。请写出甲实验中两个主要反应的化学方程式: 。烧瓶中除加入浓硫酸和无水乙醇外,还需要加入 。装置中氢氧化钠溶液的作用是 。
(2)乙考察了甲的实验过程,发现下
列两个问题:
①当温度升到160℃左右时混合液
呈黑色,在超过170℃后生成气体
的速率明显加快并有刺激性气味
的气体生成。则乙同学观察到的黑
色物质是_ ___________,刺激性
气味的气体是_________。
②当一定量的溴水中的溴全部褪色时,所消耗乙醇和浓硫酸混合液的量比正常情况下超过许多。如果装置的气密性没有问题,则其可能的原因是_________。
(3)丙为验证生成的气体与溴水的反应是加成而不是取代,提出甲的装置必须先作“在A、B之间增加一个装有烧碱溶液的洗气装置后再开始加热”的改进,然后用pH试纸来测试反应后B中溶液的酸性即可验证,则丙提出的增加一个洗气装置的理由是 ,此时用pH试纸来进行实验能够达到实验目的的原因是 。丙认为按甲的装置进行实验,烧瓶内混合液在实验过程中可能还有另外两种气体产生,这两种气体是 。
四、本题包括2小题,共14分。
17.(6分)已知尼泊金酸的结构简式为: ,其酸性比乙酸强。
据此请回答:
(1)尼泊金酸的分子式为__________。
(2)写出在一定条件下尼泊金酸与金属钠反应的化学方程式________;将此反应生成的有机物溶于适量的水中形成溶液,向该溶液中通入足量的二氧化碳,则这时又可生成的有机物的结构简式为_____ __。
18.(8分)已知在一定条件下,醇A跟羧酸B发生酯化反应可以得到酯C,氧化A可得到B。又知C的分子式为C14H12O2,且C不能使溴的四氯化碳溶液褪色。请回答:
(1)C的烃基中是否含有碳碳双键或碳碳叁键?答: 。(填“含有”或“不含有”)
(2)B的结构简式为 。
(3)A的同分异构体有多种,请按下列要求各写出其一种有关同分异构体的结构简式:
①可以跟氢氧化钠反应的同分异构体 。
②分子结构中没有羟基的同分异构体 。
五、本题包括1小题,共12分。
19.(12分)右图是一种化学能与电能相互转化的装置。
已知:①甲池的总反应式为:
2CH3OH +3O2 + 4KOH 2K2CO3 + 6H2O
②甲池中盛有200 mL 0.2 mol/L的氢氧化钾溶液,
两电极均为铂电极。
请回答下列问题:
(1)甲池是 装置,通入O2的电极上的电
极反应式是 。
(2)乙池是 装置,铁电极上的电极反应式
是 。乙池中反应的化学方程式为 。
(3)当乙池中铁电极的质量增加9.72 g时,则甲池溶液中的OH 的物质的量浓度为 __ ___。(设甲中溶液的体积没有变化)
六、本题包括1小题,共14分。
20.(14分)已知:
Ⅰ. (X表示卤素原子,下同)
Ⅱ.
Ⅲ.当一取代苯继续发生取代反应时,再引进的取代基受到原取代基的影响而取代邻位、对位或间位。可以使再引进的取代基进入它的邻位、对位的常见取代基有:-CH3、
-NH2、-X等;可以使再引进的取代基进入它的间位的常见取代基有:-COOH、
-NO2等。
又知有机物F的商品名称为“敌稗(Propanil)”,是一种优良的水稻除草剂,E呈酸性,现通过下列合成路线制备F:
请结合以上信息,回答下列问题:
(1)A的结构简式为 。反应②条件为 。
(2)反应⑤的化学方程式为 ;该反应的反应类型为 。
(3)若只考虑苯环上的位置异构,则C的异构体有 种。
(4)请你设计D→E(C3H6O2)的合成反应流程图(有机物写结构简式)。
要求:①合成过程中无机试剂任选、有机原料的碳原子不超过2个;②合成反应流程图表示方法示例如下:
七、本题包括1小题,共12分。
21.(12分)由碳、氢、氧三种元素组成的某有机物分子中共含有13个原子,其原子核外共有40个电子,l mol该有机物在氧气中完全燃烧时需消耗5.5 mol O2。请回答:
(1)试求出该有机物的分子式。
(2)若该有机物可使溴水褪色,且分子中不含有甲基,也不能发生银镜反应,取0.1 mol该有机物与足量钠反应,能产生1.12 L H2(标准状况),则该有机物的结构简式可能是 ;该有机物在一定条件下发生聚合反应的化学方程式是 。
(3)若该有机物能发生银镜反应,且分子中只含有一个甲基,则其结构简式是 。
(4)若该有机物的结构呈环状,且既不含甲基又不含羟基,则其键线式是 。
徐州市2007——2008学年度第一学期期末考试
高二化学试题(选修)参考答案和评分标准
说明:学生解答主观性试题时,使用与本答案不同的其它合理答案的也给分。
一、共24分。每小题3分。每小题只有一个选项符合题意。
1.D 2.A 3.C 4.C 5.B 6.B 7.D 8.A
二、共24分。每小题4分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个,该小题就为0分。
9.BD 10.D 11.C 12.CD 13.AC 14.B
三、共20分。第15题4分。第16题16分,第(1)、(3)题各6分,第(2)题4分。
15.ADF
16.(1)CH3CH2OH CH2=CH2↑ + H2O
CH2=CH2 + Br2 Br-CH2CH2-Br
碎瓷片(或沸石) 吸收尾气,防止污染
(2)①C SO2
②一是实验中乙醇和浓硫酸的混合液没迅速达到170℃(或控温不当),二是乙烯发生(或通过溴水)速率过快,三是乙烯中混有一定量的SO2等
(3)除去SO2等酸性气体 如起取代反应则有HBr生成,溶液酸性增强
CO、CO2等
四、共14分。第17题6分,每空各2分。第18题8分,每空各2分。
17.(1)C7H6O3
(2)
18.(1)不含有
(2)
(3)①
②
五、共12分。第19题12分,每空各2分。
19.(1)原电池 O2 + 4e- + 2H2O = 4OH―
(2)电解池 Ag+ + e— = Ag
4AgNO4 +2H2O 4Ag + O2↑+ 4HNO3
(3)0.05 mol/L
六、共14分。第20题14分,第(1)、(2)、(4)题各4分,第(3)题2分。
20.(1)
(2)
(3)6
(4)
七、共12分。第21题12分,第(1)题4分,其余每空2分。
21.(1)C4H8O
(2)CH2=CHCH2CH2OH
(3)CH3CH2CH2CHO
(4)
同课章节目录
