燃料燃烧释放的热量(浙江省舟山市)
图片预览










文档简介
课件30张PPT。第二单元 化学反应中的热量碧莲中学 罗正将
2007.4.10(第二课时)三、热化学方程式书写热化学方程式注意事项:
(1)反应物和生成物要标明其聚集状态,用g、l、s分别代表气态、液态、固态。
(2)方程式右端用△H 标明恒压条件下反应放出或吸收的热量,放热为负,吸热为正。
表示化学反应中放出或吸收的热量的化学方程式。(3)热化学方程式中各物质前的化学计量数不表示分子个数,只表示物质的量,因此可以是整数或分数。
(4)对于相同物质的反应,当化学计量数不同时,其△H 也不同,即△H 的值与计量数成正比。
(5)物质的状态不同,其△H 也不同。
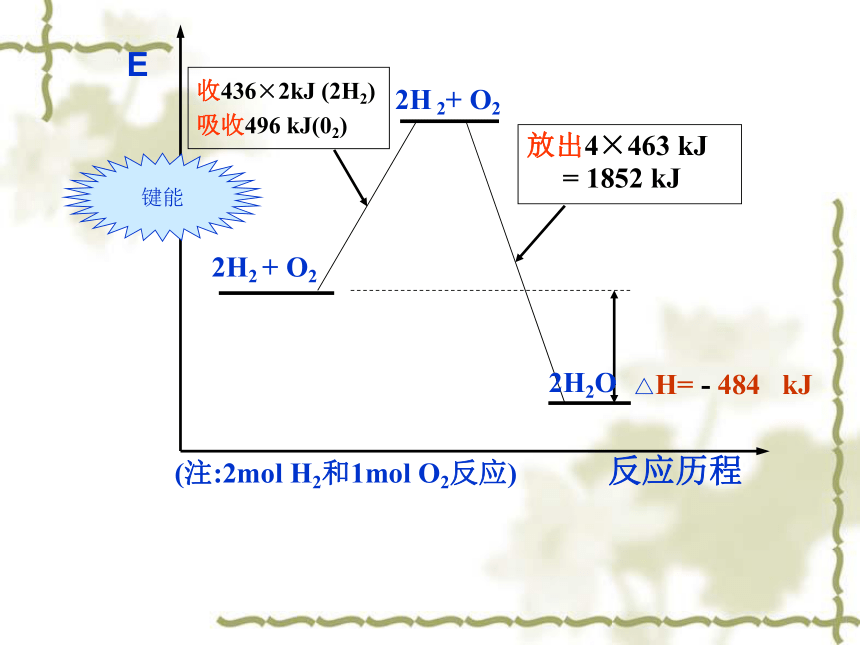
① 2H2(g) + O2 (g) = 2H2O( l ) △H = -571.6kJmol-1② H2(g) +1/2 O2 (g) = H2O( l ) △H = -285.8kJmol-1③ H2(g) + 1/2 O2 (g) = H2O( g) △H = -241.8kJmol-1你能解释氢气和氯气反应放热的道理吗? 交流与讨论:根据键能,你能计算2mol H2和1mol O2反应,生成2molH2O气体放出的热量吗?E反应历程△H= - 484 kJ收436×2kJ (2H2)
吸收496 kJ(02)放出4×463 kJ
= 1852 kJ(注:2mol H2和1mol O2反应) 键能二、反应热
化学反应过程中放出或吸收的热量
用△H表示,单位:kJ·mol-1
△H<0时,为放热反应;
△H>0时,为吸热反应。
2H2 (g) + O2 (g) = 2H20(l) △H= -484kJ·mol-1 燃烧中的热量变化化学反应根据能量
变化情况放热反应吸热反应1、燃烧中的能量变化2、燃烧中能量变化的实质键形成放热反应物键断裂吸热生成物一、燃料的燃烧1、燃烧:可燃物与氧气发生的发光、 发热的剧烈的化学反应。
实例:煤、石油、天然气的燃烧。2、燃烧的条件A、与氧气接触
B、达到着火点质量相同的不同燃料,完全燃烧后放出的热量不相等。我国目前使用的主要燃料是什么?燃烧值或热值来表示3、常见的燃料
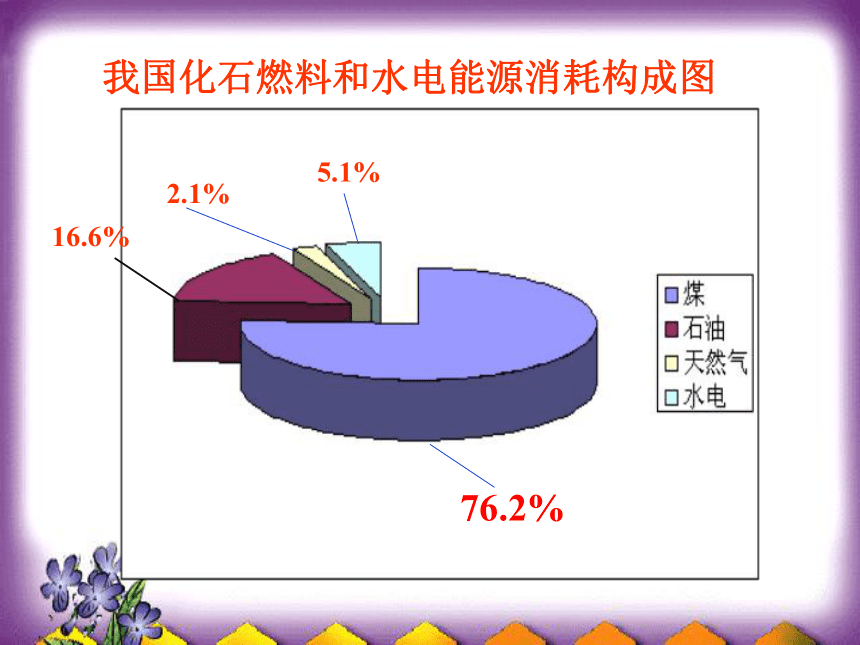
煤、石油、天然气-----化石燃料4、如何提高燃料的使用效率A、防止环境污染、发展洁净煤技术 B、提高热效率 C、开发高能清洁能源 D、开发综合利用煤的新技术16.6%2.1%5.1%76.2%我国化石燃料和水电能源消耗构成图大量使用化石燃料燃烧时,会带来哪些问题呢?交流与讨论:化石燃料仍然是当今世界使用最多的能源,面对现状,我们怎么办? 如何提高燃料的使用效率?
使燃料充分燃烧
简要说明使煤炉中的煤充分燃烧所应采取的措施。
怎样高效、清洁地利用煤炭?
怎样提高固体和液体燃料的燃烧效率?
开发洁净、高效的新能源
要有适当过量的空气、
燃料与空气要有足够大的接触面积
将固体燃料粉碎,或将液体燃料以雾状喷出,以增大燃料与空气的接触面煤的干馏
等综合利用打开炉门在煤饼上打孔
燃烧时要有足够多的空气燃料与空气要有足够大的接触面美国通用汽车公司氢燃料电池车“氢动一号”日前走出实验室,标志着以零尾气排放为目标的清洁汽车距其实用阶段又近了一步。测试表明,“氢动一号”原型车时速从0—100公里的加速时间只需16秒,最高时速达140公里,可持续行驶400公里。
据悉,“氢动一号”与普通车最大的区别在于动力系统,其核心是200块燃料电池串联成、尺寸与普通汽车动力单元相当的电池组,使用储存在防热传导和防蒸发的特制不锈钢储罐中的液氢为燃料,储罐则安装在后座下面和后轴前。氢与氧燃烧产生动力,而燃烧产物是无污染的水。
练习:1980年我国首次制成燃氢汽车,乘员12人以50km/h行驶了40km。为了有效发展民用氢能源,首先必须制得廉价的氢气,下列可供开发,而经济的制氢方法是 。
A.电解水 B.锌和稀硫酸反应
C.光解海水C新能源简介 目前人类所消耗的能源的70%来自煤、石油、天然气等化石燃料,在现有技术条件下,化石能源的大量使用给地球环境造成了严重危害,使人类生存空间受到了极大的威胁.科学家预言,尽管化石燃料能源未来仍将占有相当大比重,但其一统天下的局面将逐渐结束(地球上2亿年形成的化石燃料,大体只够人类使用300余年),可再生的清洁能源可望撑起未来世界能源供给的半壁江山.核能太阳能其他能源风能核能清华大学核物理研究中心原子弹爆炸太阳能太阳能汽车太阳能太阳能发电站风能 现在风能已成为一种新能源而被人们广泛地使用。如右图的风力发电机,可以为人们发电。其他新能源其他新能源阿里地区地热田其他新能源羊八井地热电站其他新能源江厦潮汐试验电站能源的利用让我们
共同节约利用
我们的自然资源保护我们共同的家园!
2007.4.10(第二课时)三、热化学方程式书写热化学方程式注意事项:
(1)反应物和生成物要标明其聚集状态,用g、l、s分别代表气态、液态、固态。
(2)方程式右端用△H 标明恒压条件下反应放出或吸收的热量,放热为负,吸热为正。
表示化学反应中放出或吸收的热量的化学方程式。(3)热化学方程式中各物质前的化学计量数不表示分子个数,只表示物质的量,因此可以是整数或分数。
(4)对于相同物质的反应,当化学计量数不同时,其△H 也不同,即△H 的值与计量数成正比。
(5)物质的状态不同,其△H 也不同。
① 2H2(g) + O2 (g) = 2H2O( l ) △H = -571.6kJmol-1② H2(g) +1/2 O2 (g) = H2O( l ) △H = -285.8kJmol-1③ H2(g) + 1/2 O2 (g) = H2O( g) △H = -241.8kJmol-1你能解释氢气和氯气反应放热的道理吗? 交流与讨论:根据键能,你能计算2mol H2和1mol O2反应,生成2molH2O气体放出的热量吗?E反应历程△H= - 484 kJ收436×2kJ (2H2)
吸收496 kJ(02)放出4×463 kJ
= 1852 kJ(注:2mol H2和1mol O2反应) 键能二、反应热
化学反应过程中放出或吸收的热量
用△H表示,单位:kJ·mol-1
△H<0时,为放热反应;
△H>0时,为吸热反应。
2H2 (g) + O2 (g) = 2H20(l) △H= -484kJ·mol-1 燃烧中的热量变化化学反应根据能量
变化情况放热反应吸热反应1、燃烧中的能量变化2、燃烧中能量变化的实质键形成放热反应物键断裂吸热生成物一、燃料的燃烧1、燃烧:可燃物与氧气发生的发光、 发热的剧烈的化学反应。
实例:煤、石油、天然气的燃烧。2、燃烧的条件A、与氧气接触
B、达到着火点质量相同的不同燃料,完全燃烧后放出的热量不相等。我国目前使用的主要燃料是什么?燃烧值或热值来表示3、常见的燃料
煤、石油、天然气-----化石燃料4、如何提高燃料的使用效率A、防止环境污染、发展洁净煤技术 B、提高热效率 C、开发高能清洁能源 D、开发综合利用煤的新技术16.6%2.1%5.1%76.2%我国化石燃料和水电能源消耗构成图大量使用化石燃料燃烧时,会带来哪些问题呢?交流与讨论:化石燃料仍然是当今世界使用最多的能源,面对现状,我们怎么办? 如何提高燃料的使用效率?
使燃料充分燃烧
简要说明使煤炉中的煤充分燃烧所应采取的措施。
怎样高效、清洁地利用煤炭?
怎样提高固体和液体燃料的燃烧效率?
开发洁净、高效的新能源
要有适当过量的空气、
燃料与空气要有足够大的接触面积
将固体燃料粉碎,或将液体燃料以雾状喷出,以增大燃料与空气的接触面煤的干馏
等综合利用打开炉门在煤饼上打孔
燃烧时要有足够多的空气燃料与空气要有足够大的接触面美国通用汽车公司氢燃料电池车“氢动一号”日前走出实验室,标志着以零尾气排放为目标的清洁汽车距其实用阶段又近了一步。测试表明,“氢动一号”原型车时速从0—100公里的加速时间只需16秒,最高时速达140公里,可持续行驶400公里。
据悉,“氢动一号”与普通车最大的区别在于动力系统,其核心是200块燃料电池串联成、尺寸与普通汽车动力单元相当的电池组,使用储存在防热传导和防蒸发的特制不锈钢储罐中的液氢为燃料,储罐则安装在后座下面和后轴前。氢与氧燃烧产生动力,而燃烧产物是无污染的水。
练习:1980年我国首次制成燃氢汽车,乘员12人以50km/h行驶了40km。为了有效发展民用氢能源,首先必须制得廉价的氢气,下列可供开发,而经济的制氢方法是 。
A.电解水 B.锌和稀硫酸反应
C.光解海水C新能源简介 目前人类所消耗的能源的70%来自煤、石油、天然气等化石燃料,在现有技术条件下,化石能源的大量使用给地球环境造成了严重危害,使人类生存空间受到了极大的威胁.科学家预言,尽管化石燃料能源未来仍将占有相当大比重,但其一统天下的局面将逐渐结束(地球上2亿年形成的化石燃料,大体只够人类使用300余年),可再生的清洁能源可望撑起未来世界能源供给的半壁江山.核能太阳能其他能源风能核能清华大学核物理研究中心原子弹爆炸太阳能太阳能汽车太阳能太阳能发电站风能 现在风能已成为一种新能源而被人们广泛地使用。如右图的风力发电机,可以为人们发电。其他新能源其他新能源阿里地区地热田其他新能源羊八井地热电站其他新能源江厦潮汐试验电站能源的利用让我们
共同节约利用
我们的自然资源保护我们共同的家园!
