等效平衡与产率
图片预览




文档简介
课件11张PPT。 等效平衡问题及解题思路1、等效平衡的含义 在一定条件(定温、定容或定温、定压)
下,只是起始加入情况不同的同一可逆反应
达到平衡后,任何相同组分的分数(体积、物
质的量)均相同,这样的化学平衡互称等效平衡。2、等效平衡的分类⑴、定温、定容条件下的等效平衡I 类:对于一般可逆反应,在定T、V条件下,
改变起始加入情况,只要按可逆反应的化学
计量数比换算成平衡式左右两边同一边物质
的量与原平衡起始量相同,则两平衡等效。Ⅲ类:对于一般可逆反应,在定T、P条件下,
改变起始加入情况,只要按可逆反应的化学
计量数比换算成平衡式左右两边同一边物质
的量比与原平衡相同,则两平衡等效。⑵、定温、定压条件下的等效平衡Ⅱ类:对于一般可逆反应,在定T、V条件下,
对于反应前后气体分子数不变的可逆反应,
只要反应物(或生成物)的物质的量的比与原
平衡相同,则两平衡等效。 定T、V定T、Pm + n≠p+qm + n = p+q极限相等法极限成比例法极限成比例法m+n≠p+qm+n = p+q1、在一定容密闭容器中,加入m mol A,
n mol B发生下列反应:
mA(气) +nB(气) pC(气),平衡时C的
浓度为w mol·L-1,若维持容器体积和温度
不变,起始加入a molA,b molB,c molC,
要使平衡后C的浓度仍为w mol·L-1,则:
a、b、c必须满足的关系是
(A) a:b:c=m:n:p
(B) a:b=m:n; ap/m+c=p
(C) mc/p+a=m;nc/p+b=n
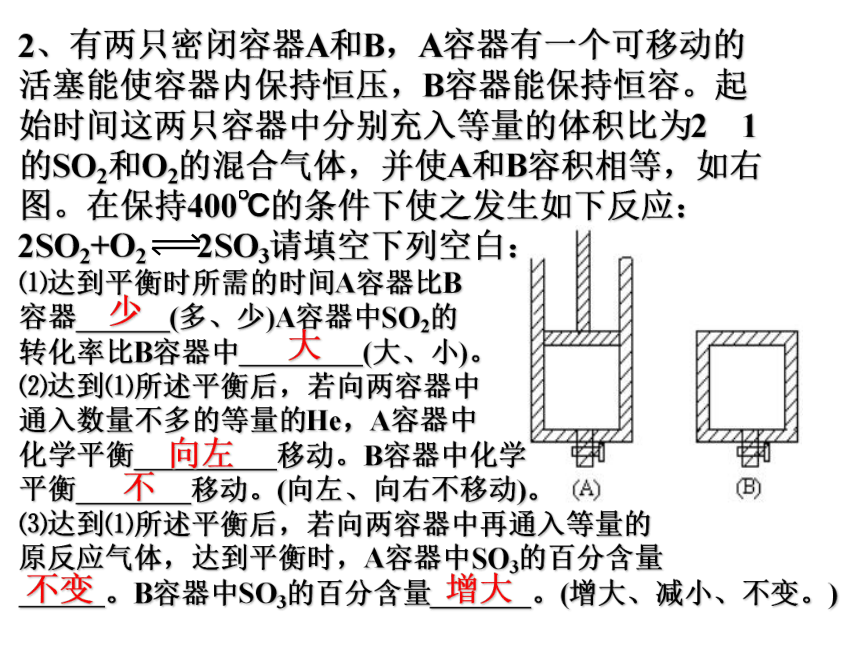
(D) a=m/3;b=n/3; c=p/3 B C课堂练习2、有两只密闭容器A和B,A容器有一个可移动的
活塞能使容器内保持恒压,B容器能保持恒容。起
始时间这两只容器中分别充入等量的体积比为2∶1
的SO2和O2的混合气体,并使A和B容积相等,如右
图。在保持400℃的条件下使之发生如下反应:
2SO2+O2 2SO3请填空下列空白:
⑴达到平衡时所需的时间A容器比B
容器 (多、少)A容器中SO2的
转化率比B容器中 (大、小)。
⑵达到⑴所述平衡后,若向两容器中
通入数量不多的等量的He,A容器中
化学平衡 移动。B容器中化学
平衡 移动。(向左、向右不移动)。
⑶达到⑴所述平衡后,若向两容器中再通入等量的
原反应气体,达到平衡时,A容器中SO3的百分含量
。B容器中SO3的百分含量 。(增大、减小、不变。)少 大向左 不 不变 增大 3、已知T℃、p kPa时,往容积可变的密闭容器中充入2 mol X和1 mol Y,此时容积为VL。保持恒温恒压,发生反应:2X(气)+Y(气) 2Z(气),达到平衡时,平衡气中Z的体积分数为0.4。试回答下列有关问题:
(1)使温度和压强在上述条件下恒定不变,再往上述密闭容器内充入4molZ,则反应达到平衡时,容器的容积为 ,平衡气中Z的体积分数为 。
(2)若另选一个容积固定不变的密闭容器,仍控制温度为T℃,使4molX和2molY反应,达到平衡状态时, 平衡气中Z的体积分数仍为0.4,则该密闭容器的容积为 。
(3)若控制温度仍为T℃,另选一容积为VL的固定不变的密闭容器,往其中充入一定量的X和Y,使反应达到平衡,这时平衡气中Z的体积分数仍为0.4。则充入的X和Y的物质的量应满足的关系是:an(Y)< n(X)< bn(Y),其中a为 ,b为 。2.5V0.45/3V1/25 有关化学平衡的计算1、可逆反应达到平衡过程中物质浓度的变化关系⑵生成物的平衡量 == 起始量 + 转化量 ⑶各物质转化浓度之比等于它们在化学方程式中
化学计量数之比⑷化学平衡前后,同种元素原子的物质的量相等2、反应的转化率(体积变化也可以) 反应达到平衡后,C A ↑ ,B的转化率可提高,但A
的转化率一般降低; C B ↑ ,A的转化率可提高,但B
的转化率一般降低。4、反应物转化率与浓度的关系⑴对于多种物质参加的反应(气、液态)3、产率⑵对于分解反应,要视反应前后物质的化学
计量数而定。不论如何改变反应物的浓度,
反应物的转化率都不变。增加反应物的浓度时,
反应物的转化率减小。m = n + pm < n +pm > n+ p增加反应物的浓度时,
反应物的转化率增大。1、某体积可变的密闭容器,盛有一定质量的A和B
的混合气体,在一定条件下发生反应:
A+3B 2C,若维持温度和压强不变当达到平衡
时,容器的体积为VL,其中C的气体体积占10% ,
下列推断正确的是( )
①原混合气体的体积为1.2VL②原混合气体的体积
为1.1VL③反应达到平衡时气体A消耗掉0.05VL
④反应达到平衡时气体B消耗掉0.05VL
A.②③ B.②④ C.①③ D.①④
2、在一密闭容器中,用等物质的量的A和B发生
如下反应:A(g)+2B(g) 2C(g),反应达到平衡时,
若混合气体A和B的物质的量之和与C的物质的量相
等,则这时A的转化率为( )
A.40% B.50% C.60% D.70%AA课堂练习3、在一个容积固定的反应器中,有一个可左右滑动
的隔板,两侧分别进行如图所示的可逆反应。各物质
的起始加入量如下:A、B、C均为4.0mol,D为6.5mol,
F为2.0mol。设E为Xmol 。当X在一定范围内变化时,
均可以通过调节反应器的温度,使两侧反应都达到平衡,
并且隔板恰好处于反应器的正中位置。请填写如下空白:
⑴若X=4.5时,则右侧反应在起始时间
(填“正反应”“逆反应”)方向进行。欲使起始反应维持向
该方向进行,则X的最大取值应小于 。
⑵若X分别为4.5和5.0时,则在这两种情况下,为反应
达平衡时,A的物质的量是否相等?
(填“相等”、“不相等”或“不能确定”)。
其理由是 。正反应 7.0 不相等 因为两种情况是在两个不同温度下建立的化学
平衡,平衡状态不同,所以物质的量也不相同。 9、对于反应:2A+B 2C在反应过程中C的
百分含量随温度变化如右图所示,则:
⑴T0对应的V正与V逆的关系是_________.
⑵正反应为_________热反应.
⑶A、B两点正反应速率的大小关系
是________________.
⑷温度T 是_______________.V正=V逆放V(A)正<V(B)正反应正向进行
下,只是起始加入情况不同的同一可逆反应
达到平衡后,任何相同组分的分数(体积、物
质的量)均相同,这样的化学平衡互称等效平衡。2、等效平衡的分类⑴、定温、定容条件下的等效平衡I 类:对于一般可逆反应,在定T、V条件下,
改变起始加入情况,只要按可逆反应的化学
计量数比换算成平衡式左右两边同一边物质
的量与原平衡起始量相同,则两平衡等效。Ⅲ类:对于一般可逆反应,在定T、P条件下,
改变起始加入情况,只要按可逆反应的化学
计量数比换算成平衡式左右两边同一边物质
的量比与原平衡相同,则两平衡等效。⑵、定温、定压条件下的等效平衡Ⅱ类:对于一般可逆反应,在定T、V条件下,
对于反应前后气体分子数不变的可逆反应,
只要反应物(或生成物)的物质的量的比与原
平衡相同,则两平衡等效。 定T、V定T、Pm + n≠p+qm + n = p+q极限相等法极限成比例法极限成比例法m+n≠p+qm+n = p+q1、在一定容密闭容器中,加入m mol A,
n mol B发生下列反应:
mA(气) +nB(气) pC(气),平衡时C的
浓度为w mol·L-1,若维持容器体积和温度
不变,起始加入a molA,b molB,c molC,
要使平衡后C的浓度仍为w mol·L-1,则:
a、b、c必须满足的关系是
(A) a:b:c=m:n:p
(B) a:b=m:n; ap/m+c=p
(C) mc/p+a=m;nc/p+b=n
(D) a=m/3;b=n/3; c=p/3 B C课堂练习2、有两只密闭容器A和B,A容器有一个可移动的
活塞能使容器内保持恒压,B容器能保持恒容。起
始时间这两只容器中分别充入等量的体积比为2∶1
的SO2和O2的混合气体,并使A和B容积相等,如右
图。在保持400℃的条件下使之发生如下反应:
2SO2+O2 2SO3请填空下列空白:
⑴达到平衡时所需的时间A容器比B
容器 (多、少)A容器中SO2的
转化率比B容器中 (大、小)。
⑵达到⑴所述平衡后,若向两容器中
通入数量不多的等量的He,A容器中
化学平衡 移动。B容器中化学
平衡 移动。(向左、向右不移动)。
⑶达到⑴所述平衡后,若向两容器中再通入等量的
原反应气体,达到平衡时,A容器中SO3的百分含量
。B容器中SO3的百分含量 。(增大、减小、不变。)少 大向左 不 不变 增大 3、已知T℃、p kPa时,往容积可变的密闭容器中充入2 mol X和1 mol Y,此时容积为VL。保持恒温恒压,发生反应:2X(气)+Y(气) 2Z(气),达到平衡时,平衡气中Z的体积分数为0.4。试回答下列有关问题:
(1)使温度和压强在上述条件下恒定不变,再往上述密闭容器内充入4molZ,则反应达到平衡时,容器的容积为 ,平衡气中Z的体积分数为 。
(2)若另选一个容积固定不变的密闭容器,仍控制温度为T℃,使4molX和2molY反应,达到平衡状态时, 平衡气中Z的体积分数仍为0.4,则该密闭容器的容积为 。
(3)若控制温度仍为T℃,另选一容积为VL的固定不变的密闭容器,往其中充入一定量的X和Y,使反应达到平衡,这时平衡气中Z的体积分数仍为0.4。则充入的X和Y的物质的量应满足的关系是:an(Y)< n(X)< bn(Y),其中a为 ,b为 。2.5V0.45/3V1/25 有关化学平衡的计算1、可逆反应达到平衡过程中物质浓度的变化关系⑵生成物的平衡量 == 起始量 + 转化量 ⑶各物质转化浓度之比等于它们在化学方程式中
化学计量数之比⑷化学平衡前后,同种元素原子的物质的量相等2、反应的转化率(体积变化也可以) 反应达到平衡后,C A ↑ ,B的转化率可提高,但A
的转化率一般降低; C B ↑ ,A的转化率可提高,但B
的转化率一般降低。4、反应物转化率与浓度的关系⑴对于多种物质参加的反应(气、液态)3、产率⑵对于分解反应,要视反应前后物质的化学
计量数而定。不论如何改变反应物的浓度,
反应物的转化率都不变。增加反应物的浓度时,
反应物的转化率减小。m = n + pm < n +pm > n+ p增加反应物的浓度时,
反应物的转化率增大。1、某体积可变的密闭容器,盛有一定质量的A和B
的混合气体,在一定条件下发生反应:
A+3B 2C,若维持温度和压强不变当达到平衡
时,容器的体积为VL,其中C的气体体积占10% ,
下列推断正确的是( )
①原混合气体的体积为1.2VL②原混合气体的体积
为1.1VL③反应达到平衡时气体A消耗掉0.05VL
④反应达到平衡时气体B消耗掉0.05VL
A.②③ B.②④ C.①③ D.①④
2、在一密闭容器中,用等物质的量的A和B发生
如下反应:A(g)+2B(g) 2C(g),反应达到平衡时,
若混合气体A和B的物质的量之和与C的物质的量相
等,则这时A的转化率为( )
A.40% B.50% C.60% D.70%AA课堂练习3、在一个容积固定的反应器中,有一个可左右滑动
的隔板,两侧分别进行如图所示的可逆反应。各物质
的起始加入量如下:A、B、C均为4.0mol,D为6.5mol,
F为2.0mol。设E为Xmol 。当X在一定范围内变化时,
均可以通过调节反应器的温度,使两侧反应都达到平衡,
并且隔板恰好处于反应器的正中位置。请填写如下空白:
⑴若X=4.5时,则右侧反应在起始时间
(填“正反应”“逆反应”)方向进行。欲使起始反应维持向
该方向进行,则X的最大取值应小于 。
⑵若X分别为4.5和5.0时,则在这两种情况下,为反应
达平衡时,A的物质的量是否相等?
(填“相等”、“不相等”或“不能确定”)。
其理由是 。正反应 7.0 不相等 因为两种情况是在两个不同温度下建立的化学
平衡,平衡状态不同,所以物质的量也不相同。 9、对于反应:2A+B 2C在反应过程中C的
百分含量随温度变化如右图所示,则:
⑴T0对应的V正与V逆的关系是_________.
⑵正反应为_________热反应.
⑶A、B两点正反应速率的大小关系
是________________.
⑷温度T
同课章节目录
