化学电源
图片预览







文档简介
课件24张PPT。化学电源电极材料
电子流向
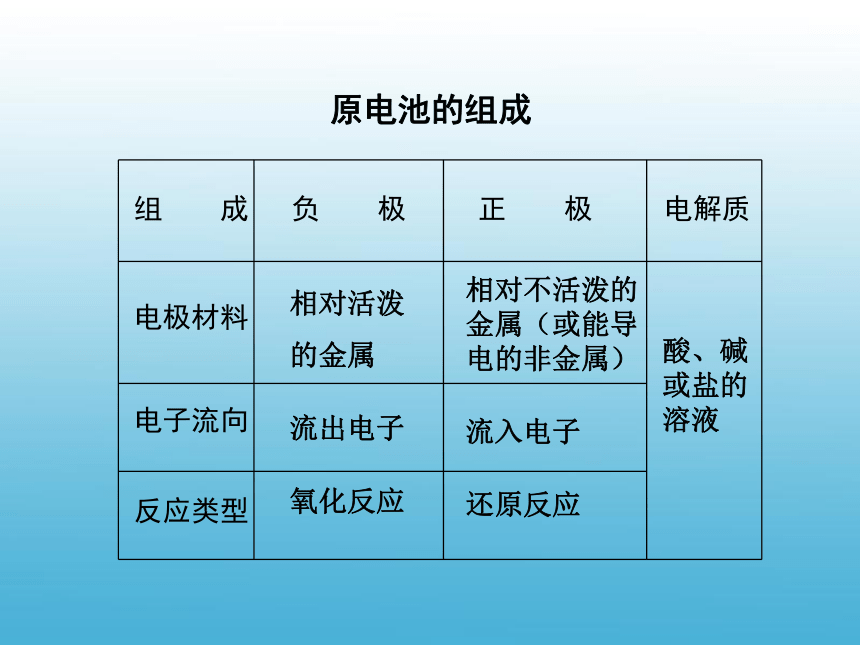
反应类型组 成 负 极 正 极 电解质相对活泼
的金属
流出电子
氧化反应酸、碱
或盐的
溶液相对不活泼的金属(或能导电的非金属)
流入电子
还原反应原电池的组成 家庭小实验(教材107页)
在一瓣橘子上相隔0.5 cm分别插一小段铜片和铝片,把铜片和铝片的另一端通过导线接触耳机的两极,试试能否听到“嘎嘎”声。能够从耳机中听到“嘎嘎”声,说明了什么?用其他金属、水果、液体再试一试。研究性课题(教材106页)
调查常用电池的种类、使用范围、性能和价格,以及电池中的氧化剂和还原剂。调查废旧电池是如何处理的,以及回收废旧电池的意义和价值。干电池负极:Zn – 2e- = Zn2+(负极)(正极)2NH4++ 2e- = 2NH3+H2总反应:Zn +2NH4+= Zn2++ 2NH3+H22MnO2+H2=2MnO(OH)
ZnCl2+4NH3=[Zn(NH3)4]Cl2正极:干电池负极:Zn – 2e- = Zn2+(负极)(正极)正极:2NH4++ 2e- = 2NH3+H2总反应:Zn +2NH4+= Zn2++ 2NH3+H22MnO2+H2=2MnO(OH)
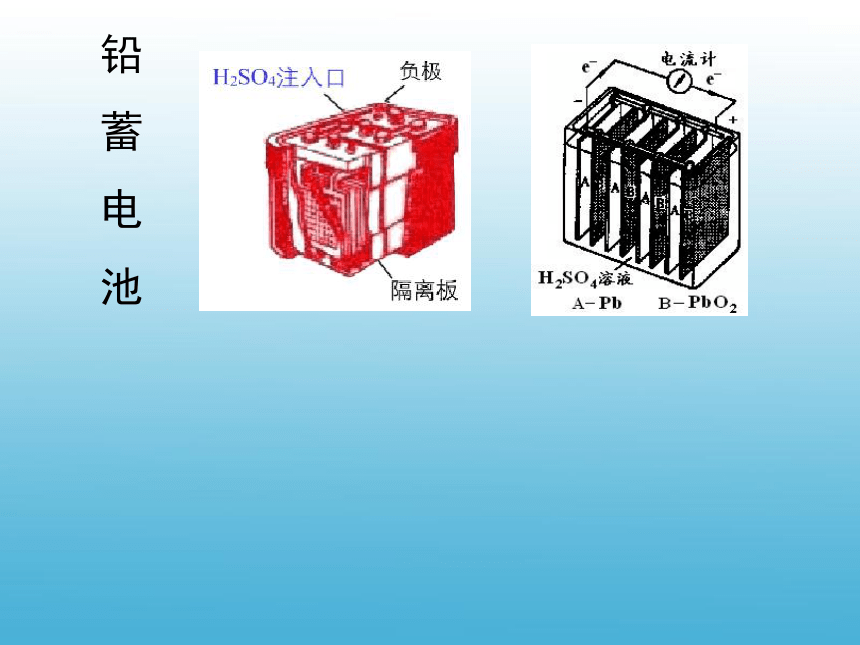
ZnCl2+4NH3=[Zn(NH3)4]Cl2铅
蓄
电
池(见初中《化学》48页) 通电后,两电极上都有气体产生。其中,与电源正极相连的试管内得到氧气,而与电源负极相连的试管内得到氢气,两者的体积比约为1:2。铅
蓄
电
池总反应:Pb+PbO2+2H2SO4=2PbSO4+2H2OPb+PbO2+4H++2SO42-=2PbSO4+2H2O负极:Pb-2e-+SO42-=PbSO4正极:PbO2+2e-+4H++SO42-=PbSO4+2H2O铅
蓄
电
池总反应:Pb+PbO2+2H2SO4=2PbSO4+2H2OPb+PbO2+4H++2SO42-=2PbSO4+2H2O负极:Pb-2e-+SO42-=PbSO4正极:PbO2+2e-+4H++SO42-=PbSO4+2H2O其他蓄电池:镍-镉蓄电池、银-锌蓄电池等优点:可反复使用 缺点:污染大燃料电池 把能源中燃料燃烧反应的化学能直接转化为电能的“能量转换器”氢氧燃料电池多孔性金属电极,具有催化性能燃料电池 把能源中燃料燃烧反应的化学能直接转化为电能的“能量转换器”氢氧燃料电池 常见的燃料电池还有甲烷燃料电池、铝-空气燃料电池、熔融盐燃料电池等优点:效率高、无污染,装置可持续使用多孔性金属电极,具有催化性能化学电源的分类类 型一次电池
二次电池
燃料电池只能使用一次,不能充电复原继续使用的化学电池酸(或碱)性锌-锰干电池、银-锌纽扣电池、放电后能充电复原继续使用的化学电池铅蓄电池、镍-镉蓄电池、银-锌蓄电池将燃料燃烧的化学能直接转变成电能的电池氢氧燃料电池、铝-空气燃料电池、熔融盐燃料电池 含 义示 例电极材料
电子流向
反应类型组 成 负 极 正 极 电解质相对活泼
的金属
流出电子
氧化反应酸、碱
或盐的
溶液相对不活泼的金属(或能导电的非金属)
流入电子
还原反应原电池的组成 化学电池的组成 电极材料
电极上发生反应的物质能导电的物质还原性较强的物质(大多是金属电极本身)氧化性较强的物质酸、碱、盐溶液或熔融液减 少 污 染
节 约 资 源 熔融盐燃料电池具有高的发电效率,因而受到重视,可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为阳极燃气,空气与CO2的混合气体为阴极助燃气,制得在650℃下工作的燃料电池,完成有关的电池反应式:
阳极反应式:2CO+2CO32- →4CO2+4e-
阴极反应式:________________________
总电池反应式:______________________练习与巩固2CO+O2→2CO2O2+2CO2+4e-→2CO32- 随着人们生活质量的不断提高,废电池必须进行集中处理的问题被提到议事日程,其首要原因是
A.利用电池外壳的金属材料
B.防止电池中汞、镉和铅等重金属离子对土壤和水源的污染
C.不使电池中渗泄的电解液腐蚀其他物品
D.回收其中石墨电极练习与巩固答案为B2NH4++ 2e- = 2NH3+H22H++2e- = H2返回
电子流向
反应类型组 成 负 极 正 极 电解质相对活泼
的金属
流出电子
氧化反应酸、碱
或盐的
溶液相对不活泼的金属(或能导电的非金属)
流入电子
还原反应原电池的组成 家庭小实验(教材107页)
在一瓣橘子上相隔0.5 cm分别插一小段铜片和铝片,把铜片和铝片的另一端通过导线接触耳机的两极,试试能否听到“嘎嘎”声。能够从耳机中听到“嘎嘎”声,说明了什么?用其他金属、水果、液体再试一试。研究性课题(教材106页)
调查常用电池的种类、使用范围、性能和价格,以及电池中的氧化剂和还原剂。调查废旧电池是如何处理的,以及回收废旧电池的意义和价值。干电池负极:Zn – 2e- = Zn2+(负极)(正极)2NH4++ 2e- = 2NH3+H2总反应:Zn +2NH4+= Zn2++ 2NH3+H22MnO2+H2=2MnO(OH)
ZnCl2+4NH3=[Zn(NH3)4]Cl2正极:干电池负极:Zn – 2e- = Zn2+(负极)(正极)正极:2NH4++ 2e- = 2NH3+H2总反应:Zn +2NH4+= Zn2++ 2NH3+H22MnO2+H2=2MnO(OH)
ZnCl2+4NH3=[Zn(NH3)4]Cl2铅
蓄
电
池(见初中《化学》48页) 通电后,两电极上都有气体产生。其中,与电源正极相连的试管内得到氧气,而与电源负极相连的试管内得到氢气,两者的体积比约为1:2。铅
蓄
电
池总反应:Pb+PbO2+2H2SO4=2PbSO4+2H2OPb+PbO2+4H++2SO42-=2PbSO4+2H2O负极:Pb-2e-+SO42-=PbSO4正极:PbO2+2e-+4H++SO42-=PbSO4+2H2O铅
蓄
电
池总反应:Pb+PbO2+2H2SO4=2PbSO4+2H2OPb+PbO2+4H++2SO42-=2PbSO4+2H2O负极:Pb-2e-+SO42-=PbSO4正极:PbO2+2e-+4H++SO42-=PbSO4+2H2O其他蓄电池:镍-镉蓄电池、银-锌蓄电池等优点:可反复使用 缺点:污染大燃料电池 把能源中燃料燃烧反应的化学能直接转化为电能的“能量转换器”氢氧燃料电池多孔性金属电极,具有催化性能燃料电池 把能源中燃料燃烧反应的化学能直接转化为电能的“能量转换器”氢氧燃料电池 常见的燃料电池还有甲烷燃料电池、铝-空气燃料电池、熔融盐燃料电池等优点:效率高、无污染,装置可持续使用多孔性金属电极,具有催化性能化学电源的分类类 型一次电池
二次电池
燃料电池只能使用一次,不能充电复原继续使用的化学电池酸(或碱)性锌-锰干电池、银-锌纽扣电池、放电后能充电复原继续使用的化学电池铅蓄电池、镍-镉蓄电池、银-锌蓄电池将燃料燃烧的化学能直接转变成电能的电池氢氧燃料电池、铝-空气燃料电池、熔融盐燃料电池 含 义示 例电极材料
电子流向
反应类型组 成 负 极 正 极 电解质相对活泼
的金属
流出电子
氧化反应酸、碱
或盐的
溶液相对不活泼的金属(或能导电的非金属)
流入电子
还原反应原电池的组成 化学电池的组成 电极材料
电极上发生反应的物质能导电的物质还原性较强的物质(大多是金属电极本身)氧化性较强的物质酸、碱、盐溶液或熔融液减 少 污 染
节 约 资 源 熔融盐燃料电池具有高的发电效率,因而受到重视,可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为阳极燃气,空气与CO2的混合气体为阴极助燃气,制得在650℃下工作的燃料电池,完成有关的电池反应式:
阳极反应式:2CO+2CO32- →4CO2+4e-
阴极反应式:________________________
总电池反应式:______________________练习与巩固2CO+O2→2CO2O2+2CO2+4e-→2CO32- 随着人们生活质量的不断提高,废电池必须进行集中处理的问题被提到议事日程,其首要原因是
A.利用电池外壳的金属材料
B.防止电池中汞、镉和铅等重金属离子对土壤和水源的污染
C.不使电池中渗泄的电解液腐蚀其他物品
D.回收其中石墨电极练习与巩固答案为B2NH4++ 2e- = 2NH3+H22H++2e- = H2返回
