江西省2008年化学中考复习研讨
图片预览








文档简介
课件47张PPT。2019/2/271————江西省2008年化学中考复习研讨
九江十一中 刘卫玲2019/2/272用好教材、合理安排;
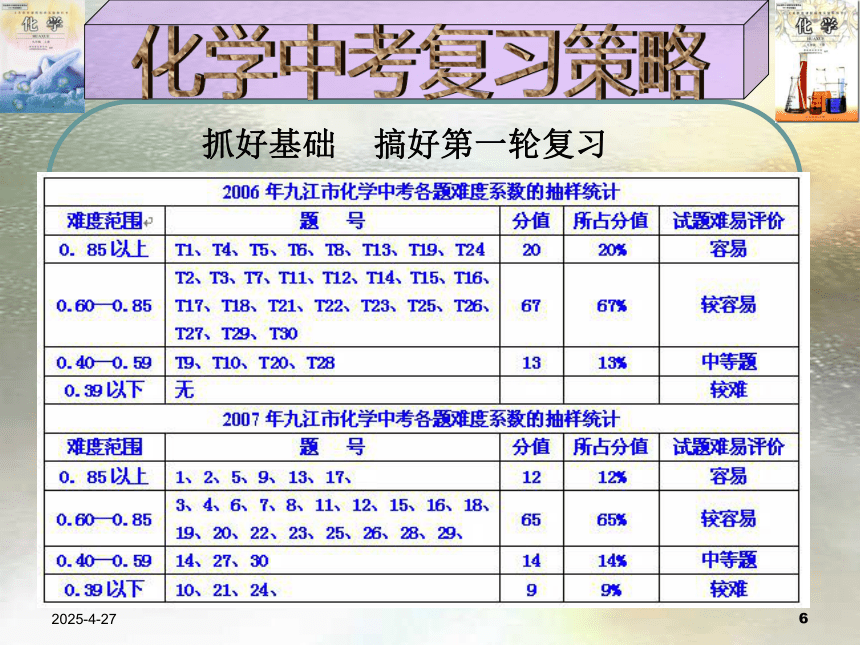
研究课标、把握难度;
选好例题、提高效度。 2019/2/273用好教材 合理安排用好教材:
关注教材的变化;
关注不同版本的教材;
关注课标与教材之间的关联;
结合学生的实际,利用当地的课程资源
丰富教材的内涵。2019/2/274复习模式上合理安排:
第一轮按教材的单元顺序先基础后练习,同时穿插小专题;
第二轮专题复习,针对第一轮复习的补充与提高,加强应用能力训练;
第三轮综合训练,提高解题能力的训练以及归类和创新能力的训练。用好教材 合理安排2019/2/275合理安排时间
第一轮复习大约四周半;
第二轮复习大约一周半;
第三轮复习约二周左右。用好教材 合理安排2019/2/276抓好基础 搞好第一轮复习2019/2/2772019/2/2782019/2/2792019/2/27102019/2/27112019/2/2712专题1:将一些容易混淆的概念及知识引导学生归类;
专题2:结合身边的化学物质进行推理判断题的训练;
专题3:结合身边的化学物质进行科学探究的专项训练;
专题4:计算题的综合训练。用好教材 合理安排用好教材 合理安排2019/2/2713专题1:将一些容易混淆的概念及知识引导学生归类;
专题2:结合身边的化学物质进行推理判断题的训练;
专题3:结合身边的化学物质进行科学探究的专项训练;
专题4:计算题的综合训练。用好教材 合理安排显酸性的溶液不一定是酸溶液;
显碱性的溶液不一定是碱溶液;
盐溶液不一定显中性;
有盐和水生成的反应不一定是中和反应;
均一、稳定的液体不一定是溶液;
饱和溶液不一定是浓溶液;
往饱和溶液中加入某种物质后,饱和溶液质量不一定不变;
发光发热的变化不一定是燃烧等。用好教材 合理安排2019/2/2714专题1:将一些容易混淆的概念及知识引导学生归类;
专题2:结合身边的化学物质进行推理判断题的训练;
专题3:结合身边的化学物质进行科学探究的专项训练;
专题4:计算题的综合训练。用好教材 合理安排2019/2/2715研究课标 把握难度 为什么要研究课标呢?从理论上来分析,化学课程标准是执行教育方针的学科准则,是培养学生相关习惯和潜能的基本要求,学科教学目标是依据课程目标来设计的,课程目标应该贯穿和体现于教学目标之中。从中考情况而言,我省化学中考说明是根据化学课程标准制订出来的,只是中考说明比课程标准在有些方面更加具体化,而化学中考说明又是中考化学命题的具体依据,教学目标是课程的具体内容标准的体现,即依据课程目标、课程具体内容标准和教学实际从知识与技能、过程与方法、情感态度与价值观三方面来设计教学目标。2019/2/2716研究课标 把握难度考点1:“能进行药品的取用、简单仪器的使用和连接、加热等基本的实验操作”;“能在教师的指导下根据实验目的选择实验药品和仪器,并能安全操作”。
(1)写出试管、试管夹、玻璃棒、酒精灯、铁架台、烧杯、量筒、胶头滴管(滴瓶)、集气瓶、蒸发皿、漏斗、水槽和托盘天平的名称,初步学会它们的用途和操作原理(使用方法及注意事项)。
(2)能熟练进行药品的取用、玻璃仪器的洗涤、装置气密性检查、气体收集、过滤、加热、蒸发、溶液配制等基本操作,懂得操作的原理。研究课标 把握难度2019/2/2717答案:不应在实验室内打闹;不能在实验室里吃喝食物(或尝药品的味道);不能用手直接拿着试管加热;不能把烧杯直接放在酒精灯火焰上加热;不能把废液直接倒入水池中;使用试管夹时,手指不能按在短柄上等。 (07江西)做化学实验时,应严格遵守实验室 规则和操作规程。请仔细观察右图,找出其中存在的安全隐患(任写两种): ① ; ② 。2019/2/2718 2019/2/2719研究课标 把握难度考点2:知道二氧化碳的主要性质和用途
以化学性质为例:
(1)不能燃烧,通常情况下,二氧化碳也不支持燃烧。
(2)跟水反应:二氧化碳通入水中生成碳酸
(3)跟碱反应生成盐和水
(用澄清的石灰水鉴定二氧化碳)
(4)与炽热的炭反应
(5)二氧化碳与水在光和叶绿素的作用下生成葡萄糖
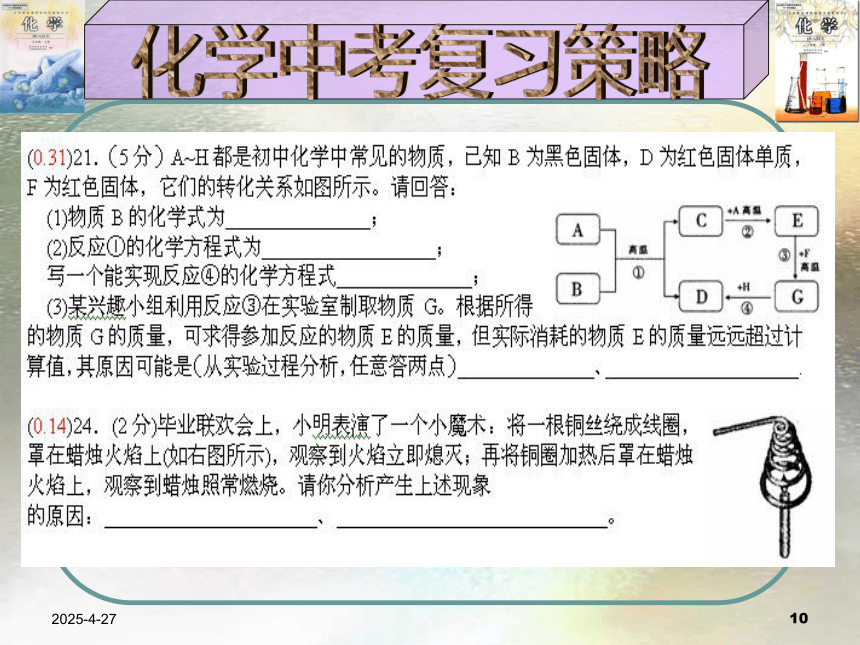
和氧气(即参与光合作用)研究课标 把握难度2019/2/2720(3)某兴趣小组利用反应③在实验室制取物质G。根据所得的物质G的质量,可求得参加反应的物质E的质量,但实际消耗的物质E的质量远远超过计算值,其原因可能是(从实验过程分析,任意答两点)答案:(1)CuO
(2)C+2CuO=====2Cu+CO2;Fe+CuSO4=Cu+FeSO4等; (07江西)A~H都是初中化学中常见的物质,已知B为黑色固体,D为红色固体单质,F为红色固体,它们的转化关系如图所示。请回答:(1)物质B的化学式为 ;(2)反应①的化学方程式为 ;
写一个能实现反应④的化学方程 ;2019/2/2721(07南京)学习化学要求熟悉物质的性质以及物质之间的相互转化。以下框图中的物质均为初中化学中的常见物质,其中甲、乙、丙、丁、戊均为单质,常温下,丁为黑色固体,戊为紫红色金属。农业上常用F改良酸性土壤。常温下,G是一种具有刺激性气味的气体,其水溶液显碱性,工业上用甲和丙化合制备G。 (1)写出A、F和G的化学式:A F G
(2)写出高温条件下B分解为C和D的化学方程式:
(3)写出H和E在加热条件下生成C和戊的化学方程式: 答案:(1)H2O Ca(OH)2 NH3 2019/2/2722(05杨州)沐浴在阳光下的绿色植物悄悄地进行着一个重要化学变化——“光合作用”。请写出这个变化的化学方程式: ;该反应的反应物与生成物中,属于单质的是 (填化学式),属于氧化物的有 、 (填化学式);该反应将 能转化成了有机物中的化学能。答案:6CO2 + 6H2O ====== C6H12O6 + 6O2 。
O2 , CO2 、H2O ;光(能)或太阳(能)。2019/2/27232019/2/2724研究课标 把握难度考点3:认识燃烧、缓慢氧化和爆炸的条件及防火灭火、防范爆炸的措施(“认识”是课程目标中的中等水平要求)
(1)燃烧的三个条件,并会用来解释生活中一些相关的现象。
(2)爆炸形成的条件,可燃物燃烧剧烈程度的影响因素。懂得常见易燃、易爆物的储存、运输、使用的注意点,熟悉相关标志。
(3)可燃性气体或粉尘发生爆炸的条件。知道引爆的常见因素(明火、电火花、高温、撞击等)。
(4)灭火的基本原理和常见方法,常见火灾的处理方法。在被困火灾区时,能懂得区分不同情况的自救方法。
(5)常见灭火器材及其使用方法、适用范围(主要指泡沫灭火器、液态二氧化碳灭火器的适用范围)。2019/2/27252019/2/2726研究课标 把握难度考点4:了解饱和溶液和溶解度的涵义
要求从文字描述以及溶解度曲线等不同的方式中理解饱和溶液及溶解度的涵义,会查阅有关物质的溶解性或溶解度,依据给定的数据绘制溶解度曲线,从溶解度曲线图获取与饱和溶液和溶解度有关的信息。课标中并未直接提到溶解度曲线的问题,但是了解溶解度曲线是了解溶解度的含义的一个层面.研究课标 把握难度2019/2/2727(07江西)甲、乙、丙三种物质的溶解度曲线
如右图所示。据图回答:(1)50℃时,乙物质的溶解度是 g;
(2)30℃时,三种物质的溶解度由大到小的顺
序为 ;
(3)要使接近饱和的丙物质溶液变为饱和,可
采取的一种措施是 ;
(4)50℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至
10℃时,析出晶体最多的是 ,所得溶液中溶质质量分数最小的
是 。
答案:(1)40 (2)升高温度(或加入丙物质、恒温蒸发溶剂等)
(3)乙>甲>丙 (4)甲;丙。2019/2/2728(07陕西)如图为KNO3、NaNO2(亚硝酸钠)、NaCl的溶解度曲线,请分析图象回答下列问题:(1)60℃时,KNO3饱和溶液
中溶质的质量分数 (填
“大于”、“等于”、“小于”)
NaNO2饱和溶液中溶质的质量分数。
(2)NaNO2因外观与NaCl相似,
经常会出现误食中毒的事件。
20℃时,取这两种固体各50g,分别加入到100g水中充分搅拌后,没有溶解完的固体是 ,固体完全溶解的溶液属于 (填“饱和”或“不饱和”)溶液。
答案:(1)等于 (2)NaCl 不饱和2019/2/2729
(06宜昌)
右图是甲、乙两固体物质的溶解度随温度变化的曲线图,据此我能回答下列问题:
⑴ 40℃时,甲物质溶解度为 g。
⑵ 溶解度随温度变化影响比较大
的物质是 。
⑶ 30℃时,向100g水中加入30g
乙物质,充分溶解后,所得溶液
是 溶液(填“饱和”或“不饱和”),
所得溶液中溶质的质量分数为 。
答案:⑴ 35 ⑵ 甲 ⑶ 饱和 20%2019/2/2730答案:(07宜昌)2019/2/2731研究课标 把握难度考点5:知道常见酸碱的主要性质
酸:(1)酸溶液使使紫色的石蕊试液变红色,不能使无色的酚酞试液变色;
(2)酸与金属发生置换
(3)酸与金属氧化物反应(写化学方程式)
(4)酸与碱反应(写化学方程式)
(5)酸与盐反应
碱:(1)?碱溶液能跟酸碱指示剂起反应。
(2)?碱能跟多数非金属氧化物起反应,生成盐和水。
(3)碱能跟酸起中和反应,生成盐和水。
(4?)碱能跟某些盐起反应,生成另一种盐和另一种碱研究课标 把握难度2019/2/2732(07汕头)右图中每条连线表
示两端的物质可以发生化学反
应,甲、乙、丙、丁分别为Mg、
BaCl2、Na2CO3、HCl中的一种。
(1)写出乙和丙的化学式:
乙 ,丙 。
(2)写出下列化学方程式:
甲和乙: , 丙和丁: 。
(3)图中反应①属于基本反应类型中的 反应,又称为 反应。答案:(1) Na2CO3 HCl
(2) BaCl2+ Na2CO3=BaCO3↓+2NaCl
Mg+2HCI=MgCl2+H2↑
(3)复分解 中和2019/2/2733试根据实验过程和发生的现象填写以下空白:
(1)产生的气体B的气味为 。
(2)溶液G中,一定存在的溶质是(写化学式) 。
(3)混合物A中,肯定存在的物质是(写化学式) 。
(4)写出实验过程④中可能发生的化学反应中的1个化学方程式: 。
答案:(1)刺激性气味 (2)CuSO4(3)NH4NO3
(4)Cu(OH)2+ H2SO4= CuSO4+2H2O CuO+ H2SO4= CuSO4+H2O
Mg(OH)2+ H2SO4= MgSO4+2H2O(07济南)现欲探究一固体混合物A的成分,已知其中可能含有Mg(OH)2、CuCl2、NH4NO3、 (NH4)2SO4、 CuO五种物质中的两种或多种。按图所示进行实验,出现的现象如图所示(设过程中所有可能发生的反应均恰好完全反应)。 2019/2/2734选好例题 提高效度 在进行第二轮的专题复习时根据实际情况我们只是对某些部分进行了复习。复习时间很短,所以要特别注意一题多解与一题多变。拓展学生思维,提高解题灵活性,使学生对所学的知识融会贯通、举一反三。2019/2/2735选好例题 提高效度 例1:某化学兴趣小组用化学方法测定一种钢样品中铁的含量。同学们称取了5.7g钢样品,投入装有10.0g稀盐酸(足量)的烧杯(烧杯质量也为10.0g)中。当反应结束后,称得烧杯及所盛药品质量为25.5 g ,求这种样品中铁的质量分数?所用盐酸中溶质的质量分数是多少?反应后所得溶液中溶质的质量分数又是多少?选好例题 提高效度 2019/2/2736选好例题 提高效度 变换1: 某化学兴趣小组用化学方法测定一种钢样品中铁的含量。同学们称取了5.7g钢样品,投入装有10.0g稀盐酸(足量)的烧杯(烧杯质量也为10.0g)中。在化学反应过程中对烧杯(包括溶液和残余固体)进行了四次称量,记录如下表:
求这种样品中铁的质量分数?所用盐酸中溶质的质量分数是多少?反应后所得溶液中溶质的质量分数又是多少?选好例题 提高效度 2019/2/2737变换2: 某化学兴趣小组用化学方法测定一种钢样品中铁的含量。同学们称取了5.7g钢样品,投入装有10.0g稀盐酸(足量)的烧杯(烧杯质量也为10.0g)中。在化学反应过程中对烧杯(包括溶液和残余固体)质量与反应时间的关系如下图所示。计算这种样品中铁的质量分数?所用盐酸中溶质的质量分数是多少?反应后所得溶液中溶质的质量分数又是多少?2019/2/2738选好例题 提高效度 2019/2/2739选好例题 提高效度 2019/2/2740 课程目标中明确指出: 通过义务教育阶段化学课程的学习,学生要在以下方面得到发展:了解化学与社会和技术的相互联系,并能以此分析有关的简单问题;能用变化与联系的观点分析化学现象,解决一些简单的化学问题;初步学会运用观察、实验等方法获取信息,能用文字、图表和化学语言表述有关的信息。选好例题 提高效度 2019/2/2741如:在两支试管中分别装有稀硫酸和澄清的石灰水,但到底哪支试管装的稀硫酸,哪支试管装的是澄清的石灰水,请你来鉴别它。学生讨论有如下答案:(1)紫色石蕊溶液(2)无色的酚酞溶液(3)锌粒等(4)氧化铜等(5)碳酸钠溶液(6)二氧化碳
教师归纳:
(1)所用试剂涉及到指示剂、活泼金属、金属氧化物、非金属氧化物、盐溶液
(2)涉及到的知识:酸的通性,碱的通性。
所以在第二轮的短时间复习内,充分利用典型例题对知识的条理化、系统化、网络化起到不可忽略的作用。选好例题 提高效度 2019/2/2742 比如在复习实验探究时,我们选择下列例题:
(07陕西)学校实验室的废液缸中收集了学生在实验室制取CO2后残留的废液。小红同学想探究废液中溶质的成分,请你一同参与探究并回答下列问题:[提出问题]废液中的溶质是什么物质?
[做出猜想]小红认为废液中溶质只有CaCl2,你认为还可能含有的溶质是 (填化学式)。
[查阅资料]CaCl2溶液呈中性。
[实验与结论] ①小红取少量CaCl2溶液分别加入到2支试管中,并向其中分别滴入无色酚酞试液作对比实验,结果两试管中溶液均无色,于是小红认为自己的猜想是正确的。
②你认为小红的实验 (填“能”或“不能”)证明他的猜想,理由是 。
③如果要证明你的猜想是正确的,你选择的试剂是 ,实验中可以看到的现象是 。 选好例题 提高效度 2019/2/2743 [拓展与应用]①若实验证明你的猜想是正确的,想要处理废液只得到CaCl2溶液,应向废液中加入过量的 ,反应完成后过滤。
②通过以上探究,你认为实验室的废液未经处理直接倒入下水道,可能造成的危害是 (写一条)。
答案:HCl 不能 酚酞遇盐酸也不变色,
无法确定是否含有HCl
紫色石蕊试液或碳酸钠溶液或较活泼的金属
溶液变红或生成气泡
CaCO3 可能腐蚀铁制下水管道或污染水质2019/2/2744(07无锡)中和反应在日常生活和工农业生产中有广泛的应用。某化学兴趣小组的同学在老师的指导下对酸碱中和反应进行了探究
【提出问题】能否用碳酸钾溶液验证硫酸与氢氧化钠溶液发生中和反应。
【实验药品】稀硫酸、稀氢氧化钠溶液、碳酸钾溶液。
【实验仪器】试管、滴管、10mL量筒等
【设计方案并实验】 小江同学的实验:在试管中加入2mL稀硫酸,逐滴加入__①__溶液,振荡后,再滴入V1mL__②__溶液,实验过程中无气泡逸出。反应的化学方程式为__③________________。
小伟同学的实验:在试管中加入2mL稀硫酸,逐滴加入氢氧化钠溶液,振荡后,再滴入碳酸钾溶液,有气泡逸出,继续滴加碳酸钾溶液至恰好无气泡时,共消耗碳酸钾溶液V2mL。
小明同学的判断:小江的实验说明能用碳酸钾溶液来验证;小伟的实验还不能,需再做一个实验才能说明。 选好例题 提高效度 2019/2/2745实验并判断:另取一支试管,加入2mL稀硫酸,_④____(写出实验步骤、现象和判断依据)。
【结论】能用碳酸钾溶液验证硫酸与氢氧化钠溶液发生中和反应。
【反思】在小江的实验中,碳酸钾溶液的作用是_⑤ _ (填字母)。A.仅是反应物 B.相当于指示剂 C.作催化剂
答案:
①NaOH ②K2CO3 ③H2SO4+2NaOH===Na2SO4+2H2O
④逐滴加入碳酸钾溶液至无气泡产生,记录消耗的碳酸钾溶液体积为V3mL,V3mL>V2mL。[加入与小伟的实验不等量的氢氧化钠溶液(不足量),再逐滴加入碳酸钾溶液至无气泡产生,记录消耗的碳酸钾溶液体积为V3mL,V3mL≠V2mL。(或消耗的碳酸钾溶液体积与小伟实验的碳酸钾溶液体积不等)]
⑤B2019/2/2746 化学中考目标,是基于化学课程目标和课程的具体内容标准的一种测量标准。中考目标的制定,应有两种情况:一是学业考试目标,应完全以课程目标和课程的具体内容标准为基础;二是选拔考试,应在课程目标和课程的具体内容标准的基础上,侧重于学生学习能力和学习方法的考查。而目前根据我省初中毕业水平考试与高中选拔考试两考合一且两卷合一的现状,所以我省的中考目标的制订综合考虑了上述两种情况。 选好例题 提高效度 2019/2/2747 不妥之处,请多指正!
谢 谢 大家!
九江十一中 刘卫玲2019/2/272用好教材、合理安排;
研究课标、把握难度;
选好例题、提高效度。 2019/2/273用好教材 合理安排用好教材:
关注教材的变化;
关注不同版本的教材;
关注课标与教材之间的关联;
结合学生的实际,利用当地的课程资源
丰富教材的内涵。2019/2/274复习模式上合理安排:
第一轮按教材的单元顺序先基础后练习,同时穿插小专题;
第二轮专题复习,针对第一轮复习的补充与提高,加强应用能力训练;
第三轮综合训练,提高解题能力的训练以及归类和创新能力的训练。用好教材 合理安排2019/2/275合理安排时间
第一轮复习大约四周半;
第二轮复习大约一周半;
第三轮复习约二周左右。用好教材 合理安排2019/2/276抓好基础 搞好第一轮复习2019/2/2772019/2/2782019/2/2792019/2/27102019/2/27112019/2/2712专题1:将一些容易混淆的概念及知识引导学生归类;
专题2:结合身边的化学物质进行推理判断题的训练;
专题3:结合身边的化学物质进行科学探究的专项训练;
专题4:计算题的综合训练。用好教材 合理安排用好教材 合理安排2019/2/2713专题1:将一些容易混淆的概念及知识引导学生归类;
专题2:结合身边的化学物质进行推理判断题的训练;
专题3:结合身边的化学物质进行科学探究的专项训练;
专题4:计算题的综合训练。用好教材 合理安排显酸性的溶液不一定是酸溶液;
显碱性的溶液不一定是碱溶液;
盐溶液不一定显中性;
有盐和水生成的反应不一定是中和反应;
均一、稳定的液体不一定是溶液;
饱和溶液不一定是浓溶液;
往饱和溶液中加入某种物质后,饱和溶液质量不一定不变;
发光发热的变化不一定是燃烧等。用好教材 合理安排2019/2/2714专题1:将一些容易混淆的概念及知识引导学生归类;
专题2:结合身边的化学物质进行推理判断题的训练;
专题3:结合身边的化学物质进行科学探究的专项训练;
专题4:计算题的综合训练。用好教材 合理安排2019/2/2715研究课标 把握难度 为什么要研究课标呢?从理论上来分析,化学课程标准是执行教育方针的学科准则,是培养学生相关习惯和潜能的基本要求,学科教学目标是依据课程目标来设计的,课程目标应该贯穿和体现于教学目标之中。从中考情况而言,我省化学中考说明是根据化学课程标准制订出来的,只是中考说明比课程标准在有些方面更加具体化,而化学中考说明又是中考化学命题的具体依据,教学目标是课程的具体内容标准的体现,即依据课程目标、课程具体内容标准和教学实际从知识与技能、过程与方法、情感态度与价值观三方面来设计教学目标。2019/2/2716研究课标 把握难度考点1:“能进行药品的取用、简单仪器的使用和连接、加热等基本的实验操作”;“能在教师的指导下根据实验目的选择实验药品和仪器,并能安全操作”。
(1)写出试管、试管夹、玻璃棒、酒精灯、铁架台、烧杯、量筒、胶头滴管(滴瓶)、集气瓶、蒸发皿、漏斗、水槽和托盘天平的名称,初步学会它们的用途和操作原理(使用方法及注意事项)。
(2)能熟练进行药品的取用、玻璃仪器的洗涤、装置气密性检查、气体收集、过滤、加热、蒸发、溶液配制等基本操作,懂得操作的原理。研究课标 把握难度2019/2/2717答案:不应在实验室内打闹;不能在实验室里吃喝食物(或尝药品的味道);不能用手直接拿着试管加热;不能把烧杯直接放在酒精灯火焰上加热;不能把废液直接倒入水池中;使用试管夹时,手指不能按在短柄上等。 (07江西)做化学实验时,应严格遵守实验室 规则和操作规程。请仔细观察右图,找出其中存在的安全隐患(任写两种): ① ; ② 。2019/2/2718 2019/2/2719研究课标 把握难度考点2:知道二氧化碳的主要性质和用途
以化学性质为例:
(1)不能燃烧,通常情况下,二氧化碳也不支持燃烧。
(2)跟水反应:二氧化碳通入水中生成碳酸
(3)跟碱反应生成盐和水
(用澄清的石灰水鉴定二氧化碳)
(4)与炽热的炭反应
(5)二氧化碳与水在光和叶绿素的作用下生成葡萄糖
和氧气(即参与光合作用)研究课标 把握难度2019/2/2720(3)某兴趣小组利用反应③在实验室制取物质G。根据所得的物质G的质量,可求得参加反应的物质E的质量,但实际消耗的物质E的质量远远超过计算值,其原因可能是(从实验过程分析,任意答两点)答案:(1)CuO
(2)C+2CuO=====2Cu+CO2;Fe+CuSO4=Cu+FeSO4等; (07江西)A~H都是初中化学中常见的物质,已知B为黑色固体,D为红色固体单质,F为红色固体,它们的转化关系如图所示。请回答:(1)物质B的化学式为 ;(2)反应①的化学方程式为 ;
写一个能实现反应④的化学方程 ;2019/2/2721(07南京)学习化学要求熟悉物质的性质以及物质之间的相互转化。以下框图中的物质均为初中化学中的常见物质,其中甲、乙、丙、丁、戊均为单质,常温下,丁为黑色固体,戊为紫红色金属。农业上常用F改良酸性土壤。常温下,G是一种具有刺激性气味的气体,其水溶液显碱性,工业上用甲和丙化合制备G。 (1)写出A、F和G的化学式:A F G
(2)写出高温条件下B分解为C和D的化学方程式:
(3)写出H和E在加热条件下生成C和戊的化学方程式: 答案:(1)H2O Ca(OH)2 NH3 2019/2/2722(05杨州)沐浴在阳光下的绿色植物悄悄地进行着一个重要化学变化——“光合作用”。请写出这个变化的化学方程式: ;该反应的反应物与生成物中,属于单质的是 (填化学式),属于氧化物的有 、 (填化学式);该反应将 能转化成了有机物中的化学能。答案:6CO2 + 6H2O ====== C6H12O6 + 6O2 。
O2 , CO2 、H2O ;光(能)或太阳(能)。2019/2/27232019/2/2724研究课标 把握难度考点3:认识燃烧、缓慢氧化和爆炸的条件及防火灭火、防范爆炸的措施(“认识”是课程目标中的中等水平要求)
(1)燃烧的三个条件,并会用来解释生活中一些相关的现象。
(2)爆炸形成的条件,可燃物燃烧剧烈程度的影响因素。懂得常见易燃、易爆物的储存、运输、使用的注意点,熟悉相关标志。
(3)可燃性气体或粉尘发生爆炸的条件。知道引爆的常见因素(明火、电火花、高温、撞击等)。
(4)灭火的基本原理和常见方法,常见火灾的处理方法。在被困火灾区时,能懂得区分不同情况的自救方法。
(5)常见灭火器材及其使用方法、适用范围(主要指泡沫灭火器、液态二氧化碳灭火器的适用范围)。2019/2/27252019/2/2726研究课标 把握难度考点4:了解饱和溶液和溶解度的涵义
要求从文字描述以及溶解度曲线等不同的方式中理解饱和溶液及溶解度的涵义,会查阅有关物质的溶解性或溶解度,依据给定的数据绘制溶解度曲线,从溶解度曲线图获取与饱和溶液和溶解度有关的信息。课标中并未直接提到溶解度曲线的问题,但是了解溶解度曲线是了解溶解度的含义的一个层面.研究课标 把握难度2019/2/2727(07江西)甲、乙、丙三种物质的溶解度曲线
如右图所示。据图回答:(1)50℃时,乙物质的溶解度是 g;
(2)30℃时,三种物质的溶解度由大到小的顺
序为 ;
(3)要使接近饱和的丙物质溶液变为饱和,可
采取的一种措施是 ;
(4)50℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至
10℃时,析出晶体最多的是 ,所得溶液中溶质质量分数最小的
是 。
答案:(1)40 (2)升高温度(或加入丙物质、恒温蒸发溶剂等)
(3)乙>甲>丙 (4)甲;丙。2019/2/2728(07陕西)如图为KNO3、NaNO2(亚硝酸钠)、NaCl的溶解度曲线,请分析图象回答下列问题:(1)60℃时,KNO3饱和溶液
中溶质的质量分数 (填
“大于”、“等于”、“小于”)
NaNO2饱和溶液中溶质的质量分数。
(2)NaNO2因外观与NaCl相似,
经常会出现误食中毒的事件。
20℃时,取这两种固体各50g,分别加入到100g水中充分搅拌后,没有溶解完的固体是 ,固体完全溶解的溶液属于 (填“饱和”或“不饱和”)溶液。
答案:(1)等于 (2)NaCl 不饱和2019/2/2729
(06宜昌)
右图是甲、乙两固体物质的溶解度随温度变化的曲线图,据此我能回答下列问题:
⑴ 40℃时,甲物质溶解度为 g。
⑵ 溶解度随温度变化影响比较大
的物质是 。
⑶ 30℃时,向100g水中加入30g
乙物质,充分溶解后,所得溶液
是 溶液(填“饱和”或“不饱和”),
所得溶液中溶质的质量分数为 。
答案:⑴ 35 ⑵ 甲 ⑶ 饱和 20%2019/2/2730答案:(07宜昌)2019/2/2731研究课标 把握难度考点5:知道常见酸碱的主要性质
酸:(1)酸溶液使使紫色的石蕊试液变红色,不能使无色的酚酞试液变色;
(2)酸与金属发生置换
(3)酸与金属氧化物反应(写化学方程式)
(4)酸与碱反应(写化学方程式)
(5)酸与盐反应
碱:(1)?碱溶液能跟酸碱指示剂起反应。
(2)?碱能跟多数非金属氧化物起反应,生成盐和水。
(3)碱能跟酸起中和反应,生成盐和水。
(4?)碱能跟某些盐起反应,生成另一种盐和另一种碱研究课标 把握难度2019/2/2732(07汕头)右图中每条连线表
示两端的物质可以发生化学反
应,甲、乙、丙、丁分别为Mg、
BaCl2、Na2CO3、HCl中的一种。
(1)写出乙和丙的化学式:
乙 ,丙 。
(2)写出下列化学方程式:
甲和乙: , 丙和丁: 。
(3)图中反应①属于基本反应类型中的 反应,又称为 反应。答案:(1) Na2CO3 HCl
(2) BaCl2+ Na2CO3=BaCO3↓+2NaCl
Mg+2HCI=MgCl2+H2↑
(3)复分解 中和2019/2/2733试根据实验过程和发生的现象填写以下空白:
(1)产生的气体B的气味为 。
(2)溶液G中,一定存在的溶质是(写化学式) 。
(3)混合物A中,肯定存在的物质是(写化学式) 。
(4)写出实验过程④中可能发生的化学反应中的1个化学方程式: 。
答案:(1)刺激性气味 (2)CuSO4(3)NH4NO3
(4)Cu(OH)2+ H2SO4= CuSO4+2H2O CuO+ H2SO4= CuSO4+H2O
Mg(OH)2+ H2SO4= MgSO4+2H2O(07济南)现欲探究一固体混合物A的成分,已知其中可能含有Mg(OH)2、CuCl2、NH4NO3、 (NH4)2SO4、 CuO五种物质中的两种或多种。按图所示进行实验,出现的现象如图所示(设过程中所有可能发生的反应均恰好完全反应)。 2019/2/2734选好例题 提高效度 在进行第二轮的专题复习时根据实际情况我们只是对某些部分进行了复习。复习时间很短,所以要特别注意一题多解与一题多变。拓展学生思维,提高解题灵活性,使学生对所学的知识融会贯通、举一反三。2019/2/2735选好例题 提高效度 例1:某化学兴趣小组用化学方法测定一种钢样品中铁的含量。同学们称取了5.7g钢样品,投入装有10.0g稀盐酸(足量)的烧杯(烧杯质量也为10.0g)中。当反应结束后,称得烧杯及所盛药品质量为25.5 g ,求这种样品中铁的质量分数?所用盐酸中溶质的质量分数是多少?反应后所得溶液中溶质的质量分数又是多少?选好例题 提高效度 2019/2/2736选好例题 提高效度 变换1: 某化学兴趣小组用化学方法测定一种钢样品中铁的含量。同学们称取了5.7g钢样品,投入装有10.0g稀盐酸(足量)的烧杯(烧杯质量也为10.0g)中。在化学反应过程中对烧杯(包括溶液和残余固体)进行了四次称量,记录如下表:
求这种样品中铁的质量分数?所用盐酸中溶质的质量分数是多少?反应后所得溶液中溶质的质量分数又是多少?选好例题 提高效度 2019/2/2737变换2: 某化学兴趣小组用化学方法测定一种钢样品中铁的含量。同学们称取了5.7g钢样品,投入装有10.0g稀盐酸(足量)的烧杯(烧杯质量也为10.0g)中。在化学反应过程中对烧杯(包括溶液和残余固体)质量与反应时间的关系如下图所示。计算这种样品中铁的质量分数?所用盐酸中溶质的质量分数是多少?反应后所得溶液中溶质的质量分数又是多少?2019/2/2738选好例题 提高效度 2019/2/2739选好例题 提高效度 2019/2/2740 课程目标中明确指出: 通过义务教育阶段化学课程的学习,学生要在以下方面得到发展:了解化学与社会和技术的相互联系,并能以此分析有关的简单问题;能用变化与联系的观点分析化学现象,解决一些简单的化学问题;初步学会运用观察、实验等方法获取信息,能用文字、图表和化学语言表述有关的信息。选好例题 提高效度 2019/2/2741如:在两支试管中分别装有稀硫酸和澄清的石灰水,但到底哪支试管装的稀硫酸,哪支试管装的是澄清的石灰水,请你来鉴别它。学生讨论有如下答案:(1)紫色石蕊溶液(2)无色的酚酞溶液(3)锌粒等(4)氧化铜等(5)碳酸钠溶液(6)二氧化碳
教师归纳:
(1)所用试剂涉及到指示剂、活泼金属、金属氧化物、非金属氧化物、盐溶液
(2)涉及到的知识:酸的通性,碱的通性。
所以在第二轮的短时间复习内,充分利用典型例题对知识的条理化、系统化、网络化起到不可忽略的作用。选好例题 提高效度 2019/2/2742 比如在复习实验探究时,我们选择下列例题:
(07陕西)学校实验室的废液缸中收集了学生在实验室制取CO2后残留的废液。小红同学想探究废液中溶质的成分,请你一同参与探究并回答下列问题:[提出问题]废液中的溶质是什么物质?
[做出猜想]小红认为废液中溶质只有CaCl2,你认为还可能含有的溶质是 (填化学式)。
[查阅资料]CaCl2溶液呈中性。
[实验与结论] ①小红取少量CaCl2溶液分别加入到2支试管中,并向其中分别滴入无色酚酞试液作对比实验,结果两试管中溶液均无色,于是小红认为自己的猜想是正确的。
②你认为小红的实验 (填“能”或“不能”)证明他的猜想,理由是 。
③如果要证明你的猜想是正确的,你选择的试剂是 ,实验中可以看到的现象是 。 选好例题 提高效度 2019/2/2743 [拓展与应用]①若实验证明你的猜想是正确的,想要处理废液只得到CaCl2溶液,应向废液中加入过量的 ,反应完成后过滤。
②通过以上探究,你认为实验室的废液未经处理直接倒入下水道,可能造成的危害是 (写一条)。
答案:HCl 不能 酚酞遇盐酸也不变色,
无法确定是否含有HCl
紫色石蕊试液或碳酸钠溶液或较活泼的金属
溶液变红或生成气泡
CaCO3 可能腐蚀铁制下水管道或污染水质2019/2/2744(07无锡)中和反应在日常生活和工农业生产中有广泛的应用。某化学兴趣小组的同学在老师的指导下对酸碱中和反应进行了探究
【提出问题】能否用碳酸钾溶液验证硫酸与氢氧化钠溶液发生中和反应。
【实验药品】稀硫酸、稀氢氧化钠溶液、碳酸钾溶液。
【实验仪器】试管、滴管、10mL量筒等
【设计方案并实验】 小江同学的实验:在试管中加入2mL稀硫酸,逐滴加入__①__溶液,振荡后,再滴入V1mL__②__溶液,实验过程中无气泡逸出。反应的化学方程式为__③________________。
小伟同学的实验:在试管中加入2mL稀硫酸,逐滴加入氢氧化钠溶液,振荡后,再滴入碳酸钾溶液,有气泡逸出,继续滴加碳酸钾溶液至恰好无气泡时,共消耗碳酸钾溶液V2mL。
小明同学的判断:小江的实验说明能用碳酸钾溶液来验证;小伟的实验还不能,需再做一个实验才能说明。 选好例题 提高效度 2019/2/2745实验并判断:另取一支试管,加入2mL稀硫酸,_④____(写出实验步骤、现象和判断依据)。
【结论】能用碳酸钾溶液验证硫酸与氢氧化钠溶液发生中和反应。
【反思】在小江的实验中,碳酸钾溶液的作用是_⑤ _ (填字母)。A.仅是反应物 B.相当于指示剂 C.作催化剂
答案:
①NaOH ②K2CO3 ③H2SO4+2NaOH===Na2SO4+2H2O
④逐滴加入碳酸钾溶液至无气泡产生,记录消耗的碳酸钾溶液体积为V3mL,V3mL>V2mL。[加入与小伟的实验不等量的氢氧化钠溶液(不足量),再逐滴加入碳酸钾溶液至无气泡产生,记录消耗的碳酸钾溶液体积为V3mL,V3mL≠V2mL。(或消耗的碳酸钾溶液体积与小伟实验的碳酸钾溶液体积不等)]
⑤B2019/2/2746 化学中考目标,是基于化学课程目标和课程的具体内容标准的一种测量标准。中考目标的制定,应有两种情况:一是学业考试目标,应完全以课程目标和课程的具体内容标准为基础;二是选拔考试,应在课程目标和课程的具体内容标准的基础上,侧重于学生学习能力和学习方法的考查。而目前根据我省初中毕业水平考试与高中选拔考试两考合一且两卷合一的现状,所以我省的中考目标的制订综合考虑了上述两种情况。 选好例题 提高效度 2019/2/2747 不妥之处,请多指正!
谢 谢 大家!
同课章节目录
