混合物的分离和提纯(山东省青岛市)
图片预览






文档简介
课件18张PPT。第一节化学实验基本方法(2)过 滤 和 蒸 发混合物的分离和提纯1. 同学们都听过“吹尽黄沙始见金”,你知道淘金者是利用什么方法和性质将黄金从沙里分离出来的吗?他们利用的是黄金和沙的密度不同2.如果有铁和铜的混合物,你能用哪些方法将铁铜分离?淘金者的方法用磁铁吸引铁加盐酸讨论:在分离和提纯物质时,要除掉杂质.化学上指的杂质都是有害或无价值的吗?请举例说明一. 粗盐的提纯1.溶解2.过滤3.蒸发过滤时注意事项:玻璃棒的用途是什么?何时停止加热?*加入的液体不超过蒸发皿容积的2/3。
*蒸发过程中要用玻棒不断搅拌(以防溶液因局部过热而造成液滴飞溅)。
*加热至出现较多量固体时,停止加热,利用余温使滤液蒸干。
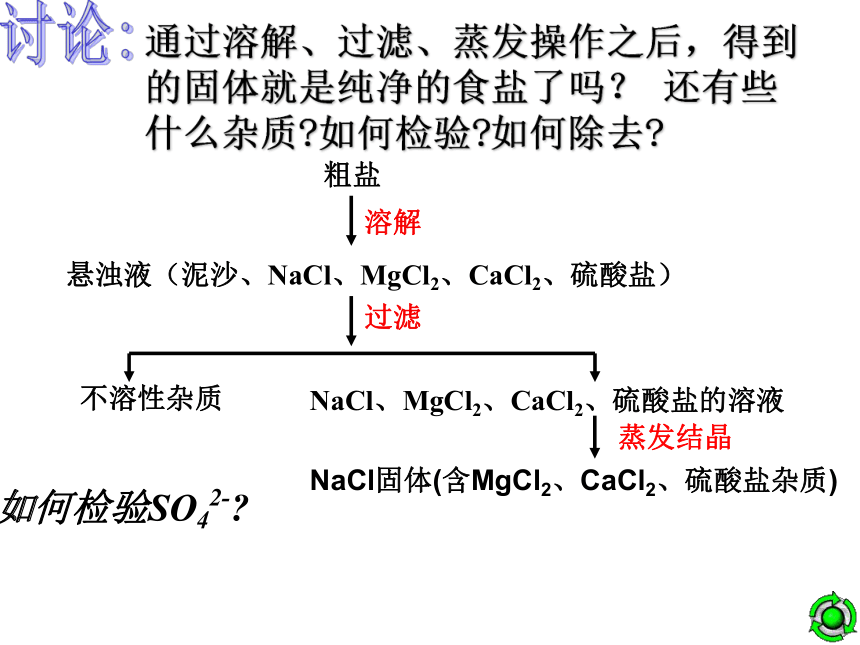
*热的蒸发皿不可直接放在实验桌上,要垫上石棉网。2.蒸发操作时的注意事项?1.蒸发的目的是什么?探讨通过溶解、过滤、蒸发操作之后,得到的固体就是纯净的食盐了吗? 还有些什么杂质?如何检验?如何除去?如何检验SO42-?讨论:问题1.如何检验SO42- ?先加入盐酸再加入BaCl2问题2.如何除去Mg2+和Ca2+ ?1、对于上述食盐所配溶液( NaCl溶液 )要除去可溶杂质离子是:选择要加入的除杂试剂:引入了新的离子:讨论:2、加入试剂的正确顺序(尽量不引入新的杂质离子)1.BaCl2→NaOH →Na2CO3 →HCl
2. BaCl2→ Na2CO3 → NaOH →HCl
3. NaOH →BaCl2→ Na2CO3 →HCl
加入除杂试剂的顺序可以是:【练习】
进行过滤操作应选用的一组用品是
A. 烧杯、酒精灯、试管、铁架台、漏斗
B. 烧杯、漏斗、玻璃棒、漏斗架、滤纸
C. 滤纸、烧杯、试管夹、漏斗、玻璃棒
D. 滤纸、试管、漏斗、铁架台、玻璃棒B【练习】
在蒸发皿中蒸发液体,下列操作不正确的是
A.直接用酒精灯的外焰加热蒸发皿
B.加热过程中不断用玻璃棒搅拌
C.加热到液体全部消失
D.蒸发皿中出现多量晶体、少量液体时,停止加热,利用蒸发皿的余热烘干C练习2.为除去粗盐中的Ca2+、Mg2+、SO42—和泥沙,可将粗盐溶于水,再进行下列操作①过滤②加过量的NaOH溶液③加适量的盐酸④加过量的Na2CO3溶液⑤加过量的BaCl2溶液.正确的排列顺序是____________1.在进行沉淀实验时,如何认定沉淀已经完全? 静置,取上层清夜继续加沉淀剂无现象
(条件: );
静置,在上层清夜中继续加沉淀剂无现象,
(条件: )几种答案情况?第一节化学实验基本方法(3)蒸 馏 和 萃 取对于液态混合物可以利用混合物中各组分的沸点相差较大,用蒸馏的方法除去难挥发或不挥发的杂质分离乙醇的水溶液可以用什么方法?蒸 馏例:实验室通过蒸馏的方法除去自来水中的Cl—等杂质制取蒸馏水(Cl—的化合物难挥发)沸石1.温度计的水银球应置于__以测__温度2.沸石有何用途?3.冷凝管有什么作用?4.冷凝管中水下进上出的原因是什么?5.水流方向与蒸汽方向_____。蒸 馏萃 取用CCl4萃取碘的饱和水溶液。
针对问题:
①碘水呈什么颜色?CCl4有什么颜色?
②振荡前出现什么现象,原因为何?
③振荡后又出现什么现象,为什么?
④通过上述实验,请描述萃取的原理.
⑤若将CCl4改用密度比水小的有机物苯,则会出现什么现象?
现有碘的水溶液,若要得到固体碘应怎么操作?请同学们列举出已学过的分离和提纯的方法及依据的性质
物质分离和提纯的方法注意点:
①先物理方法后化学方法
②遵循三个必须:
a.所加试剂须过量
b.过量试剂须易除去
c.实验方法须最佳,操作易行,步骤少 归纳为“不增、不减、易分、复原” 总结本节重点:
*蒸发过程中要用玻棒不断搅拌(以防溶液因局部过热而造成液滴飞溅)。
*加热至出现较多量固体时,停止加热,利用余温使滤液蒸干。
*热的蒸发皿不可直接放在实验桌上,要垫上石棉网。2.蒸发操作时的注意事项?1.蒸发的目的是什么?探讨通过溶解、过滤、蒸发操作之后,得到的固体就是纯净的食盐了吗? 还有些什么杂质?如何检验?如何除去?如何检验SO42-?讨论:问题1.如何检验SO42- ?先加入盐酸再加入BaCl2问题2.如何除去Mg2+和Ca2+ ?1、对于上述食盐所配溶液( NaCl溶液 )要除去可溶杂质离子是:选择要加入的除杂试剂:引入了新的离子:讨论:2、加入试剂的正确顺序(尽量不引入新的杂质离子)1.BaCl2→NaOH →Na2CO3 →HCl
2. BaCl2→ Na2CO3 → NaOH →HCl
3. NaOH →BaCl2→ Na2CO3 →HCl
加入除杂试剂的顺序可以是:【练习】
进行过滤操作应选用的一组用品是
A. 烧杯、酒精灯、试管、铁架台、漏斗
B. 烧杯、漏斗、玻璃棒、漏斗架、滤纸
C. 滤纸、烧杯、试管夹、漏斗、玻璃棒
D. 滤纸、试管、漏斗、铁架台、玻璃棒B【练习】
在蒸发皿中蒸发液体,下列操作不正确的是
A.直接用酒精灯的外焰加热蒸发皿
B.加热过程中不断用玻璃棒搅拌
C.加热到液体全部消失
D.蒸发皿中出现多量晶体、少量液体时,停止加热,利用蒸发皿的余热烘干C练习2.为除去粗盐中的Ca2+、Mg2+、SO42—和泥沙,可将粗盐溶于水,再进行下列操作①过滤②加过量的NaOH溶液③加适量的盐酸④加过量的Na2CO3溶液⑤加过量的BaCl2溶液.正确的排列顺序是____________1.在进行沉淀实验时,如何认定沉淀已经完全? 静置,取上层清夜继续加沉淀剂无现象
(条件: );
静置,在上层清夜中继续加沉淀剂无现象,
(条件: )几种答案情况?第一节化学实验基本方法(3)蒸 馏 和 萃 取对于液态混合物可以利用混合物中各组分的沸点相差较大,用蒸馏的方法除去难挥发或不挥发的杂质分离乙醇的水溶液可以用什么方法?蒸 馏例:实验室通过蒸馏的方法除去自来水中的Cl—等杂质制取蒸馏水(Cl—的化合物难挥发)沸石1.温度计的水银球应置于__以测__温度2.沸石有何用途?3.冷凝管有什么作用?4.冷凝管中水下进上出的原因是什么?5.水流方向与蒸汽方向_____。蒸 馏萃 取用CCl4萃取碘的饱和水溶液。
针对问题:
①碘水呈什么颜色?CCl4有什么颜色?
②振荡前出现什么现象,原因为何?
③振荡后又出现什么现象,为什么?
④通过上述实验,请描述萃取的原理.
⑤若将CCl4改用密度比水小的有机物苯,则会出现什么现象?
现有碘的水溶液,若要得到固体碘应怎么操作?请同学们列举出已学过的分离和提纯的方法及依据的性质
物质分离和提纯的方法注意点:
①先物理方法后化学方法
②遵循三个必须:
a.所加试剂须过量
b.过量试剂须易除去
c.实验方法须最佳,操作易行,步骤少 归纳为“不增、不减、易分、复原” 总结本节重点:
同课章节目录
- 专题一 物质的分离与提纯
- 课题1 海带中碘元素的分离及检验
- 拓展课题1-1 茶叶中某些元素的鉴定
- 课题2 用纸层析法分离铁离子和铜离子
- 拓展课题1-2 菠菜的叶绿体中色素的提取和分离
- 拓展课题1-3 用粉笔进行层析分离
- 课题3 硝酸钾晶体的制备
- 拓展课题1-4 粗盐提纯
- 专题二 物质性质的研究
- 课题1 铝及其化合物的性质
- 拓展课题2-1 铝热反应
- 课题2 乙醇和苯酚的性质
- 拓展课题2-2 苯酚与甲醛的反应
- 专题三 物质的检验与鉴别
- 课题1 牙膏和火柴中某些成分的检验
- 拓展课题3-1 新装修居室内空气中甲醛浓度的检测
- 拓展课题3-2 汽车尾气成分的检验
- 课题2 亚硝酸钠和食盐的鉴别
- 拓展课题3-3 真假碘盐的鉴别
- 专题四 化学反应条件的控制
- 课题1 硫代硫酸钠与酸反应速率的影响因素
- 拓展课题4-1 “蓝瓶子”实验
- 课题2 催化剂对过氧化氢分解反应速率的影响
- 拓展课题4-2 过氧化氢酶的催化作用
- 拓展课题4-3 蔗糖的燃烧
- 课题3 反应条件对化学平衡的影响
- 拓展课题4-4 淀粉与碘显色现象的探究
- 拓展课题4-5 压强对化学平衡的影响
- 专题五 电化学问题研究
- 课题1 原电池
- 拓展课题5-1 干电池模拟实验
- 课题2 电解与电镀
- 拓展课题5-2 阿伏加德罗常数的测定
- 专题六 物质的定量分析
- 课题1 食醋总酸含量的测定
- 拓展课题6-1 配制并标定氢氧化钠溶液
- 课题2 镀锌铁皮锌镀层厚度的测定
- 拓展课题6-2 水果中维生素C含量的测定
- 专题七 物质的制备与合成
- 课题1 硫酸亚铁铵的制备
- 拓展课题7-1 用制氢废液制备硫酸锌晶体
- 课题2 阿司匹林的合成
- 拓展课题7-2 对氨基苯磺酸的合成
