不同晶体类型
图片预览




文档简介
课件22张PPT。第二课时不同类型的晶体食盐晶体金刚石水晶铝冰干冰交流与讨论问题一:什么是晶体?有哪些特征?
问题二:为什么外观看上去相似的晶体,它
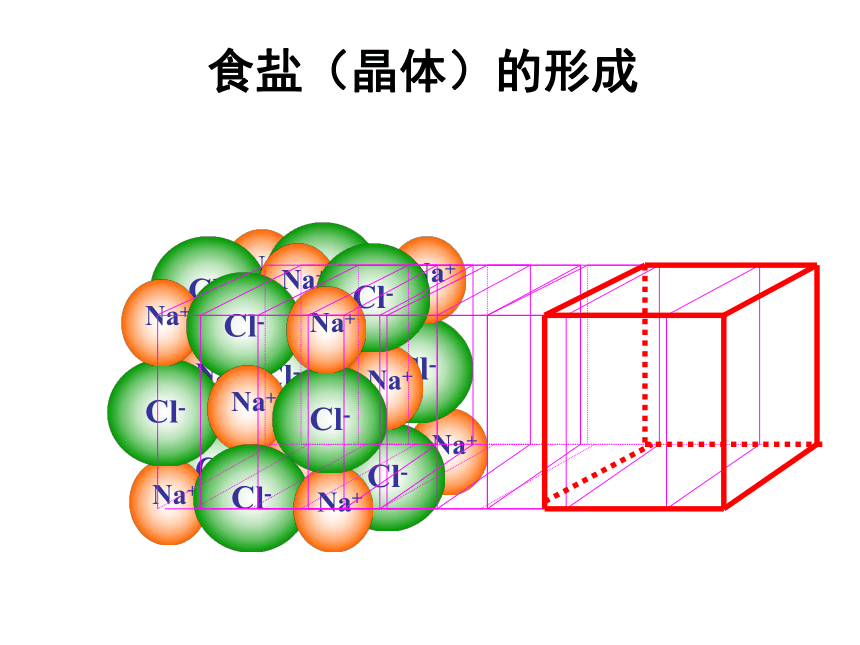
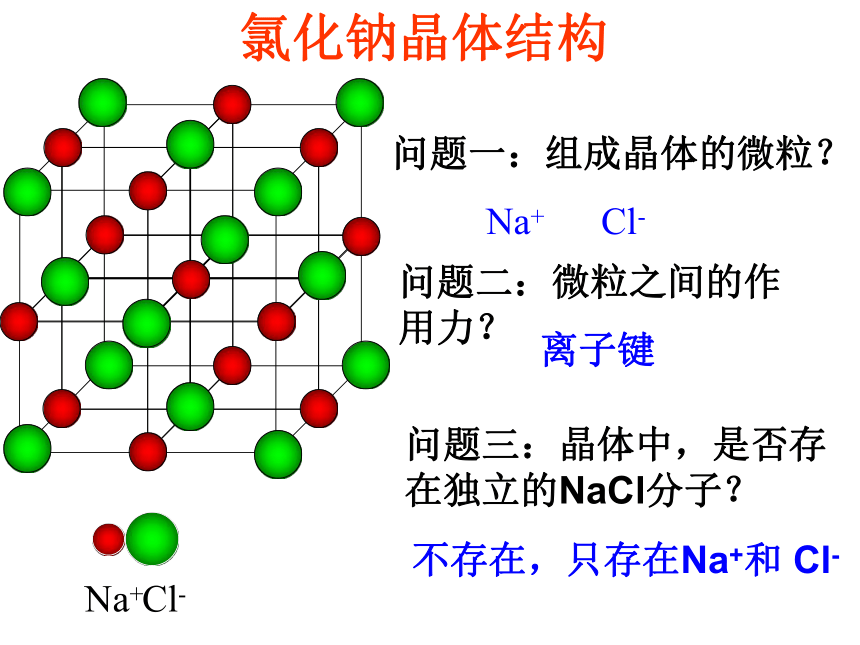
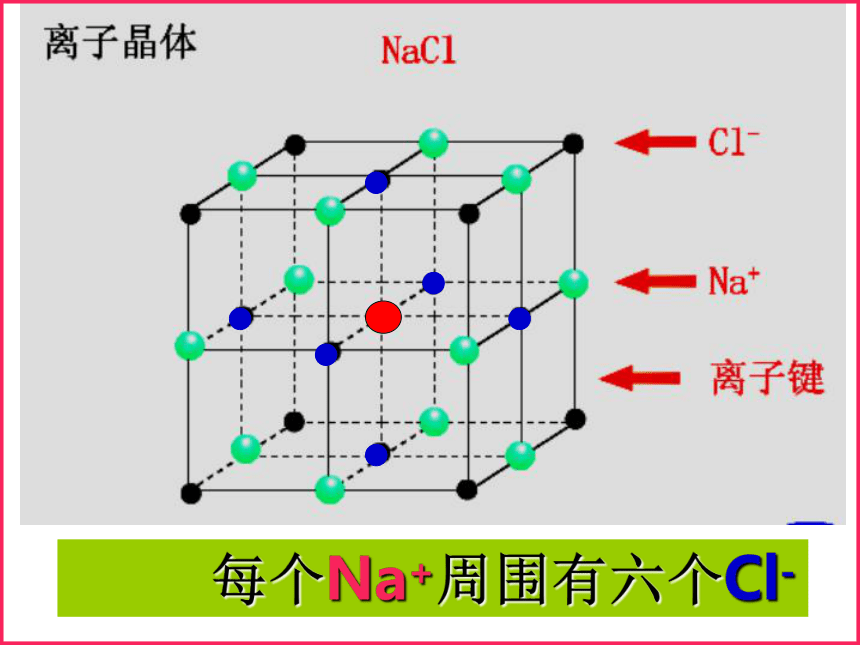
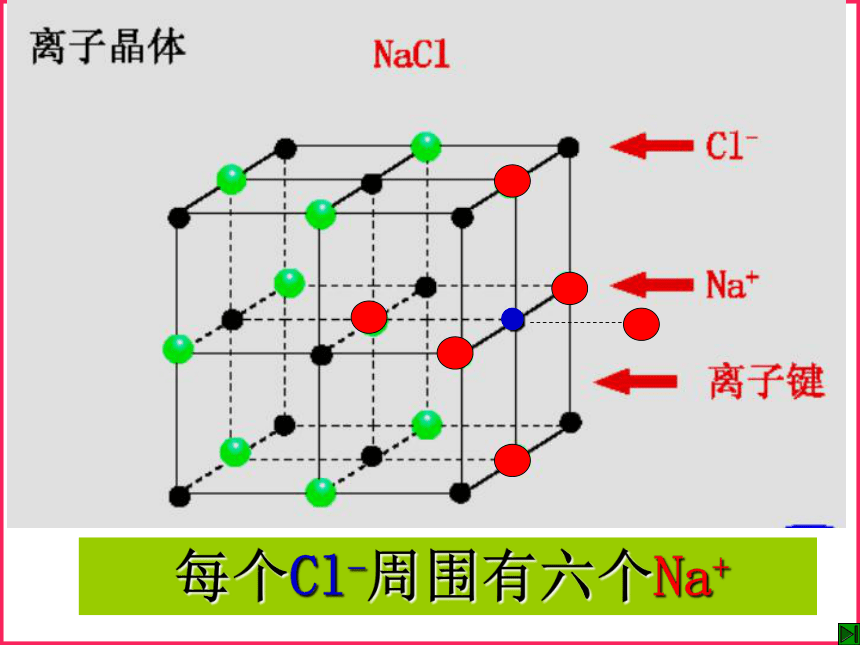
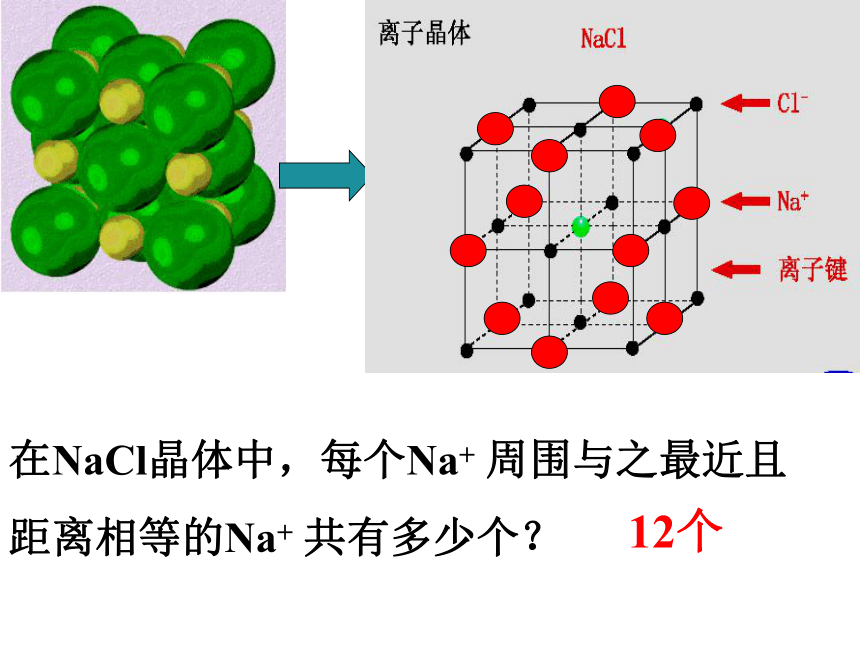
们的物理性质却有这么大的差别?食盐(晶体)的形成氯化钠晶体结构Na+Cl-问题一:组成晶体的微粒?问题三:晶体中,是否存在独立的NaCl分子?不存在,只存在Na+和 Cl-问题二:微粒之间的作用力?离子键 每个Na+周围有六个Cl- 每个Cl-周围有六个Na+在NaCl晶体中,每个Na+ 周围与之最近且
距离相等的Na+ 共有多少个?12个1、定义:一、离子晶体2、实例:食盐、氯化铯3、物理性质:4、形成离子晶体的物质归类: 离子化合物中的阴、阳离子按一定的方式有规则
地排列而形成的晶体叫做离子晶体。熔沸点较高,在熔融状态或水溶液中能导电金属氧化物、盐类离子化合物等CsCl的晶体结构示意图返回分子间作用力共价键干冰的晶体结构示意图问题一:组成晶体的微粒?CO2分子问题二:微粒之间的作用力?问题三:晶体中,是否存在独立的CO2分子?存在干冰晶体结构示意由此可见,每个二氧化碳分子周围有12个二氧化碳分子。 二、分子晶体3、物理性质:1、定义:2、实例:如干冰、冰、碘单质等4、形成分子晶体的物质:熔、沸点低,硬度小H2、Cl2、He 、HCl 、H2O、CO2等分子间通过分子间作用力相结合的晶体常温下为气态、液态的物质所形成的晶体一般为分子晶体碘单质Sio二氧化硅的晶体结构示意图问题一:组成晶体的微粒?硅原子、氧原子问题二:微粒之间的作用力?共价键问题三:晶体中,是否存在独立的SiO2分子?不存在,只存在Si和O原子三、原子晶体1、定义:2、实例:3、物理性质:熔沸点很高,硬度很大,难溶于水,
一般不导电。金刚石、金刚砂(SiC)、
晶体硅、石英(SiO2)相邻原子通过共价键结合而形成
空间网状结构的晶体,叫做原子晶体。109o28′金刚石的晶体结构示意图共价键返回金属晶体金属原子自由电子金属的延展性金属原子自由电子小结1、离子晶体、分子晶体、原子晶体结构与性质关系的比较:阴、阳离子分子原子金属阳离子和自由移动电子离子键分子间
作用力共价键金属键差距大大小较大较大小高差距大导电不导电溶液有些导电熔融或溶液导电随堂练习判断下列物质的晶体类型
氧化钠晶体、二氧化硫晶体、三氧化硫晶
体、冰、氢氧化钠晶体、硫酸晶体、铁、硫
磺
如何判断晶体类型?晶体类型的判断1.依据构成晶体的微粒及微粒间的关系2.依据物质的分类3.依据晶体的熔点4.依据导电性判断5.依据硬度立方型晶胞中粒子数的计算方法:(1)处于立方体顶点的微粒同时为8个晶胞所共有,每个微粒有1/8属于该晶胞
(2)处于立方体棱上的微粒同时为4个晶胞所共有,每个微粒有1/4属于该晶胞
(3)处于立方体面上的微粒同时为2个晶胞所共有,每个微粒有1/2属于该晶胞
(4)处于立方体内部的微粒,完全属于该晶胞
问题二:为什么外观看上去相似的晶体,它
们的物理性质却有这么大的差别?食盐(晶体)的形成氯化钠晶体结构Na+Cl-问题一:组成晶体的微粒?问题三:晶体中,是否存在独立的NaCl分子?不存在,只存在Na+和 Cl-问题二:微粒之间的作用力?离子键 每个Na+周围有六个Cl- 每个Cl-周围有六个Na+在NaCl晶体中,每个Na+ 周围与之最近且
距离相等的Na+ 共有多少个?12个1、定义:一、离子晶体2、实例:食盐、氯化铯3、物理性质:4、形成离子晶体的物质归类: 离子化合物中的阴、阳离子按一定的方式有规则
地排列而形成的晶体叫做离子晶体。熔沸点较高,在熔融状态或水溶液中能导电金属氧化物、盐类离子化合物等CsCl的晶体结构示意图返回分子间作用力共价键干冰的晶体结构示意图问题一:组成晶体的微粒?CO2分子问题二:微粒之间的作用力?问题三:晶体中,是否存在独立的CO2分子?存在干冰晶体结构示意由此可见,每个二氧化碳分子周围有12个二氧化碳分子。 二、分子晶体3、物理性质:1、定义:2、实例:如干冰、冰、碘单质等4、形成分子晶体的物质:熔、沸点低,硬度小H2、Cl2、He 、HCl 、H2O、CO2等分子间通过分子间作用力相结合的晶体常温下为气态、液态的物质所形成的晶体一般为分子晶体碘单质Sio二氧化硅的晶体结构示意图问题一:组成晶体的微粒?硅原子、氧原子问题二:微粒之间的作用力?共价键问题三:晶体中,是否存在独立的SiO2分子?不存在,只存在Si和O原子三、原子晶体1、定义:2、实例:3、物理性质:熔沸点很高,硬度很大,难溶于水,
一般不导电。金刚石、金刚砂(SiC)、
晶体硅、石英(SiO2)相邻原子通过共价键结合而形成
空间网状结构的晶体,叫做原子晶体。109o28′金刚石的晶体结构示意图共价键返回金属晶体金属原子自由电子金属的延展性金属原子自由电子小结1、离子晶体、分子晶体、原子晶体结构与性质关系的比较:阴、阳离子分子原子金属阳离子和自由移动电子离子键分子间
作用力共价键金属键差距大大小较大较大小高差距大导电不导电溶液有些导电熔融或溶液导电随堂练习判断下列物质的晶体类型
氧化钠晶体、二氧化硫晶体、三氧化硫晶
体、冰、氢氧化钠晶体、硫酸晶体、铁、硫
磺
如何判断晶体类型?晶体类型的判断1.依据构成晶体的微粒及微粒间的关系2.依据物质的分类3.依据晶体的熔点4.依据导电性判断5.依据硬度立方型晶胞中粒子数的计算方法:(1)处于立方体顶点的微粒同时为8个晶胞所共有,每个微粒有1/8属于该晶胞
(2)处于立方体棱上的微粒同时为4个晶胞所共有,每个微粒有1/4属于该晶胞
(3)处于立方体面上的微粒同时为2个晶胞所共有,每个微粒有1/2属于该晶胞
(4)处于立方体内部的微粒,完全属于该晶胞
