6月泰兴市二中高一月考化学试题
图片预览



文档简介
2008年6月15日泰兴市第二高级中学高一月考化学试题
泰 兴 市 第 二 高 级 中 学 高 一 月 考
化 学 试 题08.6.15
命题人:戴大春
可能用到的原子相对质量:H:1 C:12 O:16 Cl:35.5 Br:80 N:14
第I卷(共48分)
一、选择题(每题只有一个答案符合题意,3×8共24分)
1、前年3月11日杭甬高速公路萧山路段一辆运送化学物品的槽罐车侧翻,罐内15t苯泄入路边300m长的水渠,选成严重危险,许多新闻媒体进行了连续报道,以下报道中有科学性错误的是
A、由于大量苯溶入水中渗入土壤,会对周边农田、水源造成严重污染
B、由于苯是一种易挥发、易燃的物质,周围地区如果有一个火星就可能引起爆炸
C、可以采取抽吸水渠中上层液体的办法,达到部分清除泄漏物的目的
D、处理事故时,由于事故发生地周围比较空旷,有人提出用点火焚烧的办法来清除泄漏物,但由于苯燃烧会产生大量的黑烟扩大污染,所以该办法未被采纳
2、目前已知化合物中数量、品种最多的是IVA碳的化合物(有机化合物),下列关于其原因的叙述中不正确是
A、碳原子既可以跟自身,又可以跟其他原子(如氢原子)形成4个共价键
B、碳原子性质活泼,可以跟多数元素原子形成共价键
C、碳原子之间既可以形成稳定的单键,又可以形成稳定的双键和三键
D、多个碳原子可以形成长度不同的链、支链及环,且链、环之间又可以相互结合
3、医院里检验糖尿病的方法是将病人尿液加入到CuSO4和NaOH的混合液中,加热后产生红色沉淀说明病人的尿中含有
A、脂肪 B、乙酸 C、蛋白质 D、葡萄糖
4、1999年在一些国家的某些食品中“二恶英”含量严重超标,一时间掀起了席卷欧洲的“二恶英”恐慌症。“二恶英”是二苯基-1,4-二氧六环及其衍生物的通称,其中一种毒性最大的结构是,关于这种物质的叙述中不正确的是
A、该物质是一种芳香族化合物 B、该物质是一种卤代烃?
C、该物质是一种强烈致癌物 D、该物质分子中所有原子可能处在同一平面上
5、有机物 的正确命名为
A、2-乙基-3,3-二甲基-4-乙基戊烷 B、3,3-二甲基-4-乙基戊烷
C、3,3,4-三甲基已烷 D、2,3,3-三甲基已烷
6、炒菜时,又加料酒又加醋,可使菜变得香美可口,原因是
A、有盐类物质生成 B、有酸类物质生成
C、有油脂类物质生成 D、有酯类物质生成
7、盆烯是近年合成的一种有机物,它的分子结构可简化表示为(其中C、H原子已略去),下列关于盆烯的说法中错误的是
A、盆烯是苯的一种同分异构体
B、盆烯分子中所有的碳原子不可能在同一平面上
C、盆烯是乙烯的一种同系物 D、盆烯在一定条件下可以发生加成反应
8、有机物的天然提取和人工合成往往得到的是混合物,假设给你一种这样的有机混合物让你研究,一般要采取的几个步骤是
A、分离、提纯→确定化学式→确定实验式→确定结构式
B、分离、提纯→确定实验式→确定化学式→确定结构式
C、分离、提纯→确定结构式→确定实验式→确定化学式
D、确定化学式→确定实验式→确定结构式→分离、提纯
二、选择题(每题有1到2个答案符合题意,4×6共24分,部分分2分)
9、下列各组物质中,属于同分异构体的是
A、O2和O3 B、CH2=CHCH2CH3和CH3CH=CHCH3
C、CH3CH2CH3和CH3(CH2)2CH3 D、CH3CH2OH和CH3OCH3
10、某化合物6.4 g在氧气中完全燃烧,只生成8.8 g CO2和7.2 g H2O。下列说法正确的是
A、该化合物仅含碳、氢两种元素 B、该化合物中碳、氢原子个数比为1:4
C、无法确定该化合物是否含有氧元素 D、该化合物中一定含有氧元素
11、下列物质一定属于同系物的是
A、④和⑧ B、①、②和③ C、⑤和⑦ D、④、⑥和⑧
12、氯仿可用作全身麻醉剂,但在光照条件下,易被氧化成生成剧毒的光气(COCl2) 2CHCl3 +O2 2HCl+2COCl2 为防止发生医疗事故,在使用前要先检查是否
变质。下列那种试剂用于检验效果最好
A、烧碱溶液 B、溴水 C、KI淀粉溶液 D、AgNO3溶液
13、m mol C2H2跟n mol H2在密闭容器中反应,当该可逆反应达到平衡时,生成p mol C2H4。将反应后的混合气体完全燃烧,生成CO2和H2O,所需要氧气的物质的是
A、(3m+n)mol B、 C、(3m+n+2p)mol D、
14、拟除虫菊酯是一类高效、低毒、对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如图,下列对该化合物叙述正确的是
A、属于芳香烃 B、不能使酸性高锰酸钾溶液褪色
C、在酸性条件下不水解 D、在一定条件下可以发生加成反应
第Ⅱ卷(共72分)
三、实验题(本大题共2小题,共22分)
15、(10分)某同学为测定维生素C中碳、氢的质量分数,取维生素C样品研碎,称取该试样0.352 g,置于铂舟并放入燃烧管中,不断通入氧气流。用酒精喷灯持续加热样品,将生成物先后通过浓硫酸和碱石灰,两者分别增重0.144 g和0.528 g,生成物完全被吸收。试回答以下问题:
(1)维生素C中碳的质量分数是_______________,氢的质量分数____________________
(2)维生素中是否含有氧元素?为什么?(试通过计算说明)
_____________________________________________________________
(3)如果需要你确定维生素C的分子式,你还需要哪些信息?
_________________________________________________________________________
16、(12分)如右图,在左试管中先加入2mL 95%的乙醇,并在摇动下缓缓加入3mL浓硫酸,再加入2 mL乙酸,充分摇匀。在右试管中加入5mL饱和Na2CO3溶液。按图连接好装置,用酒精灯对右试管小火加热3~5min后,改用大火加热,当观察到左试管中有明显现象时停止实验。
(1)写出左试管中主要反应的方程式: ______________________________________________ (2)加入浓硫酸的作用:___________________________________;
(3)饱和Na2CO3的作用是____________________________________________________;
(4)反应开始时用酒精灯对左试管小火加热的原因是: _______
_____________ ______;(已知乙酸乙酯的沸点为77℃;乙醇的沸点为78.5℃;乙酸的沸点为117.9℃)
(5)分离右试管中所得乙酸乙酯和Na2CO3溶液的操作为(只填名称) ,所需主要仪器为 。
(6)实验生成的乙酸乙酯,其密度比水 ,有 气味。
四、论述题(本大题共3小题,共32分)
17、(10分)
(1)(8分)按官能团的不同,可以对有机物进行分类,请指出下列有机物的种类,填在横线上。
CH3CH2CH2COOH __________;___________;____________ ________________;
(2)(2分)写出2-甲基-1-戊烯的结构简式: ;
18、(16分)
(1)(6分)有机物的结构可用“键线式”简化表示。CH3—CH=CH-CH3可简写为 。
有机物X的键线式为:
(1)有机物Y是X的同分异构体,且属于芳香烃,写出Y的结构简式。
(2)Y在一定条件下能发生聚合反应,写出其反应的化学方程式:
(3)X与足量的H2在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有 种。
(2)(10分)已知乳酸的结构简式为 。试回答:
(1)乳酸分子中含有________和_________两种官能团(写名称);
(2)乳酸与金属钠溶液反应的化学方程式为
________________________________________________________________________;
(3)乳酸与NaHCO3溶液反应的化学方程式为
________________________________________________________________________;
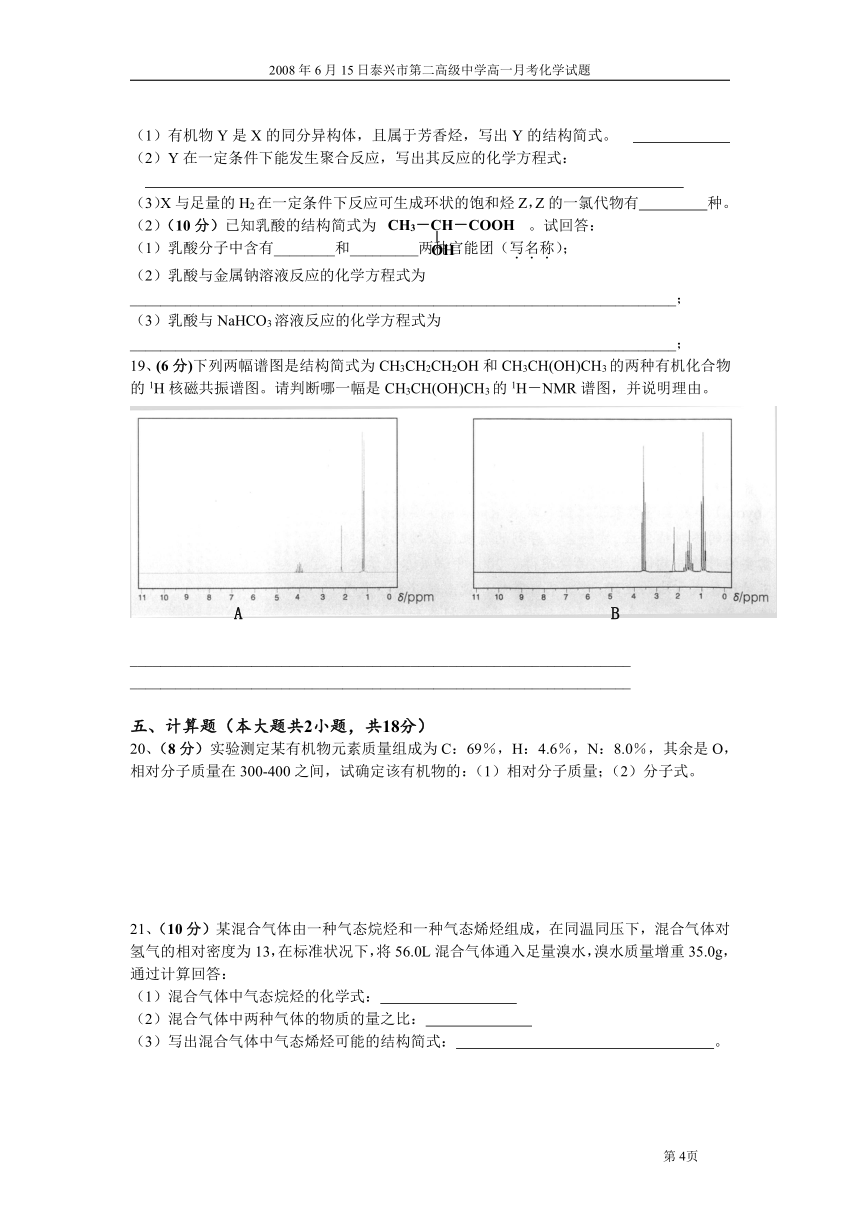
19、(6分)下列两幅谱图是结构简式为CH3CH2CH2OH和CH3CH(OH)CH3的两种有机化合物的1H核磁共振谱图。请判断哪一幅是CH3CH(OH)CH3的1H-NMR谱图,并说明理由。
__________________________________________________________________
__________________________________________________________________
五、计算题(本大题共2小题,共18分)
20、(8分)实验测定某有机物元素质量组成为C:69%,H:4.6%,N:8.0%,其余是O,相对分子质量在300-400之间,试确定该有机物的:(1)相对分子质量;(2)分子式。
21、(10分)某混合气体由一种气态烷烃和一种气态烯烃组成,在同温同压下,混合气体对氢气的相对密度为13,在标准状况下,将56.0L混合气体通入足量溴水,溴水质量增重35.0g,通过计算回答:
(1)混合气体中气态烷烃的化学式:
(2)混合气体中两种气体的物质的量之比:
(3)写出混合气体中气态烯烃可能的结构简式: 。
班级___ _ _考试号__ 泰兴市第二高级中学高一周考
姓名____ ____ 化学试题答题纸
第Ⅱ卷(共72分)
三、实验题(本大题共2小题,共22分)
15、(10分)试回答以下问题:
(1)维生素C中碳的质量分数是_______________,氢的质量分数____________________
(2)维生素中是否含有氧元素?为什么?(试通过计算说明)
____________________________________________________________________________________________________________________________________________________________________________
(3)__________________________________________________________________________________
16、(12分)
(1)化学方程式: _______________________ (2)加入浓硫酸的作用:_________________、_________________;
(3)饱和Na2CO3的作用是____________________、__________ _________、_______ ______;
(4)原因是: _______ ______ ______ ______;
(5)操作为(只填名称) ,所需主要仪器为 。
(6)其密度比水 ,有 气味。
四、论述题(本大题共3小题,共32分)
17、(10分)
(1)(8分)
CH3CH2CH2COOH __________;___________;____________ ________________;
(2)(2分)写出2-甲基-1-戊烯的结构简式: ;
18、(16分)
(1)(6分)
(1)写出Y的结构简式。
(2)反应的化学方程式:
(3)Z的一氯代物有 种。
(2)(10分)
(1)乳酸分子中含有________和_________两种官能团(写名称);
(2)
________________________________________________________________________;
(3)
________________________________________________________________________;
19、(6分)
结论:____________________________________________
理由:_________________ ____
______________________________ ____________________________________
五、计算题(本大题共2小题,共18分)
20、(8分)(1)相对分子质量____________________;(2)分子式______________。
计算过程:
21、(10分)
(1)气态烷烃的化学式:
(2)物质的量之比:
(3)写出混合气体中气态烯烃可能的结构简式: 。
计算过程:
泰兴市第二高级中学高一周考
化学试题答案
一、二、选择题
题号 1 2 3 4 5 6 7 8
答案 A B B B C D C B
题号 9 10 11 12 13 14
答案 BD BD AC D D D
15、(共10分)
(1)40.91%(2分),4.55% (2分)
(2)已知,m(H)=0.144 g÷9=0.016 g,m(C)=0.528g×12÷44=0.144g, m(H)+ m(C)=0.016g+0.144g=0.160g<0.352g,又因产物中只有H2O和CO2,故维生素中必含有氧。(结论1分,理由2分)
(3)若要确定其分子式,还要知其相对分子质量。 (3分)
16、(12分)(1)(2分)
(2)催化剂、吸水剂。(2分,每个原因1分)
(3)中和乙酸、溶解乙醇、降低乙酸乙酯的溶解度。(2分,至少2个原因,否则得1分)
(4)加快反应速率,同时又防止了反应物未来得及反应而挥发损失;(2分)
(5)分液;分液漏斗。 (各1分,共2分)
(6)小;芳香。(各1分共2分)
17、(10分)(1)羧酸类,酚类,芳香烃,酯类, (每空2分,共8分)
(2)略(2分)
18、(16分)
(1)(6分)(1) (2分)
(2)略 (2分)
(3) 2(2分)
(2)(1)羟基,羧基 (每空2分)
(2) + 2Na + H2↑ (3分)
(3) + NaHCO3 + H2O + CO2↑(3分)
19、(1)A是CH3CH(OH)CH3的1H-NMR谱图,因为从结构上分析,CH3CH(OH)CH3有三种不同化学环境的H,而分析CH3CH2CH2OH有四种不同的H,故从图上分析,A上有三个峰,而B有四个峰,故A是CH3CH(OH)CH3的1H-NMR谱图。(判断2分,解释A、B对了各2分共4分,本题共6分)
20、(8分各4分,要有计算过程,否则不得分) 348 C20H16N2O4
21、(10分)
已知混合气体的平均相对分子质量为:13×2=26,则烷烃一定为CH4,混合烃总质量为
M(混合烃)=56.0L÷22.4L/mol×26g/mol=65 g
因烯烃的分子量最小为C2H4的28。可设烯烃的分子式为CnH2n,则有m(CnH2n)=35 g,m(CH4)=65g-35g =30g;则有65÷(30÷16+35÷14n)=26,解得:n=4,
则烯烃为C4H8;n(CH4):n(C4H8)=30÷16:35÷56=3:1
(1)CH4 (3分) (2) 3:1 (3分)
(3)CH2=CH-CH2CH3,CH3-CH=CH-CH3, CH2=C(CH3)2(共4分,少一个扣2分,扣完为止)
CH3-CH-COOH
OH
A
B
CH3-CH-COONa
ONa
CH3-CH-COOH
OH
CH3-CH-COONa
OH
CH3-CH-COOH
OH
PAGE
第1页
泰 兴 市 第 二 高 级 中 学 高 一 月 考
化 学 试 题08.6.15
命题人:戴大春
可能用到的原子相对质量:H:1 C:12 O:16 Cl:35.5 Br:80 N:14
第I卷(共48分)
一、选择题(每题只有一个答案符合题意,3×8共24分)
1、前年3月11日杭甬高速公路萧山路段一辆运送化学物品的槽罐车侧翻,罐内15t苯泄入路边300m长的水渠,选成严重危险,许多新闻媒体进行了连续报道,以下报道中有科学性错误的是
A、由于大量苯溶入水中渗入土壤,会对周边农田、水源造成严重污染
B、由于苯是一种易挥发、易燃的物质,周围地区如果有一个火星就可能引起爆炸
C、可以采取抽吸水渠中上层液体的办法,达到部分清除泄漏物的目的
D、处理事故时,由于事故发生地周围比较空旷,有人提出用点火焚烧的办法来清除泄漏物,但由于苯燃烧会产生大量的黑烟扩大污染,所以该办法未被采纳
2、目前已知化合物中数量、品种最多的是IVA碳的化合物(有机化合物),下列关于其原因的叙述中不正确是
A、碳原子既可以跟自身,又可以跟其他原子(如氢原子)形成4个共价键
B、碳原子性质活泼,可以跟多数元素原子形成共价键
C、碳原子之间既可以形成稳定的单键,又可以形成稳定的双键和三键
D、多个碳原子可以形成长度不同的链、支链及环,且链、环之间又可以相互结合
3、医院里检验糖尿病的方法是将病人尿液加入到CuSO4和NaOH的混合液中,加热后产生红色沉淀说明病人的尿中含有
A、脂肪 B、乙酸 C、蛋白质 D、葡萄糖
4、1999年在一些国家的某些食品中“二恶英”含量严重超标,一时间掀起了席卷欧洲的“二恶英”恐慌症。“二恶英”是二苯基-1,4-二氧六环及其衍生物的通称,其中一种毒性最大的结构是,关于这种物质的叙述中不正确的是
A、该物质是一种芳香族化合物 B、该物质是一种卤代烃?
C、该物质是一种强烈致癌物 D、该物质分子中所有原子可能处在同一平面上
5、有机物 的正确命名为
A、2-乙基-3,3-二甲基-4-乙基戊烷 B、3,3-二甲基-4-乙基戊烷
C、3,3,4-三甲基已烷 D、2,3,3-三甲基已烷
6、炒菜时,又加料酒又加醋,可使菜变得香美可口,原因是
A、有盐类物质生成 B、有酸类物质生成
C、有油脂类物质生成 D、有酯类物质生成
7、盆烯是近年合成的一种有机物,它的分子结构可简化表示为(其中C、H原子已略去),下列关于盆烯的说法中错误的是
A、盆烯是苯的一种同分异构体
B、盆烯分子中所有的碳原子不可能在同一平面上
C、盆烯是乙烯的一种同系物 D、盆烯在一定条件下可以发生加成反应
8、有机物的天然提取和人工合成往往得到的是混合物,假设给你一种这样的有机混合物让你研究,一般要采取的几个步骤是
A、分离、提纯→确定化学式→确定实验式→确定结构式
B、分离、提纯→确定实验式→确定化学式→确定结构式
C、分离、提纯→确定结构式→确定实验式→确定化学式
D、确定化学式→确定实验式→确定结构式→分离、提纯
二、选择题(每题有1到2个答案符合题意,4×6共24分,部分分2分)
9、下列各组物质中,属于同分异构体的是
A、O2和O3 B、CH2=CHCH2CH3和CH3CH=CHCH3
C、CH3CH2CH3和CH3(CH2)2CH3 D、CH3CH2OH和CH3OCH3
10、某化合物6.4 g在氧气中完全燃烧,只生成8.8 g CO2和7.2 g H2O。下列说法正确的是
A、该化合物仅含碳、氢两种元素 B、该化合物中碳、氢原子个数比为1:4
C、无法确定该化合物是否含有氧元素 D、该化合物中一定含有氧元素
11、下列物质一定属于同系物的是
A、④和⑧ B、①、②和③ C、⑤和⑦ D、④、⑥和⑧
12、氯仿可用作全身麻醉剂,但在光照条件下,易被氧化成生成剧毒的光气(COCl2) 2CHCl3 +O2 2HCl+2COCl2 为防止发生医疗事故,在使用前要先检查是否
变质。下列那种试剂用于检验效果最好
A、烧碱溶液 B、溴水 C、KI淀粉溶液 D、AgNO3溶液
13、m mol C2H2跟n mol H2在密闭容器中反应,当该可逆反应达到平衡时,生成p mol C2H4。将反应后的混合气体完全燃烧,生成CO2和H2O,所需要氧气的物质的是
A、(3m+n)mol B、 C、(3m+n+2p)mol D、
14、拟除虫菊酯是一类高效、低毒、对昆虫具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如图,下列对该化合物叙述正确的是
A、属于芳香烃 B、不能使酸性高锰酸钾溶液褪色
C、在酸性条件下不水解 D、在一定条件下可以发生加成反应
第Ⅱ卷(共72分)
三、实验题(本大题共2小题,共22分)
15、(10分)某同学为测定维生素C中碳、氢的质量分数,取维生素C样品研碎,称取该试样0.352 g,置于铂舟并放入燃烧管中,不断通入氧气流。用酒精喷灯持续加热样品,将生成物先后通过浓硫酸和碱石灰,两者分别增重0.144 g和0.528 g,生成物完全被吸收。试回答以下问题:
(1)维生素C中碳的质量分数是_______________,氢的质量分数____________________
(2)维生素中是否含有氧元素?为什么?(试通过计算说明)
_____________________________________________________________
(3)如果需要你确定维生素C的分子式,你还需要哪些信息?
_________________________________________________________________________
16、(12分)如右图,在左试管中先加入2mL 95%的乙醇,并在摇动下缓缓加入3mL浓硫酸,再加入2 mL乙酸,充分摇匀。在右试管中加入5mL饱和Na2CO3溶液。按图连接好装置,用酒精灯对右试管小火加热3~5min后,改用大火加热,当观察到左试管中有明显现象时停止实验。
(1)写出左试管中主要反应的方程式: ______________________________________________ (2)加入浓硫酸的作用:___________________________________;
(3)饱和Na2CO3的作用是____________________________________________________;
(4)反应开始时用酒精灯对左试管小火加热的原因是: _______
_____________ ______;(已知乙酸乙酯的沸点为77℃;乙醇的沸点为78.5℃;乙酸的沸点为117.9℃)
(5)分离右试管中所得乙酸乙酯和Na2CO3溶液的操作为(只填名称) ,所需主要仪器为 。
(6)实验生成的乙酸乙酯,其密度比水 ,有 气味。
四、论述题(本大题共3小题,共32分)
17、(10分)
(1)(8分)按官能团的不同,可以对有机物进行分类,请指出下列有机物的种类,填在横线上。
CH3CH2CH2COOH __________;___________;____________ ________________;
(2)(2分)写出2-甲基-1-戊烯的结构简式: ;
18、(16分)
(1)(6分)有机物的结构可用“键线式”简化表示。CH3—CH=CH-CH3可简写为 。
有机物X的键线式为:
(1)有机物Y是X的同分异构体,且属于芳香烃,写出Y的结构简式。
(2)Y在一定条件下能发生聚合反应,写出其反应的化学方程式:
(3)X与足量的H2在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有 种。
(2)(10分)已知乳酸的结构简式为 。试回答:
(1)乳酸分子中含有________和_________两种官能团(写名称);
(2)乳酸与金属钠溶液反应的化学方程式为
________________________________________________________________________;
(3)乳酸与NaHCO3溶液反应的化学方程式为
________________________________________________________________________;
19、(6分)下列两幅谱图是结构简式为CH3CH2CH2OH和CH3CH(OH)CH3的两种有机化合物的1H核磁共振谱图。请判断哪一幅是CH3CH(OH)CH3的1H-NMR谱图,并说明理由。
__________________________________________________________________
__________________________________________________________________
五、计算题(本大题共2小题,共18分)
20、(8分)实验测定某有机物元素质量组成为C:69%,H:4.6%,N:8.0%,其余是O,相对分子质量在300-400之间,试确定该有机物的:(1)相对分子质量;(2)分子式。
21、(10分)某混合气体由一种气态烷烃和一种气态烯烃组成,在同温同压下,混合气体对氢气的相对密度为13,在标准状况下,将56.0L混合气体通入足量溴水,溴水质量增重35.0g,通过计算回答:
(1)混合气体中气态烷烃的化学式:
(2)混合气体中两种气体的物质的量之比:
(3)写出混合气体中气态烯烃可能的结构简式: 。
班级___ _ _考试号__ 泰兴市第二高级中学高一周考
姓名____ ____ 化学试题答题纸
第Ⅱ卷(共72分)
三、实验题(本大题共2小题,共22分)
15、(10分)试回答以下问题:
(1)维生素C中碳的质量分数是_______________,氢的质量分数____________________
(2)维生素中是否含有氧元素?为什么?(试通过计算说明)
____________________________________________________________________________________________________________________________________________________________________________
(3)__________________________________________________________________________________
16、(12分)
(1)化学方程式: _______________________ (2)加入浓硫酸的作用:_________________、_________________;
(3)饱和Na2CO3的作用是____________________、__________ _________、_______ ______;
(4)原因是: _______ ______ ______ ______;
(5)操作为(只填名称) ,所需主要仪器为 。
(6)其密度比水 ,有 气味。
四、论述题(本大题共3小题,共32分)
17、(10分)
(1)(8分)
CH3CH2CH2COOH __________;___________;____________ ________________;
(2)(2分)写出2-甲基-1-戊烯的结构简式: ;
18、(16分)
(1)(6分)
(1)写出Y的结构简式。
(2)反应的化学方程式:
(3)Z的一氯代物有 种。
(2)(10分)
(1)乳酸分子中含有________和_________两种官能团(写名称);
(2)
________________________________________________________________________;
(3)
________________________________________________________________________;
19、(6分)
结论:____________________________________________
理由:_________________ ____
______________________________ ____________________________________
五、计算题(本大题共2小题,共18分)
20、(8分)(1)相对分子质量____________________;(2)分子式______________。
计算过程:
21、(10分)
(1)气态烷烃的化学式:
(2)物质的量之比:
(3)写出混合气体中气态烯烃可能的结构简式: 。
计算过程:
泰兴市第二高级中学高一周考
化学试题答案
一、二、选择题
题号 1 2 3 4 5 6 7 8
答案 A B B B C D C B
题号 9 10 11 12 13 14
答案 BD BD AC D D D
15、(共10分)
(1)40.91%(2分),4.55% (2分)
(2)已知,m(H)=0.144 g÷9=0.016 g,m(C)=0.528g×12÷44=0.144g, m(H)+ m(C)=0.016g+0.144g=0.160g<0.352g,又因产物中只有H2O和CO2,故维生素中必含有氧。(结论1分,理由2分)
(3)若要确定其分子式,还要知其相对分子质量。 (3分)
16、(12分)(1)(2分)
(2)催化剂、吸水剂。(2分,每个原因1分)
(3)中和乙酸、溶解乙醇、降低乙酸乙酯的溶解度。(2分,至少2个原因,否则得1分)
(4)加快反应速率,同时又防止了反应物未来得及反应而挥发损失;(2分)
(5)分液;分液漏斗。 (各1分,共2分)
(6)小;芳香。(各1分共2分)
17、(10分)(1)羧酸类,酚类,芳香烃,酯类, (每空2分,共8分)
(2)略(2分)
18、(16分)
(1)(6分)(1) (2分)
(2)略 (2分)
(3) 2(2分)
(2)(1)羟基,羧基 (每空2分)
(2) + 2Na + H2↑ (3分)
(3) + NaHCO3 + H2O + CO2↑(3分)
19、(1)A是CH3CH(OH)CH3的1H-NMR谱图,因为从结构上分析,CH3CH(OH)CH3有三种不同化学环境的H,而分析CH3CH2CH2OH有四种不同的H,故从图上分析,A上有三个峰,而B有四个峰,故A是CH3CH(OH)CH3的1H-NMR谱图。(判断2分,解释A、B对了各2分共4分,本题共6分)
20、(8分各4分,要有计算过程,否则不得分) 348 C20H16N2O4
21、(10分)
已知混合气体的平均相对分子质量为:13×2=26,则烷烃一定为CH4,混合烃总质量为
M(混合烃)=56.0L÷22.4L/mol×26g/mol=65 g
因烯烃的分子量最小为C2H4的28。可设烯烃的分子式为CnH2n,则有m(CnH2n)=35 g,m(CH4)=65g-35g =30g;则有65÷(30÷16+35÷14n)=26,解得:n=4,
则烯烃为C4H8;n(CH4):n(C4H8)=30÷16:35÷56=3:1
(1)CH4 (3分) (2) 3:1 (3分)
(3)CH2=CH-CH2CH3,CH3-CH=CH-CH3, CH2=C(CH3)2(共4分,少一个扣2分,扣完为止)
CH3-CH-COOH
OH
A
B
CH3-CH-COONa
ONa
CH3-CH-COOH
OH
CH3-CH-COONa
OH
CH3-CH-COOH
OH
PAGE
第1页
同课章节目录
