化学与能源
图片预览






文档简介
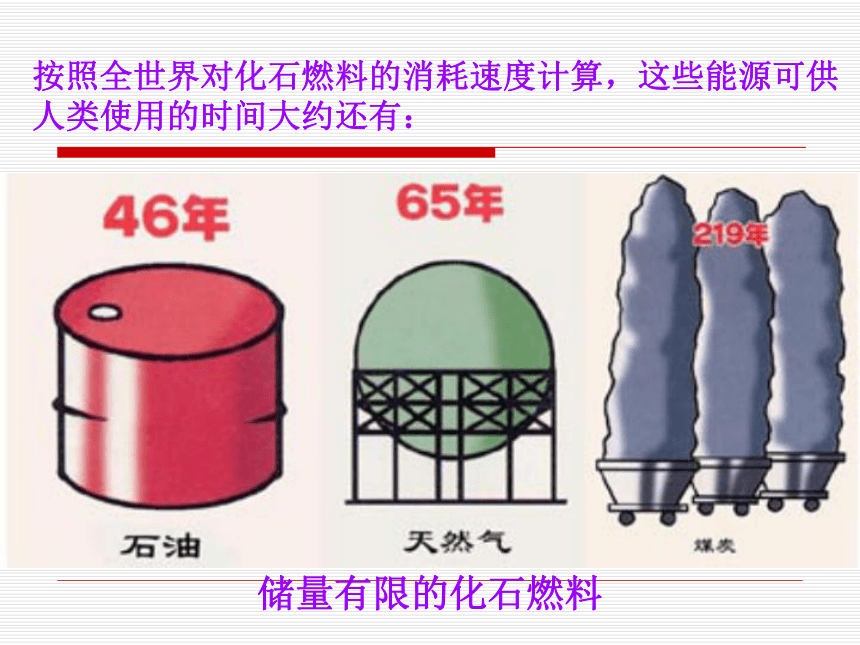
课件95张PPT。现代化学与能源一、我们所面临的能源状况目前全世界使用的能源90% 取自化石燃料,即煤炭、石油和天然气,它们经历了上亿年的时间才得以生成,因此是不可在生能源。从探明的储量分析,现在地球上的煤炭、石油和天然气的总储量分别为:
石 油:1万亿桶
天然气:120万亿立方米
煤 炭:1万亿吨按照全世界对化石燃料的消耗速度计算,这些能源可供人类使用的时间大约还有:储量有限的化石燃料我国一次能源消费总量从1978年的5.3亿吨标准煤,上升到2002年的14.3亿吨标煤。在2004年,我国石油消费量达3亿吨,其中进口1亿吨,估计到2020年,我国石油消费量要达4.5亿吨,其中进口量要达2.7亿吨,到2050年,我国石油消费量要达6亿吨,其中进口量要达4亿吨,相当于目前美国的石油进口量。大庆油田从1960年至2002年累计生产原油17多亿吨。
27年稳产在5000万吨/年以上。
1997年最高产量为5600万吨/年
2002年为5013万吨/年
2003年计划产量4830万吨/年
进入递减开采期。
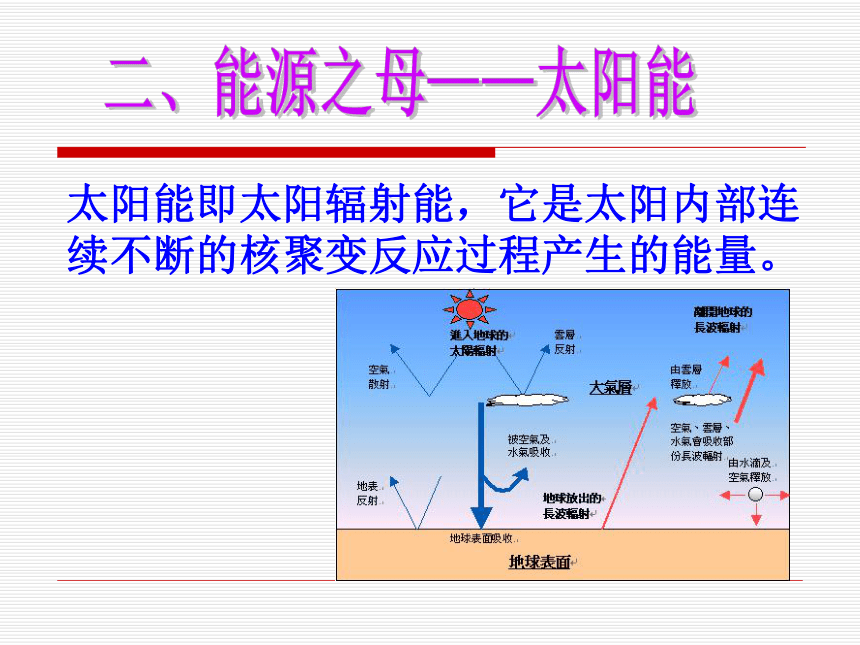
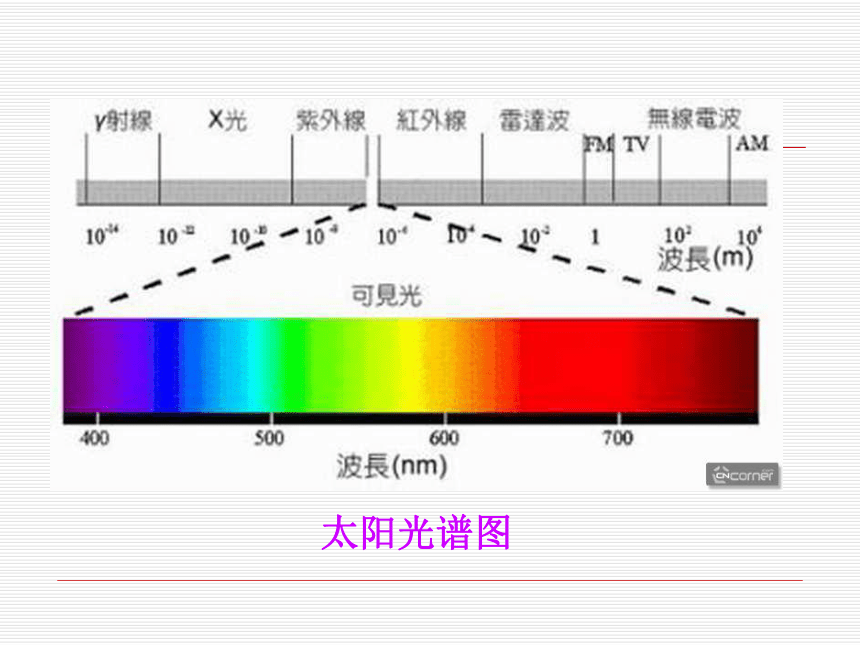
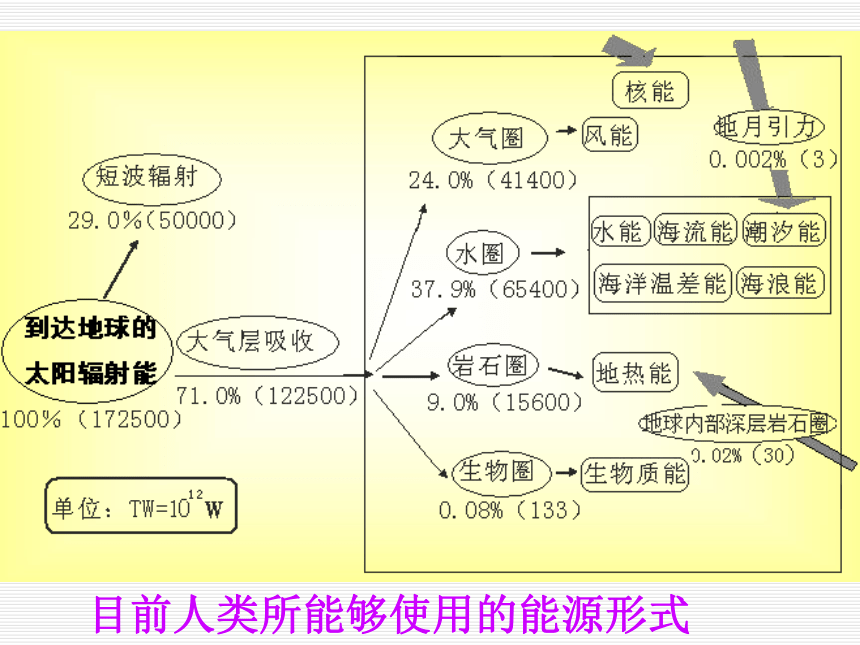
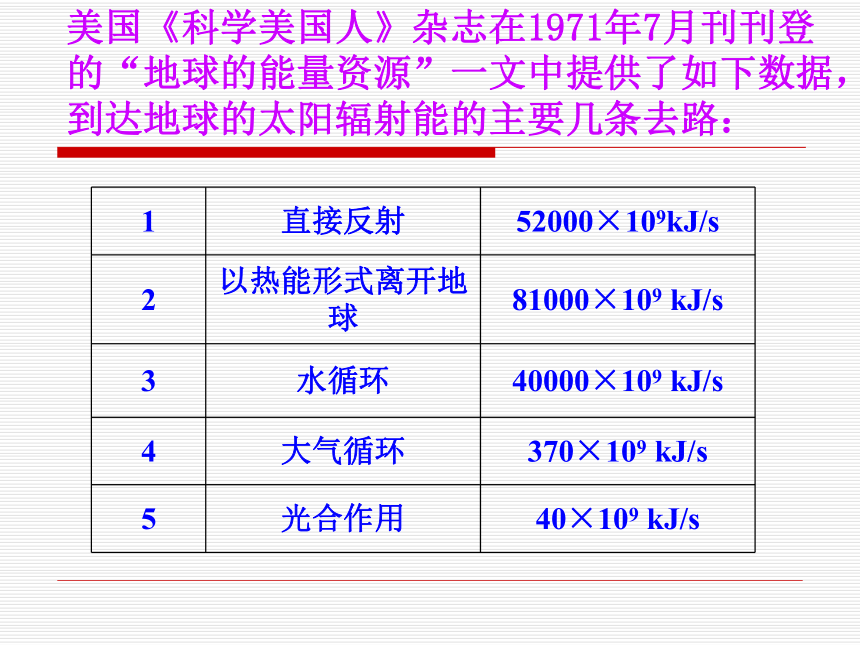
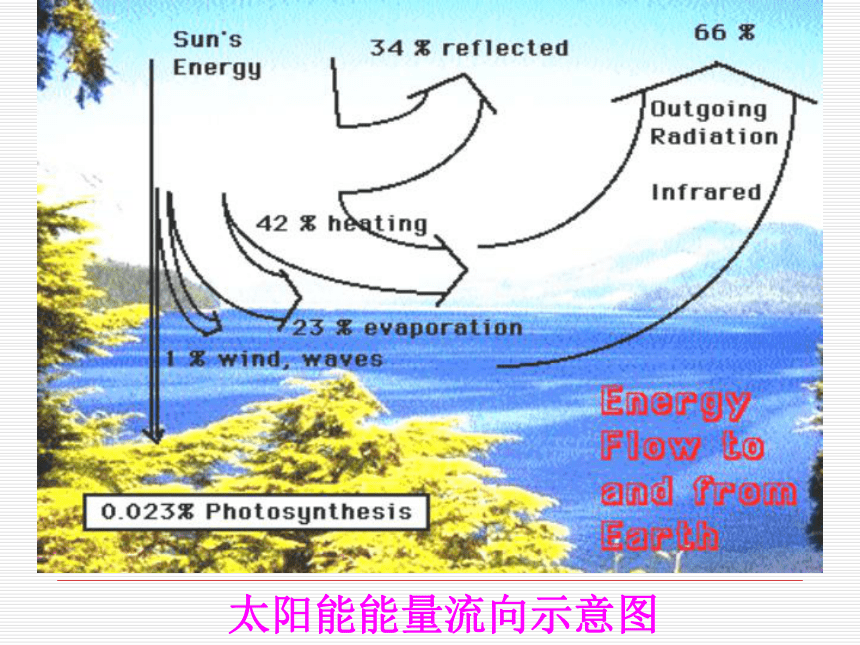
——化工报2003-1-18-1据美国石油业协会估计,在2050年之前,世界经济的发展将越来越多地依赖煤炭。其后在2250到2500年之间,煤炭也将消耗殆尽,矿物燃料供应枯竭。一些工业发达国家的天然气也将在2020年被用完;而发展中国家在2060年也将会发生天然气短缺。太阳能即太阳辐射能,它是太阳内部连续不断的核聚变反应过程产生的能量。二、能源之母——太阳能太阳光谱图地球轨道上的平均太阳辐射强度为1367kw/m2。地球赤道的周长为40000km,从而可计算出,地球获得的能量可达172,500TW。也就是说太阳每秒钟照射到地球上的能量就相当于500万吨煤。目前人类所能够使用的能源形式美国《科学美国人》杂志在1971年7月刊刊登的“地球的能量资源”一文中提供了如下数据,到达地球的太阳辐射能的主要几条去路:太阳能能量流向示意图(一)对太阳能的间接利用(1)通过光合作用的形式利用太阳能太阳能的间接利用 煤炭——当代工业的粮食
石油——当代工业的血液
天然气——最清洁的化学能源
可燃冰——未来的新能源
生物质能——前景广阔的绿色能源煤炭的结构煤炭液化 煤炭液化是指以煤炭为原料,通过化学加工过程,生产油品和石油化工产品。煤炭直接液化:煤炭间接液化:煤炭煤粉油煤浆加氢裂化液体油品煤炭、氧气、水蒸气H2和CO的混合气体石油的形成 石油是远古时代沉积在海底湖泊中的动植物的遗体,在海洋条件作用下经过千百万年的漫长转化过程而生成。水中生物的遗骸下沉而埋没于地下因地热或地压等作用变成石油石油大多集中在沙岩之类孔隙较多的岩石层中汽油性能的表征——辛烷值辛烷值是汽油抗暴性能的间接量度提高汽油辛烷值的方法:
1.提高异辛烷的含量—铂铼重整
2.加少量的四乙基铅[Pb(C2H5)2]无铅汽油与无铅抗爆剂 目前,取代四乙基铅的物质主要有:芳香烃类、甲基叔丁基醚[MTBE,CH3O(CH3)3]、三乙基丁醚、三戊基甲醚、羰基锰(MMT)、醇类等,其中以MTBE用量最大。无铅汽油不等于无害汽油(二)太阳辐射能的直接利用与其他能源相比,太阳能具有独特的优点:
(1)它没有一般煤炭、石油等矿物燃料产生的有害气体和废渣,因而不污染环境,被称作“干净能源”。
(2)到处都可以得到太阳能,使用方便、安全。
(3)成本低廉,可以再生。1、对太阳能直接利用的形式(1)对可见光的利用
主要的利用途径是光电转换,即把太阳能直接转换成电能。这是人们目前对太阳能利用的主要方式之一。太阳能电池就属于这种转换方式。传统的太阳能电池利用太阳光中高达九成以上的可见光。 太阳能电池太阳能电池主要以半导体材料为基础,利用光照产生电子空穴对,在PN结上可以产生光电流、光电压的现象(光伏效应),实现光电转换。硅是最合适最理想的太阳能电池材料。推进舱轨道舱附加舱通讯舱太阳能电池太阳能电池按照所用材料的不同:
硅太阳能电池(单晶硅、多晶硅、非晶硅)
(光电转化效率高,成本高,制备工艺复杂!)
以无机盐如砷化镓、硫化镉、铜铟硒等多元化合物为材料的电池
(镉:剧毒。铟、硒:稀有元素)
功能高分子材料制备的大阳能电池
(处于研发初期、转化效率低、使用寿命短)
染料敏化纳米晶体太阳能电池
(正在研发)
无机太阳能电池半导体中可以利用各种势垒如pn结、肖特基势垒、异质结等形成光伏效应。
当太阳能电池受到阳光照射时,光与半导体相互作用可以产生光生载流子,所产生的电子-空穴对靠半导体内形成的势垒分开到两极,正负电荷分别被上下电极收集。由电荷聚集所形成的电流通过金属导线流向电负载。 工作原理染料敏化纳米晶体太阳能电池 目前,DSSCs的光电转化效率已能稳定在10%以上,寿命能达15~20年,且其制造成本仅为硅太阳能电池的1/5~1/10. 1991年※,Gr?tzel M.于《Nature》上发表了关于染料敏化纳米
晶体太阳能电池( Dye Sensitized Solar Cells,简称DSSCs )的文
章以较低的成本得到了>7%的光电转化效率, 为利用太阳能提供
了一条新的途径.
1997年,该电池的光电转换效率达到了10%~11%,短路电流达
到18mA/cm2,开路电压达到720mV; 1998年,采用固体有机空穴传输材料替代液体电解质的全固态
Gratzel电池研制成功,其单色光电转换效率达到33%,从而引
起了全世界的关注。染料敏化太阳能电池的优点制成透明的产品,应用范围广
在各种光照条件下使用;
光的利用效率高;
对光阴影不敏感;
可在很宽温度范围内正常工作……染料敏化太阳能电池的结构 染料敏化纳米晶体太阳能电池(DSSCs)主要包括镀有透明导电膜的玻璃基底、染料敏化剂、多孔纳米晶薄膜、对电极以及电解质等几部分。叶绿体的结构纳米晶半导体网络结构相当于叶绿体的内囊体,起着支撑敏化剂染料分子、增加吸收太阳光的面积和传递电子的作用。敏化剂染料分子相当于叶绿体中的叶绿素,起着吸收太阳光光子的作用。染料敏化太阳能电池和植物的光合作用染料敏化太阳能电池的工作原理图由于TiO2的禁带宽度较大(32eV),可见光不能将其直接激发;在其表面吸附一层染料敏化剂后,染料分子可以吸收太阳光而产生电子跃迁。由于染料的激发态能级高于TiO2的导带,所以电子可以快速注入TiO2;电子在导带基底上富集,通过外电路流向对电极。染料分子输出电子后成为氧化态,它们随后被电解质中的I-还原而得以再生,而氧化态的电解质(I3-)在Pt对电极上得到电子被还原,从而完成一个光电化学反应循环。光电阳极:
Dye + hν→Dye* (染料激发)
Dye*→Dye++e-(TiO2)(产生光电流)
Dye++1.5I-→Dye+0.5I3-(染料还原)
阳极发生的净反应为:
1.5I-+hν→0.5I3-+e-(TiO2)
对电极:
0.5I3-+e-(Pt)→1.5I-(电解质还原)
整个电池的反应结果为:
e-(Pt)+hν→e-(TiO2)(光电流) 样 机太阳能电池的发展方向材料与器件结构的研究与开发
各种太阳能电池材料研究
杂质与缺陷的转换效率及稳定性影响
使用薄膜技术和剥离技术。
大规模生产技术的开发
跟踪与聚光
储电及并网发电结合
并网发电已占50%
以建成多个兆瓦级的电站,~100MW规模VS太阳能热发电站
与建筑物结合
架设太阳电池组件
日本:1994-2000年 2万套屋顶光伏系统185MW ;七万屋顶计划 280M
美国:1997~2010年 百万屋顶计划 3025MW 发电成本6美分
集成在建筑材料上
曲线形屋顶瓦、垂直幕墙、窗用玻璃太阳能发电站 太阳能光伏发电系统主要由太阳电池阵列、贮能蓄电池、防反充二极管、充电控制器及逆变器、测量设备等组成。 太阳能发电站一旦建成,不需要运行投资即能运用,但初期投资较高。 加利福尼亚一家太阳能发电站中的太阳能反射装置(2)对红外线的利用主要的利用途径是光热转换,即把太阳能直接转变成热能。太阳能热利用可分为:低温热利用、中温热利用和高温热利用。
低温热利用:地膜、塑料大棚
以及干燥器、蒸馏、供暖、太阳能热水系统
中温热利用:空调制冷、制盐以及
其它工业用热
高温热利用:聚焦形太阳灶、焊接机
和高温炉(3)对紫外线的利用紫外线具有杀菌功效。波长为300nm的紫外光的光子所具有的能量约为399kJ/mol,它比细菌的蛋白质分子中重要的化学键C-C(347 kJ/mol)、C-N(305 kJ/mol)和C-S(259 kJ/mol)键的键能大,因此紫外光的能量足以使这些化学键断裂,从而破坏细菌的蛋白质分子,达到杀菌的目的。(一)核裂变能 使一个重原子核分裂成为两个或两个以上中等质量原子核的过程,称为核裂变。核裂变是取得核能的重要途径之一。
只有一些质量非常大的原子核,像铀、钍等才能发生核裂变。原子核在发生核裂变时,释放出巨大的能量,1克235U完全发生核裂变后放出的能量相当于燃烧2.5吨煤所产生的能量。三、魔鬼与天使——核能要大规模地和平利用裂变能必须满足两个条件:
第一,重核裂变要形成链式反应;
第二,链式反应必须是可控的。实现可控链式反应的装置称为反应堆。链式反应中子鈾-235
核分裂人们将核反应堆形象地比喻为核电站的“锅炉”,在这种“锅炉”里烧的是铀、钚等核燃料。在核电站“锅炉”这个家庭中,有一个特殊成员——快中子增殖反应堆,简称“快堆”,现在已成为核反应中的佼佼者。在一般锅炉里的燃料如煤、燃油等都是越烧越少,而“快堆”的“燃料”却越烧越多,成了魔炉。“快堆”——明天的核电站“锅炉”在“快堆”中用的核燃料是239Pu(钚bù)。1个每吸收1个快中子发生裂变反应会放出2.45个快中子,除去1个用于链式裂变反应后,剩下的1.45个快中子会被装在反应区周围的238U(大量存在)吸收,产生1.45个新的核燃料原子239Pu 。“快堆”为什么会有增殖燃料的本领呢?就是说在核锅炉中一边“烧”掉,又一边使238U转为成新的,而且新产生的比“烧”掉的还多。这就使“快堆”的燃料越烧越多。“快堆”增殖核燃料把铀资源的利用率大大提高了,因为它正好解决了热中子核反应堆产生的大量238U废料堆积问题。一座快堆核电站,在5~15年的时间内可使燃料数量翻一番,通过建造快堆核电站,既能用238U发电,又能增殖燃料,因此“快堆”被人们称为“明天的核电站锅炉”。中国快堆在建设中1、放射性废料的危害
核废料是指含有α、β和γ辐射的不稳定元素并伴随有热产生的无用材料,核废料进入环境后会造成水、大气、土壤的污染,并通过各种途径进入人体,当放射性辐射超过一定水平,就能杀死生物体的细胞,妨碍正常细胞分裂和再生,引起细胞内遗传信息的突变。核裂变能的利用带来的问题研究表明,孕妇在怀孕初期腹部受过X光照射,她们生下的孩子与母亲不受X光照射的孩子相比,死于白血病的概率要大50%。受放射性污染的人在数年或数十年后,可能出现癌症、白内障、失明、生长迟缓、生育力降低等远期效应,还可能出现胎儿畸形、流产、死产等遗传效应。? 2、放射性核废料的处理
与核能相关的一个最困难的问题就是在开采、燃料生产以及反应堆的运行过程中产生的核废料的处理,如何处理这些废料可能将是最终核能使用的最大障碍。目前,核废料的处理有“天葬”、“水葬”和“火葬”三种方法。切尔诺贝利核电站所谓“天葬”是指:把核废料先固化成玻璃块,装到特制的合金棺中,在棺材外面装上隔热外套,然后用航天飞机把它带入预定的轨道,机械手随即把它推入太空,再点燃助推火箭将它送入3000千米的轨道上,让核废料远远离开人类生活的地球。“火葬”是美国能源部研制的一种处理核废料的先进方法。火葬前,先在地下挖一个深坑,把放射性物质放入坑内,用特制的盖子把坑顶盖好。将空气净化器上的一根导管从盖子上插入坑内,坑内装4个碳电极,电极接通后,就会产生一股强大的电流,使坑内的泥土温度上升到几百度。在这样的高温下,泥土开始溶化,使核废料均匀地分布在浆状的泥石溶液里。当溶化的泥石浆冷却后,与核废料一起形成了一种类似天然岩石的坚硬物质,其硬度比天然花岗石和大理石更高,渗透性更低,而且体积也缩小了好几倍。最后用泥土把坑封死,一切放射性物质均被围困在里面,不会外泄。“水葬”就是将深海作为核废料的墓场。将核废料装入密封的合金棺,再用混凝土密封在海底下面。(二)核聚变太阳的中心发生核聚变,放出巨大能量。在太阳内部,这个天然的核聚变过程以及发生了了好几十亿年了。核聚变的引发和平利用聚变能实验非常困难,因为核力是一种短程力,只有当它们之间的距离接近到大约万分之一毫米时,核力能才起作用,使两个原子核聚合在一起,放出巨大的能量。所有的原子核都带正电,两个带正电的原子核互相接近时,它们之间的库仑斥越来越大。所以实现聚变反应的条件是反应中的原子核必须具有很高的能量来克服静电斥力,使两核之间的距离进入核力力程。据测算这样的能量将使氘核的温度达到5.6×108k 。 氘原子被加热到上亿度的时候,电子就会脱离原子核的束缚,成为一团炽热的气体——等离子气体。 如何容纳这么热的等离子体强大的磁场可以牢牢地束缚住炽热的等离子体。磁场!?科学家建造了一个如同面包圈形状的空腔,空腔内是真空,其外是产生磁场的线圈。这个古怪的烤炉同时有一个古怪的名字:托卡马克(tokamak).温度高达近亿度的等离子体就被舒服在这个空腔内部,不会接触到容器壁,不会出乱子。电池的分类:
电池按照其使用性质的不同可以分为干电池、蓄电池、储备电池和燃料电池等几大类。 四、化学电池——实用的能源原电池锌锰干电池:负极是锌做的圆筒,
正极是一根探棒,周围被二氧化锰、碳粉和氯化铵的混合剂包围。干电池发电时反应如下:负极:Zn - 2e- = Zn2+
正极:2NH4+ + MnO2+2e- = 2NH3 + MnO + H2O
电池反应:Zn+2NH4Cl+MnO2=ZnCl2+2NH3+ MnO+H2O 使用过程中,负极锌筒逐渐消耗以致穿漏,正极处的MnO2的活性逐渐衰减,最后干电池不再供电而失效。蓄电池 蓄电池又称二次电池,可以通过充电使活性物质再生。蓄电池的两极均以铅板为骨架,正极铅板上是二氧化铅,负极铅板上是海绵状铅。内部构造外部构造蓄电池放电时发生下列反应:
负极(Pb):Pb+SO42--2e- = PbSO4
正极(PbO2):PbO2+4H++SO42-+2e- = PbSO4+2H2O
总反应:Pb+PbO2+2H2SO4 = 2PbSO4+2H2O
电池充电时发生与
上述反应相反的反应
电动自行车锂电池 锂电池分为一次电池和二次电池两类,照相机等耗电量较低的电子产品中主要使用不可充电的一次锂电池,而摄像机、数码相机、手机及笔记本电脑等耗电量较大的电子产品中则使用可充放电的二次锂电池。锂电池自行车目前,商业化锂离子二次电池的正极材料主要是LiCoO2,负极材料主要为C,充电时发生如下反应: ? 正极反应:LiCoO2= Li1-xCoO2 + xLi+ + xe- ? 负极反应:C + xLi+ + xe-= CLix ? 电池总反应:LiCoO2 + C=
Li1-xCoO2 + CLix ?放电时发生上述反应的逆反应。镍氢电池(高压镍氢电池)正极:Ni电极 NiO(OH)+ H2O + e- =Ni(OH)2+OH-
负极:氢电极 1/2H2 + OH- =H2O + e-
总反应: 1/2H2 + NiO(OH) = Ni(OH)2
电解质:KOH 电池内氢气的压力:0.3-4MPa燃料电池燃料电池(Fuel Cell , FC)是一种把储存在燃料和氧化剂中的化学能高效、环境友好地按电化学原理转化为电能的能量转换装置,也是一种新型的无污染、无噪音、大规模、大功率和高效率的汽车动力。作为一种最接近于实用化的环保型新能源,燃料电池已经受到了人们的广泛关注。燃料电池的原理 氢氧燃料电池工作时向负极供给燃料(氢),向正极供给氧化剂(空气或氧气)。
氢在负极解离成H+和电子,H+进入电解液中,而电子则沿外部电路移向正极,用电的负载就接在外部电路中。
在正极上,氧与电解液中的氢离子获得经外电路抵达正极上的电子而形成水。氢氧燃料电池原理图燃料电池的种类燃料电池按照电解质类型分为五种:
碱性燃料电池(AFC)
磷酸型燃料电池(PAFC)
熔融碳酸盐型燃料电池(MCFC)
固体氧化物型燃料电池(SOFC)
质子交换膜燃料电池(PEMFC)燃料电池的优点(1)能量转换效率高(节省燃料资源)。 (2)污染小、噪声低。 (3)高度的可靠性氢能源 氢能经济的背景大气中二氧化碳逐年增加,地球不断变暖,生态环境恶化,自然灾害频发,造成的损失逐年增加。
化石能源储量有限,消耗加快。
能源结构单一,过渡依赖化石能源。
经济增长、环境保护和社会发展的压力。氢:储量大,分布广,清洁无污染氢能社会构想再生能源制氢CO2处理加氢站燃料电池工厂天然气制氢电厂终端用户氢气作为能源遇到的两个问题 氢气的制备氢气的储存(一)氢气的制备(1)热化学工艺制氢
热化学工艺主要是将碳水化合物(煤、石油、天然气、生物质等) 输入高温化学反应器 ,生成由H2、CO 、CO2 和 CH4 等组成的合成气体 ,然后进行重整和水气置换反应来提高氢的产量 ,最后将氢气分离提纯得到可以用做交通燃料的氢气。甲烷重整制氢:
CH4 + H2O=3H2 + CO
这个反应是吸热反应,需要外部输入热量,反应温度大约700℃~850℃,反应压力为3×105 Pa~2.5 ×105Pa。反应产物合成气被输入到下一级水气置换反应器 ,经过水气置换反应,将CO转化为H2,提高了氢的产量。
CO + H2O = H2 + CO2
重整制氢的能量转换效率可以达到75 %~80 %,经济有效,如果将余热回收利用,效率可达85%以上部分氧化制氢是将碳氢化合物部分氧化生成CO和氢的工艺。
2CH4 + O2=4H2 +2CO
加入催化剂,系统转化效率会大大提高。反应产物合成气也和重整制氢一样,需要进行水气置换反应,以提高H2 的产量。最后再经过分离提纯,得到可以用于交通工具的燃料。由于这个生产过程中也有CO2的排放,所以也是通向环保制氢的过渡。 利用煤和生物质等气化制氢是将这些物质在高温下裂解成合成气后进行水气转换等过程,提高氢的成分,最后经过净化处理得到燃料氢。其中煤的气化制氢是目前广泛使用的制氢技术。(2)电解水制氢工艺该反应只要对电解槽通入直流电即可进行,操作简单,效率较高 ,现在已经发展了多种电解槽,如碱性电解槽、质子交换膜电解槽和固体氧化物电解槽等。用太阳能电池产生的电能电解水是制氢的一条具有十分诱人前景的途径。
人工光合作用的研究为太阳能制氢提供了另外一条途径。光合作用的核心是由太阳光驱动将水分子裂解为氧气、氢离子和电子。植物通过还原碳元素的形式将太阳能固定下来,能否不要将太阳能固定在碳元素中得到利用呢?人工光合作用将使这种想法成为可能,它完全抛弃了植物载体,只利用光合作用的原理,通过光裂解水分子,直接提取氢气。拆开水分子所需要的能量足以摧毁任何生物分子,然而植物每天都在进行着这个反应而没有任何不良后果。?秘密存在于催化核心的结构中。植物进行光合作用离不开叶绿素,而叶绿素中对光合作用起关键作用的就是催化核心。催化核心是由4个锰离子、1个钙离子、4个氧原子和至少2个水分子组成的,其中3个锰离子、1个钙离子和4个氧组成一个扭曲立方体,锰离子和钙离子通过氧原子相连接。第四个锰离子位于立方体的外部,结合着1个水分子。这一发现对于了解和复制水裂解化学过程具有重要意义。氢气的储存 硼氢化合物
热分解制氢——NH3BH3、LiBH4等
水分解制氢——NaBH4(SBH)等
BN纳米结构材料
硼促进贮氢材料含硼贮氢材料硼氢化合物贮氢Prof. A. Zuttel, Switzerland Univ Fribourg 450℃ 左右可以获得13.5 wt% H2LiBH4分解制氢强放热反应 可以获得13.6 wt% H2 LiBH4分解制氢120℃-300℃ 19.6 wt% H2
不足: NH3BH3制备成本偏高 NH3BN3分解制氢 B99N99C186 nanotubesAtomic structure modelsBN纳米结构贮氢近年来,大量的研究集中在纳米碳管储氢方面,主要是人们认为纳米碳管的储氢容量高,理论上可达10%。氢能的利用 (1)直接燃烧(2)燃料电池 谢谢大家!
石 油:1万亿桶
天然气:120万亿立方米
煤 炭:1万亿吨按照全世界对化石燃料的消耗速度计算,这些能源可供人类使用的时间大约还有:储量有限的化石燃料我国一次能源消费总量从1978年的5.3亿吨标准煤,上升到2002年的14.3亿吨标煤。在2004年,我国石油消费量达3亿吨,其中进口1亿吨,估计到2020年,我国石油消费量要达4.5亿吨,其中进口量要达2.7亿吨,到2050年,我国石油消费量要达6亿吨,其中进口量要达4亿吨,相当于目前美国的石油进口量。大庆油田从1960年至2002年累计生产原油17多亿吨。
27年稳产在5000万吨/年以上。
1997年最高产量为5600万吨/年
2002年为5013万吨/年
2003年计划产量4830万吨/年
进入递减开采期。
——化工报2003-1-18-1据美国石油业协会估计,在2050年之前,世界经济的发展将越来越多地依赖煤炭。其后在2250到2500年之间,煤炭也将消耗殆尽,矿物燃料供应枯竭。一些工业发达国家的天然气也将在2020年被用完;而发展中国家在2060年也将会发生天然气短缺。太阳能即太阳辐射能,它是太阳内部连续不断的核聚变反应过程产生的能量。二、能源之母——太阳能太阳光谱图地球轨道上的平均太阳辐射强度为1367kw/m2。地球赤道的周长为40000km,从而可计算出,地球获得的能量可达172,500TW。也就是说太阳每秒钟照射到地球上的能量就相当于500万吨煤。目前人类所能够使用的能源形式美国《科学美国人》杂志在1971年7月刊刊登的“地球的能量资源”一文中提供了如下数据,到达地球的太阳辐射能的主要几条去路:太阳能能量流向示意图(一)对太阳能的间接利用(1)通过光合作用的形式利用太阳能太阳能的间接利用 煤炭——当代工业的粮食
石油——当代工业的血液
天然气——最清洁的化学能源
可燃冰——未来的新能源
生物质能——前景广阔的绿色能源煤炭的结构煤炭液化 煤炭液化是指以煤炭为原料,通过化学加工过程,生产油品和石油化工产品。煤炭直接液化:煤炭间接液化:煤炭煤粉油煤浆加氢裂化液体油品煤炭、氧气、水蒸气H2和CO的混合气体石油的形成 石油是远古时代沉积在海底湖泊中的动植物的遗体,在海洋条件作用下经过千百万年的漫长转化过程而生成。水中生物的遗骸下沉而埋没于地下因地热或地压等作用变成石油石油大多集中在沙岩之类孔隙较多的岩石层中汽油性能的表征——辛烷值辛烷值是汽油抗暴性能的间接量度提高汽油辛烷值的方法:
1.提高异辛烷的含量—铂铼重整
2.加少量的四乙基铅[Pb(C2H5)2]无铅汽油与无铅抗爆剂 目前,取代四乙基铅的物质主要有:芳香烃类、甲基叔丁基醚[MTBE,CH3O(CH3)3]、三乙基丁醚、三戊基甲醚、羰基锰(MMT)、醇类等,其中以MTBE用量最大。无铅汽油不等于无害汽油(二)太阳辐射能的直接利用与其他能源相比,太阳能具有独特的优点:
(1)它没有一般煤炭、石油等矿物燃料产生的有害气体和废渣,因而不污染环境,被称作“干净能源”。
(2)到处都可以得到太阳能,使用方便、安全。
(3)成本低廉,可以再生。1、对太阳能直接利用的形式(1)对可见光的利用
主要的利用途径是光电转换,即把太阳能直接转换成电能。这是人们目前对太阳能利用的主要方式之一。太阳能电池就属于这种转换方式。传统的太阳能电池利用太阳光中高达九成以上的可见光。 太阳能电池太阳能电池主要以半导体材料为基础,利用光照产生电子空穴对,在PN结上可以产生光电流、光电压的现象(光伏效应),实现光电转换。硅是最合适最理想的太阳能电池材料。推进舱轨道舱附加舱通讯舱太阳能电池太阳能电池按照所用材料的不同:
硅太阳能电池(单晶硅、多晶硅、非晶硅)
(光电转化效率高,成本高,制备工艺复杂!)
以无机盐如砷化镓、硫化镉、铜铟硒等多元化合物为材料的电池
(镉:剧毒。铟、硒:稀有元素)
功能高分子材料制备的大阳能电池
(处于研发初期、转化效率低、使用寿命短)
染料敏化纳米晶体太阳能电池
(正在研发)
无机太阳能电池半导体中可以利用各种势垒如pn结、肖特基势垒、异质结等形成光伏效应。
当太阳能电池受到阳光照射时,光与半导体相互作用可以产生光生载流子,所产生的电子-空穴对靠半导体内形成的势垒分开到两极,正负电荷分别被上下电极收集。由电荷聚集所形成的电流通过金属导线流向电负载。 工作原理染料敏化纳米晶体太阳能电池 目前,DSSCs的光电转化效率已能稳定在10%以上,寿命能达15~20年,且其制造成本仅为硅太阳能电池的1/5~1/10. 1991年※,Gr?tzel M.于《Nature》上发表了关于染料敏化纳米
晶体太阳能电池( Dye Sensitized Solar Cells,简称DSSCs )的文
章以较低的成本得到了>7%的光电转化效率, 为利用太阳能提供
了一条新的途径.
1997年,该电池的光电转换效率达到了10%~11%,短路电流达
到18mA/cm2,开路电压达到720mV; 1998年,采用固体有机空穴传输材料替代液体电解质的全固态
Gratzel电池研制成功,其单色光电转换效率达到33%,从而引
起了全世界的关注。染料敏化太阳能电池的优点制成透明的产品,应用范围广
在各种光照条件下使用;
光的利用效率高;
对光阴影不敏感;
可在很宽温度范围内正常工作……染料敏化太阳能电池的结构 染料敏化纳米晶体太阳能电池(DSSCs)主要包括镀有透明导电膜的玻璃基底、染料敏化剂、多孔纳米晶薄膜、对电极以及电解质等几部分。叶绿体的结构纳米晶半导体网络结构相当于叶绿体的内囊体,起着支撑敏化剂染料分子、增加吸收太阳光的面积和传递电子的作用。敏化剂染料分子相当于叶绿体中的叶绿素,起着吸收太阳光光子的作用。染料敏化太阳能电池和植物的光合作用染料敏化太阳能电池的工作原理图由于TiO2的禁带宽度较大(32eV),可见光不能将其直接激发;在其表面吸附一层染料敏化剂后,染料分子可以吸收太阳光而产生电子跃迁。由于染料的激发态能级高于TiO2的导带,所以电子可以快速注入TiO2;电子在导带基底上富集,通过外电路流向对电极。染料分子输出电子后成为氧化态,它们随后被电解质中的I-还原而得以再生,而氧化态的电解质(I3-)在Pt对电极上得到电子被还原,从而完成一个光电化学反应循环。光电阳极:
Dye + hν→Dye* (染料激发)
Dye*→Dye++e-(TiO2)(产生光电流)
Dye++1.5I-→Dye+0.5I3-(染料还原)
阳极发生的净反应为:
1.5I-+hν→0.5I3-+e-(TiO2)
对电极:
0.5I3-+e-(Pt)→1.5I-(电解质还原)
整个电池的反应结果为:
e-(Pt)+hν→e-(TiO2)(光电流) 样 机太阳能电池的发展方向材料与器件结构的研究与开发
各种太阳能电池材料研究
杂质与缺陷的转换效率及稳定性影响
使用薄膜技术和剥离技术。
大规模生产技术的开发
跟踪与聚光
储电及并网发电结合
并网发电已占50%
以建成多个兆瓦级的电站,~100MW规模VS太阳能热发电站
与建筑物结合
架设太阳电池组件
日本:1994-2000年 2万套屋顶光伏系统185MW ;七万屋顶计划 280M
美国:1997~2010年 百万屋顶计划 3025MW 发电成本6美分
集成在建筑材料上
曲线形屋顶瓦、垂直幕墙、窗用玻璃太阳能发电站 太阳能光伏发电系统主要由太阳电池阵列、贮能蓄电池、防反充二极管、充电控制器及逆变器、测量设备等组成。 太阳能发电站一旦建成,不需要运行投资即能运用,但初期投资较高。 加利福尼亚一家太阳能发电站中的太阳能反射装置(2)对红外线的利用主要的利用途径是光热转换,即把太阳能直接转变成热能。太阳能热利用可分为:低温热利用、中温热利用和高温热利用。
低温热利用:地膜、塑料大棚
以及干燥器、蒸馏、供暖、太阳能热水系统
中温热利用:空调制冷、制盐以及
其它工业用热
高温热利用:聚焦形太阳灶、焊接机
和高温炉(3)对紫外线的利用紫外线具有杀菌功效。波长为300nm的紫外光的光子所具有的能量约为399kJ/mol,它比细菌的蛋白质分子中重要的化学键C-C(347 kJ/mol)、C-N(305 kJ/mol)和C-S(259 kJ/mol)键的键能大,因此紫外光的能量足以使这些化学键断裂,从而破坏细菌的蛋白质分子,达到杀菌的目的。(一)核裂变能 使一个重原子核分裂成为两个或两个以上中等质量原子核的过程,称为核裂变。核裂变是取得核能的重要途径之一。
只有一些质量非常大的原子核,像铀、钍等才能发生核裂变。原子核在发生核裂变时,释放出巨大的能量,1克235U完全发生核裂变后放出的能量相当于燃烧2.5吨煤所产生的能量。三、魔鬼与天使——核能要大规模地和平利用裂变能必须满足两个条件:
第一,重核裂变要形成链式反应;
第二,链式反应必须是可控的。实现可控链式反应的装置称为反应堆。链式反应中子鈾-235
核分裂人们将核反应堆形象地比喻为核电站的“锅炉”,在这种“锅炉”里烧的是铀、钚等核燃料。在核电站“锅炉”这个家庭中,有一个特殊成员——快中子增殖反应堆,简称“快堆”,现在已成为核反应中的佼佼者。在一般锅炉里的燃料如煤、燃油等都是越烧越少,而“快堆”的“燃料”却越烧越多,成了魔炉。“快堆”——明天的核电站“锅炉”在“快堆”中用的核燃料是239Pu(钚bù)。1个每吸收1个快中子发生裂变反应会放出2.45个快中子,除去1个用于链式裂变反应后,剩下的1.45个快中子会被装在反应区周围的238U(大量存在)吸收,产生1.45个新的核燃料原子239Pu 。“快堆”为什么会有增殖燃料的本领呢?就是说在核锅炉中一边“烧”掉,又一边使238U转为成新的,而且新产生的比“烧”掉的还多。这就使“快堆”的燃料越烧越多。“快堆”增殖核燃料把铀资源的利用率大大提高了,因为它正好解决了热中子核反应堆产生的大量238U废料堆积问题。一座快堆核电站,在5~15年的时间内可使燃料数量翻一番,通过建造快堆核电站,既能用238U发电,又能增殖燃料,因此“快堆”被人们称为“明天的核电站锅炉”。中国快堆在建设中1、放射性废料的危害
核废料是指含有α、β和γ辐射的不稳定元素并伴随有热产生的无用材料,核废料进入环境后会造成水、大气、土壤的污染,并通过各种途径进入人体,当放射性辐射超过一定水平,就能杀死生物体的细胞,妨碍正常细胞分裂和再生,引起细胞内遗传信息的突变。核裂变能的利用带来的问题研究表明,孕妇在怀孕初期腹部受过X光照射,她们生下的孩子与母亲不受X光照射的孩子相比,死于白血病的概率要大50%。受放射性污染的人在数年或数十年后,可能出现癌症、白内障、失明、生长迟缓、生育力降低等远期效应,还可能出现胎儿畸形、流产、死产等遗传效应。? 2、放射性核废料的处理
与核能相关的一个最困难的问题就是在开采、燃料生产以及反应堆的运行过程中产生的核废料的处理,如何处理这些废料可能将是最终核能使用的最大障碍。目前,核废料的处理有“天葬”、“水葬”和“火葬”三种方法。切尔诺贝利核电站所谓“天葬”是指:把核废料先固化成玻璃块,装到特制的合金棺中,在棺材外面装上隔热外套,然后用航天飞机把它带入预定的轨道,机械手随即把它推入太空,再点燃助推火箭将它送入3000千米的轨道上,让核废料远远离开人类生活的地球。“火葬”是美国能源部研制的一种处理核废料的先进方法。火葬前,先在地下挖一个深坑,把放射性物质放入坑内,用特制的盖子把坑顶盖好。将空气净化器上的一根导管从盖子上插入坑内,坑内装4个碳电极,电极接通后,就会产生一股强大的电流,使坑内的泥土温度上升到几百度。在这样的高温下,泥土开始溶化,使核废料均匀地分布在浆状的泥石溶液里。当溶化的泥石浆冷却后,与核废料一起形成了一种类似天然岩石的坚硬物质,其硬度比天然花岗石和大理石更高,渗透性更低,而且体积也缩小了好几倍。最后用泥土把坑封死,一切放射性物质均被围困在里面,不会外泄。“水葬”就是将深海作为核废料的墓场。将核废料装入密封的合金棺,再用混凝土密封在海底下面。(二)核聚变太阳的中心发生核聚变,放出巨大能量。在太阳内部,这个天然的核聚变过程以及发生了了好几十亿年了。核聚变的引发和平利用聚变能实验非常困难,因为核力是一种短程力,只有当它们之间的距离接近到大约万分之一毫米时,核力能才起作用,使两个原子核聚合在一起,放出巨大的能量。所有的原子核都带正电,两个带正电的原子核互相接近时,它们之间的库仑斥越来越大。所以实现聚变反应的条件是反应中的原子核必须具有很高的能量来克服静电斥力,使两核之间的距离进入核力力程。据测算这样的能量将使氘核的温度达到5.6×108k 。 氘原子被加热到上亿度的时候,电子就会脱离原子核的束缚,成为一团炽热的气体——等离子气体。 如何容纳这么热的等离子体强大的磁场可以牢牢地束缚住炽热的等离子体。磁场!?科学家建造了一个如同面包圈形状的空腔,空腔内是真空,其外是产生磁场的线圈。这个古怪的烤炉同时有一个古怪的名字:托卡马克(tokamak).温度高达近亿度的等离子体就被舒服在这个空腔内部,不会接触到容器壁,不会出乱子。电池的分类:
电池按照其使用性质的不同可以分为干电池、蓄电池、储备电池和燃料电池等几大类。 四、化学电池——实用的能源原电池锌锰干电池:负极是锌做的圆筒,
正极是一根探棒,周围被二氧化锰、碳粉和氯化铵的混合剂包围。干电池发电时反应如下:负极:Zn - 2e- = Zn2+
正极:2NH4+ + MnO2+2e- = 2NH3 + MnO + H2O
电池反应:Zn+2NH4Cl+MnO2=ZnCl2+2NH3+ MnO+H2O 使用过程中,负极锌筒逐渐消耗以致穿漏,正极处的MnO2的活性逐渐衰减,最后干电池不再供电而失效。蓄电池 蓄电池又称二次电池,可以通过充电使活性物质再生。蓄电池的两极均以铅板为骨架,正极铅板上是二氧化铅,负极铅板上是海绵状铅。内部构造外部构造蓄电池放电时发生下列反应:
负极(Pb):Pb+SO42--2e- = PbSO4
正极(PbO2):PbO2+4H++SO42-+2e- = PbSO4+2H2O
总反应:Pb+PbO2+2H2SO4 = 2PbSO4+2H2O
电池充电时发生与
上述反应相反的反应
电动自行车锂电池 锂电池分为一次电池和二次电池两类,照相机等耗电量较低的电子产品中主要使用不可充电的一次锂电池,而摄像机、数码相机、手机及笔记本电脑等耗电量较大的电子产品中则使用可充放电的二次锂电池。锂电池自行车目前,商业化锂离子二次电池的正极材料主要是LiCoO2,负极材料主要为C,充电时发生如下反应: ? 正极反应:LiCoO2= Li1-xCoO2 + xLi+ + xe- ? 负极反应:C + xLi+ + xe-= CLix ? 电池总反应:LiCoO2 + C=
Li1-xCoO2 + CLix ?放电时发生上述反应的逆反应。镍氢电池(高压镍氢电池)正极:Ni电极 NiO(OH)+ H2O + e- =Ni(OH)2+OH-
负极:氢电极 1/2H2 + OH- =H2O + e-
总反应: 1/2H2 + NiO(OH) = Ni(OH)2
电解质:KOH 电池内氢气的压力:0.3-4MPa燃料电池燃料电池(Fuel Cell , FC)是一种把储存在燃料和氧化剂中的化学能高效、环境友好地按电化学原理转化为电能的能量转换装置,也是一种新型的无污染、无噪音、大规模、大功率和高效率的汽车动力。作为一种最接近于实用化的环保型新能源,燃料电池已经受到了人们的广泛关注。燃料电池的原理 氢氧燃料电池工作时向负极供给燃料(氢),向正极供给氧化剂(空气或氧气)。
氢在负极解离成H+和电子,H+进入电解液中,而电子则沿外部电路移向正极,用电的负载就接在外部电路中。
在正极上,氧与电解液中的氢离子获得经外电路抵达正极上的电子而形成水。氢氧燃料电池原理图燃料电池的种类燃料电池按照电解质类型分为五种:
碱性燃料电池(AFC)
磷酸型燃料电池(PAFC)
熔融碳酸盐型燃料电池(MCFC)
固体氧化物型燃料电池(SOFC)
质子交换膜燃料电池(PEMFC)燃料电池的优点(1)能量转换效率高(节省燃料资源)。 (2)污染小、噪声低。 (3)高度的可靠性氢能源 氢能经济的背景大气中二氧化碳逐年增加,地球不断变暖,生态环境恶化,自然灾害频发,造成的损失逐年增加。
化石能源储量有限,消耗加快。
能源结构单一,过渡依赖化石能源。
经济增长、环境保护和社会发展的压力。氢:储量大,分布广,清洁无污染氢能社会构想再生能源制氢CO2处理加氢站燃料电池工厂天然气制氢电厂终端用户氢气作为能源遇到的两个问题 氢气的制备氢气的储存(一)氢气的制备(1)热化学工艺制氢
热化学工艺主要是将碳水化合物(煤、石油、天然气、生物质等) 输入高温化学反应器 ,生成由H2、CO 、CO2 和 CH4 等组成的合成气体 ,然后进行重整和水气置换反应来提高氢的产量 ,最后将氢气分离提纯得到可以用做交通燃料的氢气。甲烷重整制氢:
CH4 + H2O=3H2 + CO
这个反应是吸热反应,需要外部输入热量,反应温度大约700℃~850℃,反应压力为3×105 Pa~2.5 ×105Pa。反应产物合成气被输入到下一级水气置换反应器 ,经过水气置换反应,将CO转化为H2,提高了氢的产量。
CO + H2O = H2 + CO2
重整制氢的能量转换效率可以达到75 %~80 %,经济有效,如果将余热回收利用,效率可达85%以上部分氧化制氢是将碳氢化合物部分氧化生成CO和氢的工艺。
2CH4 + O2=4H2 +2CO
加入催化剂,系统转化效率会大大提高。反应产物合成气也和重整制氢一样,需要进行水气置换反应,以提高H2 的产量。最后再经过分离提纯,得到可以用于交通工具的燃料。由于这个生产过程中也有CO2的排放,所以也是通向环保制氢的过渡。 利用煤和生物质等气化制氢是将这些物质在高温下裂解成合成气后进行水气转换等过程,提高氢的成分,最后经过净化处理得到燃料氢。其中煤的气化制氢是目前广泛使用的制氢技术。(2)电解水制氢工艺该反应只要对电解槽通入直流电即可进行,操作简单,效率较高 ,现在已经发展了多种电解槽,如碱性电解槽、质子交换膜电解槽和固体氧化物电解槽等。用太阳能电池产生的电能电解水是制氢的一条具有十分诱人前景的途径。
人工光合作用的研究为太阳能制氢提供了另外一条途径。光合作用的核心是由太阳光驱动将水分子裂解为氧气、氢离子和电子。植物通过还原碳元素的形式将太阳能固定下来,能否不要将太阳能固定在碳元素中得到利用呢?人工光合作用将使这种想法成为可能,它完全抛弃了植物载体,只利用光合作用的原理,通过光裂解水分子,直接提取氢气。拆开水分子所需要的能量足以摧毁任何生物分子,然而植物每天都在进行着这个反应而没有任何不良后果。?秘密存在于催化核心的结构中。植物进行光合作用离不开叶绿素,而叶绿素中对光合作用起关键作用的就是催化核心。催化核心是由4个锰离子、1个钙离子、4个氧原子和至少2个水分子组成的,其中3个锰离子、1个钙离子和4个氧组成一个扭曲立方体,锰离子和钙离子通过氧原子相连接。第四个锰离子位于立方体的外部,结合着1个水分子。这一发现对于了解和复制水裂解化学过程具有重要意义。氢气的储存 硼氢化合物
热分解制氢——NH3BH3、LiBH4等
水分解制氢——NaBH4(SBH)等
BN纳米结构材料
硼促进贮氢材料含硼贮氢材料硼氢化合物贮氢Prof. A. Zuttel, Switzerland Univ Fribourg 450℃ 左右可以获得13.5 wt% H2LiBH4分解制氢强放热反应 可以获得13.6 wt% H2 LiBH4分解制氢120℃-300℃ 19.6 wt% H2
不足: NH3BH3制备成本偏高 NH3BN3分解制氢 B99N99C186 nanotubesAtomic structure modelsBN纳米结构贮氢近年来,大量的研究集中在纳米碳管储氢方面,主要是人们认为纳米碳管的储氢容量高,理论上可达10%。氢能的利用 (1)直接燃烧(2)燃料电池 谢谢大家!
