乙醇 醇类
图片预览





文档简介
课件19张PPT。生活中两种常见的有机物一、乙醇展示:无水乙醇。
请同学们观察乙醇的颜色、状态,并闻其气味。实验探究:
分别向装有1mL水和苯的试管中注入2mL无水乙醇,振荡、静置。观察现象。思考让我
看一看?
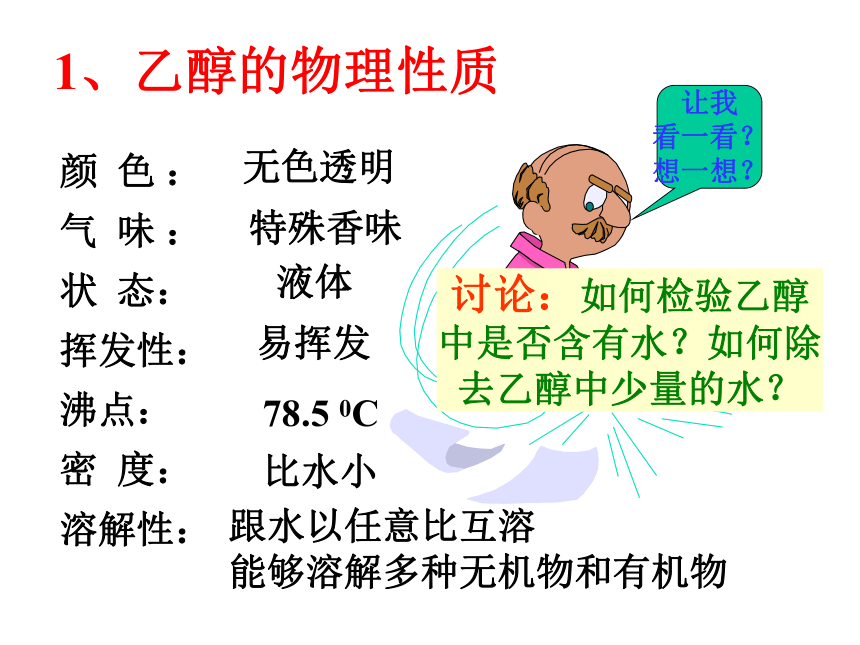
想一想?颜 色 :
气 味 :
状 态:
挥发性:
沸点:
密 度:
溶解性:无色透明特殊香味液体比水小跟水以任意比互溶
能够溶解多种无机物和有机物易挥发1、乙醇的物理性质78.5 0C讨论:如何检验乙醇中是否含有水?如何除去乙醇中少量的水? [活动与探究]
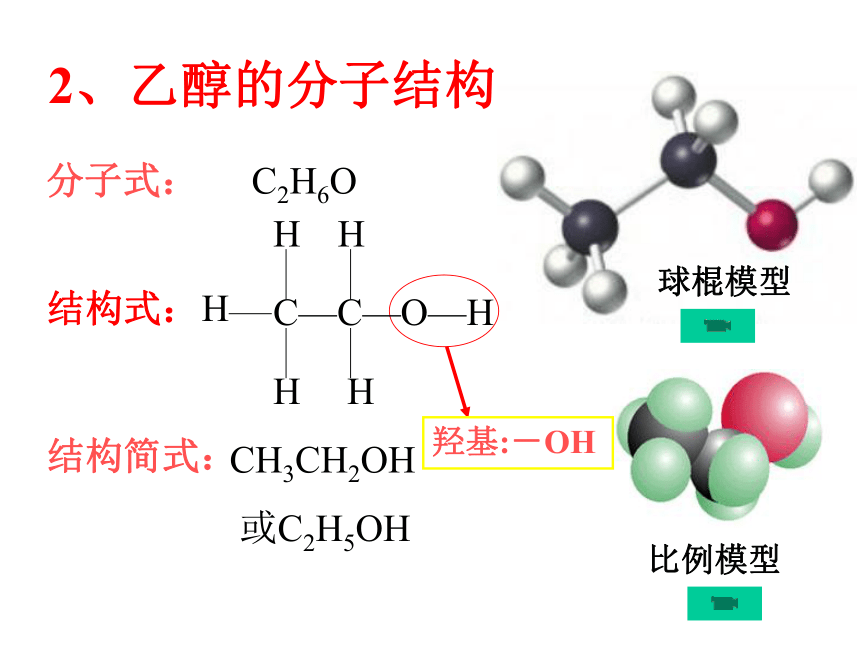
分别在1~2ml的煤油和无水乙醇中以及盛水的小烧杯中投入一小粒金属钠,观察并记录实验现象填写下列表格。思考:由上述结论我们能否推出乙醇的结构呢 ?球棍模型2、乙醇的分子结构羟基:-OH 烃的衍生物: 烃分子中的氢原子被其他原子或原子团所取代而生成的一系列化合物成为烃的衍生物。例如,一氯甲烷、二氯甲烷、三氯甲烷、四氯甲烷及硝基苯等。1、对比乙醇与乙烷、与水分子结构的异同点,推测钠与乙醇反应时断裂什么键?放出的气体是什么?想一想?H-O-H
水[结论]?1、羟基决定乙醇能和钠反应生成氢气
2、羟基中的H原子的活泼性:醇<水2CH3CH2OH+2Na→2CH3CH2ONa+H2↑ 其它活泼金属如钾、钙、镁等也可与乙醇反应3、乙醇的化学性质(1)乙醇与钠的反应例如:乙醇与镁反应的化学方程式2CH3CH2OH+Mg→(CH3CH2O)2Mg+H2↑官能团:决定有机化合物化学特性的原子或原子团称为官能团。例如:卤素原子( — X)、羟基( — OH)、硝基( — NO2)等都是官能团,烯烃中的碳碳双键也是官能团。羟基(—OH)与氢氧根的区别见下表:(2)乙醇的氧化反应a.乙醇在空气中燃烧?: 现象:产生淡蓝色火焰,同时放出大量热。 [活动与探究] ①用小试管取3~4mL无水乙醇; ②加热一端绕成螺旋状的铜丝至红热; ③将铜丝趁热插到盛有乙醇的试管底部; ④反复操作几次,观察铜丝颜色和液体气味的变化。 实验现象: a.铜丝红色→黑色→红色反复变化 b.在试管口可以闻到刺激性气味思考:铜丝在此实验中起什么作用?红色→黑色:黑色→红色:分析总反应方程式:乙醛
刺激性气味液体铜丝在实验中作催化剂 b.乙醇催化氧化: 工业上利用此原理生产乙醛C2H6OC2H4O CH3CH2OHc.乙醇被强氧化剂如酸性高锰酸钾或重铬酸钾等氧化为乙酸。思考:CH3OH和能否发生催化氧化?CH3COOH4、乙 醇 用 途 用作燃料,如酒精灯等制造饮料和香精外,食品加工业一种重要的有机化工原料,如制造乙酸、乙醚等。乙醇又是一种有机溶剂,用于溶解树 脂,制造涂料。医疗上常用75%(体积分数)的酒精作消毒剂。思考:①与活泼金属反应_______断裂
②氧化反应--燃烧_______断裂
--催化氧化______断裂 分子结构:
物理性质:
化学性质:
反应中乙醇断键位置?小 结乙醇官能团-OH1.乙醇分子中不同的化学键如图:
化学反应中乙醇的断键位置
⑴与活泼金属反应____断裂
⑵C2H5OH燃烧_____断裂
⑶在Cu或Ag催化下和O2反应键_____断裂 练 习 题?①全部①③2、能用来检验酒精中是否含有水的
试剂是( )A: CuSO4·5H2OC: 浓硫酸B:CuSO4D:金属钠练 习 题B
分别向装有1mL水和苯的试管中注入2mL无水乙醇,振荡、静置。观察现象。思考让我
看一看?
想一想?颜 色 :
气 味 :
状 态:
挥发性:
沸点:
密 度:
溶解性:无色透明特殊香味液体比水小跟水以任意比互溶
能够溶解多种无机物和有机物易挥发1、乙醇的物理性质78.5 0C讨论:如何检验乙醇中是否含有水?如何除去乙醇中少量的水? [活动与探究]
分别在1~2ml的煤油和无水乙醇中以及盛水的小烧杯中投入一小粒金属钠,观察并记录实验现象填写下列表格。思考:由上述结论我们能否推出乙醇的结构呢 ?球棍模型2、乙醇的分子结构羟基:-OH 烃的衍生物: 烃分子中的氢原子被其他原子或原子团所取代而生成的一系列化合物成为烃的衍生物。例如,一氯甲烷、二氯甲烷、三氯甲烷、四氯甲烷及硝基苯等。1、对比乙醇与乙烷、与水分子结构的异同点,推测钠与乙醇反应时断裂什么键?放出的气体是什么?想一想?H-O-H
水[结论]?1、羟基决定乙醇能和钠反应生成氢气
2、羟基中的H原子的活泼性:醇<水2CH3CH2OH+2Na→2CH3CH2ONa+H2↑ 其它活泼金属如钾、钙、镁等也可与乙醇反应3、乙醇的化学性质(1)乙醇与钠的反应例如:乙醇与镁反应的化学方程式2CH3CH2OH+Mg→(CH3CH2O)2Mg+H2↑官能团:决定有机化合物化学特性的原子或原子团称为官能团。例如:卤素原子( — X)、羟基( — OH)、硝基( — NO2)等都是官能团,烯烃中的碳碳双键也是官能团。羟基(—OH)与氢氧根的区别见下表:(2)乙醇的氧化反应a.乙醇在空气中燃烧?: 现象:产生淡蓝色火焰,同时放出大量热。 [活动与探究] ①用小试管取3~4mL无水乙醇; ②加热一端绕成螺旋状的铜丝至红热; ③将铜丝趁热插到盛有乙醇的试管底部; ④反复操作几次,观察铜丝颜色和液体气味的变化。 实验现象: a.铜丝红色→黑色→红色反复变化 b.在试管口可以闻到刺激性气味思考:铜丝在此实验中起什么作用?红色→黑色:黑色→红色:分析总反应方程式:乙醛
刺激性气味液体铜丝在实验中作催化剂 b.乙醇催化氧化: 工业上利用此原理生产乙醛C2H6OC2H4O CH3CH2OHc.乙醇被强氧化剂如酸性高锰酸钾或重铬酸钾等氧化为乙酸。思考:CH3OH和能否发生催化氧化?CH3COOH4、乙 醇 用 途 用作燃料,如酒精灯等制造饮料和香精外,食品加工业一种重要的有机化工原料,如制造乙酸、乙醚等。乙醇又是一种有机溶剂,用于溶解树 脂,制造涂料。医疗上常用75%(体积分数)的酒精作消毒剂。思考:①与活泼金属反应_______断裂
②氧化反应--燃烧_______断裂
--催化氧化______断裂 分子结构:
物理性质:
化学性质:
反应中乙醇断键位置?小 结乙醇官能团-OH1.乙醇分子中不同的化学键如图:
化学反应中乙醇的断键位置
⑴与活泼金属反应____断裂
⑵C2H5OH燃烧_____断裂
⑶在Cu或Ag催化下和O2反应键_____断裂 练 习 题?①全部①③2、能用来检验酒精中是否含有水的
试剂是( )A: CuSO4·5H2OC: 浓硫酸B:CuSO4D:金属钠练 习 题B
