化学反应速率(浙江省台州市椒江区)
图片预览








文档简介
课件25张PPT。化学反应速率你了解下列化学变化过程进行的快慢吗?
如何用一个量化的标准来表示反应的快慢呢?你知道吗12′88(2)数学表达式: (3)常用单位:mol·(L·min)-1或mol·(L·s)-1 一、化学反应速率(平均速率,均取正值)浓度的变化量练习1:已知反应2SO2+O2 2SO3在10 L的密闭容器中进行,半分钟后,测得SO3的物质的量增加了0.5 mol,求SO3的平均反应速率。
解:
0.5 mol
V = ———————— = 0.1 mol·(L·min)-1
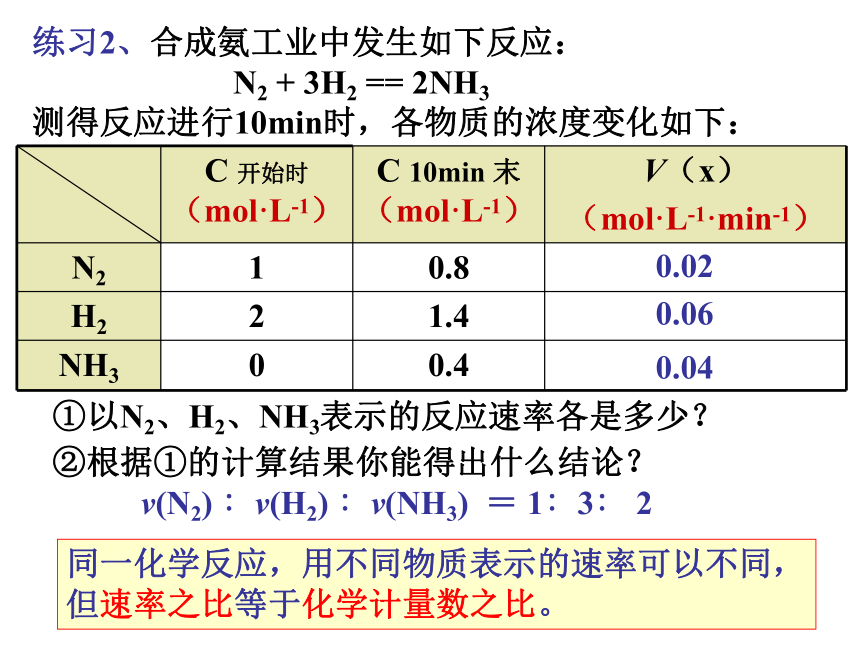
10 L×0.5 min练习2、合成氨工业中发生如下反应:
N2 + 3H2 == 2NH3
测得反应进行10min时,各物质的浓度变化如下: ②根据①的计算结果你能得出什么结论?①以N2、H2、NH3表示的反应速率各是多少?v(N2) ∶v(H2) ∶v(NH3) = 1∶3∶ 20.020.060.04同一化学反应,用不同物质表示的速率可以不同,但速率之比等于化学计量数之比。2、固体或者纯净的液体没有浓度的变化,所以不能用它们的浓度的变化来表示V的大小既V不能用固态或纯液态来表示。注意:1、对于同一化学反应,在相同的反应时间内,用不同的物质来表示的化学反应速率的数值可能是不同的。因此表示化学反应速率时,必须说明用哪种物质为基准。 已知反应 A+3B==2C+D在某一段时间内以A的浓度变化表示的化学反应速率为
1mol/ (L·min),则此段时间内以C的浓度变化表示的化学反应速率为 ( )
A.0.5mol/ (L·min) B.1mol/ (L·min)
C. 2mol/ (L·min) D. 3mol/ (L·min)
练习3C在2 L容积不变的容器中,发生 N2 + 3H2 == 2NH3的反应。现通入4 mol H2 和 4 mol N2 , 用H2 表示的反应速率为0.12 mol/(L·s) ,则10 s后容器中N2的物质的量是 ( )
A. 1.6mol B. 2.8mol
C. 3.2mol D. 3.6molC练习4 在四个不同的容器中,在不同的条件下进行合成氨的反应N2 + 3H2 == 2NH3 ,测得的速率如下,其中生成氨 的速率最快的是 ( )
A. v ( H2 )= 0.45 mol/ (L·min)
B. v ( N2 )= 0.1 mol/ (L·min)
C. v ( N2 )= 0.2mol/ (L·min)
D. v ( NH3 ) 0.3mol/ (L·min)练习5C 某温度下,物质的量浓度均为1 mol/ L 的两种气体X2和Y2在密闭容器中反应生成气体Z。一段时间后,c(X2)=0.4 mol/L, c(Y2)=0.8 mol/L , c(Z)=0.4 mol/L ,该反应的化学方程式是 ( )
A. X2 + 2Y2 ==2Z B. 2X2 + Y2 ==2Z
C. 3X2 + Y2 ==2Z D. X2 + 3Y2 ==2Z 练习6C 不同化学反应的反应速率不同。结论:主要决定于反应质本身的性质。二、影响化学反应速率的因素书P30内因决定因素 对于同一个化学反应H2+Cl2=2HCl,氢气能在氯气中安静地燃烧,而点燃或光照氢气和氯气的混合气体却会发生爆炸,这有说明了什么呢? 同一化学反应的反应速率能受
外界因素的影响。外因增大反应物的接触面积,可以加快反应速率。你知道吗 氢气能在氯气中安静地燃烧,氢气和氯气的混合气体光照时为什么会发生爆炸?结论1:同一化学反应的反应速率能受外界因素的影响。活动与探究书P30外界条件对化学反应速率的影响水浴加热产生
气泡快加入二氧化锰粉末产生气泡快加热能加快反应速率使用催化剂能加快反应速率浓度大的产生
气泡快增大反应物的浓度能加快反应速率结论4:反应物浓度越大,反应速率越大。(适用气体、溶液的反应)结论2:温度越高,反应速率越大。结论3:催化剂能显著地增大反应速率不同催化剂的催化效果不同。因为固体或者纯净的液体没有浓度的变化 对于有气体参加的反应,增大压强相当于增大气体的浓度, 可以加快反应的速率。结论5: 反应C(s)+H2O(g) CO(g)+H2(g)在可变容积的密闭容器中进行,下列的改变,不能加快化学反应速率的是( )
A、增加碳的用量
B、容器的体积缩小一半
C、保持体积不变,充入N2,使压强增大一倍
D、升高体系温度
E、将碳颗粒碾得更细
F、加入适当的催化剂A、C练习7: 问题解决2. 碳酸钙与稀盐酸反应生成的CO2气体体积随时间变化的曲线。请分析讨论以下问题。(1)在0~t1、t1~t2、 t2~t3各相同的时间段里,反应速率最大的是_______时间段,收集到气体最多的是_______时间段。t1-t2t1-t2(2)试分析三个时间段里,反应速率不同的可能原因(该反应是放热反应)。t1-t2时间段,温度升高是影响化学反应速率的主要因素;t2-t3时间段,浓度减小是影响化学反应速率的主要因素;(3)在t4后,为什么收集到的气体的体积不再增加?(2)表达式:一、化学反应速率(1)表示方法:mol·(L·min)-1或mol·(L·s)-1 单位时间内的浓度变化。二、化学反应速率的影响因素反应物的性质(决定因素)(3)常用单位:1、浓度 C增大,v增大2、压强 P增大,v增大3、温度 T增大,v增大 4、催化剂 加入催化剂,v成千上万增大5、其他:光、紫外线等(适用气体、溶液的反应)(适用气体参加的反应)(适用任何反应)与化学反应速率相关的诺贝尔化学奖练习2:增大压强,能使下列反应速率加快的是(????? ) A.Na2SO4溶液与BaCl2溶液反应 B.CO和水蒸气在一定条件下反应生
成CO2和H2 ? C.将CO2通人石灰水中 D.Na2O溶于水 BC反应物的浓度增大反应速率增大有气体参加的反应结论4:
如何用一个量化的标准来表示反应的快慢呢?你知道吗12′88(2)数学表达式: (3)常用单位:mol·(L·min)-1或mol·(L·s)-1 一、化学反应速率(平均速率,均取正值)浓度的变化量练习1:已知反应2SO2+O2 2SO3在10 L的密闭容器中进行,半分钟后,测得SO3的物质的量增加了0.5 mol,求SO3的平均反应速率。
解:
0.5 mol
V = ———————— = 0.1 mol·(L·min)-1
10 L×0.5 min练习2、合成氨工业中发生如下反应:
N2 + 3H2 == 2NH3
测得反应进行10min时,各物质的浓度变化如下: ②根据①的计算结果你能得出什么结论?①以N2、H2、NH3表示的反应速率各是多少?v(N2) ∶v(H2) ∶v(NH3) = 1∶3∶ 20.020.060.04同一化学反应,用不同物质表示的速率可以不同,但速率之比等于化学计量数之比。2、固体或者纯净的液体没有浓度的变化,所以不能用它们的浓度的变化来表示V的大小既V不能用固态或纯液态来表示。注意:1、对于同一化学反应,在相同的反应时间内,用不同的物质来表示的化学反应速率的数值可能是不同的。因此表示化学反应速率时,必须说明用哪种物质为基准。 已知反应 A+3B==2C+D在某一段时间内以A的浓度变化表示的化学反应速率为
1mol/ (L·min),则此段时间内以C的浓度变化表示的化学反应速率为 ( )
A.0.5mol/ (L·min) B.1mol/ (L·min)
C. 2mol/ (L·min) D. 3mol/ (L·min)
练习3C在2 L容积不变的容器中,发生 N2 + 3H2 == 2NH3的反应。现通入4 mol H2 和 4 mol N2 , 用H2 表示的反应速率为0.12 mol/(L·s) ,则10 s后容器中N2的物质的量是 ( )
A. 1.6mol B. 2.8mol
C. 3.2mol D. 3.6molC练习4 在四个不同的容器中,在不同的条件下进行合成氨的反应N2 + 3H2 == 2NH3 ,测得的速率如下,其中生成氨 的速率最快的是 ( )
A. v ( H2 )= 0.45 mol/ (L·min)
B. v ( N2 )= 0.1 mol/ (L·min)
C. v ( N2 )= 0.2mol/ (L·min)
D. v ( NH3 ) 0.3mol/ (L·min)练习5C 某温度下,物质的量浓度均为1 mol/ L 的两种气体X2和Y2在密闭容器中反应生成气体Z。一段时间后,c(X2)=0.4 mol/L, c(Y2)=0.8 mol/L , c(Z)=0.4 mol/L ,该反应的化学方程式是 ( )
A. X2 + 2Y2 ==2Z B. 2X2 + Y2 ==2Z
C. 3X2 + Y2 ==2Z D. X2 + 3Y2 ==2Z 练习6C 不同化学反应的反应速率不同。结论:主要决定于反应质本身的性质。二、影响化学反应速率的因素书P30内因决定因素 对于同一个化学反应H2+Cl2=2HCl,氢气能在氯气中安静地燃烧,而点燃或光照氢气和氯气的混合气体却会发生爆炸,这有说明了什么呢? 同一化学反应的反应速率能受
外界因素的影响。外因增大反应物的接触面积,可以加快反应速率。你知道吗 氢气能在氯气中安静地燃烧,氢气和氯气的混合气体光照时为什么会发生爆炸?结论1:同一化学反应的反应速率能受外界因素的影响。活动与探究书P30外界条件对化学反应速率的影响水浴加热产生
气泡快加入二氧化锰粉末产生气泡快加热能加快反应速率使用催化剂能加快反应速率浓度大的产生
气泡快增大反应物的浓度能加快反应速率结论4:反应物浓度越大,反应速率越大。(适用气体、溶液的反应)结论2:温度越高,反应速率越大。结论3:催化剂能显著地增大反应速率不同催化剂的催化效果不同。因为固体或者纯净的液体没有浓度的变化 对于有气体参加的反应,增大压强相当于增大气体的浓度, 可以加快反应的速率。结论5: 反应C(s)+H2O(g) CO(g)+H2(g)在可变容积的密闭容器中进行,下列的改变,不能加快化学反应速率的是( )
A、增加碳的用量
B、容器的体积缩小一半
C、保持体积不变,充入N2,使压强增大一倍
D、升高体系温度
E、将碳颗粒碾得更细
F、加入适当的催化剂A、C练习7: 问题解决2. 碳酸钙与稀盐酸反应生成的CO2气体体积随时间变化的曲线。请分析讨论以下问题。(1)在0~t1、t1~t2、 t2~t3各相同的时间段里,反应速率最大的是_______时间段,收集到气体最多的是_______时间段。t1-t2t1-t2(2)试分析三个时间段里,反应速率不同的可能原因(该反应是放热反应)。t1-t2时间段,温度升高是影响化学反应速率的主要因素;t2-t3时间段,浓度减小是影响化学反应速率的主要因素;(3)在t4后,为什么收集到的气体的体积不再增加?(2)表达式:一、化学反应速率(1)表示方法:mol·(L·min)-1或mol·(L·s)-1 单位时间内的浓度变化。二、化学反应速率的影响因素反应物的性质(决定因素)(3)常用单位:1、浓度 C增大,v增大2、压强 P增大,v增大3、温度 T增大,v增大 4、催化剂 加入催化剂,v成千上万增大5、其他:光、紫外线等(适用气体、溶液的反应)(适用气体参加的反应)(适用任何反应)与化学反应速率相关的诺贝尔化学奖练习2:增大压强,能使下列反应速率加快的是(????? ) A.Na2SO4溶液与BaCl2溶液反应 B.CO和水蒸气在一定条件下反应生
成CO2和H2 ? C.将CO2通人石灰水中 D.Na2O溶于水 BC反应物的浓度增大反应速率增大有气体参加的反应结论4:
