晶体类型(浙江省台州市椒江区)
图片预览



文档简介
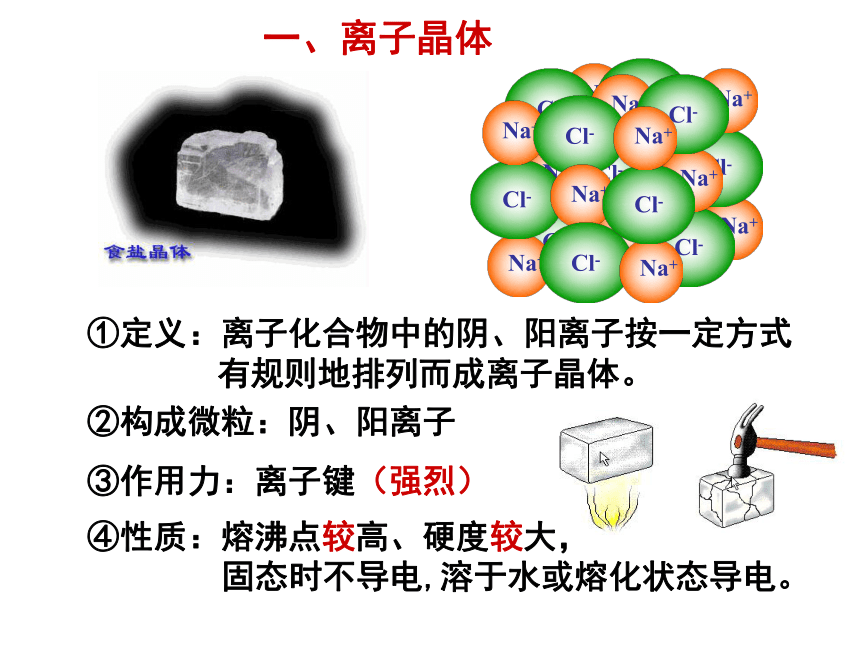
课件19张PPT。不同类型的晶体晶 体是由结晶形成的具有规则几何外形、有固定熔沸点的固体。水晶钻石雪晶体分为离子晶体、分子晶体、原子晶体、金属晶体。一、离子晶体 ①定义:离子化合物中的阴、阳离子按一定方式
有规则地排列而成离子晶体。②构成微粒:阴、阳离子③作用力:离子键(强烈)④性质:熔沸点较高、硬度较大,
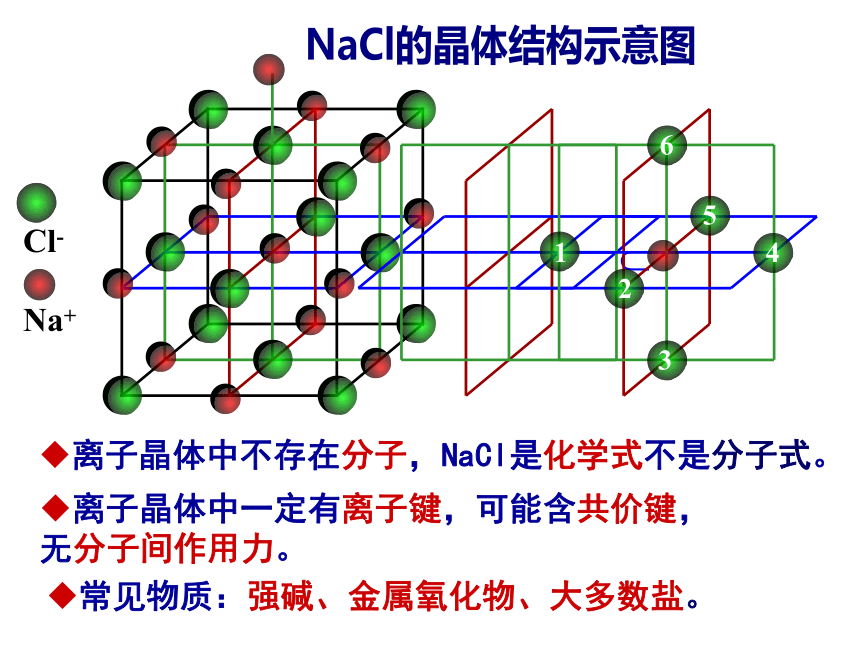
固态时不导电,溶于水或熔化状态导电。 离子晶体中不存在分子,NaCl是化学式不是分子式。Na+Cl-离子晶体中一定有离子键,可能含共价键,无分子间作用力。常见物质:强碱、金属氧化物、大多数盐。NaCl的晶体结构示意图①定义:由分子按一定方式有规则地排列而成
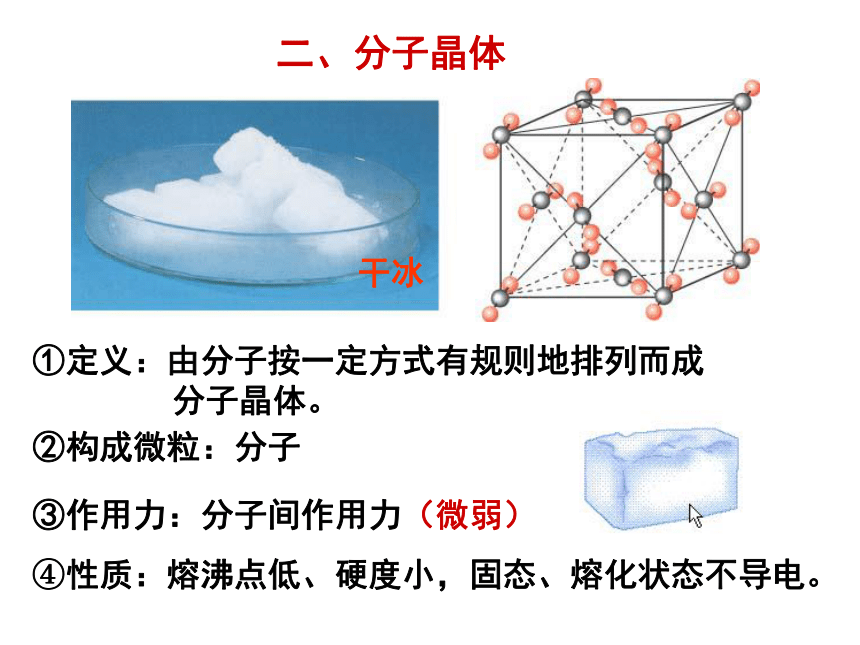
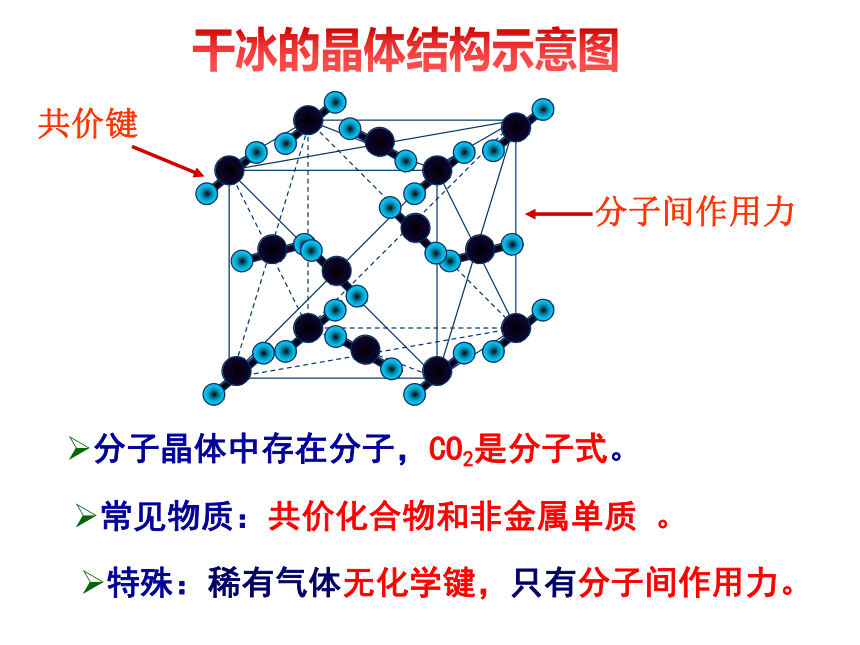
分子晶体。②构成微粒:分子③作用力:分子间作用力(微弱)④性质:熔沸点低、硬度小,固态、熔化状态不导电。干冰二、分子晶体干冰的晶体结构示意图分子晶体中存在分子,CO2是分子式。常见物质:共价化合物和非金属单质 。 特殊:稀有气体无化学键,只有分子间作用力。 CO2和SiO2的一些物理性质如下表所示,
通过比较判断SiO2晶体是否属于分子晶体。 熔 点 沸 点
干 冰(CO2) -56.2℃ -78.4℃
SiO2 1723℃ 2230℃讨论:三、原子晶体①定义:原子间通过共价键结合形成空间网状
结构的原子晶体。②构成微粒:原子③作用力:共价键(强烈)⑤性质:熔沸点很高、硬度很大,不溶解,不导电。④实例:水晶、金刚石、晶体硅、碳化硅水晶钻石Sio共价键原子晶体中不存在分子,SiO2是化学式不是分子式。原子晶体中一定有共价键,无离子键,无分子间作用力。二氧化硅的晶体结构示意图109o28′硅晶体、金刚石结构示意图四、金属晶体②构成微粒:金属阳离子和自由电子③作用力:金属键(强烈静电作用)⑤性质:有金属光泽、能导电导热、具有延展性。④实例:所有金属单质①定义:金属离子和自由电子之间通过较强作用
形成单质晶体。晶体结构与性质关系的比较阴、阳离子分子原子金属阳离子和自由电子离子键分子间
作用力共价键金属键差距大很大小较大较大小高差距大导电不导电水溶液有些导电熔融或水溶液导电判断晶体的类型方法1、从组成上判断(仅限于中学范围)
a.有无离子键?
b.是否属于“四种原子晶体”
c.以上皆否定,则多数是分子晶体
2、从性质上判断
a.熔沸点和硬度;( 很高:原子晶体;
较高:离子晶体;较低:分子晶体)
b.熔融状态的导电性。( 导电:离子晶体)2、下列各组物质发生状态变化所克服的粒子间作用力属于同种类型的是( )
A.食盐和蔗糖熔化 B.钠和硫熔化
C.碘和干冰升华 D.二氧化硅和氧化钠熔化1、判断下列晶体所属的晶体类型?
蔗糖、 冰、 铁、 BaSO4、 金刚石、
冰醋酸、 尿素、 水晶、 Na2OC课 堂 练 习3、分析物质的物理性质,判断其晶体类型:
A、碳化铝,黄色晶体,熔点2200℃,熔融态不导电;___________
B、溴化铝,无色晶体,熔点98 ℃,熔融态不导电;___________
C、物质A,固态或熔融时都能导电__________
D、物质B,无色晶体,熔融时或溶于水中都能导电_____________原子晶体分子晶体金属晶体离子晶体 液晶(1iquid crystal)是一种介于晶体状态和液态之间的中间态物质。液晶兼有液体和晶体的某些特点,表现出一些独特的性质。通常,只有那些分子较大、分子形状呈长形或碟形的物质,才易形成液晶态。液晶应用于数码显示、电光学快门、图像显示等方面,在信息技术中占有重要的位置。石墨是片层结构的混合型晶体 熔沸点很高,硬度较小,难溶于水,能导电。判断晶体的类型方法1、从组成上判断(仅限于中学范围)
a.有无离子键?
b.是否属于“四种原子晶体”
c.以上皆否定,则多数是分子晶体
2、从性质上判断
a.熔沸点和硬度;( 很高:原子晶体;
较高:离子晶体;较低:分子晶体)
b.熔融状态的导电性。( 导电:离子晶体)熔、沸点的比较不同类型:原子晶体>离子晶体>分子晶体同种类型:微粒间的作用越强,熔沸点越高原子晶体:原子半径越小,共价键越强, 熔沸点越高离子晶体:离子电荷数越多,离子半径越小,离子键 越强,熔沸点越高分子晶体:结构相似,式量越大,熔沸点越高同分异构体,支链越多,熔沸点越低有氢键的熔沸点高金属晶体:离子电荷数越多,离子半径越小,金属键 越强,熔沸点越高
有规则地排列而成离子晶体。②构成微粒:阴、阳离子③作用力:离子键(强烈)④性质:熔沸点较高、硬度较大,
固态时不导电,溶于水或熔化状态导电。 离子晶体中不存在分子,NaCl是化学式不是分子式。Na+Cl-离子晶体中一定有离子键,可能含共价键,无分子间作用力。常见物质:强碱、金属氧化物、大多数盐。NaCl的晶体结构示意图①定义:由分子按一定方式有规则地排列而成
分子晶体。②构成微粒:分子③作用力:分子间作用力(微弱)④性质:熔沸点低、硬度小,固态、熔化状态不导电。干冰二、分子晶体干冰的晶体结构示意图分子晶体中存在分子,CO2是分子式。常见物质:共价化合物和非金属单质 。 特殊:稀有气体无化学键,只有分子间作用力。 CO2和SiO2的一些物理性质如下表所示,
通过比较判断SiO2晶体是否属于分子晶体。 熔 点 沸 点
干 冰(CO2) -56.2℃ -78.4℃
SiO2 1723℃ 2230℃讨论:三、原子晶体①定义:原子间通过共价键结合形成空间网状
结构的原子晶体。②构成微粒:原子③作用力:共价键(强烈)⑤性质:熔沸点很高、硬度很大,不溶解,不导电。④实例:水晶、金刚石、晶体硅、碳化硅水晶钻石Sio共价键原子晶体中不存在分子,SiO2是化学式不是分子式。原子晶体中一定有共价键,无离子键,无分子间作用力。二氧化硅的晶体结构示意图109o28′硅晶体、金刚石结构示意图四、金属晶体②构成微粒:金属阳离子和自由电子③作用力:金属键(强烈静电作用)⑤性质:有金属光泽、能导电导热、具有延展性。④实例:所有金属单质①定义:金属离子和自由电子之间通过较强作用
形成单质晶体。晶体结构与性质关系的比较阴、阳离子分子原子金属阳离子和自由电子离子键分子间
作用力共价键金属键差距大很大小较大较大小高差距大导电不导电水溶液有些导电熔融或水溶液导电判断晶体的类型方法1、从组成上判断(仅限于中学范围)
a.有无离子键?
b.是否属于“四种原子晶体”
c.以上皆否定,则多数是分子晶体
2、从性质上判断
a.熔沸点和硬度;( 很高:原子晶体;
较高:离子晶体;较低:分子晶体)
b.熔融状态的导电性。( 导电:离子晶体)2、下列各组物质发生状态变化所克服的粒子间作用力属于同种类型的是( )
A.食盐和蔗糖熔化 B.钠和硫熔化
C.碘和干冰升华 D.二氧化硅和氧化钠熔化1、判断下列晶体所属的晶体类型?
蔗糖、 冰、 铁、 BaSO4、 金刚石、
冰醋酸、 尿素、 水晶、 Na2OC课 堂 练 习3、分析物质的物理性质,判断其晶体类型:
A、碳化铝,黄色晶体,熔点2200℃,熔融态不导电;___________
B、溴化铝,无色晶体,熔点98 ℃,熔融态不导电;___________
C、物质A,固态或熔融时都能导电__________
D、物质B,无色晶体,熔融时或溶于水中都能导电_____________原子晶体分子晶体金属晶体离子晶体 液晶(1iquid crystal)是一种介于晶体状态和液态之间的中间态物质。液晶兼有液体和晶体的某些特点,表现出一些独特的性质。通常,只有那些分子较大、分子形状呈长形或碟形的物质,才易形成液晶态。液晶应用于数码显示、电光学快门、图像显示等方面,在信息技术中占有重要的位置。石墨是片层结构的混合型晶体 熔沸点很高,硬度较小,难溶于水,能导电。判断晶体的类型方法1、从组成上判断(仅限于中学范围)
a.有无离子键?
b.是否属于“四种原子晶体”
c.以上皆否定,则多数是分子晶体
2、从性质上判断
a.熔沸点和硬度;( 很高:原子晶体;
较高:离子晶体;较低:分子晶体)
b.熔融状态的导电性。( 导电:离子晶体)熔、沸点的比较不同类型:原子晶体>离子晶体>分子晶体同种类型:微粒间的作用越强,熔沸点越高原子晶体:原子半径越小,共价键越强, 熔沸点越高离子晶体:离子电荷数越多,离子半径越小,离子键 越强,熔沸点越高分子晶体:结构相似,式量越大,熔沸点越高同分异构体,支链越多,熔沸点越低有氢键的熔沸点高金属晶体:离子电荷数越多,离子半径越小,金属键 越强,熔沸点越高
