会考复习元素化合物--钠、镁及其化合物(浙江省舟山市)
文档属性
| 名称 | 会考复习元素化合物--钠、镁及其化合物(浙江省舟山市) |

|
|
| 格式 | rar | ||
| 文件大小 | 282.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2008-08-30 00:00:00 | ||
图片预览

文档简介
课件7张PPT。会考复习元素化合物
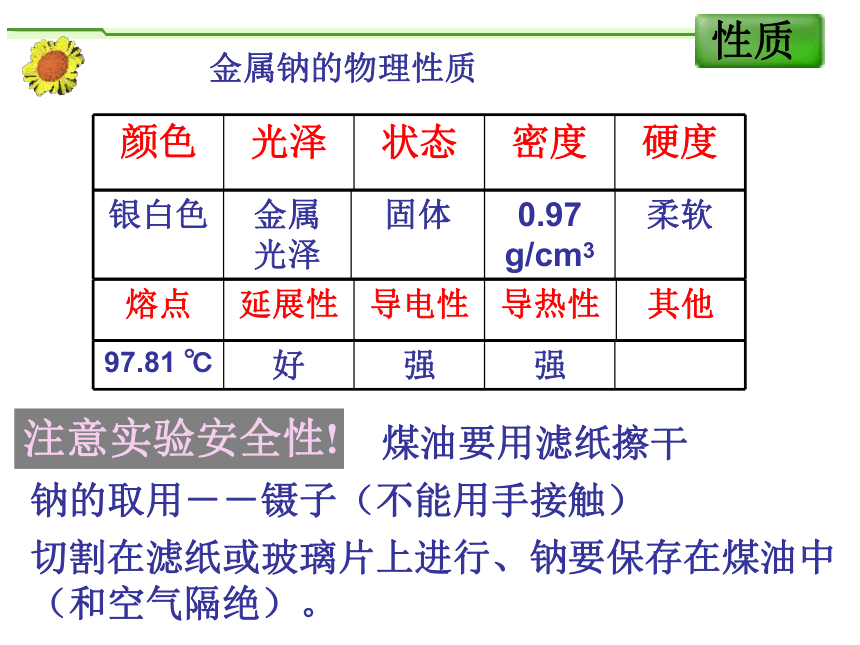
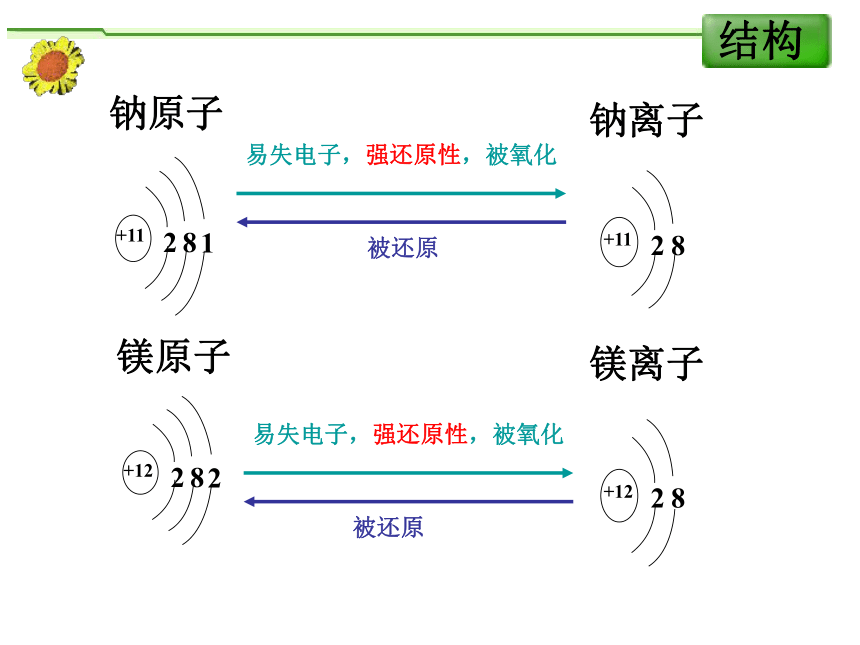
--钠、镁及其化合物金属钠的物理性质注意实验安全性!钠的取用--镊子(不能用手接触)煤油要用滤纸擦干切割在滤纸或玻璃片上进行、钠要保存在煤油中(和空气隔绝)。易失电子,强还原性,被氧化被还原易失电子,强还原性,被氧化被还原1、与非金属反应常温:生成氧化膜(发生钝化)镁(2)与其他非金属反应 钠 镁钠(1)与氧气反应:2、与水反应:钠2Na + 2H2O == 2NaOH + H2↑2Na + 2H2O ==2Na+ + 2OH- +H2↑Mg+2H2O(热水)== Mg(OH)2 +H2↑3.与酸反应:2Na+2HCl=2NaCl+H2↑ 4.与CO2反应剧烈燃烧,发出耀眼白光,瓶的内壁附着有黑色物质和白色物质Mg +H2SO 4 =MgSO 4 + H2 ↑钠、镁的生产原理电解熔融的氯化镁可以得到金属镁 电解熔融的氯化钠可以得到金属钠用途:
1、钠:冶炼某些贵金属、快种子反应堆作热交换剂、
高压钠灯、制Na2O2
2、镁:Mg-Al用于制造火箭、导弹和飞机部件、制造信
号弹和焰火、氧化镁做耐高温材料
--钠、镁及其化合物金属钠的物理性质注意实验安全性!钠的取用--镊子(不能用手接触)煤油要用滤纸擦干切割在滤纸或玻璃片上进行、钠要保存在煤油中(和空气隔绝)。易失电子,强还原性,被氧化被还原易失电子,强还原性,被氧化被还原1、与非金属反应常温:生成氧化膜(发生钝化)镁(2)与其他非金属反应 钠 镁钠(1)与氧气反应:2、与水反应:钠2Na + 2H2O == 2NaOH + H2↑2Na + 2H2O ==2Na+ + 2OH- +H2↑Mg+2H2O(热水)== Mg(OH)2 +H2↑3.与酸反应:2Na+2HCl=2NaCl+H2↑ 4.与CO2反应剧烈燃烧,发出耀眼白光,瓶的内壁附着有黑色物质和白色物质Mg +H2SO 4 =MgSO 4 + H2 ↑钠、镁的生产原理电解熔融的氯化镁可以得到金属镁 电解熔融的氯化钠可以得到金属钠用途:
1、钠:冶炼某些贵金属、快种子反应堆作热交换剂、
高压钠灯、制Na2O2
2、镁:Mg-Al用于制造火箭、导弹和飞机部件、制造信
号弹和焰火、氧化镁做耐高温材料
同课章节目录
