气体摩尔体积(浙江省台州市椒江区)
图片预览




文档简介
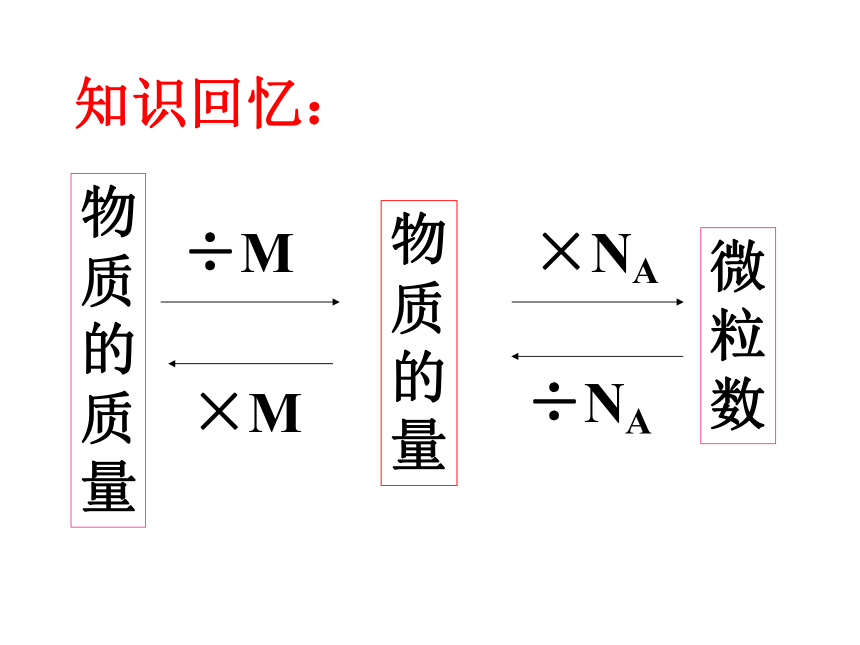
课件17张PPT。物质
的质量物质
的量微粒
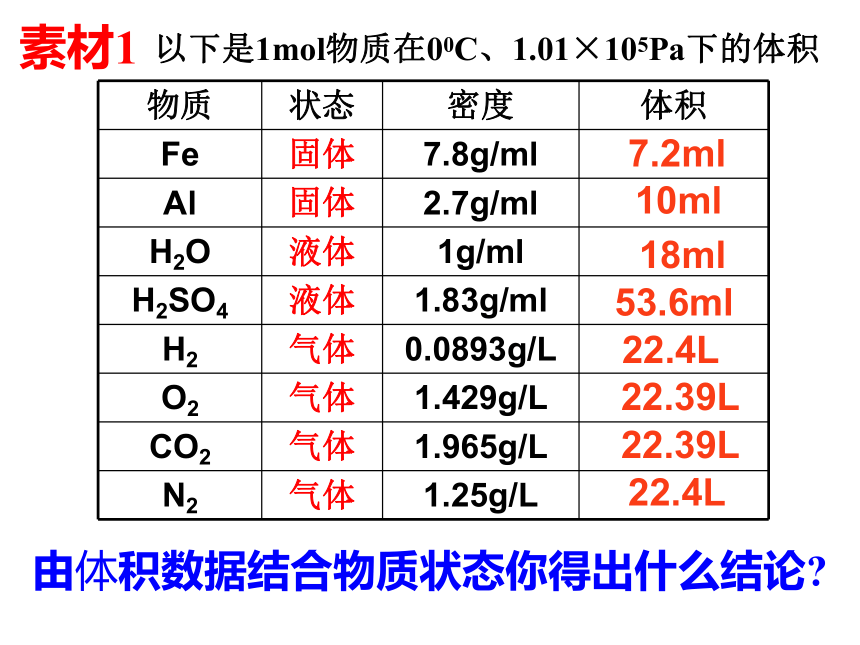
数÷M×M×NA÷NA知识回忆:物质的聚集状态: 气态(g)液态(L)固态(S) 在实验室或在生产中,对于气态物质我们常常使用它的体积而不是质量。疑问:那么物质的量与气体体积之间有什么关系?素材1以下是1mol物质在00C、1.01×105Pa下的体积由体积数据结合物质状态你得出什么结论?7.2ml10ml18ml53.6ml22.4L22.39L22.39L22.4L结论1.在相同状态下,1mol不同的固态或液态的物质所占的体积不同。为什么?2.在相同状态下,1mol气体的体积基本相同。 [提示]决定物质体积大小的因素有哪些?3.相同条件下,1mol气体体积远大于1mol固,液体的体积①物质的粒子数目;②粒子的大小;③粒子之间的距离;决定物质体积大小的因素有:(平均距离)用d表示固体和液体气 体
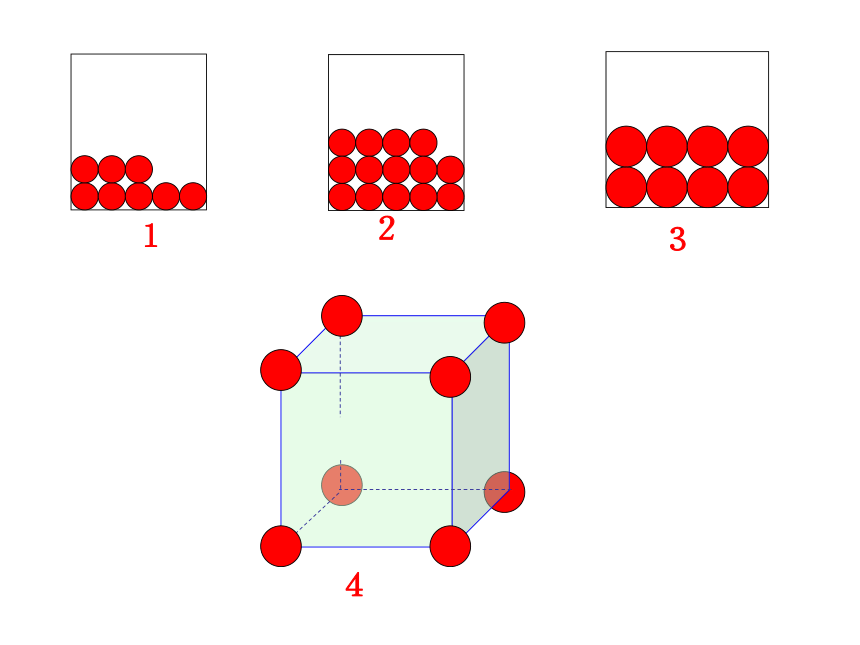
固体、液体物质粒子间间隔很小,在
粒子数目相同( 1mol )的情况下,固体、液体的体积主要由粒子本身大小决定。
气体粒子间间隔很大,在粒子数目相
同( 1mol )的情况下,气体的体积主要由粒子间平均距离决定。
[结论] 分子间的平均距离的影响条件: 在同温同压下,粒子数目相同( 1mol )的任何气体的体积相同。 气体摩尔体积1.定义:单位物质的量的气体所占的体积。
2.符号:Vm
3.单位:L/mol 或 m3/mol等
4.对象:任何气体(纯净或混合气体)5.公式:变形公式:在同温同压下, Vm 是一个定值。故: 标准状况(S.T.P)下 ,1mol任何气体体积约22.4L。即:标准状况 ( 温度0 oC、压强 1.01×105 Pa)下, Vm约为22.4L/mol。特殊的值: V=n×22.4L/mol[练习]1. 标准状况下,1mol任何物质的体积都约是22.4L。(错,物质应是气体)2. 1mol气体的体积约为22.4L。(错,应标明条件-标准状况)3. 标准状况下,1molO2和N2混合气体的体积约为22.4L。(对,气体体积与分子种类无关)4. 22.4L气体所含分子数一定大于11.2L气体所含的分子数。(错,未指明气体体积是否在相同条件下测定)5. 标准状况下,气体的摩尔体积都是22.4L。(错,“约为”;单位应为L/mol)6. 只有在标准状况下,气体的摩尔体积才可能约为22.4L/mol。(错,不一定 )7.在标况下,1molH2O的体积约是22.4L(错,这时的水不是气态)物质
质量物质
的量微粒
数÷M×M×NA÷NA×22.4L/mol÷22.4L/mol[小结](标准状况)气体体积[练习]1、下列说法正确的是( )
(A)在标准状况下,1mol水和1molH2的
体积都约是22.4L
(B)2gH2和44gCO2的体积相等
(C)1mol某气体的体积为22.4L,则该气体
一定处于标准状况
(D)标准状况,1gH2和11.2LO2的物质的量
相等[答案] (D) 2.在标况下
1) 0.5mol HCl气体占有的体积是多少?
2) 3.36LH2 的物质的量是多少?3.在标况下
1) 16克氧气的体积是多少?
2) 44.8L氮气中含有的分子数是多少?11.2L0.15mol1.204×102411.2L4.在标准状况下,多少克CO2与4克氢气的体积相同?88g5. 在同温、同压、相同质量的下列气体占有的体积由大到小的顺序是:
①Cl2 ②N2 ③ H2 ④ CO2 ⑤ O2③②⑤④①再见
的质量物质
的量微粒
数÷M×M×NA÷NA知识回忆:物质的聚集状态: 气态(g)液态(L)固态(S) 在实验室或在生产中,对于气态物质我们常常使用它的体积而不是质量。疑问:那么物质的量与气体体积之间有什么关系?素材1以下是1mol物质在00C、1.01×105Pa下的体积由体积数据结合物质状态你得出什么结论?7.2ml10ml18ml53.6ml22.4L22.39L22.39L22.4L结论1.在相同状态下,1mol不同的固态或液态的物质所占的体积不同。为什么?2.在相同状态下,1mol气体的体积基本相同。 [提示]决定物质体积大小的因素有哪些?3.相同条件下,1mol气体体积远大于1mol固,液体的体积①物质的粒子数目;②粒子的大小;③粒子之间的距离;决定物质体积大小的因素有:(平均距离)用d表示固体和液体气 体
固体、液体物质粒子间间隔很小,在
粒子数目相同( 1mol )的情况下,固体、液体的体积主要由粒子本身大小决定。
气体粒子间间隔很大,在粒子数目相
同( 1mol )的情况下,气体的体积主要由粒子间平均距离决定。
[结论] 分子间的平均距离的影响条件: 在同温同压下,粒子数目相同( 1mol )的任何气体的体积相同。 气体摩尔体积1.定义:单位物质的量的气体所占的体积。
2.符号:Vm
3.单位:L/mol 或 m3/mol等
4.对象:任何气体(纯净或混合气体)5.公式:变形公式:在同温同压下, Vm 是一个定值。故: 标准状况(S.T.P)下 ,1mol任何气体体积约22.4L。即:标准状况 ( 温度0 oC、压强 1.01×105 Pa)下, Vm约为22.4L/mol。特殊的值: V=n×22.4L/mol[练习]1. 标准状况下,1mol任何物质的体积都约是22.4L。(错,物质应是气体)2. 1mol气体的体积约为22.4L。(错,应标明条件-标准状况)3. 标准状况下,1molO2和N2混合气体的体积约为22.4L。(对,气体体积与分子种类无关)4. 22.4L气体所含分子数一定大于11.2L气体所含的分子数。(错,未指明气体体积是否在相同条件下测定)5. 标准状况下,气体的摩尔体积都是22.4L。(错,“约为”;单位应为L/mol)6. 只有在标准状况下,气体的摩尔体积才可能约为22.4L/mol。(错,不一定 )7.在标况下,1molH2O的体积约是22.4L(错,这时的水不是气态)物质
质量物质
的量微粒
数÷M×M×NA÷NA×22.4L/mol÷22.4L/mol[小结](标准状况)气体体积[练习]1、下列说法正确的是( )
(A)在标准状况下,1mol水和1molH2的
体积都约是22.4L
(B)2gH2和44gCO2的体积相等
(C)1mol某气体的体积为22.4L,则该气体
一定处于标准状况
(D)标准状况,1gH2和11.2LO2的物质的量
相等[答案] (D) 2.在标况下
1) 0.5mol HCl气体占有的体积是多少?
2) 3.36LH2 的物质的量是多少?3.在标况下
1) 16克氧气的体积是多少?
2) 44.8L氮气中含有的分子数是多少?11.2L0.15mol1.204×102411.2L4.在标准状况下,多少克CO2与4克氢气的体积相同?88g5. 在同温、同压、相同质量的下列气体占有的体积由大到小的顺序是:
①Cl2 ②N2 ③ H2 ④ CO2 ⑤ O2③②⑤④①再见
