化学反应原理绪言(黑龙江省鹤岗市萝北县)
文档属性
| 名称 | 化学反应原理绪言(黑龙江省鹤岗市萝北县) |

|
|
| 格式 | rar | ||
| 文件大小 | 483.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2008-09-05 00:00:00 | ||
图片预览








文档简介
课件25张PPT。高二化学学什么?2020-2-18高二化学选修学习内容《化学反应原理》
《有机化学基础》
《物质结构与性质》
《实验化学》
《化学与技术》
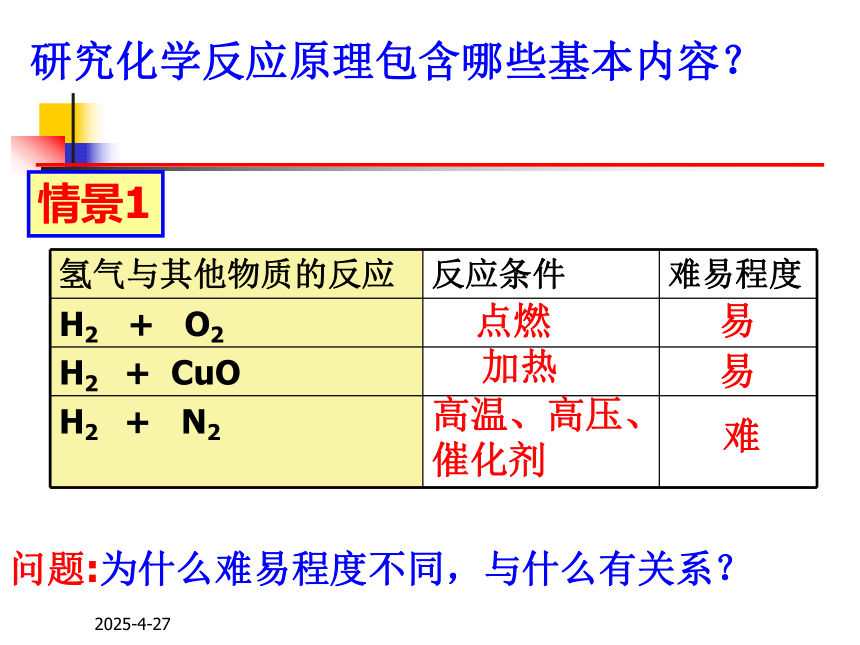
《化学与生活》六个选修模块上学期下学期2020-2-182020-2-18化学反应原理绪 言问题:1、化学研究的核心问题是:2、化学中最具有创造性的工作是:3、如何实现这个过程?化学反应设计和创造新的分子利用已发现的原理来进行设计并实现这个过程2020-2-18研究化学反应原理包含哪些基本内容?情景1问题:为什么难易程度不同,与什么有关系?点燃加热高温、高压、
催化剂易易难2020-2-18情景2 将H2 +O2混合,在室温条件下可以稳定存在数百年,但点燃后却会发生剧烈的爆炸反应,而且只要配比相当,可以完
全转化成生成物。这说明了什么?不同的外界条件都能够
改变化学反应的速率。情景3 H2+N2即使在高温、高压、催化剂的条件下反应也不能完全转化为生成物,这又说明了什么?有些反应是有一定限度的化学反应原理所研究的范围是1、化学反应的速率、方向及限度的问题2、水溶液中的离子反应的问题3、化学反应与能量的问题2020-2-18分子相互碰撞是引发反应的必要条件。3、是不是所有的碰撞都能引发反应?2、分子间发生化学反应的必要条件是什么?1、化学反应的本质是什么问题探讨 反应物中旧化学键的断裂
生成物中新的化学键的形成《简化后的有效碰撞模型》2020-2-18一、有效碰撞2.有效碰撞是发生化学反应的充分条件。1.分子相互碰撞是引发反应的必要条件。科学探究某一化学反应的速率大小与单位时间内有效碰撞的次数有关2020-2-18问题: 为什么有的碰撞可以发生反应,
而有的不能发生反应?
与哪些因素有关系?2020-2-18 分子的碰撞不一定都是有效碰撞,反应物分子间发生有效碰撞,必须同时满足两个条件:一是反应物分子必须有足够的能量,二是反应物分子必须按一定取向互相碰撞,即“碰撞得法”,才能引起旧键断裂,新键形成。
2020-2-18活 化 分 子结论:发生有效碰撞的分子一定是活化分子,
但活化分子的碰撞不一定是有效碰撞。推论:有效碰撞次数的多少与单位体积内反应物中活化分子
的多少有关。2020-2-18活化分子的多少又与什么有关?问题:2020-2-18活化能:活化分子高出反应物分子平均能量的部分E1
能量反应过程生成物反应物反应热E1E2活化分子该反应是放热反还是吸热反应?科学探究活 化 能2020-2-18结论:活化分子的多少与该反应的活化能的大小有关,活化能的大小是由反应物分子的性质决定。推论:活化能越小则一般分子成为活化分子越容易,则活化分子越多,则单位时间内有效碰撞越多,则反应速率越快。2020-2-18问题研究1.对于“活化能的大小虽然意味着一般分子成为活化分子的难易,但是却对这个化学反应前后的能量变化并不产生任何影响”这一句话如何理解?2.有没有活化能为0的反应?举例说明? 有, 参阅课文P4中间一段。2020-2-183、怎样改变反应的活化能为来加快反应的速率?
是何措施?能量反应过程生成物反应物反应热E1E2活化分子加了催化剂没加催化剂问题研究2020-2-18小 结碰撞 有效碰撞 活化分子 活化能 就下列的每个词说句话,试试看: 能发生化学反应的碰撞叫有效碰撞。是发生化学反应的充分条件。 具有足够的能量,取向合适能发生有效碰撞的分子叫活化分子。活化分子间要发生有效碰撞,还要有合适的取向。 活化分子所多出的那部分能量叫活化能。在相同条件下,反应的活化能越大,则该反应的速率越小。碰撞是发生化学反应的必要条件。2020-2-18归 纳 总 结一个反应要发生一般要经历哪些过程?普通
分子活化
能活化
分子合理
取向的
碰撞有效
碰撞2020-2-18解 释 问 题 为什么可燃物有氧气参与,还必
须达到着火点才能燃烧?2020-2-18再 见 常温常压下,每个氢分子和氧分子自身或它们之间每秒平均碰撞2.355×1010次,如果每一次碰撞都能发生反应,那么整个容器内的氢气和氧气将在瞬间变成水。
2020-2-18其中E1为活化能E2-E1是反应热2020-2-18
《有机化学基础》
《物质结构与性质》
《实验化学》
《化学与技术》
《化学与生活》六个选修模块上学期下学期2020-2-182020-2-18化学反应原理绪 言问题:1、化学研究的核心问题是:2、化学中最具有创造性的工作是:3、如何实现这个过程?化学反应设计和创造新的分子利用已发现的原理来进行设计并实现这个过程2020-2-18研究化学反应原理包含哪些基本内容?情景1问题:为什么难易程度不同,与什么有关系?点燃加热高温、高压、
催化剂易易难2020-2-18情景2 将H2 +O2混合,在室温条件下可以稳定存在数百年,但点燃后却会发生剧烈的爆炸反应,而且只要配比相当,可以完
全转化成生成物。这说明了什么?不同的外界条件都能够
改变化学反应的速率。情景3 H2+N2即使在高温、高压、催化剂的条件下反应也不能完全转化为生成物,这又说明了什么?有些反应是有一定限度的化学反应原理所研究的范围是1、化学反应的速率、方向及限度的问题2、水溶液中的离子反应的问题3、化学反应与能量的问题2020-2-18分子相互碰撞是引发反应的必要条件。3、是不是所有的碰撞都能引发反应?2、分子间发生化学反应的必要条件是什么?1、化学反应的本质是什么问题探讨 反应物中旧化学键的断裂
生成物中新的化学键的形成《简化后的有效碰撞模型》2020-2-18一、有效碰撞2.有效碰撞是发生化学反应的充分条件。1.分子相互碰撞是引发反应的必要条件。科学探究某一化学反应的速率大小与单位时间内有效碰撞的次数有关2020-2-18问题: 为什么有的碰撞可以发生反应,
而有的不能发生反应?
与哪些因素有关系?2020-2-18 分子的碰撞不一定都是有效碰撞,反应物分子间发生有效碰撞,必须同时满足两个条件:一是反应物分子必须有足够的能量,二是反应物分子必须按一定取向互相碰撞,即“碰撞得法”,才能引起旧键断裂,新键形成。
2020-2-18活 化 分 子结论:发生有效碰撞的分子一定是活化分子,
但活化分子的碰撞不一定是有效碰撞。推论:有效碰撞次数的多少与单位体积内反应物中活化分子
的多少有关。2020-2-18活化分子的多少又与什么有关?问题:2020-2-18活化能:活化分子高出反应物分子平均能量的部分E1
能量反应过程生成物反应物反应热E1E2活化分子该反应是放热反还是吸热反应?科学探究活 化 能2020-2-18结论:活化分子的多少与该反应的活化能的大小有关,活化能的大小是由反应物分子的性质决定。推论:活化能越小则一般分子成为活化分子越容易,则活化分子越多,则单位时间内有效碰撞越多,则反应速率越快。2020-2-18问题研究1.对于“活化能的大小虽然意味着一般分子成为活化分子的难易,但是却对这个化学反应前后的能量变化并不产生任何影响”这一句话如何理解?2.有没有活化能为0的反应?举例说明? 有, 参阅课文P4中间一段。2020-2-183、怎样改变反应的活化能为来加快反应的速率?
是何措施?能量反应过程生成物反应物反应热E1E2活化分子加了催化剂没加催化剂问题研究2020-2-18小 结碰撞 有效碰撞 活化分子 活化能 就下列的每个词说句话,试试看: 能发生化学反应的碰撞叫有效碰撞。是发生化学反应的充分条件。 具有足够的能量,取向合适能发生有效碰撞的分子叫活化分子。活化分子间要发生有效碰撞,还要有合适的取向。 活化分子所多出的那部分能量叫活化能。在相同条件下,反应的活化能越大,则该反应的速率越小。碰撞是发生化学反应的必要条件。2020-2-18归 纳 总 结一个反应要发生一般要经历哪些过程?普通
分子活化
能活化
分子合理
取向的
碰撞有效
碰撞2020-2-18解 释 问 题 为什么可燃物有氧气参与,还必
须达到着火点才能燃烧?2020-2-18再 见 常温常压下,每个氢分子和氧分子自身或它们之间每秒平均碰撞2.355×1010次,如果每一次碰撞都能发生反应,那么整个容器内的氢气和氧气将在瞬间变成水。
2020-2-18其中E1为活化能E2-E1是反应热2020-2-18
