物质的量第二课时
图片预览







文档简介
课件25张PPT。物质的量
(二) 什么是物质的量?什么是摩尔?
它们的使用范围是什么? 物质的量是表示物质所含粒子多少的物理量,摩尔是物质的量的单位。每摩尔物质都含有阿伏加德罗常数个粒子,阿伏加德罗常数的近似值为 。物质的量和摩尔都只适用于微观粒子,不能用于宏观物体。在使用物质的量时应该用化学式指明粒子的种类。
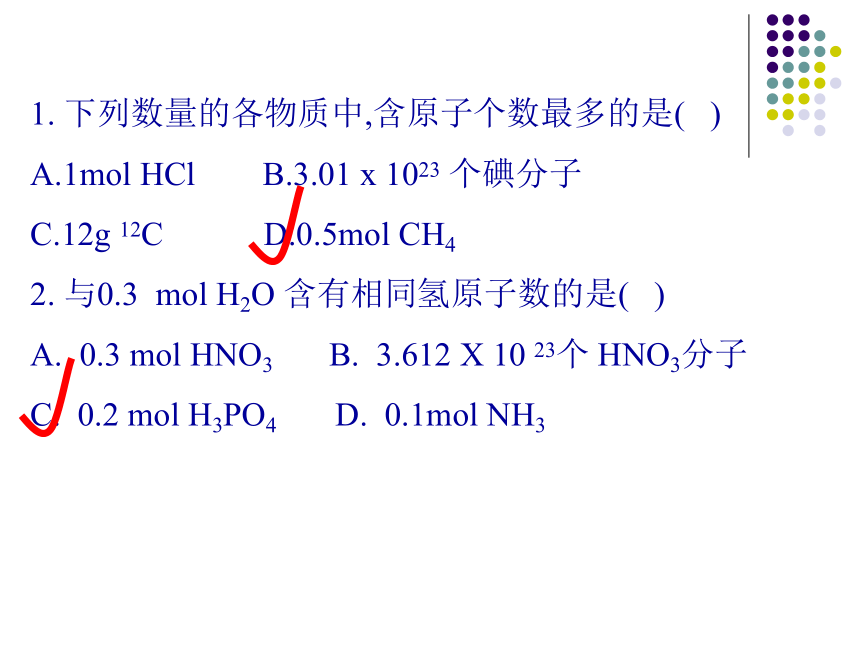
1. 下列数量的各物质中,含原子个数最多的是( )
A.1mol HCl B.3.01 x 1023 个碘分子
C.12g 12C D.0.5mol CH4
2. 与0.3 mol H2O 含有相同氢原子数的是( )
A. 0.3 mol HNO3 B. 3.612 X 10 23个 HNO3分子
C. 0.2 mol H3PO4 D. 0.1mol NH33、3molH2SO4中有___________个
H2SO4,可电离出_____mol H+ ___________个SO42-3×6.02×102363×6.02×1023 4、下列各物质所含原子个数按由大到小的序排列的是________________
①0.5molNH3? ②1molHe?
③0.5molH2O? ④0.2molH3PO4① ④ ③ ②思考:1mol任何粒子所含的粒子数是相同的,那么,1mol不同微粒的质量是否相同呢?微观粒子宏观质量一个C
原子一个O
原子一个Fe
原子扩大6.02 ×10231molC
原子1molO
原子1molFe
原子0.012kg16g56g12g相对原子
质量165612结论:1摩尔任何原子的质量如果以克为单位,在
数值上等于该原子的相对原子质量分析推理:相对原子质量 =一个某原子的质量(克)1/12 ×一个C-12原子质量(克)1mol某原子的质量(克)NA个C-12原子质量(克)结论:1摩尔某原子的质量以克为单位,在数值上
正好等 于该原子的相对原子质量×NA×NA12克 1克科学计算:由以上推理和计算结果可得出什么规律?①1mol任何原子的质量在数值上等于
这种原子的相对原子质量。
②1mol任何分子的质量在数值上等于
这种分子的相对分子质量。
③1mol任何离子的质量在数值上等于
这种离子的式量。 结论: 1mol任何物质的质量以克为单位,在数值上正好等于该物质的原子(分子)的相对原子质量(相对分子质量)。如:1摩尔O的质量为16克;1摩尔S的质量为32克;1摩尔Na的质量为23克;1摩尔H的质量为1克;二、摩尔质量1.1mol物质质量 1mol任何粒子或物质的质量是以克为单位,在数值上都与该粒子相对原子质量或相对分子质量相等。 例1.填写下列空白:
(1)1molCu 原子质量是??????? 克
(2) 1molO2分子质量是??????? 克
(3) 1molCO2分子质量是??????? 克
(4) 1molCl1-离子质量是??????? 克
(5) 1molNa+离子质量是??????? 克
(6) 1molNaCl质量是??????? 克 64g 32g 44g 35.5g 23g 58.5g 2.摩尔质量 (1)定义:单位物质的量的物质所具有的
质量叫做摩尔质量。符号M。
(2)单位:g/mol或kg/mol。
(3)数值: (当单位为 g/mol )等于物质或粒
子的相对式量。注意:摩尔质量只与物质的种类有关,与物质的量、
物质的质量无关 例2.回答下列问题
(1)O2 的摩尔质量是多少?
(2)H2SO4 的摩尔质量是多少?M(O2)=32g/molM(H2SO4 )=98g/mol练习 1.下列物质各多少克?含粒子数多少个? 2.下列物质的物质的量是多少?含有多少个粒子? (1)100molH2O ???? (2)0.1molOH- (1)90g水 (2)56g氮气物质的量 (mol) 物质的质量 (g)摩尔质量 (g/mol) n = m / M=两个变式:m=n?M3、物质的量(n)、物质的质量(m)和摩尔质量(M)之间的关系: 课堂练习:(1)、O2的摩尔质量是多少?
(2)、H2SO4的摩尔质量是多少?
(3)、100molH2O的质量是多少克?
(4)、0.1molOH-的质量是多少克?
(5)、34gNH3的物质的量是多少?32g.mol-198g.mol-11800g1.7g2molH2O物质的量(mol) 摩尔质量(g/mol) 质量(g)
1
2
0.5
完成表格18 g/mol18 g/mol18 g/mol18 g36 g9 g微粒的摩尔质量是固定的、不变的。物质的量的意义:是联系宏观和微观的纽带或桥梁。[例 1] 90克水相当于多少摩水?解: 水的式量是18,水的摩尔质量是 18g/mol 。n (H2O) = 90g18g/mol= 5 mol答:90克水相当于5mol水。[例 2] 2. 5 mol 铜原子的质量是多少克?解: 铜的原子量是 64 ,铜的摩尔质量是 64g/mol 。m (Cu) = 2.5 mol 64g/mol ×= 160g答:2.5mol 铜原子的质量等于 160g 。[例 3] 4. 9 克硫酸里含有多少个硫酸分子?解: 硫酸的式量是98,硫酸的摩尔质量是 98g/mol 。n (H2SO4) = 4. 9 g98g/mol= 0.05 mol答:4.9克硫酸里含有 3.01×1022个硫酸分子。N (H2SO4) =0.05 mol × 6.02 × 1023mol-1=3.01×1022[例 4] 20. 2 克硝酸钾中,氧元素的质量是多少克?解: 硝酸钾的式量是101,硝酸钾的摩尔质量是 101g/mol 。n (KNO3) = 20.2 g101g/mol= 0.2 mol答:20.2克硝酸钾中,氧元素的质量是 9. 6 g 。n (O) =0.2 mol×3 = 0.6 molm (O) =0. 6 mol×16g/mol = 9.6 g【例 5 】:有五种物质:
①6gH2;②0.5molCO2;③1.204×1024个HCl分子;
④147gH2SO4;⑤92g乙醇(C2H5OH);
请回答:
⑴物质的量最大的是 ;
⑵所含分子数最多的是 ;
⑶所含原子数最多的是 ; ①①⑤【例 6 】 :若杯中水的质量是54g,大家能算出里面所含的水分子的个数吗?n(H2O)==3mol N(H2O)=n?NA=3×6.02×1023=1.806×1024个练习2.含有6.02X1022 个分子的物质,其质量为
0.7g,求该物质的相对分子质量。练习3. 0.2molKClO3中所含的 Cl原子数与多克
CaCl2中所含的 Cl-离子个数相等? 练一练:小 结二、摩尔质量
???1.1mol物质的质量
??? 2.摩尔质量
三、关于物质的量的计算
(-)依据
????? 1.准确掌握物质的量、摩尔、摩尔质量等概念。
????? 2.掌握好有关物质质量(m)、物质的量(n)和粒子
数(N)之间的关系。
(二)类型
1.物质的质量,物质的量和粒子数之间的相互换算。
2.不同物质中,某粒子数相当的计算。
(二) 什么是物质的量?什么是摩尔?
它们的使用范围是什么? 物质的量是表示物质所含粒子多少的物理量,摩尔是物质的量的单位。每摩尔物质都含有阿伏加德罗常数个粒子,阿伏加德罗常数的近似值为 。物质的量和摩尔都只适用于微观粒子,不能用于宏观物体。在使用物质的量时应该用化学式指明粒子的种类。
1. 下列数量的各物质中,含原子个数最多的是( )
A.1mol HCl B.3.01 x 1023 个碘分子
C.12g 12C D.0.5mol CH4
2. 与0.3 mol H2O 含有相同氢原子数的是( )
A. 0.3 mol HNO3 B. 3.612 X 10 23个 HNO3分子
C. 0.2 mol H3PO4 D. 0.1mol NH33、3molH2SO4中有___________个
H2SO4,可电离出_____mol H+ ___________个SO42-3×6.02×102363×6.02×1023 4、下列各物质所含原子个数按由大到小的序排列的是________________
①0.5molNH3? ②1molHe?
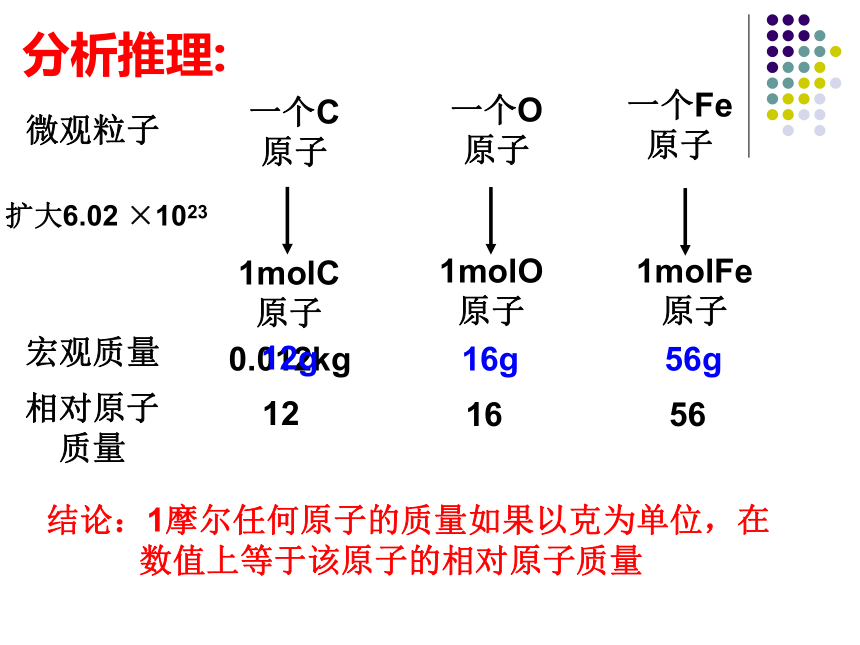
③0.5molH2O? ④0.2molH3PO4① ④ ③ ②思考:1mol任何粒子所含的粒子数是相同的,那么,1mol不同微粒的质量是否相同呢?微观粒子宏观质量一个C
原子一个O
原子一个Fe
原子扩大6.02 ×10231molC
原子1molO
原子1molFe
原子0.012kg16g56g12g相对原子
质量165612结论:1摩尔任何原子的质量如果以克为单位,在
数值上等于该原子的相对原子质量分析推理:相对原子质量 =一个某原子的质量(克)1/12 ×一个C-12原子质量(克)1mol某原子的质量(克)NA个C-12原子质量(克)结论:1摩尔某原子的质量以克为单位,在数值上
正好等 于该原子的相对原子质量×NA×NA12克 1克科学计算:由以上推理和计算结果可得出什么规律?①1mol任何原子的质量在数值上等于
这种原子的相对原子质量。
②1mol任何分子的质量在数值上等于
这种分子的相对分子质量。
③1mol任何离子的质量在数值上等于
这种离子的式量。 结论: 1mol任何物质的质量以克为单位,在数值上正好等于该物质的原子(分子)的相对原子质量(相对分子质量)。如:1摩尔O的质量为16克;1摩尔S的质量为32克;1摩尔Na的质量为23克;1摩尔H的质量为1克;二、摩尔质量1.1mol物质质量 1mol任何粒子或物质的质量是以克为单位,在数值上都与该粒子相对原子质量或相对分子质量相等。 例1.填写下列空白:
(1)1molCu 原子质量是??????? 克
(2) 1molO2分子质量是??????? 克
(3) 1molCO2分子质量是??????? 克
(4) 1molCl1-离子质量是??????? 克
(5) 1molNa+离子质量是??????? 克
(6) 1molNaCl质量是??????? 克 64g 32g 44g 35.5g 23g 58.5g 2.摩尔质量 (1)定义:单位物质的量的物质所具有的
质量叫做摩尔质量。符号M。
(2)单位:g/mol或kg/mol。
(3)数值: (当单位为 g/mol )等于物质或粒
子的相对式量。注意:摩尔质量只与物质的种类有关,与物质的量、
物质的质量无关 例2.回答下列问题
(1)O2 的摩尔质量是多少?
(2)H2SO4 的摩尔质量是多少?M(O2)=32g/molM(H2SO4 )=98g/mol练习 1.下列物质各多少克?含粒子数多少个? 2.下列物质的物质的量是多少?含有多少个粒子? (1)100molH2O ???? (2)0.1molOH- (1)90g水 (2)56g氮气物质的量 (mol) 物质的质量 (g)摩尔质量 (g/mol) n = m / M=两个变式:m=n?M3、物质的量(n)、物质的质量(m)和摩尔质量(M)之间的关系: 课堂练习:(1)、O2的摩尔质量是多少?
(2)、H2SO4的摩尔质量是多少?
(3)、100molH2O的质量是多少克?
(4)、0.1molOH-的质量是多少克?
(5)、34gNH3的物质的量是多少?32g.mol-198g.mol-11800g1.7g2molH2O物质的量(mol) 摩尔质量(g/mol) 质量(g)
1
2
0.5
完成表格18 g/mol18 g/mol18 g/mol18 g36 g9 g微粒的摩尔质量是固定的、不变的。物质的量的意义:是联系宏观和微观的纽带或桥梁。[例 1] 90克水相当于多少摩水?解: 水的式量是18,水的摩尔质量是 18g/mol 。n (H2O) = 90g18g/mol= 5 mol答:90克水相当于5mol水。[例 2] 2. 5 mol 铜原子的质量是多少克?解: 铜的原子量是 64 ,铜的摩尔质量是 64g/mol 。m (Cu) = 2.5 mol 64g/mol ×= 160g答:2.5mol 铜原子的质量等于 160g 。[例 3] 4. 9 克硫酸里含有多少个硫酸分子?解: 硫酸的式量是98,硫酸的摩尔质量是 98g/mol 。n (H2SO4) = 4. 9 g98g/mol= 0.05 mol答:4.9克硫酸里含有 3.01×1022个硫酸分子。N (H2SO4) =0.05 mol × 6.02 × 1023mol-1=3.01×1022[例 4] 20. 2 克硝酸钾中,氧元素的质量是多少克?解: 硝酸钾的式量是101,硝酸钾的摩尔质量是 101g/mol 。n (KNO3) = 20.2 g101g/mol= 0.2 mol答:20.2克硝酸钾中,氧元素的质量是 9. 6 g 。n (O) =0.2 mol×3 = 0.6 molm (O) =0. 6 mol×16g/mol = 9.6 g【例 5 】:有五种物质:
①6gH2;②0.5molCO2;③1.204×1024个HCl分子;
④147gH2SO4;⑤92g乙醇(C2H5OH);
请回答:
⑴物质的量最大的是 ;
⑵所含分子数最多的是 ;
⑶所含原子数最多的是 ; ①①⑤【例 6 】 :若杯中水的质量是54g,大家能算出里面所含的水分子的个数吗?n(H2O)==3mol N(H2O)=n?NA=3×6.02×1023=1.806×1024个练习2.含有6.02X1022 个分子的物质,其质量为
0.7g,求该物质的相对分子质量。练习3. 0.2molKClO3中所含的 Cl原子数与多克
CaCl2中所含的 Cl-离子个数相等? 练一练:小 结二、摩尔质量
???1.1mol物质的质量
??? 2.摩尔质量
三、关于物质的量的计算
(-)依据
????? 1.准确掌握物质的量、摩尔、摩尔质量等概念。
????? 2.掌握好有关物质质量(m)、物质的量(n)和粒子
数(N)之间的关系。
(二)类型
1.物质的质量,物质的量和粒子数之间的相互换算。
2.不同物质中,某粒子数相当的计算。
