物质的量
图片预览







文档简介
课件21张PPT。物 质 的 量想一想?1.你知道古代曹冲称象的故事吗?曹冲在称象时的主导思想是什么? 化整为零,化大为小2.已知托盘天平的最小刻度为0.1克,你能用它称量一粒大米的质量吗?你的主导思想又是什么?
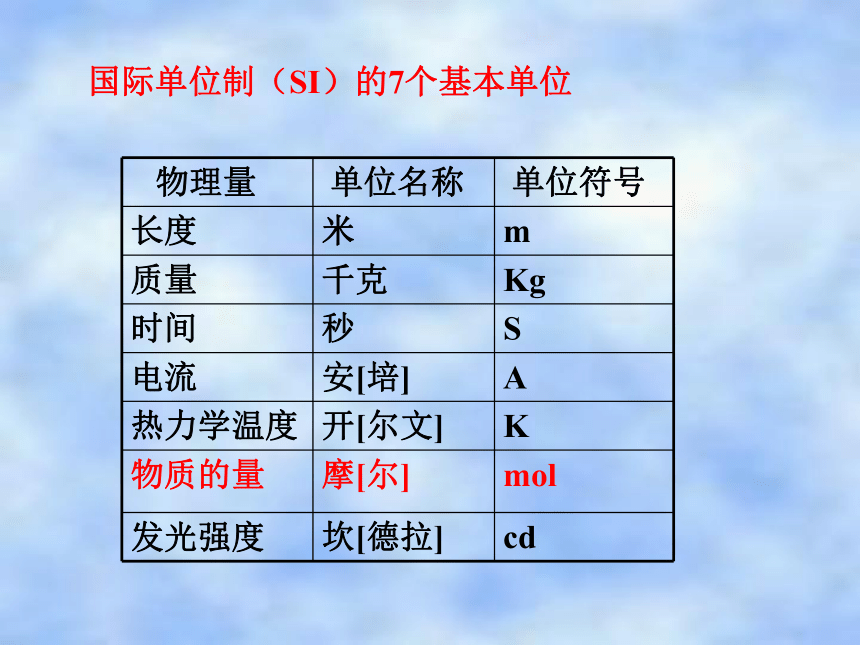
积小成大,聚微为宏问题:这4gH2中含有多少氢分子?32gO2中含有多少个氧分子?36gH2O中又含有多少个水分子?为了解决类似的问题,科学上建立一个“物理量”,叫做“物质的量”国际单位制(SI)的7个基本单位是国际单位制七个基本物理量之一表示含有一定数目粒子的集合体符号:n1、物质的量物质的量与长度、质量、时间等一样是一个基本物理量的名称,不能当成物质的数量或质量来理解。
2、摩尔 物质的量的单位是 摩尔△ 如何定义 1 mol ?在定义 1 mol 要
考虑哪些因素?米 的 基 准 1791年法国决定把通过巴黎的地球子午线从赤道到北极的长度的1/1000000规定为1米。1983年第11届国际计量大会决定用光速米,规定1米等于光在真空中于1/299792485秒时间间隔内所经过的路径的长度。 1 摩尔:含有与 0.012 Kg 12C 中所含的碳原子数相同的粒子数,该物质的物质的量为 1 mol 。△ 0.012 Kg 12C 中究竟含有多少个 12C
原子?(已知:1个 12C 原子的质量为
1.993×10-26Kg)。 约为6.02×1023阿佛加德罗__
意大利物理学家 阿伏加德罗常数:
1 mol 任何粒子的粒子数。0.012 Kg 12C 所含的 碳原子数。符号: NA 单位: mol-1
数值:约为6.02×1023
阿伏加德罗常数约为
6.02×1023 mol-1△你知道6.02×1023数值有多大吗?▲ 6.02×1023粒稻谷平分给12亿人,按一人一
天1 Kg(约含4万粒),可以吃 3.436×107年▲ 6.02×1023个直径2.5 cm 的硬币排成一行,
可来回与地球和太阳之间240.8亿次使用摩尔表示物质的量时注意事项△ 摩尔只能描述原子、分子、离子、质子、中子和
电子等微观粒子,不能描述宏观物质。△ 用摩尔为单位表示某物质的物质的量时,必须指
明物质微粒的名称、符号或化学式。如:1 mol H
、1 mol H+、 1 mol H 2 ,这才能表达具体的微
粒。不能用 “1 mol 氢”这样含糊无意义的表示。 △ 不能用摩尔数代替物质的量。△ 物质的量的数值可以是整数,也可以是小数。N = n. NA【讨论 】
在0.5molO2中含有的氧分子数目是多少?氧原子是多少?解:氧分子数目为
N1=n × NA
=0.5 ×6.02 ×1023 =3.01×1023
氧原子数目为
N2=2 n × NA =2 × 0.5 ×6.02 ×1023
= 6.02 ×1023
【课堂练习】
1.填空:
(1)0.5mol水中含有 个水分子。
(2)2mol水中含有 个水分子,
含有 个氢原子。
(3)1mol NaOH中 含有 个氢氧根离子。
3.01 × 10231.204 × 10242.408 × 10246.02 × 1023【课堂练习】
2.填空:
(1)1mol O中含有 个O;
(2)1mol H2O中约含有 个H2O;
(3)1mol H+中约含有 个H+。3.根据摩尔的有关知识,进行下列计算:
(1)1.204 × 1024个H,合多少mol?
(2)5mol的O2中有多少个氧分子?
(3)N个水分子的物质的量是多少?(已知阿伏加
德罗常数为NA)2 mol3.01 × 1024N/NA6.02 × 10236.02 × 10236.02 × 10234.下列关于物质的量的说法中不正确的是( )
A.物质的量是国际单位制的7个基本单位之一
B.物质的量实际上是表示含有一定数目的粒子集体
C.物质的量的单位是“摩尔”
D.物质的量是表示物质数量的单位【课堂练习】【课堂练习】 5.判断正误,并说明理由。
A.1mol氢
B. 1mol CO2
C. 1mol大米错误。没有指出是分子、原子或离子正确。错误。大米不是微观粒子【课堂练习】
7. 下列数量的各物质中,含原子个数最多的是( )
A.1mol HCl B.3.01 x 1023 个碘分子
C.12g 12C D.0.5mol CH4
8. 与0.3 mol H2O 含有相同氢原子数的是( )
A. 0.3 mol HNO3 B. 3.612 X 10 23个 HNO3分子
C. 0.2 mol H3PO4 D. 0.1mol NH3【课后思考】1mol12C的质量是0.012kg,那么1mol其他物质的质量又是多少呢?
【作业布置】总 结:本节课学习了物质的量及其单位摩尔(mol)的概念,应重点掌握:①物质的量是表示含有一定数目粒子的集体的物理量,摩尔是它的单位,1mol任何粒子数叫阿伏加德罗常数。②物质的量和摩尔只适用于微观粒子,切勿乱用。③以阿伏加德罗常数为桥梁进行物质的量和粒子数之间的换算
积小成大,聚微为宏问题:这4gH2中含有多少氢分子?32gO2中含有多少个氧分子?36gH2O中又含有多少个水分子?为了解决类似的问题,科学上建立一个“物理量”,叫做“物质的量”国际单位制(SI)的7个基本单位是国际单位制七个基本物理量之一表示含有一定数目粒子的集合体符号:n1、物质的量物质的量与长度、质量、时间等一样是一个基本物理量的名称,不能当成物质的数量或质量来理解。
2、摩尔 物质的量的单位是 摩尔△ 如何定义 1 mol ?在定义 1 mol 要
考虑哪些因素?米 的 基 准 1791年法国决定把通过巴黎的地球子午线从赤道到北极的长度的1/1000000规定为1米。1983年第11届国际计量大会决定用光速米,规定1米等于光在真空中于1/299792485秒时间间隔内所经过的路径的长度。 1 摩尔:含有与 0.012 Kg 12C 中所含的碳原子数相同的粒子数,该物质的物质的量为 1 mol 。△ 0.012 Kg 12C 中究竟含有多少个 12C
原子?(已知:1个 12C 原子的质量为
1.993×10-26Kg)。 约为6.02×1023阿佛加德罗__
意大利物理学家 阿伏加德罗常数:
1 mol 任何粒子的粒子数。0.012 Kg 12C 所含的 碳原子数。符号: NA 单位: mol-1
数值:约为6.02×1023
阿伏加德罗常数约为
6.02×1023 mol-1△你知道6.02×1023数值有多大吗?▲ 6.02×1023粒稻谷平分给12亿人,按一人一
天1 Kg(约含4万粒),可以吃 3.436×107年▲ 6.02×1023个直径2.5 cm 的硬币排成一行,
可来回与地球和太阳之间240.8亿次使用摩尔表示物质的量时注意事项△ 摩尔只能描述原子、分子、离子、质子、中子和
电子等微观粒子,不能描述宏观物质。△ 用摩尔为单位表示某物质的物质的量时,必须指
明物质微粒的名称、符号或化学式。如:1 mol H
、1 mol H+、 1 mol H 2 ,这才能表达具体的微
粒。不能用 “1 mol 氢”这样含糊无意义的表示。 △ 不能用摩尔数代替物质的量。△ 物质的量的数值可以是整数,也可以是小数。N = n. NA【讨论 】
在0.5molO2中含有的氧分子数目是多少?氧原子是多少?解:氧分子数目为
N1=n × NA
=0.5 ×6.02 ×1023 =3.01×1023
氧原子数目为
N2=2 n × NA =2 × 0.5 ×6.02 ×1023
= 6.02 ×1023
【课堂练习】
1.填空:
(1)0.5mol水中含有 个水分子。
(2)2mol水中含有 个水分子,
含有 个氢原子。
(3)1mol NaOH中 含有 个氢氧根离子。
3.01 × 10231.204 × 10242.408 × 10246.02 × 1023【课堂练习】
2.填空:
(1)1mol O中含有 个O;
(2)1mol H2O中约含有 个H2O;
(3)1mol H+中约含有 个H+。3.根据摩尔的有关知识,进行下列计算:
(1)1.204 × 1024个H,合多少mol?
(2)5mol的O2中有多少个氧分子?
(3)N个水分子的物质的量是多少?(已知阿伏加
德罗常数为NA)2 mol3.01 × 1024N/NA6.02 × 10236.02 × 10236.02 × 10234.下列关于物质的量的说法中不正确的是( )
A.物质的量是国际单位制的7个基本单位之一
B.物质的量实际上是表示含有一定数目的粒子集体
C.物质的量的单位是“摩尔”
D.物质的量是表示物质数量的单位【课堂练习】【课堂练习】 5.判断正误,并说明理由。
A.1mol氢
B. 1mol CO2
C. 1mol大米错误。没有指出是分子、原子或离子正确。错误。大米不是微观粒子【课堂练习】
7. 下列数量的各物质中,含原子个数最多的是( )
A.1mol HCl B.3.01 x 1023 个碘分子
C.12g 12C D.0.5mol CH4
8. 与0.3 mol H2O 含有相同氢原子数的是( )
A. 0.3 mol HNO3 B. 3.612 X 10 23个 HNO3分子
C. 0.2 mol H3PO4 D. 0.1mol NH3【课后思考】1mol12C的质量是0.012kg,那么1mol其他物质的质量又是多少呢?
【作业布置】总 结:本节课学习了物质的量及其单位摩尔(mol)的概念,应重点掌握:①物质的量是表示含有一定数目粒子的集体的物理量,摩尔是它的单位,1mol任何粒子数叫阿伏加德罗常数。②物质的量和摩尔只适用于微观粒子,切勿乱用。③以阿伏加德罗常数为桥梁进行物质的量和粒子数之间的换算
