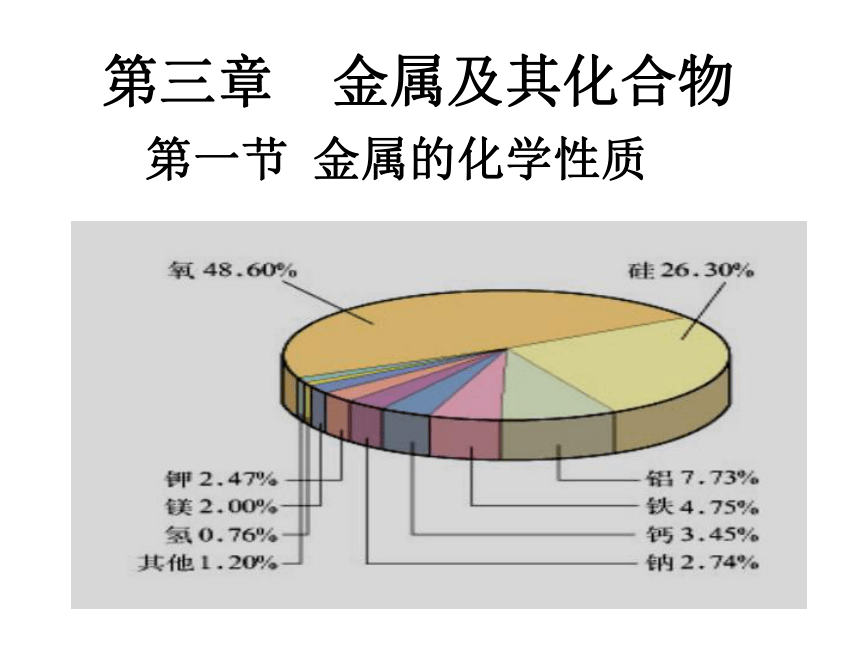
金属的化学性质
图片预览


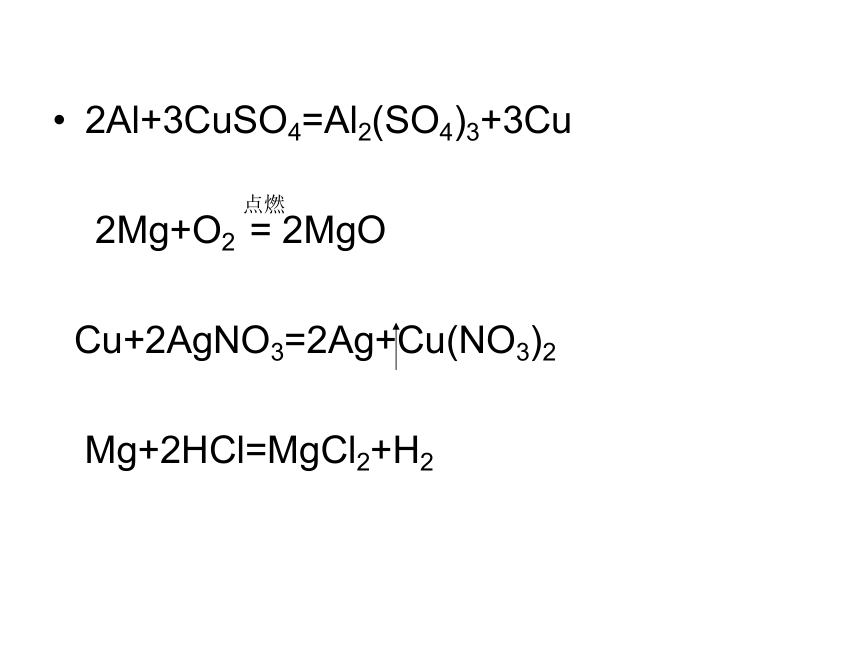


文档简介
课件12张PPT。 第三章 金属及其化合物第一节 金属的化学性质 1 金属可发生的反应有:②相互置换反应③与氧气反应① 活泼金属能与酸反应2Al+3CuSO4=Al2(SO4)3+3Cu
2Mg+O2 = 2MgO
Cu+2AgNO3=2Ag+Cu(NO3)2
Mg+2HCl=MgCl2+H2点燃物理性质:质软(硬度小)、密度比煤油大、银白色有金属光泽的固体。化学性质:很活泼,容易被空气中的氧
气氧化4Na + O2 == 2Na2O从实验3-1中我们可以知道:物理性质:化学性质:钠的熔点低。 受热后剧烈燃烧,发出黄色火焰,生成淡黄色的Na2O2。 从实验3-2中我们可以知道:科学探究加热铝箔实验现象:铝箔熔化,失去光泽,熔化的铝并不滴落实验结论:在常温下,铝能够与空气里面的氧气反应,生成一层致密而坚固的氧化物薄膜。铝是一种活泼金属。(打磨后)铝箔熔化,失去光泽,熔化的铝还是不滴落 人们通常用金属器皿盛水,也用铁、铜制水壶烧水。是不是所有金属都不与水反应呢? 当金属钠遇上水,会是怎么样呢?猜 一 猜想一想 演示实验3-3实验现象:钠浮在水面上熔化成一个小球游动,发出响声酚酞后溶液变红实验结论:密度比水小熔点低有气体生成有碱生成1、金属钠在氧气中燃烧所产生的现象是……( )
A.黄烟,生成白色固体
B.黄雾,生成淡黄色固体
C.黄色火焰,生成淡黄色固体
D.黄色火焰,生成白色固体C2、下列关于钠的物理性质的叙述中正确的是…( )
①银白色金属 ②质软,可用小刀切割
③密度比煤油大
④熔点低于100℃ ⑤热和电的良导体
A.全部正确 B.除②外全部正确
C.仅①③⑤正确 D.除④外全部正确 A课堂练习:课 后 思 考 1.将金属钠投入煤油和水的混合物中,会有何现象?
2.如果金属钠长时间暴露在空气中,最后会生成什么物质?小结:一 金属于非金属的反应
钠于氧气的反应
常温
加热
4Na + O2 == 2Na2O
2Mg+O2 = 2MgO
Cu+2AgNO3=2Ag+Cu(NO3)2
Mg+2HCl=MgCl2+H2点燃物理性质:质软(硬度小)、密度比煤油大、银白色有金属光泽的固体。化学性质:很活泼,容易被空气中的氧
气氧化4Na + O2 == 2Na2O从实验3-1中我们可以知道:物理性质:化学性质:钠的熔点低。 受热后剧烈燃烧,发出黄色火焰,生成淡黄色的Na2O2。 从实验3-2中我们可以知道:科学探究加热铝箔实验现象:铝箔熔化,失去光泽,熔化的铝并不滴落实验结论:在常温下,铝能够与空气里面的氧气反应,生成一层致密而坚固的氧化物薄膜。铝是一种活泼金属。(打磨后)铝箔熔化,失去光泽,熔化的铝还是不滴落 人们通常用金属器皿盛水,也用铁、铜制水壶烧水。是不是所有金属都不与水反应呢? 当金属钠遇上水,会是怎么样呢?猜 一 猜想一想 演示实验3-3实验现象:钠浮在水面上熔化成一个小球游动,发出响声酚酞后溶液变红实验结论:密度比水小熔点低有气体生成有碱生成1、金属钠在氧气中燃烧所产生的现象是……( )
A.黄烟,生成白色固体
B.黄雾,生成淡黄色固体
C.黄色火焰,生成淡黄色固体
D.黄色火焰,生成白色固体C2、下列关于钠的物理性质的叙述中正确的是…( )
①银白色金属 ②质软,可用小刀切割
③密度比煤油大
④熔点低于100℃ ⑤热和电的良导体
A.全部正确 B.除②外全部正确
C.仅①③⑤正确 D.除④外全部正确 A课堂练习:课 后 思 考 1.将金属钠投入煤油和水的混合物中,会有何现象?
2.如果金属钠长时间暴露在空气中,最后会生成什么物质?小结:一 金属于非金属的反应
钠于氧气的反应
常温
加热
4Na + O2 == 2Na2O
