物质的量及其单位--摩尔
图片预览




文档简介
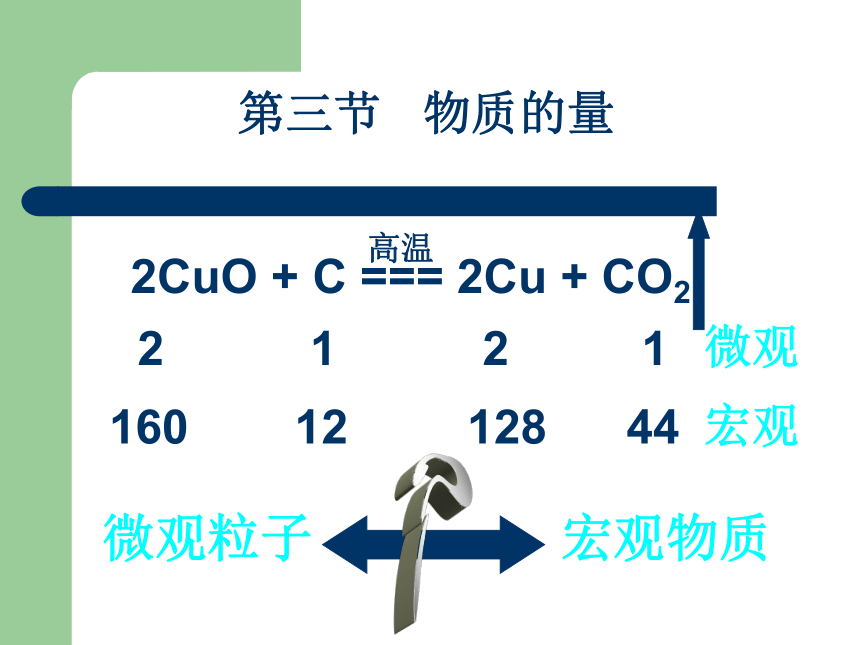
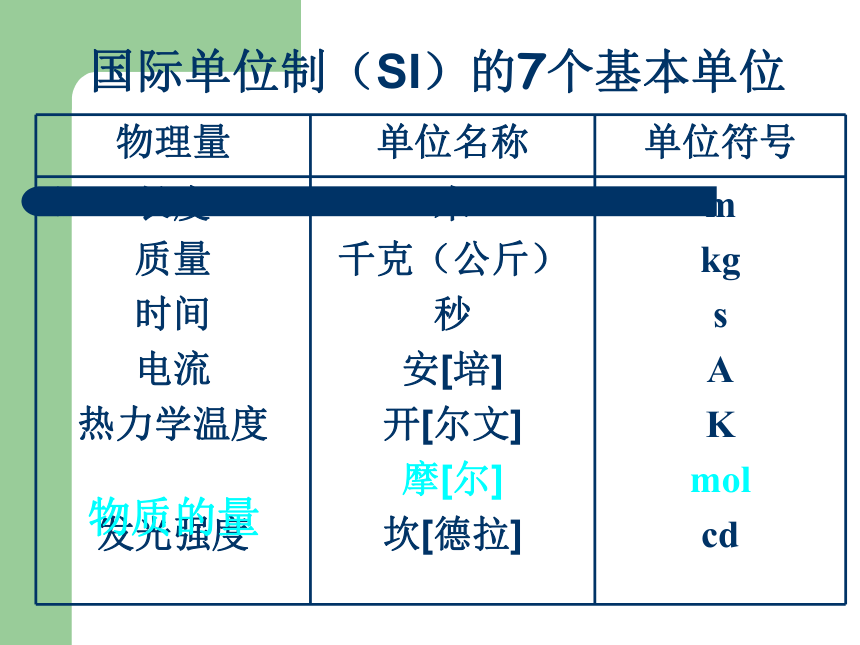
课件16张PPT。第三节 物质的量2CuO + C === 2Cu + CO2高温2 1 2 1160 12 128 44微观粒子 宏观物质?微观宏观物质的量及其单位摩尔国际单位制(SI)的7个基本单位
物质的量说明:⒈物质的量与长度、质量、时间等一样是一个基本物理量的名称⒉摩尔如同米、千克、秒一样是该物理量的单位
⒊“物质的量”四个字是一个整体。由固定的字数组成,不能多,也不能少。物质的量:表示含有一定数目粒子的集体。符号:n摩尔:物质的量的单位,简称摩。符号:mol1、研究对象:
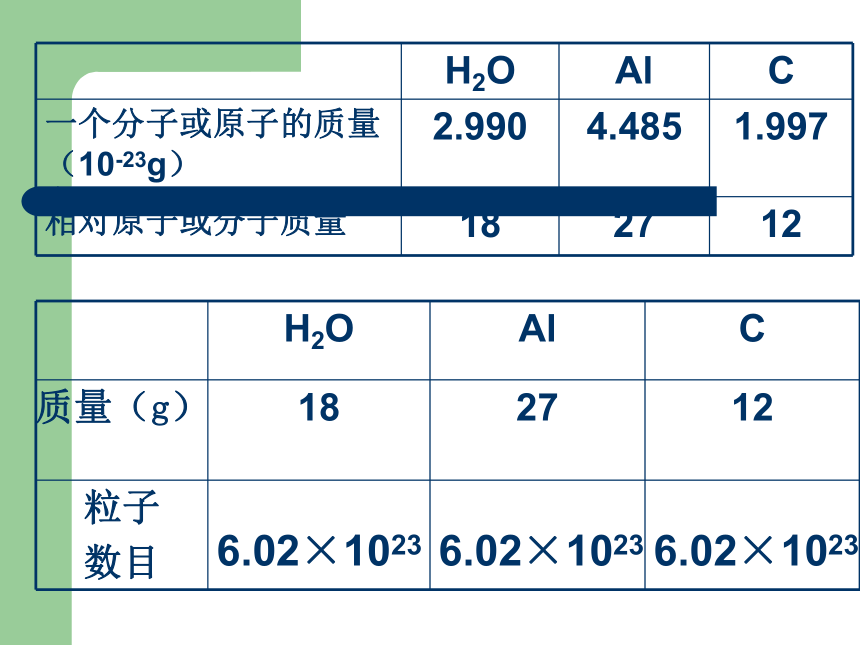
粒子集体—微观粒子,包括原子、分子、离子原子团、电子、质子、中子2、物质的量使用时要用化学式或名称指明 粒子的种类,如1mol Al 4 molH2O、3 mol硫酸根离子、5mol e-6.02×10236.02×10236.02×1023“物质的量”基准:把约含有6.02×1023个粒子的任何粒子集体定义为1 mol阿伏加德罗常数:科学上把6.02×1023mol-1称为阿伏加德罗常数,是一个物理量.符号:NA,单位:mol-1实验表明,任何粒子或物质的质量以克为单位,在数值上等于相对原子或相对分子质量时,所含粒子的数目都约为6.02×1023个1、1mol O约含有___________________个O2、3molH2SO4中约有______________________
个H2SO43、1.204×1024个H2O,其物质的量
为___________2mol6.02×10233×6.02×10234、1.806×1023个H2O,其物质的量
为___________0.3 mol课堂练习物质的量(n)、粒子数目(N)、阿伏加德罗常数(NA)三者关系思考:1molH2O中含有多少摩尔H?多少摩尔O?共含有多少个原子n=(N=n NA)×NNA
1、0.5molNa2SO4含有___mol Na+ ___mol SO42-、____mol O、 约含___________个O1.204×102410.52课堂练习2、0.1molNH4+中约含 _________
个N,共含有___________ 个原子,
约含有___________个e-6.02×10223.01×10236.02×1023[小结]本节课学习了物质的量(n)及其单位(mol)的概念,应重点掌握:
①物质的量是表示含有一定数目粒子的集体的物理量,摩尔是它的单位,6.02×1023mol-1叫做阿伏加德罗常数
②物质的量和摩尔只适用于微观粒子,切勿乱用
③以阿伏加德罗常数为桥梁进行物质的量和粒子数之间的换算(n= )NNA一、选择题
1、下列说法正确的是( )
A、0.1mol Fe B、0.5 Na2CO3
C、0.2mol H2SO4 D、1mol氧A、C自我检测题2、下列说法正确的是( )
A、物质的量是把物质的质量同微观粒子联系起来的一个基本物理量
B、摩尔是国际单位制中七个基本物理量之一
C、1mol任何物质的质量等于该物质的相对原子或相对分子质量
A二、下列说法是否正确?
1、物质的量就是物质的质量。
2、每摩尔物质含有6.02×1023个粒子。
3、摩尔是七个基本物理量之一。
4、摩尔是物质的数量单位。5、摩尔是物质的质量单位。
6、1mol小麦约含6.02×1023个麦粒5、摩尔是物质的质量单位。
6、1mol小麦约含6.02×1023个麦粒。
1、4molO2中约含有__________个O2
2、10molNa+约含有_________个Na+
3、1.806×1023个e-的物质的量约为_____2.408×10246.02×1024三、计算题0.3 mol作业:
1、0.2molH2O含有多少个H20分子?这些水中含有多少个H原子?
2、含3.01×1023个分子的H2SO4的物质的量是多少?
物质的量说明:⒈物质的量与长度、质量、时间等一样是一个基本物理量的名称⒉摩尔如同米、千克、秒一样是该物理量的单位
⒊“物质的量”四个字是一个整体。由固定的字数组成,不能多,也不能少。物质的量:表示含有一定数目粒子的集体。符号:n摩尔:物质的量的单位,简称摩。符号:mol1、研究对象:
粒子集体—微观粒子,包括原子、分子、离子原子团、电子、质子、中子2、物质的量使用时要用化学式或名称指明 粒子的种类,如1mol Al 4 molH2O、3 mol硫酸根离子、5mol e-6.02×10236.02×10236.02×1023“物质的量”基准:把约含有6.02×1023个粒子的任何粒子集体定义为1 mol阿伏加德罗常数:科学上把6.02×1023mol-1称为阿伏加德罗常数,是一个物理量.符号:NA,单位:mol-1实验表明,任何粒子或物质的质量以克为单位,在数值上等于相对原子或相对分子质量时,所含粒子的数目都约为6.02×1023个1、1mol O约含有___________________个O2、3molH2SO4中约有______________________
个H2SO43、1.204×1024个H2O,其物质的量
为___________2mol6.02×10233×6.02×10234、1.806×1023个H2O,其物质的量
为___________0.3 mol课堂练习物质的量(n)、粒子数目(N)、阿伏加德罗常数(NA)三者关系思考:1molH2O中含有多少摩尔H?多少摩尔O?共含有多少个原子n=(N=n NA)×NNA
1、0.5molNa2SO4含有___mol Na+ ___mol SO42-、____mol O、 约含___________个O1.204×102410.52课堂练习2、0.1molNH4+中约含 _________
个N,共含有___________ 个原子,
约含有___________个e-6.02×10223.01×10236.02×1023[小结]本节课学习了物质的量(n)及其单位(mol)的概念,应重点掌握:
①物质的量是表示含有一定数目粒子的集体的物理量,摩尔是它的单位,6.02×1023mol-1叫做阿伏加德罗常数
②物质的量和摩尔只适用于微观粒子,切勿乱用
③以阿伏加德罗常数为桥梁进行物质的量和粒子数之间的换算(n= )NNA一、选择题
1、下列说法正确的是( )
A、0.1mol Fe B、0.5 Na2CO3
C、0.2mol H2SO4 D、1mol氧A、C自我检测题2、下列说法正确的是( )
A、物质的量是把物质的质量同微观粒子联系起来的一个基本物理量
B、摩尔是国际单位制中七个基本物理量之一
C、1mol任何物质的质量等于该物质的相对原子或相对分子质量
A二、下列说法是否正确?
1、物质的量就是物质的质量。
2、每摩尔物质含有6.02×1023个粒子。
3、摩尔是七个基本物理量之一。
4、摩尔是物质的数量单位。5、摩尔是物质的质量单位。
6、1mol小麦约含6.02×1023个麦粒5、摩尔是物质的质量单位。
6、1mol小麦约含6.02×1023个麦粒。
1、4molO2中约含有__________个O2
2、10molNa+约含有_________个Na+
3、1.806×1023个e-的物质的量约为_____2.408×10246.02×1024三、计算题0.3 mol作业:
1、0.2molH2O含有多少个H20分子?这些水中含有多少个H原子?
2、含3.01×1023个分子的H2SO4的物质的量是多少?
