从自然界获取铁和铜1
图片预览





文档简介
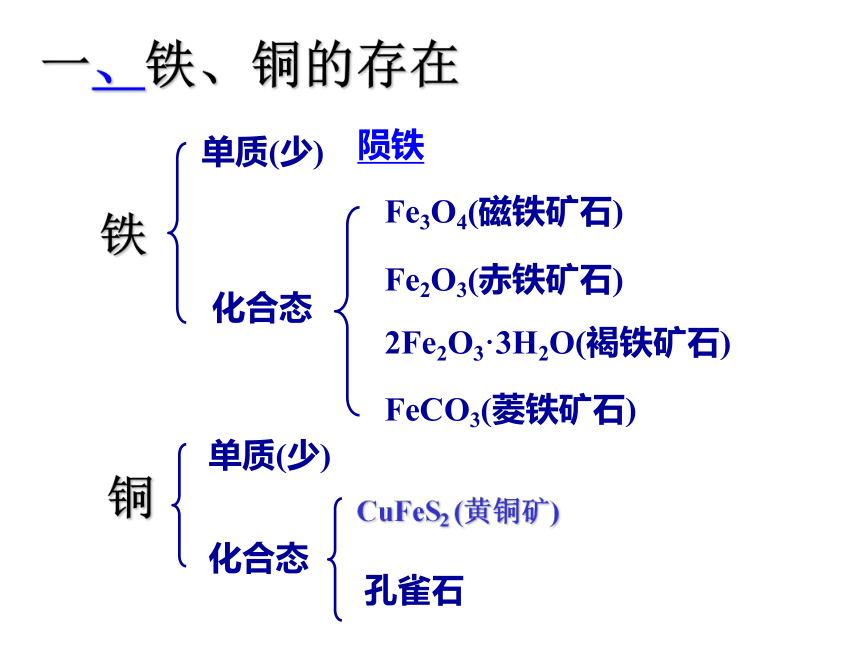
课件14张PPT。第二单元 铁、铜的获取及应用3.2.1 从自然界获取铁和铜一、铁、铜的存在铁化合态Fe3O4(磁铁矿石)Fe2O3(赤铁矿石)2Fe2O3·3H2O(褐铁矿石)FeCO3(菱铁矿石)单质(少)陨铁铜单质(少)化合态CuFeS2 (黄铜矿)孔雀石趁热打铁 古代冶炼生铁的方法:即在1200℃左右用木炭把铁矿石还原成固态铁。其中夹杂着没有烧完的木炭和炼铁时产生的熔渣而呈团块状。然后趁热锻打,挤出其中的夹杂物,并利用铁的延展性和锻打时局部产生的热使小块的铁锻接成一体,变成可以进一步制作铁器的铁材。古代炼铁图从自然界获取铁和铜二、炼铁:铁矿石(化合态)→铁单质(游离态)(2)基本反应原理:3CO+ Fe2O3=====2Fe+3CO2高温利用氧化还原反应,在高温下,用还原剂(主要是CO)从铁矿石中还原出铁。(3)设备:高炉(1)原料:铁矿石,焦炭,石灰石,空气 (4)炼铁的主要反应过程:
从自然界获取铁和铜高炉炼铁的主要反应过程①产生还原剂: C+O2=CO2 CO2+C=2CO
(热空气,焦炭) ②还原铁矿石: Fe2O3+3CO==2Fe+3CO2
(铁矿石) ③造渣(除脉石): CaCO3===CO2+CaO
CaO+SiO2=CaSiO3
(熔剂:石灰石)高温高温(5)炼铁产品:生铁(6)炼铁和环保节能高炉煤气:CO、CO2、N2课堂练习:
目前我们已经学习了的金属冶炼方法有哪些?请总结!古代湿法炼铜 铜盐溶液里的铜能被铁置换,古代劳动人民从而发明了水法炼铜。它成为湿法冶金术的先驱,在世界化学史上占有光辉的一页。
在汉代许多著作里有记载“石胆能化铁为铜”,晋葛洪《抱朴子内篇·黄白》中也有“以曾青涂铁,铁赤色如铜”的记载。南北朝时更进一步认识到不仅硫酸铜,其他可溶性铜盐也能与铁发生置换反应。
水法炼铜的原理是:
CuSO4 + Fe == Cu + FeSO4 首先把精矿砂、熔剂(石灰石、砂等)和燃料(焦炭或木炭)混合,投入“密闭”鼓风炉中,在1000 ℃左右进行熔炼。 2CuFeS2+O2==Cu2S+2FeS+SO2
部分FeS 转变为 FeO: 2FeS+3O2=2FeO+2SO2
Cu2S跟剩余的FeS等便熔融在一起而形成“冰铜” ,FeO跟SiO2形成熔渣: FeO+SiO2=FeSiO3
加入熔剂(石英砂)后鼓入空气进行吹炼(1100~1300 ℃)冰铜中的FeS先转变为FeO,跟熔剂结合成渣,而后Cu2S才转变为Cu2O,Cu2O跟Cu2S反应生成粗铜(含铜量约为98.5%)。
2Cu2S+3O2=2Cu2O+2SO2
2Cu2O+Cu2S=6Cu+SO2↑
高温冶炼黄铜矿 金属冶炼方法小结1.电解法制活泼金属:2NaCl==2Na+Cl2↑MgCl2==Mg+Cl2↑2Al2O3==4Al+3O2↑2.热还原法:3CO+ Fe2O3====2Fe+3CO22Al+ Fe2O3====2Fe+Al2O3Cr2O3+2Al====2Cr+Al2O3(铝热法)高温高温高温电解电解电解鞍钢2000立方米高炉外景图120吨转炉炼钢时的情景高炉结构图C+O2=CO2CO2+C=2CO3CO+Fe2O3
=2Fe+3CO2
从自然界获取铁和铜高炉炼铁的主要反应过程①产生还原剂: C+O2=CO2 CO2+C=2CO
(热空气,焦炭) ②还原铁矿石: Fe2O3+3CO==2Fe+3CO2
(铁矿石) ③造渣(除脉石): CaCO3===CO2+CaO
CaO+SiO2=CaSiO3
(熔剂:石灰石)高温高温(5)炼铁产品:生铁(6)炼铁和环保节能高炉煤气:CO、CO2、N2课堂练习:
目前我们已经学习了的金属冶炼方法有哪些?请总结!古代湿法炼铜 铜盐溶液里的铜能被铁置换,古代劳动人民从而发明了水法炼铜。它成为湿法冶金术的先驱,在世界化学史上占有光辉的一页。
在汉代许多著作里有记载“石胆能化铁为铜”,晋葛洪《抱朴子内篇·黄白》中也有“以曾青涂铁,铁赤色如铜”的记载。南北朝时更进一步认识到不仅硫酸铜,其他可溶性铜盐也能与铁发生置换反应。
水法炼铜的原理是:
CuSO4 + Fe == Cu + FeSO4 首先把精矿砂、熔剂(石灰石、砂等)和燃料(焦炭或木炭)混合,投入“密闭”鼓风炉中,在1000 ℃左右进行熔炼。 2CuFeS2+O2==Cu2S+2FeS+SO2
部分FeS 转变为 FeO: 2FeS+3O2=2FeO+2SO2
Cu2S跟剩余的FeS等便熔融在一起而形成“冰铜” ,FeO跟SiO2形成熔渣: FeO+SiO2=FeSiO3
加入熔剂(石英砂)后鼓入空气进行吹炼(1100~1300 ℃)冰铜中的FeS先转变为FeO,跟熔剂结合成渣,而后Cu2S才转变为Cu2O,Cu2O跟Cu2S反应生成粗铜(含铜量约为98.5%)。
2Cu2S+3O2=2Cu2O+2SO2
2Cu2O+Cu2S=6Cu+SO2↑
高温冶炼黄铜矿 金属冶炼方法小结1.电解法制活泼金属:2NaCl==2Na+Cl2↑MgCl2==Mg+Cl2↑2Al2O3==4Al+3O2↑2.热还原法:3CO+ Fe2O3====2Fe+3CO22Al+ Fe2O3====2Fe+Al2O3Cr2O3+2Al====2Cr+Al2O3(铝热法)高温高温高温电解电解电解鞍钢2000立方米高炉外景图120吨转炉炼钢时的情景高炉结构图C+O2=CO2CO2+C=2CO3CO+Fe2O3
=2Fe+3CO2
