氯气实验室制备
图片预览





文档简介
课件21张PPT。WELCOME TO MY CLASS氯气的制备问题:一套完整的制取气体的装置包括哪几个环节
【活动一】、探究氯气制备过程的设计思考1、氯气实验室制备的药品,制备原理? 实验室一般用二氧化锰与浓盐酸为原料,反应制取氯气
反应方程式:
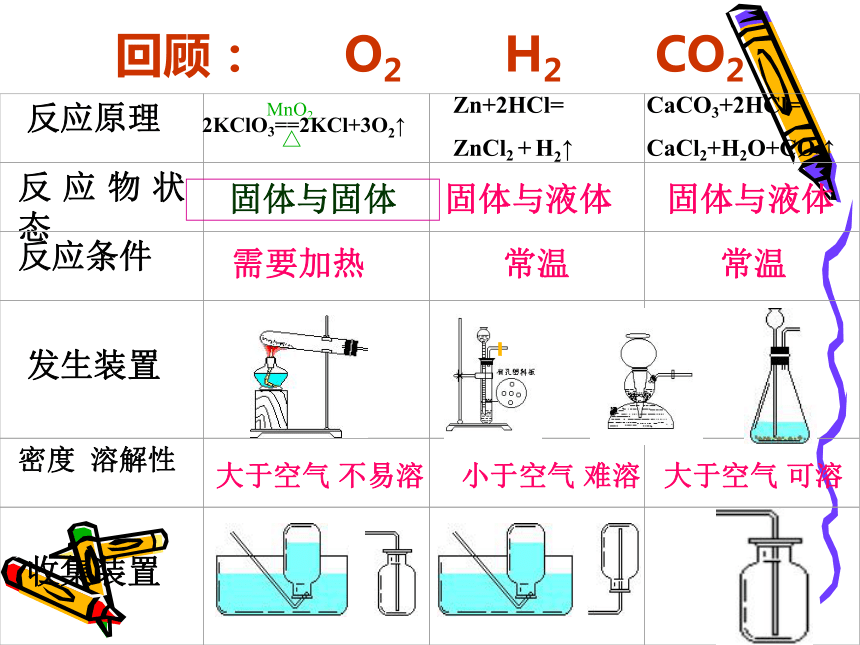
离子方程式:回顾: O2 H2 CO2固体与固体固体与液体固体与液体需要加热常温常温大于空气 不易溶小于空气 难溶大于空气 可溶思考2、根据表1,总结气体发生装置的主要依据是什么? 思考3、根据表1,总结气体收集装置的主要依据是什么?密度: 1、小于空气且不与空气中的气体发生反应, 可用向下排空气法收集;
2、大于空气,可用向上排空气法;
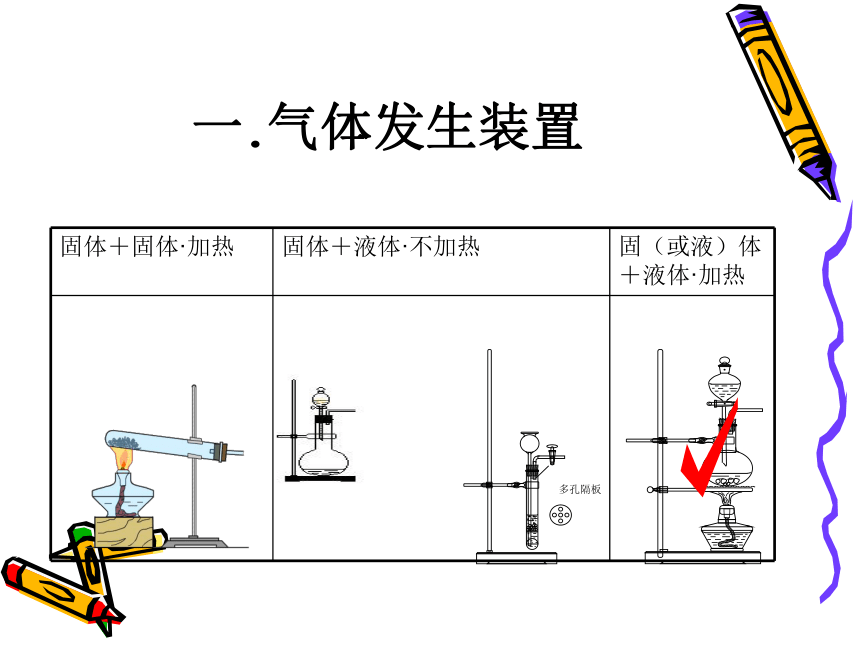
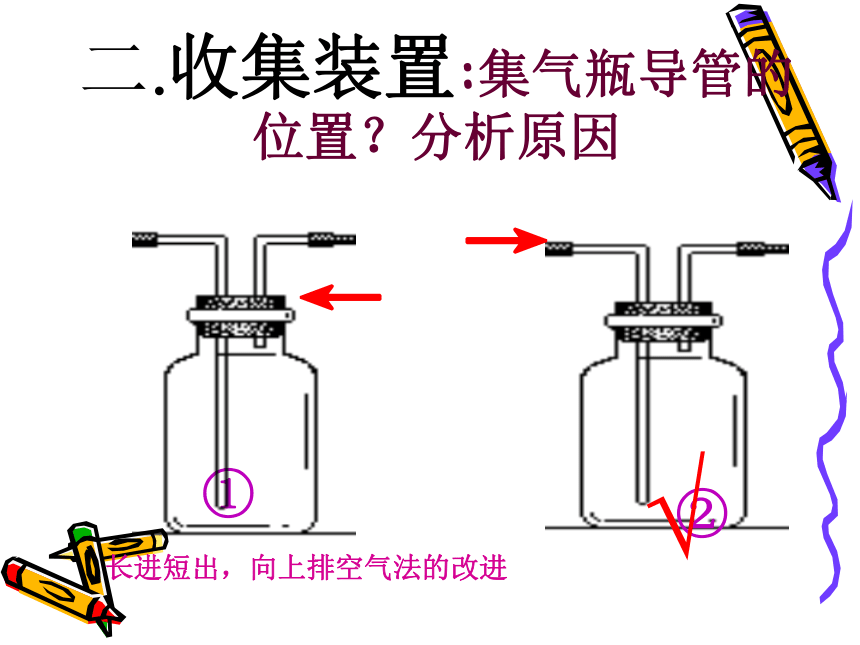
溶解性:3、不易溶于水的气体,可用排水法收集。go一.气体发生装置二.收集装置:集气瓶导管的位置?分析原因①→→②√长进短出,向上排空气法的改进
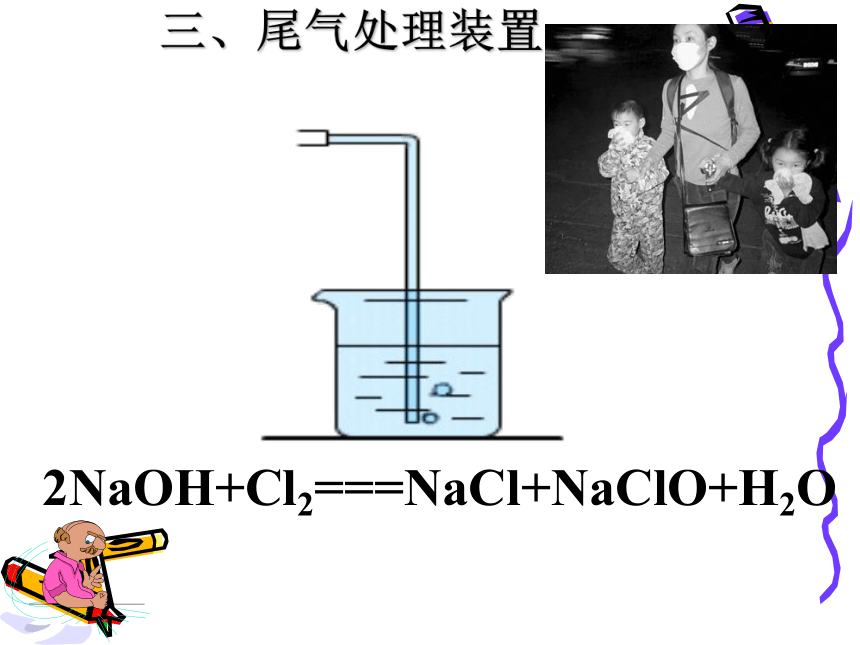
2NaOH+Cl2===NaCl+NaClO+H2O 三、尾气处理装置Cl2的制备【活动二】、探究对氯气制备的进一步思考
思考1、在上述实验中,收集到的氯气中有杂质吗?如果有,主要有哪些?用什么试剂除去?除去的先后顺序?
思考2、如何制得纯净干燥的氯气?
Cl2中可能含的杂质:HCl H2O
除杂装置如下:干燥,纯净Cl2制备装置如下【小结】
思考1、总结一套完整的制气装置应包括哪些?
思考2、总结实验室制取气体的过程?
气体发生 气体净化 气体收集 尾气吸收
气体发生→气体净化→气体干燥→气体收集→尾气吸收
①连接好装置,检查气密性②在烧瓶中加入二氧化锰粉末③往分液漏斗中加入浓盐酸,
再缓缓滴入烧瓶中④缓缓加热,加快反应,使气体均匀逸出⑤用向上排空气法收集氯气,
尾气导入吸收剂中实验步骤总结讨论:如何验满或检验生成的气体是氯气?1.观察: 黄绿色、有刺激性气味的气体 (色、态、味)
2.检验: 湿润的淀粉KI试纸(变蓝);
下图是实验室用来制取干燥、纯净氯气的装置;由于装置和使用药品有错误而未能在D瓶中收集到Cl2;请指出装置中的错误讨论 ①长颈漏斗应改为分液漏斗.
②烧瓶下应垫石棉网.
③应用酒精灯加热.
④稀盐酸应改为浓盐酸.
⑤多余Cl2应通入NaOH溶液中使浓盐酸与足量的MnO2共热制Cl2、实际产生的Cl2总比理论值低,其主要原因是什么?稀盐酸与MnO2不反应,随着反应的进行,浓盐酸的浓度逐渐变小。讨论随堂检测4 验室用MnO2制取Cl2的叙述正确的是( )
A、MnO2与稀盐酸共热 B、缓慢加热反应
C、用向下排空气法收集Cl2
D、多余氯气常用较浓碱液吸收
6.实验室要制得干燥纯净的氯气,应让产生的氯气依次通过的试剂是( )
A、浓H2SO4,碱石灰 B、饱和食盐水,浓H2SO4
C、碱石灰,浓H2SO4 D、水,饱和食盐水
2、实验室制氯气时,二氧化锰的作用是 ( )
A 催化剂 B 氧化剂
C 还原剂 D 反应物再 见谢谢
【活动一】、探究氯气制备过程的设计思考1、氯气实验室制备的药品,制备原理? 实验室一般用二氧化锰与浓盐酸为原料,反应制取氯气
反应方程式:
离子方程式:回顾: O2 H2 CO2固体与固体固体与液体固体与液体需要加热常温常温大于空气 不易溶小于空气 难溶大于空气 可溶思考2、根据表1,总结气体发生装置的主要依据是什么? 思考3、根据表1,总结气体收集装置的主要依据是什么?密度: 1、小于空气且不与空气中的气体发生反应, 可用向下排空气法收集;
2、大于空气,可用向上排空气法;
溶解性:3、不易溶于水的气体,可用排水法收集。go一.气体发生装置二.收集装置:集气瓶导管的位置?分析原因①→→②√长进短出,向上排空气法的改进
2NaOH+Cl2===NaCl+NaClO+H2O 三、尾气处理装置Cl2的制备【活动二】、探究对氯气制备的进一步思考
思考1、在上述实验中,收集到的氯气中有杂质吗?如果有,主要有哪些?用什么试剂除去?除去的先后顺序?
思考2、如何制得纯净干燥的氯气?
Cl2中可能含的杂质:HCl H2O
除杂装置如下:干燥,纯净Cl2制备装置如下【小结】
思考1、总结一套完整的制气装置应包括哪些?
思考2、总结实验室制取气体的过程?
气体发生 气体净化 气体收集 尾气吸收
气体发生→气体净化→气体干燥→气体收集→尾气吸收
①连接好装置,检查气密性②在烧瓶中加入二氧化锰粉末③往分液漏斗中加入浓盐酸,
再缓缓滴入烧瓶中④缓缓加热,加快反应,使气体均匀逸出⑤用向上排空气法收集氯气,
尾气导入吸收剂中实验步骤总结讨论:如何验满或检验生成的气体是氯气?1.观察: 黄绿色、有刺激性气味的气体 (色、态、味)
2.检验: 湿润的淀粉KI试纸(变蓝);
下图是实验室用来制取干燥、纯净氯气的装置;由于装置和使用药品有错误而未能在D瓶中收集到Cl2;请指出装置中的错误讨论 ①长颈漏斗应改为分液漏斗.
②烧瓶下应垫石棉网.
③应用酒精灯加热.
④稀盐酸应改为浓盐酸.
⑤多余Cl2应通入NaOH溶液中使浓盐酸与足量的MnO2共热制Cl2、实际产生的Cl2总比理论值低,其主要原因是什么?稀盐酸与MnO2不反应,随着反应的进行,浓盐酸的浓度逐渐变小。讨论随堂检测4 验室用MnO2制取Cl2的叙述正确的是( )
A、MnO2与稀盐酸共热 B、缓慢加热反应
C、用向下排空气法收集Cl2
D、多余氯气常用较浓碱液吸收
6.实验室要制得干燥纯净的氯气,应让产生的氯气依次通过的试剂是( )
A、浓H2SO4,碱石灰 B、饱和食盐水,浓H2SO4
C、碱石灰,浓H2SO4 D、水,饱和食盐水
2、实验室制氯气时,二氧化锰的作用是 ( )
A 催化剂 B 氧化剂
C 还原剂 D 反应物再 见谢谢
