电解池工作复习
图片预览




文档简介
课件27张PPT。电解池工作复习 【复习目标】
1、掌握电解池的概念及原理;
2、学会正确书写电极反应及总反应方程式,掌握常见离子放电的规律。 【复习重点】
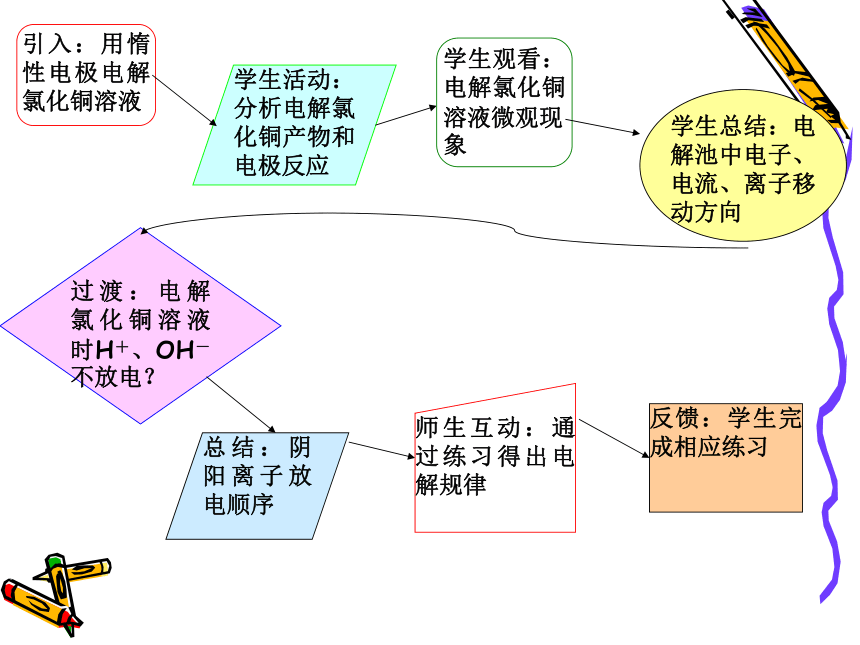
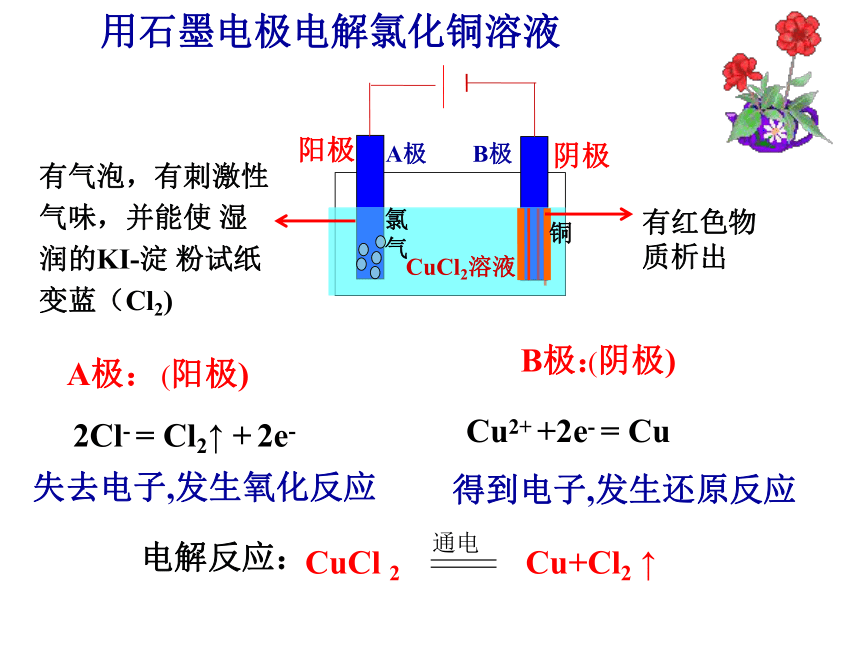
电解池的概念及原理引入:用惰性电极电解氯化铜溶液用石墨电极电解氯化铜溶液有气泡,有刺激性气味,并能使 湿润的KI-淀 粉试纸变蓝(Cl2)2Cl- = Cl2↑ + 2e-阴极阳极氯
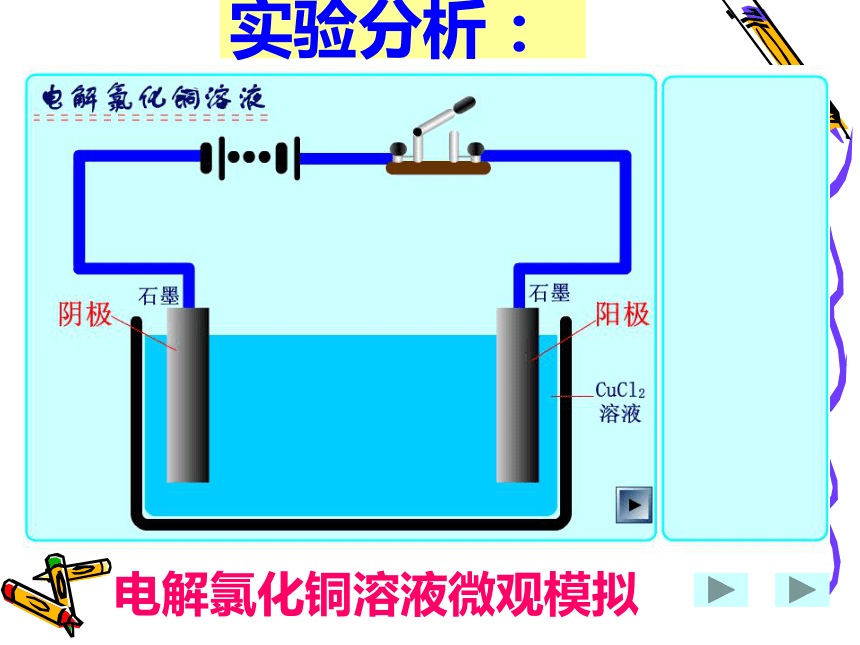
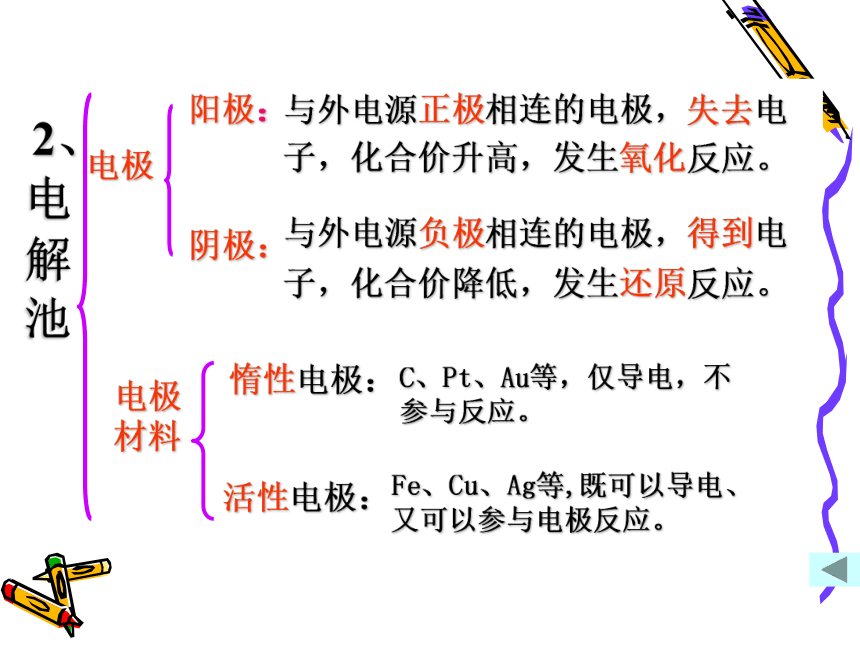
气铜CuCl2溶液A极B极 A极: (阳极)失去电子,发生氧化反应 有红色物质析出Cu2+ +2e- = Cu 得到电子,发生还原反应 B极: (阴极)1、电解:使电流通过电解质溶液或熔融的电解质,而在阴阳两个电极分别发生氧化和还原反应的过程一、电解原理2、电解池定义:把电能转化为化学能的装置。组成:两个电极、电解质溶液或熔融电解质直流电源、电解氯化铜溶液微观模拟实验分析:电极阳极:与外电源正极相连的电极,失去电子,化合价升高,发生氧化反应。阴极:与外电源负极相连的电极,得到电子,化合价降低,发生还原反应。惰性电极:C、Pt、Au等,仅导电,不参与反应。活性电极:Fe、Cu、Ag等,既可以导电、又可以参与电极反应。电 解 池2、电极材料电 解 池2、电子流动方向:离子定向移动的方向:电子从外加电源的负极流出,流到电解池的阴极,再从阳极流回电源正极。 阳离子向阴极移动,
阴离子向阳极移动。电流流
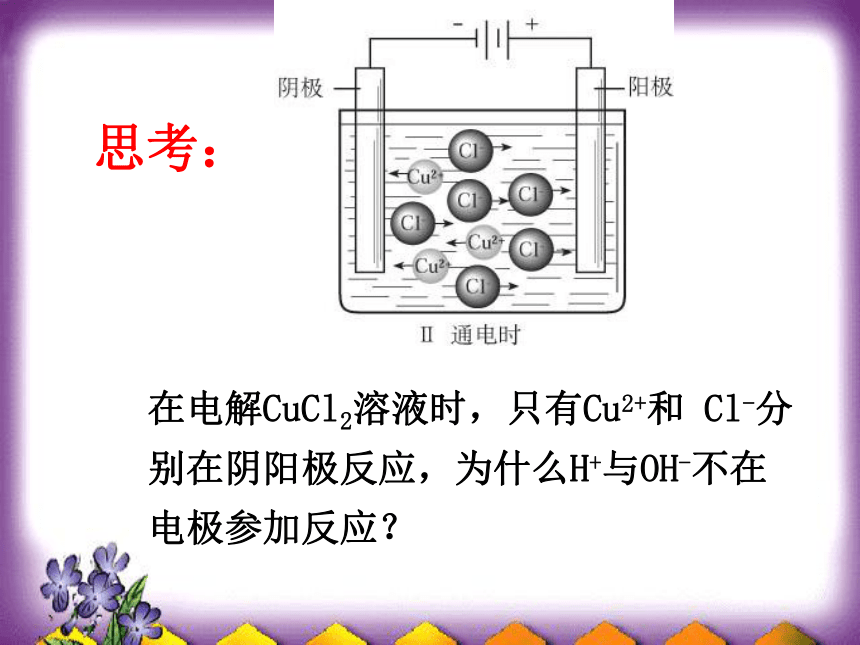
动方向:电流从外加电源的正极流向负极思考:在电解CuCl2溶液时,只有Cu2+和 Cl-分别在阴阳极反应,为什么H+与OH-不在电极参加反应?放电:阴离子失去电子而阳离子得到电子的过程 ①活性材料作电极时(Fe、Cu 等):金属在阳极失电子被氧化 成阳离子进人溶液。
②用惰性电极(Pt、Au、石墨、钛等)时:溶液中阴离子的放电顺序(由难到易)是:S 2- > I - > Br - > Cl - > OH - > NO3->SO42-(等含氧酸根离子)>F-阳极:二、电解产物的确定 离子放电顺序Ag+ > Fe3+ > Cu2+ > Pb2+ > Sn2+ > Fe2+ > Zn2+ > H+ > Al3+ > Mg2+ > Na+ > Ca2+ > K+ 无论是惰性电极还是活性电极都不参与电极反应,发生反应的是溶液中的阳离子。
阳离子在阴极上放电顺序是:阴极:二、电解产物的确定 离子放电顺序思考:在电解CuCl2溶液时,只有Cu2+和 Cl-分别在阴阳极反应,为什么H+与OH-不在电极参加反应?想一想: 如下图:电解氯化铜溶液,电极反应情况又如何?阳极:Fe = Fe 2+ +2e-阴极:Cu2+ +2e- = Cu阳极阴极阳极为活性电极,则电极自身被氧化阳离子放电顺序:Cu2+> H+三、电极反应式、电解方程式的书写:例:写出用石墨做电极电解CuSO4溶液的电极反应式及总的电解方程式. 阴极:阳极:③最后使得失数相等,两极反应相加得总方程式阴极:阳极:4OH- -4e - =O2↑+2H2O2Cu2++4e - =2CuOH- > SO42-H+ < Cu2+①首先分析、比较出阴阳极的放电离子:②然后写电极反应式 :2Cu+O2↑+4H+或2CuSO4+2H2O
(电解反应的化学方程式)2Cu+O2↑+2H2SO42Cu2++2H2O(电解反应的离子方程式)完成下列溶液的电极反应(以石墨为电极电解)(1)NaOH溶液:
(2)盐酸溶液:知识反馈一阳极C阴极C氧气氢
气阳极: 4OH- → 2H2O+O2 ↑ + 4e-阴极: 4H ++ 4e- → 2H2 ↑变大变
大 加
H2O
NaOH溶液2H2O 2H2 ↑ + O2 ↑阳极:2Cl--2 e- =Cl2↑阴极:2H+ + 2e-=H2↓减小增大HCl
阳极C阴极C氯气氢
气盐酸溶液四、电解规律(惰性电极)小结 阳极:S2- > I- > Br- > Cl- > OH- > 含氧酸根 > F- 简单阴离子复杂阴离子阴极:Ag+>Fe3+>Cu2+ >Fe2+> Zn2+ > H+>Al3+>Mg2+>Na+ >K+活泼金属离子不活泼金属离子 电解质溶液用惰性电极电解的示例:含氧酸H2SO4强碱NaOH活泼金属的含氧酸盐Na2SO4无氧酸HCl阳极:4OH-→4e-=O2+2H2O
阴极:4H+ + 4e- = 2H2↑减小增大不变H2O阳极:2Cl- → 2e-=Cl2↑
阴极:2H++2e- = H2↑增大HCl不活泼金属的无氧酸盐CuCl2阳极:2Cl- → 2e- =Cl2↑
阴极:Cu2++2e- = Cu减少CuCl2活泼金属的无氧酸盐NaCl阳极:2Cl- → 2e- =Cl2↑
阴极:2H++2e- =H2↑增大HCl不活泼金属的含氧酸盐CuSO4阳极:4OH- → 4e- =O2↑+2H2O
阴极:2Cu2++4e- = 2Cu减小CuO完成下列溶液的电极反应(以石墨为电极电解)(1)Na2SO4溶液:
(2)NaCl溶液:
(3)CuSO4溶液:知识反馈二阳极C阴极C氧气氢
气阳极: 4OH- → 4e- + 2H2O+O2 ↑阴极: 4H ++ 4e- → 2H2 ↑变大不
变 加
H2O
Na2SO4溶液2H2O 2H2 ↑ + O2 ↑阳极C阴极C氯气氢
气阳极: 2Cl- → 2e- + Cl 2↑阴极: 2H ++ 2e- → H2 ↑2NaCl+2H2O 2NaOH+H2↑ + Cl2↑减小增
大 加
HCl
NaCl溶液阳极C阴极C氧
气铜阳极: 4OH- → 4e- + 2H2O+O2 ↑阴极:Cu2++ 2e- → Cu减小减小 加
CuOCuSO4溶液体验高考 (2004广东、广西) PH=a>的某电解质溶液中,插入两支惰性电极通直流电一段时间后,溶液的PH>a,则该电解质可能是( )
A.NaOH B.H2SO4
C.AgNO3 D.Na2SO4A(2)写出电极反应:A中:___B中:____ C中:___ D中:___ (1)标出电源的正、负极,X为 ______,Y为______.模拟训练:由电极产物判断电源电极A:4H++4e-=2H2↑B:4OH--4e-=2H2O+O2↑C:2H++2e-=H2↑D:2Cl-+2e-=Cl2↑如图装置中,E为一只盛有AlCl3溶液的烧杯,C为铂棒、D为铁棒,X与Y为电源的电极,A、B中插入多孔的惰性电极。切断开关K1,闭合开关K2,通直流电一端时间后,A、B中液面如图所示,请回答 :正极负极阴极阳极阴极阳极作 业:在如下的装置中进行电解,并已知铁极的质量减小11.2克。
(1)A是电源的 极
(2)电解过程中,电路中通过 摩电子
(3)Ag极的电极反应是 ;析出物质是 克
(4)Cu(a)的电极反应是 ;
(5)Cu(b)的电极反应是 。再见再见
1、掌握电解池的概念及原理;
2、学会正确书写电极反应及总反应方程式,掌握常见离子放电的规律。 【复习重点】
电解池的概念及原理引入:用惰性电极电解氯化铜溶液用石墨电极电解氯化铜溶液有气泡,有刺激性气味,并能使 湿润的KI-淀 粉试纸变蓝(Cl2)2Cl- = Cl2↑ + 2e-阴极阳极氯
气铜CuCl2溶液A极B极 A极: (阳极)失去电子,发生氧化反应 有红色物质析出Cu2+ +2e- = Cu 得到电子,发生还原反应 B极: (阴极)1、电解:使电流通过电解质溶液或熔融的电解质,而在阴阳两个电极分别发生氧化和还原反应的过程一、电解原理2、电解池定义:把电能转化为化学能的装置。组成:两个电极、电解质溶液或熔融电解质直流电源、电解氯化铜溶液微观模拟实验分析:电极阳极:与外电源正极相连的电极,失去电子,化合价升高,发生氧化反应。阴极:与外电源负极相连的电极,得到电子,化合价降低,发生还原反应。惰性电极:C、Pt、Au等,仅导电,不参与反应。活性电极:Fe、Cu、Ag等,既可以导电、又可以参与电极反应。电 解 池2、电极材料电 解 池2、电子流动方向:离子定向移动的方向:电子从外加电源的负极流出,流到电解池的阴极,再从阳极流回电源正极。 阳离子向阴极移动,
阴离子向阳极移动。电流流
动方向:电流从外加电源的正极流向负极思考:在电解CuCl2溶液时,只有Cu2+和 Cl-分别在阴阳极反应,为什么H+与OH-不在电极参加反应?放电:阴离子失去电子而阳离子得到电子的过程 ①活性材料作电极时(Fe、Cu 等):金属在阳极失电子被氧化 成阳离子进人溶液。
②用惰性电极(Pt、Au、石墨、钛等)时:溶液中阴离子的放电顺序(由难到易)是:S 2- > I - > Br - > Cl - > OH - > NO3->SO42-(等含氧酸根离子)>F-阳极:二、电解产物的确定 离子放电顺序Ag+ > Fe3+ > Cu2+ > Pb2+ > Sn2+ > Fe2+ > Zn2+ > H+ > Al3+ > Mg2+ > Na+ > Ca2+ > K+ 无论是惰性电极还是活性电极都不参与电极反应,发生反应的是溶液中的阳离子。
阳离子在阴极上放电顺序是:阴极:二、电解产物的确定 离子放电顺序思考:在电解CuCl2溶液时,只有Cu2+和 Cl-分别在阴阳极反应,为什么H+与OH-不在电极参加反应?想一想: 如下图:电解氯化铜溶液,电极反应情况又如何?阳极:Fe = Fe 2+ +2e-阴极:Cu2+ +2e- = Cu阳极阴极阳极为活性电极,则电极自身被氧化阳离子放电顺序:Cu2+> H+三、电极反应式、电解方程式的书写:例:写出用石墨做电极电解CuSO4溶液的电极反应式及总的电解方程式. 阴极:阳极:③最后使得失数相等,两极反应相加得总方程式阴极:阳极:4OH- -4e - =O2↑+2H2O2Cu2++4e - =2CuOH- > SO42-H+ < Cu2+①首先分析、比较出阴阳极的放电离子:②然后写电极反应式 :2Cu+O2↑+4H+或2CuSO4+2H2O
(电解反应的化学方程式)2Cu+O2↑+2H2SO42Cu2++2H2O(电解反应的离子方程式)完成下列溶液的电极反应(以石墨为电极电解)(1)NaOH溶液:
(2)盐酸溶液:知识反馈一阳极C阴极C氧气氢
气阳极: 4OH- → 2H2O+O2 ↑ + 4e-阴极: 4H ++ 4e- → 2H2 ↑变大变
大 加
H2O
NaOH溶液2H2O 2H2 ↑ + O2 ↑阳极:2Cl--2 e- =Cl2↑阴极:2H+ + 2e-=H2↓减小增大HCl
阳极C阴极C氯气氢
气盐酸溶液四、电解规律(惰性电极)小结 阳极:S2- > I- > Br- > Cl- > OH- > 含氧酸根 > F- 简单阴离子复杂阴离子阴极:Ag+>Fe3+>Cu2+ >Fe2+> Zn2+ > H+>Al3+>Mg2+>Na+ >K+活泼金属离子不活泼金属离子 电解质溶液用惰性电极电解的示例:含氧酸H2SO4强碱NaOH活泼金属的含氧酸盐Na2SO4无氧酸HCl阳极:4OH-→4e-=O2+2H2O
阴极:4H+ + 4e- = 2H2↑减小增大不变H2O阳极:2Cl- → 2e-=Cl2↑
阴极:2H++2e- = H2↑增大HCl不活泼金属的无氧酸盐CuCl2阳极:2Cl- → 2e- =Cl2↑
阴极:Cu2++2e- = Cu减少CuCl2活泼金属的无氧酸盐NaCl阳极:2Cl- → 2e- =Cl2↑
阴极:2H++2e- =H2↑增大HCl不活泼金属的含氧酸盐CuSO4阳极:4OH- → 4e- =O2↑+2H2O
阴极:2Cu2++4e- = 2Cu减小CuO完成下列溶液的电极反应(以石墨为电极电解)(1)Na2SO4溶液:
(2)NaCl溶液:
(3)CuSO4溶液:知识反馈二阳极C阴极C氧气氢
气阳极: 4OH- → 4e- + 2H2O+O2 ↑阴极: 4H ++ 4e- → 2H2 ↑变大不
变 加
H2O
Na2SO4溶液2H2O 2H2 ↑ + O2 ↑阳极C阴极C氯气氢
气阳极: 2Cl- → 2e- + Cl 2↑阴极: 2H ++ 2e- → H2 ↑2NaCl+2H2O 2NaOH+H2↑ + Cl2↑减小增
大 加
HCl
NaCl溶液阳极C阴极C氧
气铜阳极: 4OH- → 4e- + 2H2O+O2 ↑阴极:Cu2++ 2e- → Cu减小减小 加
CuOCuSO4溶液体验高考 (2004广东、广西) PH=a>的某电解质溶液中,插入两支惰性电极通直流电一段时间后,溶液的PH>a,则该电解质可能是( )
A.NaOH B.H2SO4
C.AgNO3 D.Na2SO4A(2)写出电极反应:A中:___B中:____ C中:___ D中:___ (1)标出电源的正、负极,X为 ______,Y为______.模拟训练:由电极产物判断电源电极A:4H++4e-=2H2↑B:4OH--4e-=2H2O+O2↑C:2H++2e-=H2↑D:2Cl-+2e-=Cl2↑如图装置中,E为一只盛有AlCl3溶液的烧杯,C为铂棒、D为铁棒,X与Y为电源的电极,A、B中插入多孔的惰性电极。切断开关K1,闭合开关K2,通直流电一端时间后,A、B中液面如图所示,请回答 :正极负极阴极阳极阴极阳极作 业:在如下的装置中进行电解,并已知铁极的质量减小11.2克。
(1)A是电源的 极
(2)电解过程中,电路中通过 摩电子
(3)Ag极的电极反应是 ;析出物质是 克
(4)Cu(a)的电极反应是 ;
(5)Cu(b)的电极反应是 。再见再见
