把握命题方向__提高复习效度
图片预览








文档简介
课件55张PPT。江苏省栟茶高级中学 丛 高 把握命题方向 提高复习效度
——谈新高考模式下的高三化学复习 把握命题方向 提高复习效度
——谈新高考模式下的高三化学复习 一、08江苏高考试题特点分析
二、科学应对新高考 提高化学匹配率一、08江苏高考试题特点分析1、突显新课程这一主题(1)充分体现“新课改”理念(2)着力反映“课程标准教学要求”(3)较好地遵循“考试说明”2、 “四基”为主,凸显“素养和能力要求”3、注重模块融合反映了“课程标准”的三个基本特征 试题的设计注意了课程的三维目标等多方面要求;
试题也符合课程内容标准,即注重高三学生水平、化学科知识和社会发展三方面内容的整合;
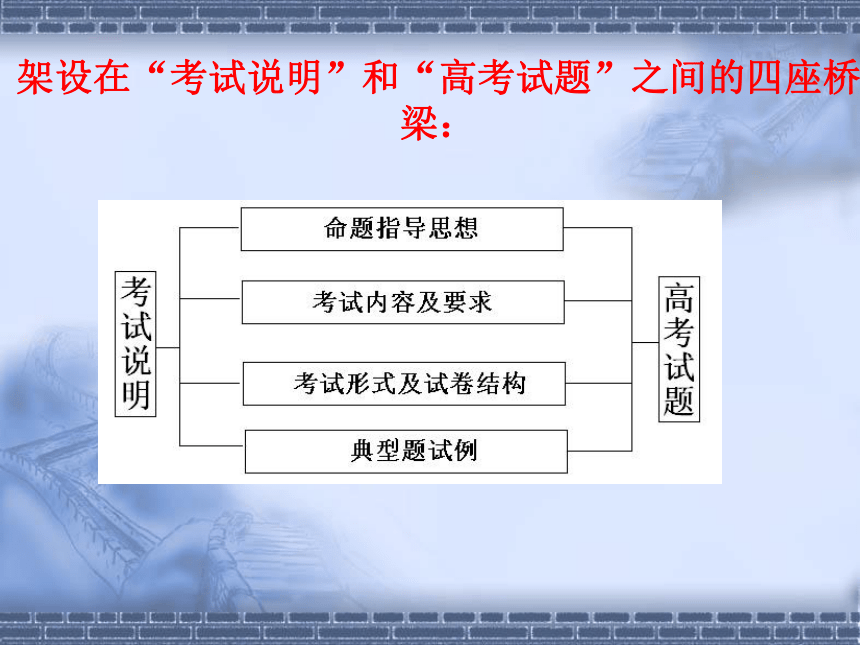
试题的设计也符合课程要求,即通过结合具体知识点,突显化学科的特点,达到从化学视角分析和解决问题的能力等一系列过程性、体验性目标。 架设在“考试说明”和“高考试题”之间的四座桥梁: “吻合度”
“难易度”
“新颖度”
“区分度”
“影响度” 由定性到定量的思想——精细化
结构决定性质,性质反映结构的思想——因果化
抽象问题具体化的思想——直观化
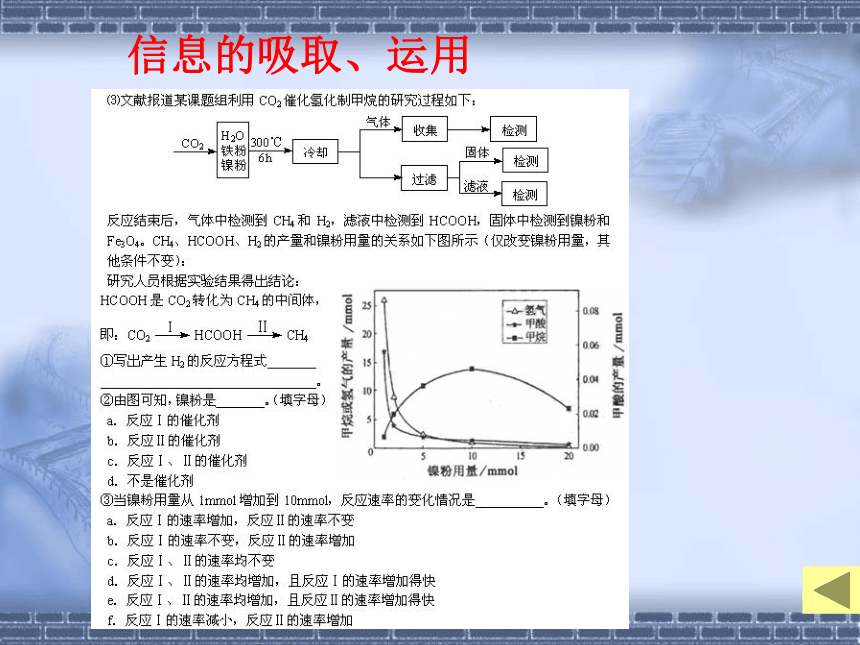
密切联系生产生活的思想——实用化部分体现化学学科思想方法的试题列举信息的吸取、运用08江苏卷模块融合考查分析表 1、关于“变与不变”的思考 理念、方案在变,考试标准没有变。 载体、情境在变,考查的知识点没有变。 二、科学应对新高考 提高化学匹配率《课程标准教学要求》对高考命题具有决定性影响
《考试说明》在高考命题中的作用也有着不可替代的地位
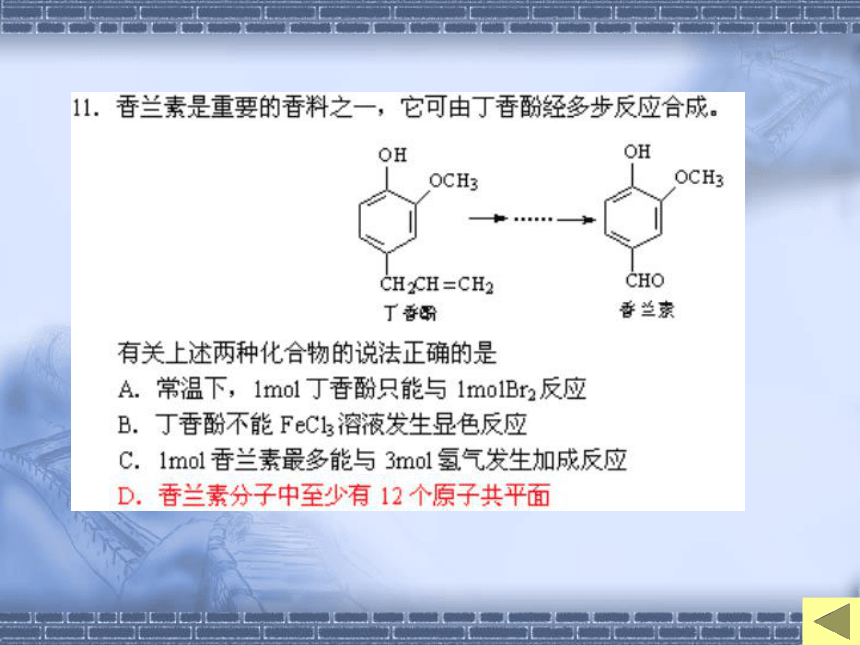
教材与高考的关系 “结构决定性质,性质反映结构”
考查观察能力和运用有机官能团知识解决问题的能力 例2610415“科学性、
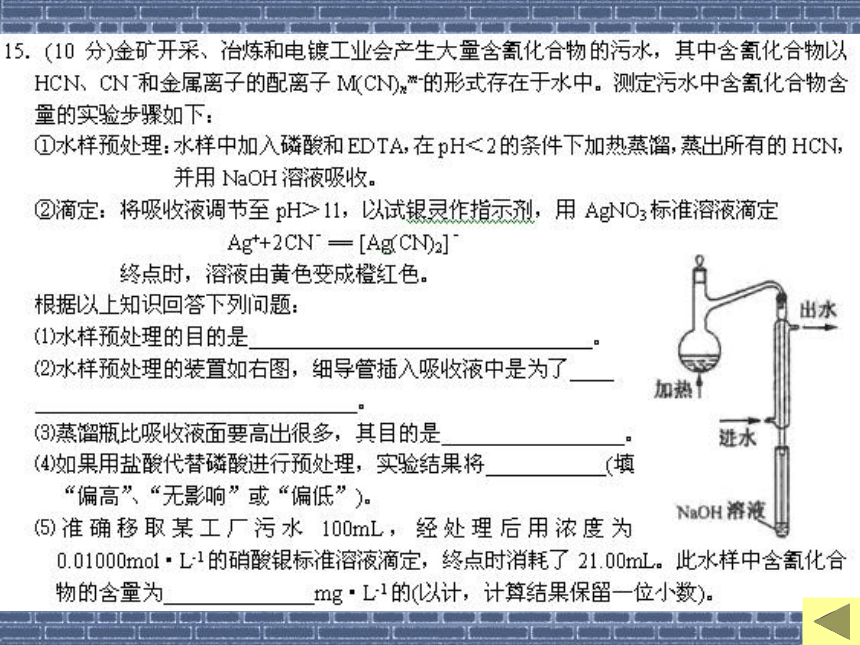
可行性、
简约性、
安全性 ”
能运用观察、实验、阅读资料等多种手段收集证据,能运用比较、分类、归纳、概括等方法形成探究结论 1、关于“变与不变”的思考 二、科学应对新高考 提高化学匹配率2、强化复习“过程意识” (1)呈现知识的梳理、延伸等归纳过程(2)呈现问题解决的分析、推理、反思等演绎过程1、关于“变与不变”的思考 二、科学应对新高考 提高化学匹配率2、强化复习“过程意识” 3、实施精细化教学管理 经典试题 情景试题 示例样题问题情景化 问题探究化 在盛有水的电解槽中加入等物质的量的Ag+、Pb2+、Na+、NO3—、SO42—、Cl—,混合后用惰性电极电解,片刻后,所得氧化产物与还原产物的质量比为
A.8:1 B.35.5:108
C.16:207 D.108:35.5原子结构分子构型晶体结构和性质(08南通二模)A【物质结构与性质】纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域。⑴A和B的单质单位质量的燃烧热大,可用作燃料。已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:①某同学根据上述信息,推断B的核外电子排布如右图所示,该同学所画的电子排布图违背了 。
②根据价层电子对互斥理论,预测A和氯元素形成的简单分子空间构型为 。能量最低原理直线型原子结构分子构型①已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145~140pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确并阐述理由 。
②科学家把C60和K掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示,该物质在低温时是一种超导体。该物质的K原子和C60分子的个数比为 。
③继C60后,科学家又合成了Si60、N60,C、Si、N原子电负性由大到小的顺序是 。Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则Si60分子中π键的数目为 。⑵氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料。不正确 C60是分子晶体,熔化时不需破坏化学键3∶1N、C、Si30晶体结构均摊法电负性 短周期元素X、Y形成的化合物中,X、Y的原子个数比为1∶3,当Y的原子序数为m时,X的原子序数为 ① m-4 ②m+4
③m+8 ④m-2 ⑤m+6 ⑥m+5
A.①②③ B.①②③④
C.①②③④⑤ D.①②③④⑤⑥ 讲评原则 时效性原则 主体性原则 拓展性原则 将铝粉与某铁的氧化物FeO·2Fe2O3粉末配制成铝热剂,分成两等份。一份直接放入足量的烧碱溶液中,充分反应后放出气体在标准状况下的体积为15.68L;另一份在高温下恰好反应完全,反应后的混合物与足量的盐酸反应后,放出的气体在标准状况下的体积为
A.11.20L B.15.68L
C.22.40L D.31.36L 若原子核外电子排布的基本规律为最外层电子数不超过5个,次外层电子数不超过10个,倒数第三层电子数不超过15个,而各电子层电子的最大容量仍为2n2,则元素周期表中第三、四、五周期含有的元素分别有( )
A.5种、10种、15种 B.8种、18种、18种
C.8种、10种、15种 D.9种、10种、15种
13962775068
cgbz@163.com
谢谢必修与选修模块间的逻辑递进关系 从得氧和失氧看氧化还原反应 从化合价升降看氧化还原反应 从电子的得失看氧化还原反应 从电化学(原电池、电解池)
看氧化还原反应 从加氢和去氢看有机反应
中的氧化还原反应 ↑↑↑↑知 识能 力试题情境事实性知识原理性知识方法性知识常规叙述新物质、新提问方式新化学反应、实验情境新图表、数据复述、辨认、识图辨析、比较、找特征迁移、分析、评价推理运用、新旧融合 化学用语、NA、氧化还原反应、电化学基础、化学实验基础知识、化学实验装置分析、元素周期律知识应用、离子共存、离子方程式判断、离子浓度关系、化学反应速率和平衡、常见元素的单质及化合物性质、有机结构和性质的分析、化学与STSE等 高考Ⅰ卷经典考点
——谈新高考模式下的高三化学复习 把握命题方向 提高复习效度
——谈新高考模式下的高三化学复习 一、08江苏高考试题特点分析
二、科学应对新高考 提高化学匹配率一、08江苏高考试题特点分析1、突显新课程这一主题(1)充分体现“新课改”理念(2)着力反映“课程标准教学要求”(3)较好地遵循“考试说明”2、 “四基”为主,凸显“素养和能力要求”3、注重模块融合反映了“课程标准”的三个基本特征 试题的设计注意了课程的三维目标等多方面要求;
试题也符合课程内容标准,即注重高三学生水平、化学科知识和社会发展三方面内容的整合;
试题的设计也符合课程要求,即通过结合具体知识点,突显化学科的特点,达到从化学视角分析和解决问题的能力等一系列过程性、体验性目标。 架设在“考试说明”和“高考试题”之间的四座桥梁: “吻合度”
“难易度”
“新颖度”
“区分度”
“影响度” 由定性到定量的思想——精细化
结构决定性质,性质反映结构的思想——因果化
抽象问题具体化的思想——直观化
密切联系生产生活的思想——实用化部分体现化学学科思想方法的试题列举信息的吸取、运用08江苏卷模块融合考查分析表 1、关于“变与不变”的思考 理念、方案在变,考试标准没有变。 载体、情境在变,考查的知识点没有变。 二、科学应对新高考 提高化学匹配率《课程标准教学要求》对高考命题具有决定性影响
《考试说明》在高考命题中的作用也有着不可替代的地位
教材与高考的关系 “结构决定性质,性质反映结构”
考查观察能力和运用有机官能团知识解决问题的能力 例2610415“科学性、
可行性、
简约性、
安全性 ”
能运用观察、实验、阅读资料等多种手段收集证据,能运用比较、分类、归纳、概括等方法形成探究结论 1、关于“变与不变”的思考 二、科学应对新高考 提高化学匹配率2、强化复习“过程意识” (1)呈现知识的梳理、延伸等归纳过程(2)呈现问题解决的分析、推理、反思等演绎过程1、关于“变与不变”的思考 二、科学应对新高考 提高化学匹配率2、强化复习“过程意识” 3、实施精细化教学管理 经典试题 情景试题 示例样题问题情景化 问题探究化 在盛有水的电解槽中加入等物质的量的Ag+、Pb2+、Na+、NO3—、SO42—、Cl—,混合后用惰性电极电解,片刻后,所得氧化产物与还原产物的质量比为
A.8:1 B.35.5:108
C.16:207 D.108:35.5原子结构分子构型晶体结构和性质(08南通二模)A【物质结构与性质】纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域。⑴A和B的单质单位质量的燃烧热大,可用作燃料。已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:①某同学根据上述信息,推断B的核外电子排布如右图所示,该同学所画的电子排布图违背了 。
②根据价层电子对互斥理论,预测A和氯元素形成的简单分子空间构型为 。能量最低原理直线型原子结构分子构型①已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145~140pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确并阐述理由 。
②科学家把C60和K掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示,该物质在低温时是一种超导体。该物质的K原子和C60分子的个数比为 。
③继C60后,科学家又合成了Si60、N60,C、Si、N原子电负性由大到小的顺序是 。Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则Si60分子中π键的数目为 。⑵氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料。不正确 C60是分子晶体,熔化时不需破坏化学键3∶1N、C、Si30晶体结构均摊法电负性 短周期元素X、Y形成的化合物中,X、Y的原子个数比为1∶3,当Y的原子序数为m时,X的原子序数为 ① m-4 ②m+4
③m+8 ④m-2 ⑤m+6 ⑥m+5
A.①②③ B.①②③④
C.①②③④⑤ D.①②③④⑤⑥ 讲评原则 时效性原则 主体性原则 拓展性原则 将铝粉与某铁的氧化物FeO·2Fe2O3粉末配制成铝热剂,分成两等份。一份直接放入足量的烧碱溶液中,充分反应后放出气体在标准状况下的体积为15.68L;另一份在高温下恰好反应完全,反应后的混合物与足量的盐酸反应后,放出的气体在标准状况下的体积为
A.11.20L B.15.68L
C.22.40L D.31.36L 若原子核外电子排布的基本规律为最外层电子数不超过5个,次外层电子数不超过10个,倒数第三层电子数不超过15个,而各电子层电子的最大容量仍为2n2,则元素周期表中第三、四、五周期含有的元素分别有( )
A.5种、10种、15种 B.8种、18种、18种
C.8种、10种、15种 D.9种、10种、15种
13962775068
cgbz@163.com
谢谢必修与选修模块间的逻辑递进关系 从得氧和失氧看氧化还原反应 从化合价升降看氧化还原反应 从电子的得失看氧化还原反应 从电化学(原电池、电解池)
看氧化还原反应 从加氢和去氢看有机反应
中的氧化还原反应 ↑↑↑↑知 识能 力试题情境事实性知识原理性知识方法性知识常规叙述新物质、新提问方式新化学反应、实验情境新图表、数据复述、辨认、识图辨析、比较、找特征迁移、分析、评价推理运用、新旧融合 化学用语、NA、氧化还原反应、电化学基础、化学实验基础知识、化学实验装置分析、元素周期律知识应用、离子共存、离子方程式判断、离子浓度关系、化学反应速率和平衡、常见元素的单质及化合物性质、有机结构和性质的分析、化学与STSE等 高考Ⅰ卷经典考点
同课章节目录
