硫酸的工业制法
图片预览



文档简介
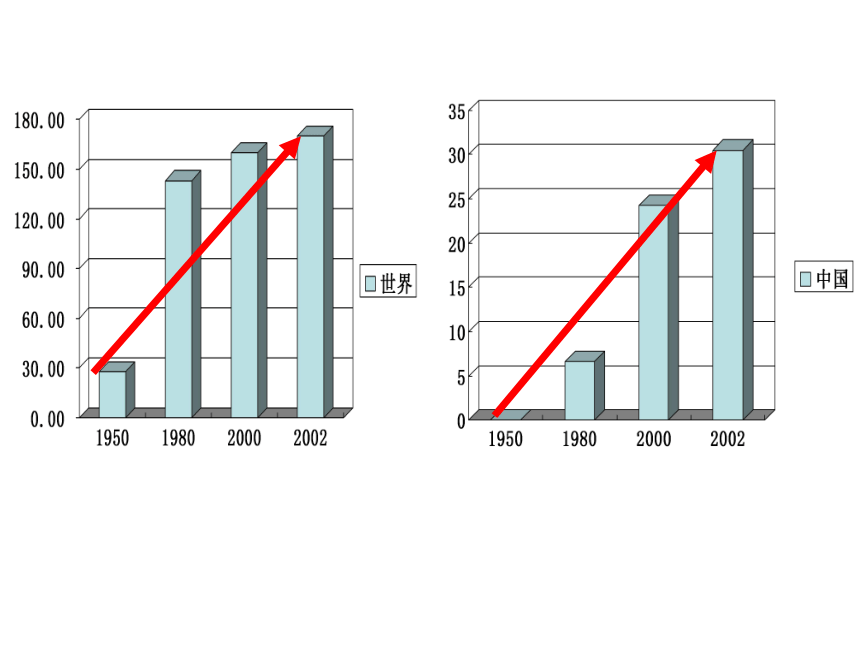
课件21张PPT。接触法制硫酸硫酸工业硫酸的消费量常被视为一个国家工业发达的水平的一种标志。【 探究】
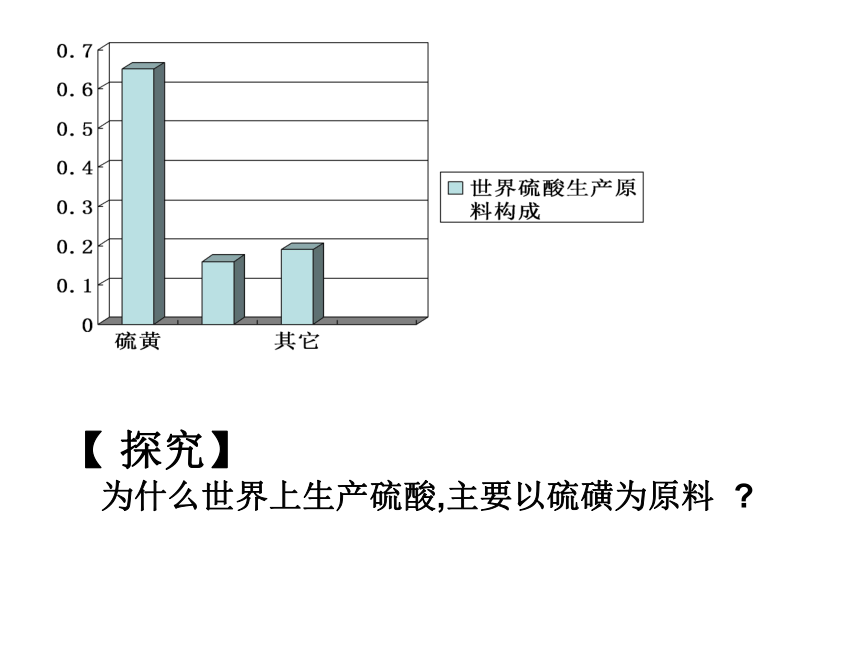
为什么世界上生产硫酸,主要以硫磺为原料 ? 【探究】
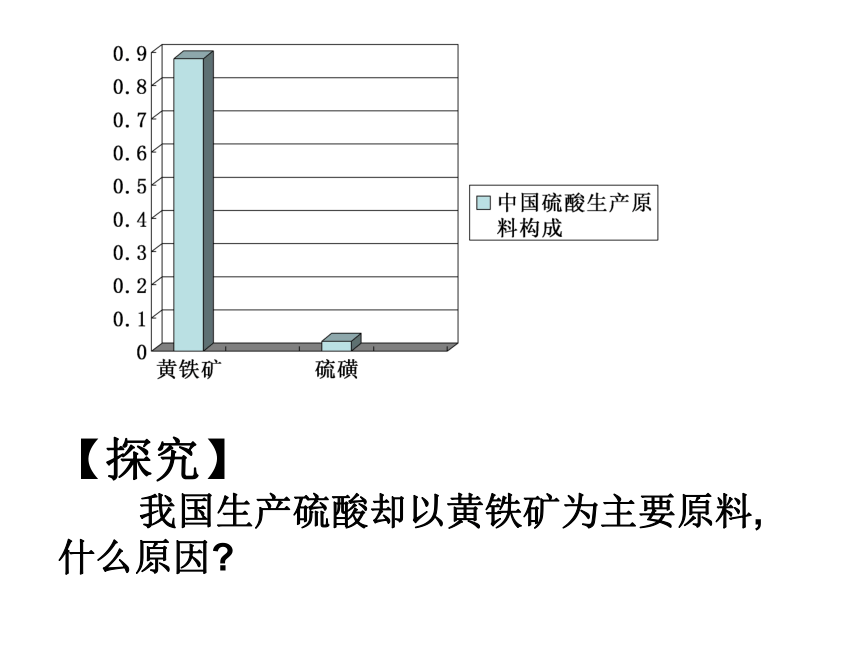
我国生产硫酸却以黄铁矿为主要原料,
什么原因? 一、反应原理 4FeS2 +11 O2 2Fe2O3 + 8SO2
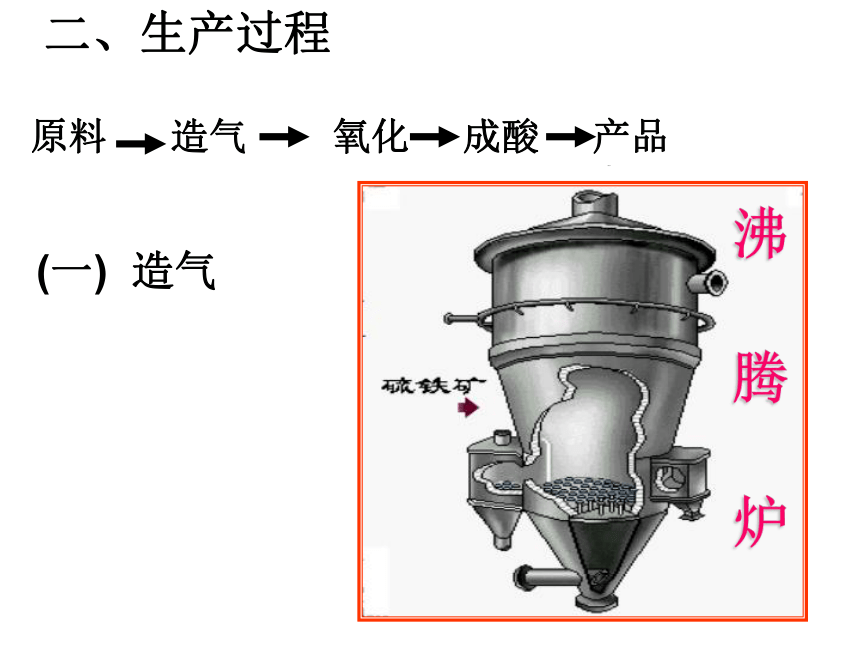
高 温第一步:第二步:第三步:以上反应均为放热反应 接触法制硫酸(一) 造气沸腾炉沸 腾 炉(一) 造气1、本阶段反应设备?
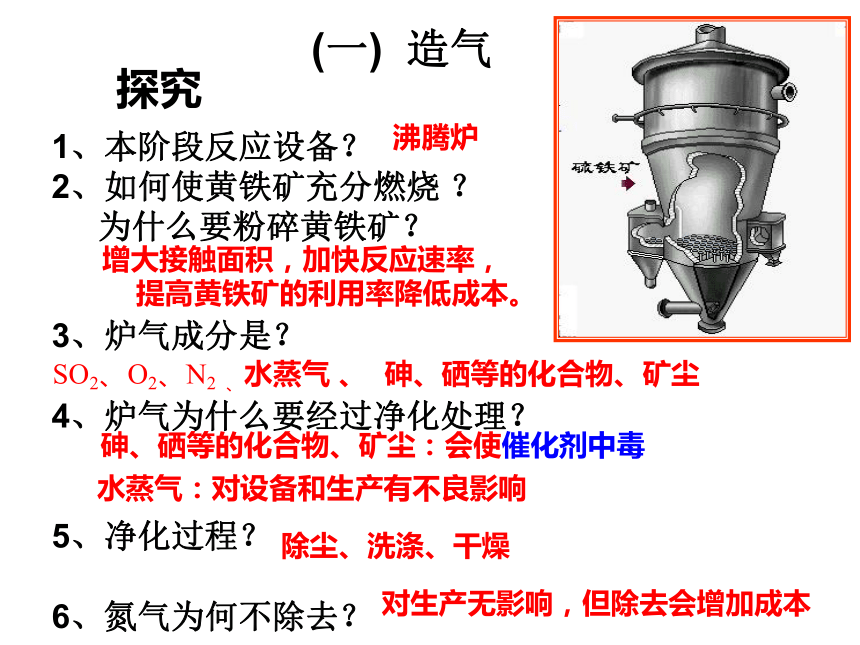
2、如何使黄铁矿充分燃烧 ?
为什么要粉碎黄铁矿?
3、炉气成分是?
4、炉气为什么要经过净化处理?
5、净化过程?
6、氮气为何不除去?
SO2、O2、N2 、水蒸气 、 砷、硒等的化合物、矿尘砷、硒等的化合物、矿尘:会使催化剂中毒水蒸气:对设备和生产有不良影响除尘、洗涤、干燥对生产无影响,但除去会增加成本沸腾炉增大接触面积,加快反应速率,
提高黄铁矿的利用率降低成本。探究(二)so2接触氧化 (2)根据平衡移动原理,反应在较高还 是较低的温度下进行更有利? (1)2SO2(g)+O2(g) 2SO3(g);
△H=-196.6kJ/mol
该反应的特点是什么? 催化剂(3)根据平衡移动原理,反应在较高
还是较低的压强下进行更有利? ①可逆反应 ②放热反应
③正反应体积缩小 ④反应需要催化剂较低的温度下较高的压强下 1、反应特点: ①可逆反应 ②放热反应
③正反应体积缩小 ④反应需要催化剂实际应用中:400-500℃ 常压 催化剂探究:
进入接触室的二氧化硫需要预热,二氧化硫催
化氧化生成三氧化硫需要放热而环境温度太高不利于
三氧化硫的生成;怎样充分利用这部分热量? (二)so2接触氧化硫酸工业生产流程动画沸 腾 炉接 触 室净化冷 却3、接触室(三)so3的吸收硫酸工业生产流程动画吸 收 塔冷 却探究
1、吸收SO3不用水和稀硫酸
而用98.3%的浓硫酸?
2、浓硫酸从塔顶喷下来,
并且在吸收塔内叠放许
多瓷环的原因?
3、从塔顶从塔顶到出的气体
能否直接排入空气中?
防止酸雾的形成,有利于三氧化硫的吸收利用逆流使其充分接触,吸收更完全气体中含有二氧化硫会污染环境,
必须回收处理硫酸工业生产流程动画 硫酸的工业生产沸 腾 炉接 触 室吸 收 塔净化冷 却小结:课堂习题反馈:
书本68页课后习题一[投影]练习题1:燃烧1吨含二硫化亚铁90%的黄铁矿,
在理论上能生产多吨98%的硫酸(设有1.5%的硫留
在炉渣里)?[试题分析]本题考查化学运算技能,
同学们常用的方法是分步计算法,根据方程式先
求出二氧化亚铁的质量,再求二氧化硫和三氧化硫
的质量,最后求出硫酸的质量,但这种方法要求的
量太多、太麻烦,题目中只要求求出硫酸的质量,
因此可以直接找到起始物质与最终产物硫酸的关系
式求解。
解析:由工业生产硫酸的反应方程式可得下列关系式:
设:能生成98%的硫酸x吨
FeS2 → 2SO2 → 2SO3 → 2H2SO4
120 2×98
1t×90%×(1-1.5%) xt×98%
、2、现有1 L含SO3为30%的发烟硫酸(密度为1.95g/cm3),要把它稀释成浓度为95%的浓硫酸,要加水约为 ( )
A.120 mL B.180 mL
C.240 mL D.300 mL1L含SO3为30%的发烟硫酸中含SO3为1000cm3×1.95g/cm3×30%=585g,
与SO3反应所需水量为585g/80g/mol×18g/mol=131.625g,则H2SO4为:
1000cm3×1.95g/cm3+131.625g=2081.625g 95% H2SO4溶液中溶剂为:95×5=110 g
2081.625 g所以,总共需加水为:
131.625 g+110 g=241.625 g
课后作业:
一、完成优化设计
巩固类习题。
二、调查我们周
围的环境污
染状况
为什么世界上生产硫酸,主要以硫磺为原料 ? 【探究】
我国生产硫酸却以黄铁矿为主要原料,
什么原因? 一、反应原理 4FeS2 +11 O2 2Fe2O3 + 8SO2
高 温第一步:第二步:第三步:以上反应均为放热反应 接触法制硫酸(一) 造气沸腾炉沸 腾 炉(一) 造气1、本阶段反应设备?
2、如何使黄铁矿充分燃烧 ?
为什么要粉碎黄铁矿?
3、炉气成分是?
4、炉气为什么要经过净化处理?
5、净化过程?
6、氮气为何不除去?
SO2、O2、N2 、水蒸气 、 砷、硒等的化合物、矿尘砷、硒等的化合物、矿尘:会使催化剂中毒水蒸气:对设备和生产有不良影响除尘、洗涤、干燥对生产无影响,但除去会增加成本沸腾炉增大接触面积,加快反应速率,
提高黄铁矿的利用率降低成本。探究(二)so2接触氧化 (2)根据平衡移动原理,反应在较高还 是较低的温度下进行更有利? (1)2SO2(g)+O2(g) 2SO3(g);
△H=-196.6kJ/mol
该反应的特点是什么? 催化剂(3)根据平衡移动原理,反应在较高
还是较低的压强下进行更有利? ①可逆反应 ②放热反应
③正反应体积缩小 ④反应需要催化剂较低的温度下较高的压强下 1、反应特点: ①可逆反应 ②放热反应
③正反应体积缩小 ④反应需要催化剂实际应用中:400-500℃ 常压 催化剂探究:
进入接触室的二氧化硫需要预热,二氧化硫催
化氧化生成三氧化硫需要放热而环境温度太高不利于
三氧化硫的生成;怎样充分利用这部分热量? (二)so2接触氧化硫酸工业生产流程动画沸 腾 炉接 触 室净化冷 却3、接触室(三)so3的吸收硫酸工业生产流程动画吸 收 塔冷 却探究
1、吸收SO3不用水和稀硫酸
而用98.3%的浓硫酸?
2、浓硫酸从塔顶喷下来,
并且在吸收塔内叠放许
多瓷环的原因?
3、从塔顶从塔顶到出的气体
能否直接排入空气中?
防止酸雾的形成,有利于三氧化硫的吸收利用逆流使其充分接触,吸收更完全气体中含有二氧化硫会污染环境,
必须回收处理硫酸工业生产流程动画 硫酸的工业生产沸 腾 炉接 触 室吸 收 塔净化冷 却小结:课堂习题反馈:
书本68页课后习题一[投影]练习题1:燃烧1吨含二硫化亚铁90%的黄铁矿,
在理论上能生产多吨98%的硫酸(设有1.5%的硫留
在炉渣里)?[试题分析]本题考查化学运算技能,
同学们常用的方法是分步计算法,根据方程式先
求出二氧化亚铁的质量,再求二氧化硫和三氧化硫
的质量,最后求出硫酸的质量,但这种方法要求的
量太多、太麻烦,题目中只要求求出硫酸的质量,
因此可以直接找到起始物质与最终产物硫酸的关系
式求解。
解析:由工业生产硫酸的反应方程式可得下列关系式:
设:能生成98%的硫酸x吨
FeS2 → 2SO2 → 2SO3 → 2H2SO4
120 2×98
1t×90%×(1-1.5%) xt×98%
、2、现有1 L含SO3为30%的发烟硫酸(密度为1.95g/cm3),要把它稀释成浓度为95%的浓硫酸,要加水约为 ( )
A.120 mL B.180 mL
C.240 mL D.300 mL1L含SO3为30%的发烟硫酸中含SO3为1000cm3×1.95g/cm3×30%=585g,
与SO3反应所需水量为585g/80g/mol×18g/mol=131.625g,则H2SO4为:
1000cm3×1.95g/cm3+131.625g=2081.625g 95% H2SO4溶液中溶剂为:95×5=110 g
2081.625 g所以,总共需加水为:
131.625 g+110 g=241.625 g
课后作业:
一、完成优化设计
巩固类习题。
二、调查我们周
围的环境污
染状况
