电化学复习
图片预览







文档简介
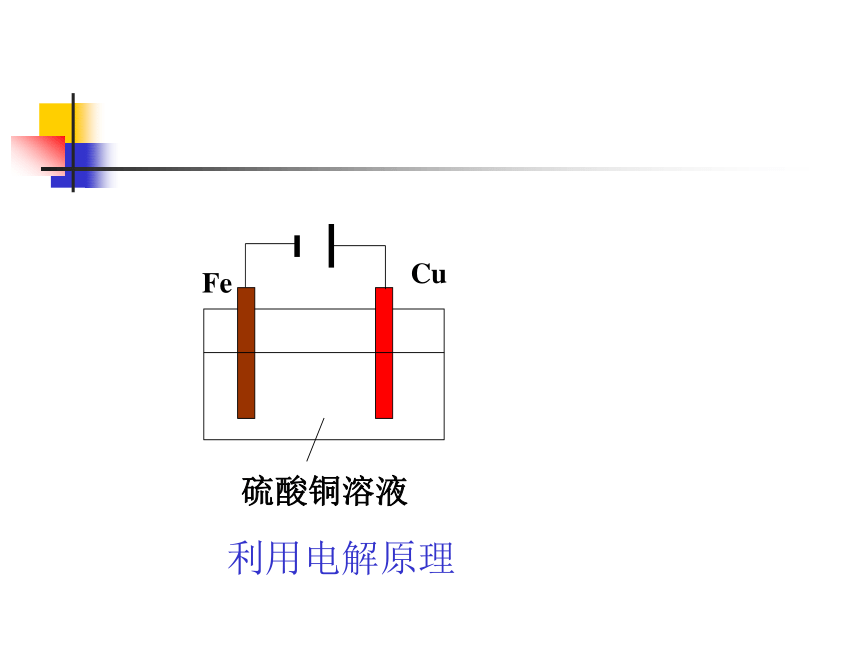
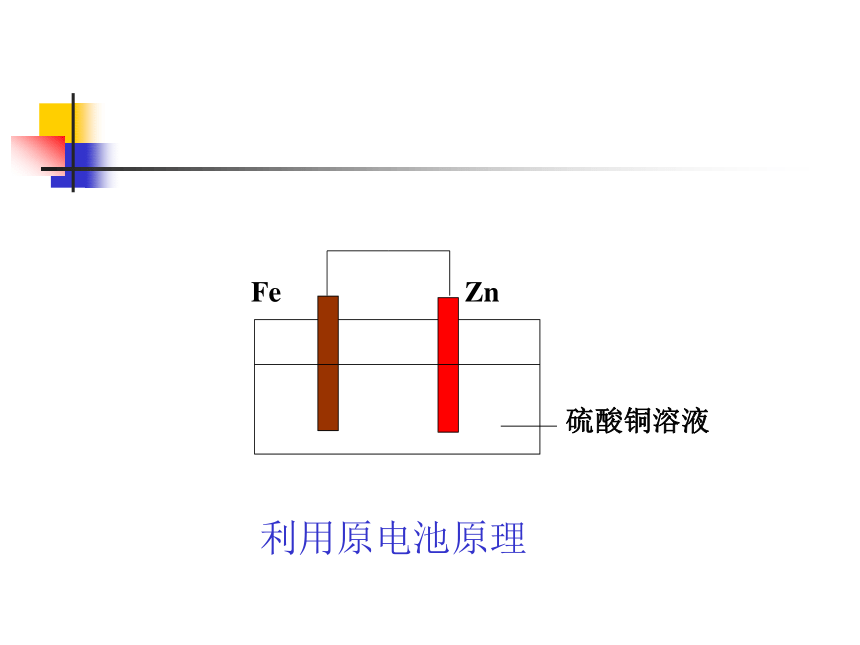
课件28张PPT。电化学实验德清一中 高金松如图把铁棒放入硫酸铜溶液中有何现象 ?回忆: 如何使图中的铁棒上析出铜,而铁的质量不变?问题讨论:利用电解原理利用原电池原理请同学写出电极反应式电化学中的实验1。预备知识回忆。原电池电极反应:负极:氧化反应,金属失电 子
正极:还原反应,溶液中的阳离子得电子或氧气得电子 电解池电极反应:阳极:氧化反应,溶液中的阴离子或电极金属失电子
阴极:还原反应,溶液中的阳离子得电子 放电顺序: ⑴阳极:
(活泼电极)> S2 — >I — >Br — >Cl — >OH — >含氧酸根>F —
⑵阴极:Ag+ > Fe3+ > Cu2+ > H+原电池中电子流向: 由负极沿导线流向正极 原电池中转移电子数 = 阳极失电子数
= 阴极得电子数G例:某学生试图用电解法来验证阿伏加德罗常数,实验装置图如下:思考:验证NA的原理是什么?G通过电量Q3Q = I t = n NA e思考:根据此原理,本实验
中需测哪些数据?方案一:I 、 t 、 m (铜)方案二:I 、 t 、 V (氯气)分析两种方案的合理性?问题透析Q = I t = n NA e推出NA的计算公式?NA = 32 I t / m e 思考: I 、 t 、m 如何测得?问题透析铜的质量的测得:用蒸馏水冲洗电极
低温烘干
烘干至恒重假设 I 和 t 测量正确,但某同
学求出NA比理论值要小,请帮
该同学分析可能的原因?NA = 32 I t / m e 问题透析该装置中的电源为铅蓄电池,实
验后称得铜质量为64克,求消耗
的硫酸的物质的量提示:原电池中转移电子数= 阴极得电子数铅蓄电池使用日久后,正
负极标志模糊,用现存材
料如何来判断正负极?问题透析1.电解法:将碳棒上的铜线分别与蓄电池两极相连,然后将碳棒插入氯化铜溶液中,经一段时间后碳棒上有红色物质析出的所连电极为负极。
2.用电流表整个实验有什么不足之处?应如何加以改进 ?问题透析思考: 用铁棒、碳棒,硫酸钠溶液,电源等为材料,设计一个实验制取氢氧化亚铁白色沉淀。画出装置图。铁棒碳棒小结:1。电化学知识回忆。2。例题分析同学们,再见
正极:还原反应,溶液中的阳离子得电子或氧气得电子 电解池电极反应:阳极:氧化反应,溶液中的阴离子或电极金属失电子
阴极:还原反应,溶液中的阳离子得电子 放电顺序: ⑴阳极:
(活泼电极)> S2 — >I — >Br — >Cl — >OH — >含氧酸根>F —
⑵阴极:Ag+ > Fe3+ > Cu2+ > H+原电池中电子流向: 由负极沿导线流向正极 原电池中转移电子数 = 阳极失电子数
= 阴极得电子数G例:某学生试图用电解法来验证阿伏加德罗常数,实验装置图如下:思考:验证NA的原理是什么?G通过电量Q3Q = I t = n NA e思考:根据此原理,本实验
中需测哪些数据?方案一:I 、 t 、 m (铜)方案二:I 、 t 、 V (氯气)分析两种方案的合理性?问题透析Q = I t = n NA e推出NA的计算公式?NA = 32 I t / m e 思考: I 、 t 、m 如何测得?问题透析铜的质量的测得:用蒸馏水冲洗电极
低温烘干
烘干至恒重假设 I 和 t 测量正确,但某同
学求出NA比理论值要小,请帮
该同学分析可能的原因?NA = 32 I t / m e 问题透析该装置中的电源为铅蓄电池,实
验后称得铜质量为64克,求消耗
的硫酸的物质的量提示:原电池中转移电子数= 阴极得电子数铅蓄电池使用日久后,正
负极标志模糊,用现存材
料如何来判断正负极?问题透析1.电解法:将碳棒上的铜线分别与蓄电池两极相连,然后将碳棒插入氯化铜溶液中,经一段时间后碳棒上有红色物质析出的所连电极为负极。
2.用电流表整个实验有什么不足之处?应如何加以改进 ?问题透析思考: 用铁棒、碳棒,硫酸钠溶液,电源等为材料,设计一个实验制取氢氧化亚铁白色沉淀。画出装置图。铁棒碳棒小结:1。电化学知识回忆。2。例题分析同学们,再见
