08年高考试题分析和09年复习备考建议(有机化学)
文档属性
| 名称 | 08年高考试题分析和09年复习备考建议(有机化学) |  | |
| 格式 | rar | ||
| 文件大小 | 679.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2009-01-28 11:59:00 | ||
图片预览



文档简介
本资料来自于资源最齐全的21世纪教育网www.21cnjy.com
08年高考试题分析和09年复习备考建议(有机化学)
温州中学 赵彦海
一、08年有机考查的内容
对比浙江省用的全国卷Ⅰ和全国卷Ⅱ以及使用新教材的山东和宁夏四份试卷
试卷类别 总分化学分 有机题序、分值、内容 占化学比例 说明
全国卷Ⅰ 300108 8题(6分,同分异构体:根据有机物名称写出结构简式的能力)29题(16分,有机综合:以醇、酚、芳香酸等物质为依托,框图形式体现,考查结构简式、分子式、化学方程式的书写,官能团的名称或书写)共22分 22/108=20.4% 理科综合试卷
全国卷Ⅱ 300108 6题(6分,烷烃:考查分子结构、取代反应、熔沸点、石油化工)29题(17分,有机综合:以烯烃、醛、酸、醇等物质为依托,框图形式体现,考查结构简式、化学方程式的书写和反应类型)共23分 23/108=21.3%
山东卷(新课程) 24078 9题(3分,两个选项是有机,高分子材料及白色污染)10题(1.5分,一个选项是有机,化学史)12题(4分,考查石油化工、乙醇、乙酸及碳的成键特点)33题(8分,官能团性质、反应类型、结构简式和化学方程式)29题(以有机物为依托,但考查的是化学能量问题)共16.5分 16.5/78=21.2%
宁夏卷(新课程) 300100 8题(6分,分子结构:有机物分子共面问题)9题(6分,乙醇与乙酸的物理性质和化学性质)36题(15分,有机综合:燃烧法求分子式、结构简式、化学方程式、反应类型、官能团的名称、光谱的性质)共27分 27/100=27%
二、试题分析与反思
(一)试题分析
1.从试题的结构和考查的内容看:有机试题的题型,比例和分值都相对比较稳定,综观前几年和今年的几份试卷,都有一个有机推断题和一道有机选择题,山东卷与宁夏卷在选择题上稍有差异,所占分值占整个化学试题的20%左右,宁夏试卷有机比例稍大。考查内容主要涉及到有机物分子式、结构简式、化学方程式的书写;典型官能团的结构和性质判断;同分异构体的判断及书写;有机反应类型的判断,几乎涵盖了所有有机化学内容,推断题大多都以醇、醛、羧酸、酯等主要有机物为依托,选择题考查知识点的随机性较大,课本上的任何一处都可能成为考试的“热点”。
2.从试题考查的要求看:知识以理解层次居多,物质间相互联系是重点。试题特别强调能力和素质的考查,注重考查考生对基础知识的理解能力以及运用这些基础知识分析、解决问题的能力,体现了学以致用、理论联系实际的思想。如上述几份试卷通过对醇、醛、酸、酚等物质性质的理解,考查反应类型、结构简式与化学方程式的书写等,都体现了这个特点。命题者的意图就是想通过考生对有机物结构式的确定以及同分异构体、化学方程式的书写,来考查考生运用有机化学基础知识分析问题和解决问题的能力。
3.从命题的着眼点看:无论是结构简式、化学方程式的书写,还是有机反应类型的判断,高考试题的根都根植于教材之中。虽然高考的题目常考常新,但万变不离其宗。在教学中要做好“用教材教”、“用考纲指导方向”,决不能抛开教材和考纲,凭自己所谓的老经验盲目指导,在考纲没明确时,应该认真研究省学科指导意见。尤其今年第一界新课程高考,命题形式还不十分明确,更应该加强研究、合作交流,并多听取省市的精神,及时调整自己复习的方向,反对闭门造车。
4.从学生的答题情况看,常见的主要错误有:
①审题不仔细,没按题目要求准确作答;
②结构简式的书写不规范:a.多写或少写H原子;b.官能团之间的连接线没有对准所连接的原子或连接的原子不正确;c.书写方程式时丢产物(如水等小分子),忘了配平或注明反应条件等;
③对一些复杂有机物结构或同分异构体的书写等,很难完整写出。
5.对全国卷Ⅰ29题的商讨:
中学化学谈到苯酚与浓溴水的反应时,仅谈生成邻对位的产物,甚至大学有机化学也是不谈间位的产物,29题(1)谈到“C与溴水反应生成的一溴代物只有两种”,如果按照教材介绍的“不考虑间位产物之意”则C是邻位甲基苯酚;如果不管实际有无这样的产物,只要位置许可就算一种,则C是对位甲基苯酚。答案中给的是对位甲基苯酚,说明出题者考虑的是不论有无间位产物均可,这样出题无可厚非,但需要说明,否则会使学生无从入手,造成困惑,尤其对考虑问题比较全面的同学更不公平。
(二)试题分析的反思
通过对几份试卷和几年来有机试题的分析,对今后的教学有这样几点不成熟的思考:
1.一个“坚持”:有机复习始终坚持中学化学的基础知识,不论高考怎么出题,复习时一定要针对中学教材的基本有机物、基本反应等知识反复训练,不搞偏题、怪题,这是以不变应万变的唯一途径。
2.二个“不要”:对于教师不要仅凭自己的老经验指导学生,要躬身学习、交流讨论,这样才能吃透新课程,较好地指导学生;不要完全相信学生所谓的“听懂了”,很多问题要让学生动笔写出才算掌握。
3.三个“研究”:研究教材和考纲,准确把握知识的广度和深度;研究考题,分析试卷结构、试题的出题形式和变化趋势;研究学生,根据学生对知识的掌握情况合理分配复习时间和讲授的侧重点。
4.四个“必须”:必须在全面复习的基础上重点突破,不能有投机心理;必须在知识点熟练和理解的基础上加强应用,不能一步过难;必须强化学生规范书写的落实,不要怕浪费时间;必须教师精选习题让学生来完成,不能填鸭式的将一本厚厚的资料从头做到尾。
三、课时分配与复习备考建议
(一)复习备考建议
1.复习安排:大体分两阶段。第一阶段基础巩固;第二阶段综合提高。
2.复习方法:大体分“讲”、“练”、“评”三个环节。
①精讲:讲解知识、抓住本质、建立知识结构、使有机内容网络化;
②精练;科学选题、强化训练、训练思维并巩固知识。要想将学生从茫茫题海中解脱出来,教师则必须深入题海潜心研究,抓特点、求新意、寻变化,建立适合自己学校学生的习题,这样才能提高练习效率;
③细评:这里的评包括对学生作业或试卷的批改和讲评,细致讲评、指导解题思路和解题技巧。
经过“精练”、“细评”这种形式能发现学生哪些知识出错率最高,哪些知识还较模糊,哪些知识学生已掌握,哪些知识还没有掌握,哪些能力还不具备,然后再有目的讲评,有针对性地查漏补缺。
3.具体操作:依据有机物的结构特点和性质递变规律,采用“立体交叉法”来复习各类有机物的有关性质和有机反应类型等相关知识点。
①以研究有机物的过程为线索,建立知识体系
研究有机物主要从以下线索进行:有机物的组成(组成元素、最简式、分子式等)→有机物的结构(碳的成键特点、结构表示方法、分子空间构型、同系物和同分异构体等)→有机反应和通性(反应机理、有机物的特点、命名和分类等)
②以官能团之间的联系为主线,构建知识框架
将各类物质或官能团的性质分别突破以后,知识觉得有些散乱,应该以一些重要物质或官能团为主线,建立它们之间的联系,从而构建有机知识框架,为有机合成和推断提供了明确的思路。
③以有机反应类型为分类标准,重新划分类别
不同的物质可能都发生同一类反应,以反应类型为分类标准,归类总结都哪些物质发生这个反应,可以使学生知识掌握的更加系统、更为明了。如发生取代反应有:烷烃的取代,芳香烃及其衍生物的卤代、硝化,酯和卤代烃的水解,醇的分子间脱水,醇与氢卤酸的反应,酯化反应等;
4.有机习题教学反思:习题教学是提高学生成绩的最直接途径,如何在有限的时间内使教学效果达到最佳,一直是老师们追求的目标。下面仅从三方面反思:
①审题:审题是解任何试题的关键问题,对于有机试题的审题,应该从两反面加强:一是解决思维定势的问题,部分学生因作题目较多,很多题目都似曾相识,而不耐心审题,导致出错。要求对题干逐字逐句分析(可以举两个题干相似的问题让学生做,根据学生的错误,教育学生,从而培养学生认真的态度);二是挖掘提取信息的能力,信息迁移题是有机试题的常见题型,能否较好地发现并利用信息是能否解题的关键,在读题时将信息知识与后面的问题或框图联系起来,大胆迁移、细心应用,既可作答。信息知识一般不要求知道为什么,只要会应用即可。
②训练:训练是改变眼高手低的捷径,训练必须动笔,不能单靠看或说,一些学生有这样的缺点,在与大家一切讨论的时候,讲的很好,但让他自己写就丢三落四,这样的同学在目前的考试制度下特别吃亏,动笔书写能培养学生独立思考和连续思考的能力,同时也检验和改变了书写不规范的问题。教学时师生都要注意细节问题
③讲评:精选例题讲评是习题课的最重要环节,首先,例题要有针对性、示范性、启发性,在讲解时要思维发散,不要就题论题,要根据题目的特征进行延伸,变式训练,培养学生思维的深刻性;还要分析学生解题出错的原因,培养思维的严密性。其次,要注意,讲课时总结一些规律和解题方法是必要的,但规律太多、方法太离奇往往效果不好,如果掌握方法和记忆规律本身很难,对学生的提高会起反作用。再次,要把握好考纲,不要对超纲内容或题目中出现的信息知识任意添加,加重学生的负担。
5.复习注意事宜:在复习时除了注意“试卷分析的反思”所说的几方面外(一个坚持、两个不要、三个研究、四个必须),还要始终注意下面两方面的问题:
①打好基础,是复习备考的首要任务。
一轮复习,夯实基础是复习的首要目的,但复习时也要注意,夯实基础并不是知识的简单重复,尽量利用旧知识创设新情景,并注重知识的具体应用。通过一轮复习,使学生对知识达到熟练的程度,熟练的标准为:一提到某一有机物,立刻能反应出它的各项性质;一提到某一官能团,便知道其相应的化学性质;一提到某一反应类型,便知道那些物质发生此类反应。
②培养能力,是复习备考的重要目的。
新课程对学生的能力提高提出了较高的要求。试题的命制越来越凸现知识与能力并重,以基础知识为载体来强化对能力的考查是命题的趋势,为此要求学生对知识不能仅停留在掌握的水平,更重要的是灵活应用的程度。因此要注意培养学生的自学能力、信息迁移能力、创新能力以及全面分析问题的综合应用能力等。
(二)课时分配建议
1.基础巩固阶段(一轮复习)
将化学必修2(简称甲)的有机部分与1A有机化学基础(简称乙)合到一起复习。复习时即要加强教材上知识的巩固又要将知识前后结合起来,形成立体的网状知识结构,做到既全面又节省时间。大约用18-20个课时,具体课时分配如下:
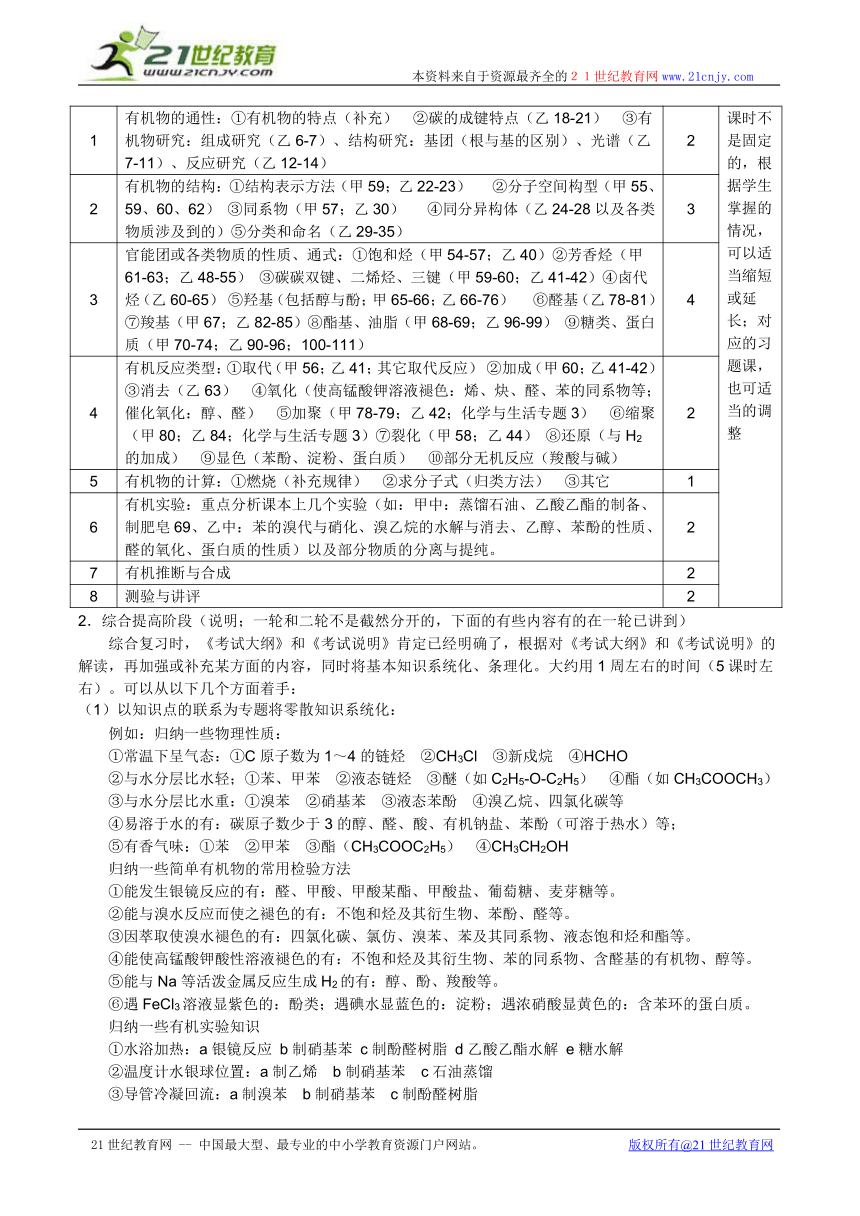
编号 知识内容及在教材中的位置 课时 说明
1 有机物的通性:①有机物的特点(补充) ②碳的成键特点(乙18-21) ③有机物研究:组成研究(乙6-7)、结构研究:基团(根与基的区别)、光谱(乙7-11)、反应研究(乙12-14) 2 课时不是固定的,根据学生掌握的情况,可以适当缩短或延长;对应的习题课,也可适当的调整
2 有机物的结构:①结构表示方法(甲59;乙22-23) ②分子空间构型(甲55、59、60、62) ③同系物(甲57;乙30) ④同分异构体(乙24-28以及各类物质涉及到的)⑤分类和命名(乙29-35) 3
3 官能团或各类物质的性质、通式:①饱和烃(甲54-57;乙40)②芳香烃(甲61-63;乙48-55) ③碳碳双键、二烯烃、三键(甲59-60;乙41-42)④卤代烃(乙60-65) ⑤羟基(包括醇与酚;甲65-66;乙66-76) ⑥醛基(乙78-81) ⑦羧基(甲67;乙82-85)⑧酯基、油脂(甲68-69;乙96-99) ⑨糖类、蛋白质(甲70-74;乙90-96;100-111) 4
4 有机反应类型:①取代(甲56;乙41;其它取代反应) ②加成(甲60;乙41-42) ③消去(乙63) ④氧化(使高锰酸钾溶液褪色:烯、炔、醛、苯的同系物等;催化氧化:醇、醛) ⑤加聚(甲78-79;乙42;化学与生活专题3) ⑥缩聚 (甲80;乙84;化学与生活专题3)⑦裂化(甲58;乙44) ⑧还原(与H2的加成) ⑨显色(苯酚、淀粉、蛋白质) ⑩部分无机反应(羧酸与碱) 2
5 有机物的计算:①燃烧(补充规律) ②求分子式(归类方法) ③其它 1
6 有机实验:重点分析课本上几个实验(如:甲中:蒸馏石油、乙酸乙酯的制备、制肥皂69、乙中:苯的溴代与硝化、溴乙烷的水解与消去、乙醇、苯酚的性质、醛的氧化、蛋白质的性质)以及部分物质的分离与提纯。 2
7 有机推断与合成 2
8 测验与讲评 2
2.综合提高阶段(说明;一轮和二轮不是截然分开的,下面的有些内容有的在一轮已讲到)
综合复习时,《考试大纲》和《考试说明》肯定已经明确了,根据对《考试大纲》和《考试说明》的解读,再加强或补充某方面的内容,同时将基本知识系统化、条理化。大约用1周左右的时间(5课时左右)。可以从以下几个方面着手:
(1)以知识点的联系为专题将零散知识系统化:
例如:归纳一些物理性质:
①常温下呈气态:①C原子数为1~4的链烃 ②CH3Cl ③新戍烷 ④HCHO
②与水分层比水轻;①苯、甲苯 ②液态链烃 ③醚(如C2H5-O-C2H5) ④酯(如CH3COOCH3)
③与水分层比水重:①溴苯 ②硝基苯 ③液态苯酚 ④溴乙烷、四氯化碳等
④易溶于水的有:碳原子数少于3的醇、醛、酸、有机钠盐、苯酚(可溶于热水)等;
⑤有香气味:①苯 ②甲苯 ③酯(CH3COOC2H5) ④CH3CH2OH
归纳一些简单有机物的常用检验方法
①能发生银镜反应的有:醛、甲酸、甲酸某酯、甲酸盐、葡萄糖、麦芽糖等。
②能与溴水反应而使之褪色的有:不饱和烃及其衍生物、苯酚、醛等。
③因萃取使溴水褪色的有:四氯化碳、氯仿、溴苯、苯及其同系物、液态饱和烃和酯等。
④能使高锰酸钾酸性溶液褪色的有:不饱和烃及其衍生物、苯的同系物、含醛基的有机物、醇等。
⑤能与Na等活泼金属反应生成H2的有:醇、酚、羧酸等。
⑥遇FeCl3溶液显紫色的:酚类;遇碘水显蓝色的:淀粉;遇浓硝酸显黄色的:含苯环的蛋白质。
归纳一些有机实验知识
①水浴加热:a银镜反应 b制硝基苯 c制酚醛树脂 d乙酸乙酯水解 e糖水解
②温度计水银球位置:a制乙烯 b制硝基苯 c石油蒸馏
③导管冷凝回流:a制溴苯 b制硝基苯 c制酚醛树脂
④冷凝不回流:石油蒸馏(冷凝管)
⑤防倒吸:a制溴苯 b制乙酸乙酯
⑥有机物分离提纯方法:a萃取分液法 b蒸馏分馏法 c洗气法(还有渗析、盐析、沉淀法等)。
(2)按有机反应类型为专题将知识系统化
归纳出何种有机物能发生相关反应,并且写出典型的化学反应方程式。例如:
①取代反应:包括卤代,硝化,卤代烃水解,醇的分子间脱水,醇与氢卤酸的反应,酯化反应等;
②加成反应:包括碳碳加成,碳氧加成等;
③消去反应:包括卤代烃消去,醇的消去等;
④氧化反应:包括烯、炔、苯的同系物的氧化,醇、醛的氧化等;
⑤还原反应:包括醛、酮的还原,不饱和烃与氢气的加成等;
⑥加聚反应:包括烯、炔的加聚,碳氧双键的加聚等;
⑦缩聚反应:包括氨基酸,二元醇,二元羟酸等多官能团的缩聚。
(3)以解题规律为专题使思考问题条理化:
指导学生解有机框图题的思路为:认真读题,审清题意,采集信息,积极思考。抓住特征条件,从中找出突破口,再从突破口向外发散,通过顺推法、逆推法、顺逆综合法、假设法、知识迁移法得出结论,最后作全面检查,验证结论是否符合题意,概括起来就是“审、破、推、答”四个字。
指导学生解有机化学计算题:抓住以下关键:①混合物平均分子量;②气体体积变化;③气体压强变化;④气体密度变化;⑤质量变化等。
四、与1B内容的联系
(一)化学与生活
此模块与有机化学模块的联系可以概括为下列四大方面
1.营养物质中的“糖类”、“油脂”、“蛋白质”与有机化学模块中基本一样,可以不用再占时间复习,但增加了维生素的内容。
2.高分子材料中关于反应类型“加聚反应”、“缩聚反应”的知识,与有机化学模块中基本一样,也可以合并复习。废弃塑料的裂解可看作高分子断裂为小分子过程。
3.部分生活中的有机物,主要是考查官能团的性质。如:居室中甲醛含量的测定(醛基)、消毒剂过氧乙酸的使用(过氧链)、皮肤接触有机磷农药(属磷酸酯类)用碱性物质洗涤、阿司匹林的结构和性质、部分抗生素的性质等。污水中BOD值既指水中有机物被氧化分解所需氧气的量。
4.有机物物理性质的应用:如,合成洗涤剂及干洗剂溶解油污,主要是利用有机物互溶原理。
(二)化学与技术
此模块的有机部分绝大多数与“化学与生活”模块相同,概括为三方面的内容:
1.有机合成
①有机高分子的合成:如酚醛树脂、橡胶、塑料等的合成(同有机模块和生活模块)、纤维素酯的制造(同有机模块)、
②有机小分子的合成:如阿司匹林的合成(同生活模块和实验模块)、洗衣粉十二烷基苯磺酸钠的合成(主要利用取代反应)、尿素的合成与转化、有机玻璃的合成(都同有机模块)。
2.合成的绿色化:
从原料的绿色化、催化剂的绿色化、溶剂的绿色化、产品的绿色化几方面分析。
3.有机物的性质:
污水中BOD值(同生活模块)、苯酚的性质、纤维素的水解(都同有机模块)、有机农药的性质、废弃塑料的降解(都同生活模块)。
五、附四套试卷中有机试题
全国理科综合卷Ⅰ
8.下列各组物质不属于同分异构体的是 [答案:D]
A.2,2-二甲基丙醇和2-甲基丁醇 B.邻氯甲苯和对氯甲苯
C.2-甲基丁烷和戊烷 D.甲基丙烯酸和甲酸丙酯
29.(16分)A、B、C、D、E、F和G都是有机化合物,它们的关系如下图所示:
(1)化合物C的分子式是C7H8O,C遇到FeCl3溶液显示紫色,C与溴水反应生成的一溴代物只有两种,则C的结构简式为 ;
(2)D为一直链化合物,其相对分子质量比化合物C的小20,它能跟NaHCO3反应放出CO2,则D分子式为 ,D具有的官能团是 ;
(3)反应①的化学方程式是 ;
(4)芳香化合物B是与A具有相同官能团的A的同分异构体,通过反应②化合物B能生成E和F,F可能的结构简式是 ;
(5)E可能的结构简式是 。
[答案]
全国理科综合卷Ⅱ
6.2008年北京奥运会的“祥云”火炬所用的燃料的主要成分是丙烷,下列有关丙烷的叙述中不正确的是
A.分子中碳原子不在一条直线上 B.光照下能够发生取代反应
C.比丁烷更易液化 D.是石油分馏的一种产品 [答案:C]
29.(17分)A、B、C、D、E、F、G、H、I、J均为有机化合物,根据以下框图,回答问题:
(1)B和C均为有支链`的有机化合物,B的结构式为 ;C在浓硫酸作用下加热反应只能生成一种烯烃D,D的结构简式为 。
(2)G能发生银镜反应,也能使溴的四氯化碳溶液褪色,则G的结构简式为
(3)写出⑤的化学反应方程式 。
⑨的化学反应方程式 。
(4)①的反应类型 ,④的反应类型 ,⑦的反应类型 。
(5)与H具有相同官能团的H的同分异构体的结构简式为 。
答案:(1), (2)
(3)
(4)水解,取代,氧化
(5)CH3CH=CHCOOH CH2=CHCH2COOH
山东理科综合卷
12.下列叙述正确的是 [答案:B]
A.汽油、柴油和植物油都是碳氢化合物
B.乙醇可以被氧化为乙酸,二者都能发生酯化反应
C.甲烷、乙烯和苯在工业上都可通过石油分馏得到
D.含5个碳原子的有机物,每个分子中最多可形成4个C-C单键
33.苯丙酸诺龙是一种兴奋剂,结构简式为:
⑴由苯丙酸诺龙的结构推测,它能 (填代号)。
a.使溴的四氯化碳溶液褪色 b.使酸性KMnO4溶液褪色
c.与银氨溶液发生银镜反应 d.与Na2CO3溶液作用生成CO2
苯丙酸诺龙的一种同分异构体A,在一定条件下可发生下列反应:
据以上信息回答⑵~⑷题: ⑵B→D的反应类型是 。
⑶C的结构简式为 。⑷F→G的化学方程式是 。
答案:⑴a、b;⑵加成反应(或还原反应)
宁夏理科综合卷
8.在①丙烯 ②氯乙烯 ③苯 ④甲苯四种有机化合物中,分子内所有原子均在同一平面的是
A.①② B.②③ C.③④ D.②④
9.下列说法错误的是 [答案:8.B 9.D ]
A.乙醇和乙酸都是常用调味品的主要成分
B.乙醇和乙酸的沸点和熔点都比C2H6、C2H4的沸点和熔点高
C.乙醇和乙酸都能发生氧化反应
D.乙醇和乙酸之间能发生酯化反应,酯化反应和皂化反应互为逆反应
36.(15分)已知化合物A中各元素的质量分数分别为C 37.5%,H 4.2%和O 58.3%。请填空
(1)0.01molA在空气中充分燃烧需消耗氧气1.01L(标准状况),则A的分子式是 ;
(2)实验表明:A不能发生银镜反应。1molA与中量的碳酸氢钠溶液反应可以放出3mol二氧化碳。在浓硫酸催化下,A与乙酸可发生酯化反应。核磁共振氢谱表明A分子中有4个氢处于完全相同的化学环境。则A的结构简式是 ;
(3)在浓硫酸催化和适宜的的反应条件下,A与足量的乙醇反应生成B(C12H20O7),B只有两种官能团,其数目比为3∶1。由A生成B的反应类型是 ,该反应的化学方程式是 ;
(4)A失去1分子水后形成化合物C,写出C的两种可能的结构简式及其官能团的名称① ,② 。
[答案]
36. (1)C6H8O7 (2)
(3)酯化反应
(4)
碳碳双键、羧基
酯基、羧基
或右侧几种
酯
醇
醛
羧酸
炔烃
烯烃
烷烃
卤代烃
加氢
加氢
卤代
水解
还原
氧化
氧化
水解
酯化
水解
酯化
消去(HX)
加成(HX、X2)
消去(HX)
加成(HX、X2)
加成(H2O)
消去H2O
.酯基 羧基
羟基 羧基 酸酐基
羟基 羧基 酸酐基
羟基 羧基 碳碳双键
羰基
21世纪教育网 -- 中国最大型、最专业的中小学教育资源门户网站。 版权所有@21世纪教育网
08年高考试题分析和09年复习备考建议(有机化学)
温州中学 赵彦海
一、08年有机考查的内容
对比浙江省用的全国卷Ⅰ和全国卷Ⅱ以及使用新教材的山东和宁夏四份试卷
试卷类别 总分化学分 有机题序、分值、内容 占化学比例 说明
全国卷Ⅰ 300108 8题(6分,同分异构体:根据有机物名称写出结构简式的能力)29题(16分,有机综合:以醇、酚、芳香酸等物质为依托,框图形式体现,考查结构简式、分子式、化学方程式的书写,官能团的名称或书写)共22分 22/108=20.4% 理科综合试卷
全国卷Ⅱ 300108 6题(6分,烷烃:考查分子结构、取代反应、熔沸点、石油化工)29题(17分,有机综合:以烯烃、醛、酸、醇等物质为依托,框图形式体现,考查结构简式、化学方程式的书写和反应类型)共23分 23/108=21.3%
山东卷(新课程) 24078 9题(3分,两个选项是有机,高分子材料及白色污染)10题(1.5分,一个选项是有机,化学史)12题(4分,考查石油化工、乙醇、乙酸及碳的成键特点)33题(8分,官能团性质、反应类型、结构简式和化学方程式)29题(以有机物为依托,但考查的是化学能量问题)共16.5分 16.5/78=21.2%
宁夏卷(新课程) 300100 8题(6分,分子结构:有机物分子共面问题)9题(6分,乙醇与乙酸的物理性质和化学性质)36题(15分,有机综合:燃烧法求分子式、结构简式、化学方程式、反应类型、官能团的名称、光谱的性质)共27分 27/100=27%
二、试题分析与反思
(一)试题分析
1.从试题的结构和考查的内容看:有机试题的题型,比例和分值都相对比较稳定,综观前几年和今年的几份试卷,都有一个有机推断题和一道有机选择题,山东卷与宁夏卷在选择题上稍有差异,所占分值占整个化学试题的20%左右,宁夏试卷有机比例稍大。考查内容主要涉及到有机物分子式、结构简式、化学方程式的书写;典型官能团的结构和性质判断;同分异构体的判断及书写;有机反应类型的判断,几乎涵盖了所有有机化学内容,推断题大多都以醇、醛、羧酸、酯等主要有机物为依托,选择题考查知识点的随机性较大,课本上的任何一处都可能成为考试的“热点”。
2.从试题考查的要求看:知识以理解层次居多,物质间相互联系是重点。试题特别强调能力和素质的考查,注重考查考生对基础知识的理解能力以及运用这些基础知识分析、解决问题的能力,体现了学以致用、理论联系实际的思想。如上述几份试卷通过对醇、醛、酸、酚等物质性质的理解,考查反应类型、结构简式与化学方程式的书写等,都体现了这个特点。命题者的意图就是想通过考生对有机物结构式的确定以及同分异构体、化学方程式的书写,来考查考生运用有机化学基础知识分析问题和解决问题的能力。
3.从命题的着眼点看:无论是结构简式、化学方程式的书写,还是有机反应类型的判断,高考试题的根都根植于教材之中。虽然高考的题目常考常新,但万变不离其宗。在教学中要做好“用教材教”、“用考纲指导方向”,决不能抛开教材和考纲,凭自己所谓的老经验盲目指导,在考纲没明确时,应该认真研究省学科指导意见。尤其今年第一界新课程高考,命题形式还不十分明确,更应该加强研究、合作交流,并多听取省市的精神,及时调整自己复习的方向,反对闭门造车。
4.从学生的答题情况看,常见的主要错误有:
①审题不仔细,没按题目要求准确作答;
②结构简式的书写不规范:a.多写或少写H原子;b.官能团之间的连接线没有对准所连接的原子或连接的原子不正确;c.书写方程式时丢产物(如水等小分子),忘了配平或注明反应条件等;
③对一些复杂有机物结构或同分异构体的书写等,很难完整写出。
5.对全国卷Ⅰ29题的商讨:
中学化学谈到苯酚与浓溴水的反应时,仅谈生成邻对位的产物,甚至大学有机化学也是不谈间位的产物,29题(1)谈到“C与溴水反应生成的一溴代物只有两种”,如果按照教材介绍的“不考虑间位产物之意”则C是邻位甲基苯酚;如果不管实际有无这样的产物,只要位置许可就算一种,则C是对位甲基苯酚。答案中给的是对位甲基苯酚,说明出题者考虑的是不论有无间位产物均可,这样出题无可厚非,但需要说明,否则会使学生无从入手,造成困惑,尤其对考虑问题比较全面的同学更不公平。
(二)试题分析的反思
通过对几份试卷和几年来有机试题的分析,对今后的教学有这样几点不成熟的思考:
1.一个“坚持”:有机复习始终坚持中学化学的基础知识,不论高考怎么出题,复习时一定要针对中学教材的基本有机物、基本反应等知识反复训练,不搞偏题、怪题,这是以不变应万变的唯一途径。
2.二个“不要”:对于教师不要仅凭自己的老经验指导学生,要躬身学习、交流讨论,这样才能吃透新课程,较好地指导学生;不要完全相信学生所谓的“听懂了”,很多问题要让学生动笔写出才算掌握。
3.三个“研究”:研究教材和考纲,准确把握知识的广度和深度;研究考题,分析试卷结构、试题的出题形式和变化趋势;研究学生,根据学生对知识的掌握情况合理分配复习时间和讲授的侧重点。
4.四个“必须”:必须在全面复习的基础上重点突破,不能有投机心理;必须在知识点熟练和理解的基础上加强应用,不能一步过难;必须强化学生规范书写的落实,不要怕浪费时间;必须教师精选习题让学生来完成,不能填鸭式的将一本厚厚的资料从头做到尾。
三、课时分配与复习备考建议
(一)复习备考建议
1.复习安排:大体分两阶段。第一阶段基础巩固;第二阶段综合提高。
2.复习方法:大体分“讲”、“练”、“评”三个环节。
①精讲:讲解知识、抓住本质、建立知识结构、使有机内容网络化;
②精练;科学选题、强化训练、训练思维并巩固知识。要想将学生从茫茫题海中解脱出来,教师则必须深入题海潜心研究,抓特点、求新意、寻变化,建立适合自己学校学生的习题,这样才能提高练习效率;
③细评:这里的评包括对学生作业或试卷的批改和讲评,细致讲评、指导解题思路和解题技巧。
经过“精练”、“细评”这种形式能发现学生哪些知识出错率最高,哪些知识还较模糊,哪些知识学生已掌握,哪些知识还没有掌握,哪些能力还不具备,然后再有目的讲评,有针对性地查漏补缺。
3.具体操作:依据有机物的结构特点和性质递变规律,采用“立体交叉法”来复习各类有机物的有关性质和有机反应类型等相关知识点。
①以研究有机物的过程为线索,建立知识体系
研究有机物主要从以下线索进行:有机物的组成(组成元素、最简式、分子式等)→有机物的结构(碳的成键特点、结构表示方法、分子空间构型、同系物和同分异构体等)→有机反应和通性(反应机理、有机物的特点、命名和分类等)
②以官能团之间的联系为主线,构建知识框架
将各类物质或官能团的性质分别突破以后,知识觉得有些散乱,应该以一些重要物质或官能团为主线,建立它们之间的联系,从而构建有机知识框架,为有机合成和推断提供了明确的思路。
③以有机反应类型为分类标准,重新划分类别
不同的物质可能都发生同一类反应,以反应类型为分类标准,归类总结都哪些物质发生这个反应,可以使学生知识掌握的更加系统、更为明了。如发生取代反应有:烷烃的取代,芳香烃及其衍生物的卤代、硝化,酯和卤代烃的水解,醇的分子间脱水,醇与氢卤酸的反应,酯化反应等;
4.有机习题教学反思:习题教学是提高学生成绩的最直接途径,如何在有限的时间内使教学效果达到最佳,一直是老师们追求的目标。下面仅从三方面反思:
①审题:审题是解任何试题的关键问题,对于有机试题的审题,应该从两反面加强:一是解决思维定势的问题,部分学生因作题目较多,很多题目都似曾相识,而不耐心审题,导致出错。要求对题干逐字逐句分析(可以举两个题干相似的问题让学生做,根据学生的错误,教育学生,从而培养学生认真的态度);二是挖掘提取信息的能力,信息迁移题是有机试题的常见题型,能否较好地发现并利用信息是能否解题的关键,在读题时将信息知识与后面的问题或框图联系起来,大胆迁移、细心应用,既可作答。信息知识一般不要求知道为什么,只要会应用即可。
②训练:训练是改变眼高手低的捷径,训练必须动笔,不能单靠看或说,一些学生有这样的缺点,在与大家一切讨论的时候,讲的很好,但让他自己写就丢三落四,这样的同学在目前的考试制度下特别吃亏,动笔书写能培养学生独立思考和连续思考的能力,同时也检验和改变了书写不规范的问题。教学时师生都要注意细节问题
③讲评:精选例题讲评是习题课的最重要环节,首先,例题要有针对性、示范性、启发性,在讲解时要思维发散,不要就题论题,要根据题目的特征进行延伸,变式训练,培养学生思维的深刻性;还要分析学生解题出错的原因,培养思维的严密性。其次,要注意,讲课时总结一些规律和解题方法是必要的,但规律太多、方法太离奇往往效果不好,如果掌握方法和记忆规律本身很难,对学生的提高会起反作用。再次,要把握好考纲,不要对超纲内容或题目中出现的信息知识任意添加,加重学生的负担。
5.复习注意事宜:在复习时除了注意“试卷分析的反思”所说的几方面外(一个坚持、两个不要、三个研究、四个必须),还要始终注意下面两方面的问题:
①打好基础,是复习备考的首要任务。
一轮复习,夯实基础是复习的首要目的,但复习时也要注意,夯实基础并不是知识的简单重复,尽量利用旧知识创设新情景,并注重知识的具体应用。通过一轮复习,使学生对知识达到熟练的程度,熟练的标准为:一提到某一有机物,立刻能反应出它的各项性质;一提到某一官能团,便知道其相应的化学性质;一提到某一反应类型,便知道那些物质发生此类反应。
②培养能力,是复习备考的重要目的。
新课程对学生的能力提高提出了较高的要求。试题的命制越来越凸现知识与能力并重,以基础知识为载体来强化对能力的考查是命题的趋势,为此要求学生对知识不能仅停留在掌握的水平,更重要的是灵活应用的程度。因此要注意培养学生的自学能力、信息迁移能力、创新能力以及全面分析问题的综合应用能力等。
(二)课时分配建议
1.基础巩固阶段(一轮复习)
将化学必修2(简称甲)的有机部分与1A有机化学基础(简称乙)合到一起复习。复习时即要加强教材上知识的巩固又要将知识前后结合起来,形成立体的网状知识结构,做到既全面又节省时间。大约用18-20个课时,具体课时分配如下:
编号 知识内容及在教材中的位置 课时 说明
1 有机物的通性:①有机物的特点(补充) ②碳的成键特点(乙18-21) ③有机物研究:组成研究(乙6-7)、结构研究:基团(根与基的区别)、光谱(乙7-11)、反应研究(乙12-14) 2 课时不是固定的,根据学生掌握的情况,可以适当缩短或延长;对应的习题课,也可适当的调整
2 有机物的结构:①结构表示方法(甲59;乙22-23) ②分子空间构型(甲55、59、60、62) ③同系物(甲57;乙30) ④同分异构体(乙24-28以及各类物质涉及到的)⑤分类和命名(乙29-35) 3
3 官能团或各类物质的性质、通式:①饱和烃(甲54-57;乙40)②芳香烃(甲61-63;乙48-55) ③碳碳双键、二烯烃、三键(甲59-60;乙41-42)④卤代烃(乙60-65) ⑤羟基(包括醇与酚;甲65-66;乙66-76) ⑥醛基(乙78-81) ⑦羧基(甲67;乙82-85)⑧酯基、油脂(甲68-69;乙96-99) ⑨糖类、蛋白质(甲70-74;乙90-96;100-111) 4
4 有机反应类型:①取代(甲56;乙41;其它取代反应) ②加成(甲60;乙41-42) ③消去(乙63) ④氧化(使高锰酸钾溶液褪色:烯、炔、醛、苯的同系物等;催化氧化:醇、醛) ⑤加聚(甲78-79;乙42;化学与生活专题3) ⑥缩聚 (甲80;乙84;化学与生活专题3)⑦裂化(甲58;乙44) ⑧还原(与H2的加成) ⑨显色(苯酚、淀粉、蛋白质) ⑩部分无机反应(羧酸与碱) 2
5 有机物的计算:①燃烧(补充规律) ②求分子式(归类方法) ③其它 1
6 有机实验:重点分析课本上几个实验(如:甲中:蒸馏石油、乙酸乙酯的制备、制肥皂69、乙中:苯的溴代与硝化、溴乙烷的水解与消去、乙醇、苯酚的性质、醛的氧化、蛋白质的性质)以及部分物质的分离与提纯。 2
7 有机推断与合成 2
8 测验与讲评 2
2.综合提高阶段(说明;一轮和二轮不是截然分开的,下面的有些内容有的在一轮已讲到)
综合复习时,《考试大纲》和《考试说明》肯定已经明确了,根据对《考试大纲》和《考试说明》的解读,再加强或补充某方面的内容,同时将基本知识系统化、条理化。大约用1周左右的时间(5课时左右)。可以从以下几个方面着手:
(1)以知识点的联系为专题将零散知识系统化:
例如:归纳一些物理性质:
①常温下呈气态:①C原子数为1~4的链烃 ②CH3Cl ③新戍烷 ④HCHO
②与水分层比水轻;①苯、甲苯 ②液态链烃 ③醚(如C2H5-O-C2H5) ④酯(如CH3COOCH3)
③与水分层比水重:①溴苯 ②硝基苯 ③液态苯酚 ④溴乙烷、四氯化碳等
④易溶于水的有:碳原子数少于3的醇、醛、酸、有机钠盐、苯酚(可溶于热水)等;
⑤有香气味:①苯 ②甲苯 ③酯(CH3COOC2H5) ④CH3CH2OH
归纳一些简单有机物的常用检验方法
①能发生银镜反应的有:醛、甲酸、甲酸某酯、甲酸盐、葡萄糖、麦芽糖等。
②能与溴水反应而使之褪色的有:不饱和烃及其衍生物、苯酚、醛等。
③因萃取使溴水褪色的有:四氯化碳、氯仿、溴苯、苯及其同系物、液态饱和烃和酯等。
④能使高锰酸钾酸性溶液褪色的有:不饱和烃及其衍生物、苯的同系物、含醛基的有机物、醇等。
⑤能与Na等活泼金属反应生成H2的有:醇、酚、羧酸等。
⑥遇FeCl3溶液显紫色的:酚类;遇碘水显蓝色的:淀粉;遇浓硝酸显黄色的:含苯环的蛋白质。
归纳一些有机实验知识
①水浴加热:a银镜反应 b制硝基苯 c制酚醛树脂 d乙酸乙酯水解 e糖水解
②温度计水银球位置:a制乙烯 b制硝基苯 c石油蒸馏
③导管冷凝回流:a制溴苯 b制硝基苯 c制酚醛树脂
④冷凝不回流:石油蒸馏(冷凝管)
⑤防倒吸:a制溴苯 b制乙酸乙酯
⑥有机物分离提纯方法:a萃取分液法 b蒸馏分馏法 c洗气法(还有渗析、盐析、沉淀法等)。
(2)按有机反应类型为专题将知识系统化
归纳出何种有机物能发生相关反应,并且写出典型的化学反应方程式。例如:
①取代反应:包括卤代,硝化,卤代烃水解,醇的分子间脱水,醇与氢卤酸的反应,酯化反应等;
②加成反应:包括碳碳加成,碳氧加成等;
③消去反应:包括卤代烃消去,醇的消去等;
④氧化反应:包括烯、炔、苯的同系物的氧化,醇、醛的氧化等;
⑤还原反应:包括醛、酮的还原,不饱和烃与氢气的加成等;
⑥加聚反应:包括烯、炔的加聚,碳氧双键的加聚等;
⑦缩聚反应:包括氨基酸,二元醇,二元羟酸等多官能团的缩聚。
(3)以解题规律为专题使思考问题条理化:
指导学生解有机框图题的思路为:认真读题,审清题意,采集信息,积极思考。抓住特征条件,从中找出突破口,再从突破口向外发散,通过顺推法、逆推法、顺逆综合法、假设法、知识迁移法得出结论,最后作全面检查,验证结论是否符合题意,概括起来就是“审、破、推、答”四个字。
指导学生解有机化学计算题:抓住以下关键:①混合物平均分子量;②气体体积变化;③气体压强变化;④气体密度变化;⑤质量变化等。
四、与1B内容的联系
(一)化学与生活
此模块与有机化学模块的联系可以概括为下列四大方面
1.营养物质中的“糖类”、“油脂”、“蛋白质”与有机化学模块中基本一样,可以不用再占时间复习,但增加了维生素的内容。
2.高分子材料中关于反应类型“加聚反应”、“缩聚反应”的知识,与有机化学模块中基本一样,也可以合并复习。废弃塑料的裂解可看作高分子断裂为小分子过程。
3.部分生活中的有机物,主要是考查官能团的性质。如:居室中甲醛含量的测定(醛基)、消毒剂过氧乙酸的使用(过氧链)、皮肤接触有机磷农药(属磷酸酯类)用碱性物质洗涤、阿司匹林的结构和性质、部分抗生素的性质等。污水中BOD值既指水中有机物被氧化分解所需氧气的量。
4.有机物物理性质的应用:如,合成洗涤剂及干洗剂溶解油污,主要是利用有机物互溶原理。
(二)化学与技术
此模块的有机部分绝大多数与“化学与生活”模块相同,概括为三方面的内容:
1.有机合成
①有机高分子的合成:如酚醛树脂、橡胶、塑料等的合成(同有机模块和生活模块)、纤维素酯的制造(同有机模块)、
②有机小分子的合成:如阿司匹林的合成(同生活模块和实验模块)、洗衣粉十二烷基苯磺酸钠的合成(主要利用取代反应)、尿素的合成与转化、有机玻璃的合成(都同有机模块)。
2.合成的绿色化:
从原料的绿色化、催化剂的绿色化、溶剂的绿色化、产品的绿色化几方面分析。
3.有机物的性质:
污水中BOD值(同生活模块)、苯酚的性质、纤维素的水解(都同有机模块)、有机农药的性质、废弃塑料的降解(都同生活模块)。
五、附四套试卷中有机试题
全国理科综合卷Ⅰ
8.下列各组物质不属于同分异构体的是 [答案:D]
A.2,2-二甲基丙醇和2-甲基丁醇 B.邻氯甲苯和对氯甲苯
C.2-甲基丁烷和戊烷 D.甲基丙烯酸和甲酸丙酯
29.(16分)A、B、C、D、E、F和G都是有机化合物,它们的关系如下图所示:
(1)化合物C的分子式是C7H8O,C遇到FeCl3溶液显示紫色,C与溴水反应生成的一溴代物只有两种,则C的结构简式为 ;
(2)D为一直链化合物,其相对分子质量比化合物C的小20,它能跟NaHCO3反应放出CO2,则D分子式为 ,D具有的官能团是 ;
(3)反应①的化学方程式是 ;
(4)芳香化合物B是与A具有相同官能团的A的同分异构体,通过反应②化合物B能生成E和F,F可能的结构简式是 ;
(5)E可能的结构简式是 。
[答案]
全国理科综合卷Ⅱ
6.2008年北京奥运会的“祥云”火炬所用的燃料的主要成分是丙烷,下列有关丙烷的叙述中不正确的是
A.分子中碳原子不在一条直线上 B.光照下能够发生取代反应
C.比丁烷更易液化 D.是石油分馏的一种产品 [答案:C]
29.(17分)A、B、C、D、E、F、G、H、I、J均为有机化合物,根据以下框图,回答问题:
(1)B和C均为有支链`的有机化合物,B的结构式为 ;C在浓硫酸作用下加热反应只能生成一种烯烃D,D的结构简式为 。
(2)G能发生银镜反应,也能使溴的四氯化碳溶液褪色,则G的结构简式为
(3)写出⑤的化学反应方程式 。
⑨的化学反应方程式 。
(4)①的反应类型 ,④的反应类型 ,⑦的反应类型 。
(5)与H具有相同官能团的H的同分异构体的结构简式为 。
答案:(1), (2)
(3)
(4)水解,取代,氧化
(5)CH3CH=CHCOOH CH2=CHCH2COOH
山东理科综合卷
12.下列叙述正确的是 [答案:B]
A.汽油、柴油和植物油都是碳氢化合物
B.乙醇可以被氧化为乙酸,二者都能发生酯化反应
C.甲烷、乙烯和苯在工业上都可通过石油分馏得到
D.含5个碳原子的有机物,每个分子中最多可形成4个C-C单键
33.苯丙酸诺龙是一种兴奋剂,结构简式为:
⑴由苯丙酸诺龙的结构推测,它能 (填代号)。
a.使溴的四氯化碳溶液褪色 b.使酸性KMnO4溶液褪色
c.与银氨溶液发生银镜反应 d.与Na2CO3溶液作用生成CO2
苯丙酸诺龙的一种同分异构体A,在一定条件下可发生下列反应:
据以上信息回答⑵~⑷题: ⑵B→D的反应类型是 。
⑶C的结构简式为 。⑷F→G的化学方程式是 。
答案:⑴a、b;⑵加成反应(或还原反应)
宁夏理科综合卷
8.在①丙烯 ②氯乙烯 ③苯 ④甲苯四种有机化合物中,分子内所有原子均在同一平面的是
A.①② B.②③ C.③④ D.②④
9.下列说法错误的是 [答案:8.B 9.D ]
A.乙醇和乙酸都是常用调味品的主要成分
B.乙醇和乙酸的沸点和熔点都比C2H6、C2H4的沸点和熔点高
C.乙醇和乙酸都能发生氧化反应
D.乙醇和乙酸之间能发生酯化反应,酯化反应和皂化反应互为逆反应
36.(15分)已知化合物A中各元素的质量分数分别为C 37.5%,H 4.2%和O 58.3%。请填空
(1)0.01molA在空气中充分燃烧需消耗氧气1.01L(标准状况),则A的分子式是 ;
(2)实验表明:A不能发生银镜反应。1molA与中量的碳酸氢钠溶液反应可以放出3mol二氧化碳。在浓硫酸催化下,A与乙酸可发生酯化反应。核磁共振氢谱表明A分子中有4个氢处于完全相同的化学环境。则A的结构简式是 ;
(3)在浓硫酸催化和适宜的的反应条件下,A与足量的乙醇反应生成B(C12H20O7),B只有两种官能团,其数目比为3∶1。由A生成B的反应类型是 ,该反应的化学方程式是 ;
(4)A失去1分子水后形成化合物C,写出C的两种可能的结构简式及其官能团的名称① ,② 。
[答案]
36. (1)C6H8O7 (2)
(3)酯化反应
(4)
碳碳双键、羧基
酯基、羧基
或右侧几种
酯
醇
醛
羧酸
炔烃
烯烃
烷烃
卤代烃
加氢
加氢
卤代
水解
还原
氧化
氧化
水解
酯化
水解
酯化
消去(HX)
加成(HX、X2)
消去(HX)
加成(HX、X2)
加成(H2O)
消去H2O
.酯基 羧基
羟基 羧基 酸酐基
羟基 羧基 酸酐基
羟基 羧基 碳碳双键
羰基
21世纪教育网 -- 中国最大型、最专业的中小学教育资源门户网站。 版权所有@21世纪教育网
同课章节目录
