碳酸钠与碳酸氢钠
图片预览





文档简介
课件23张PPT。 二、盐 1碳酸钠和碳酸氢钠物理性质
Na2CO3NaHCO3
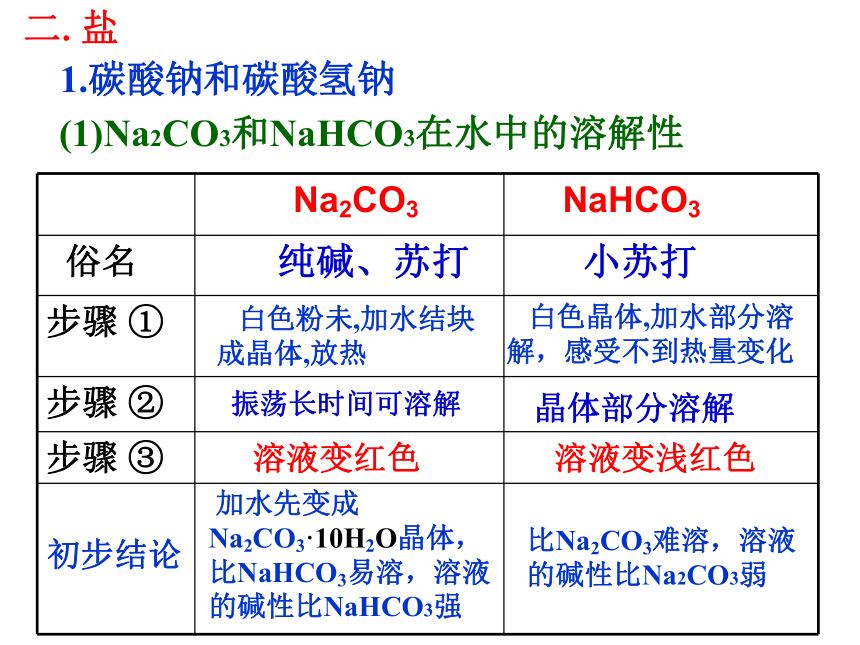
纯碱或苏打小苏打白色粉末白色细小粉末二.盐1.碳酸钠和碳酸氢钠 (1)Na2CO3和NaHCO3在水中的溶解性 晶体部分溶解溶液变浅红色 白色粉未,加水结块成晶体,放热 白色晶体,加水部分溶解,感受不到热量变化振荡长时间可溶解溶液变红色 加水先变成Na2CO3·10H2O晶体,比NaHCO3易溶,溶液的碱性比NaHCO3强
比Na2CO3难溶,溶液的碱性比Na2CO3弱初步结论 纯碱、苏打 小苏打思考:
通过滴加酚酞的对比实验,能说明一个什么问题?思考:1、在Na2CO3饱和溶液中通入CO2后有沉淀析出,
原因是什么?
[解析]
1、将CO2通入Na2CO3溶液中,发生如下反应:
Na2CO3+H2O+CO2=2NaHCO3
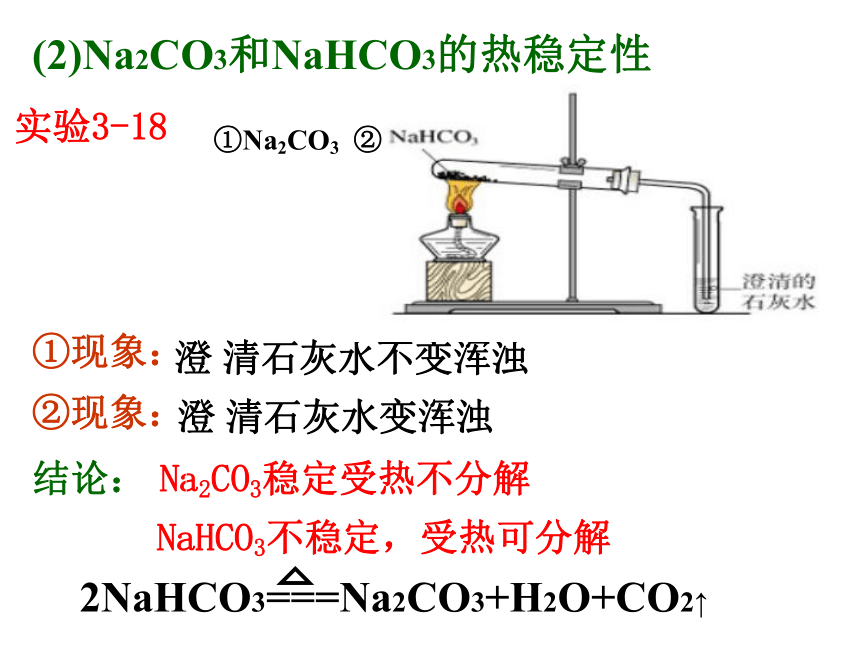
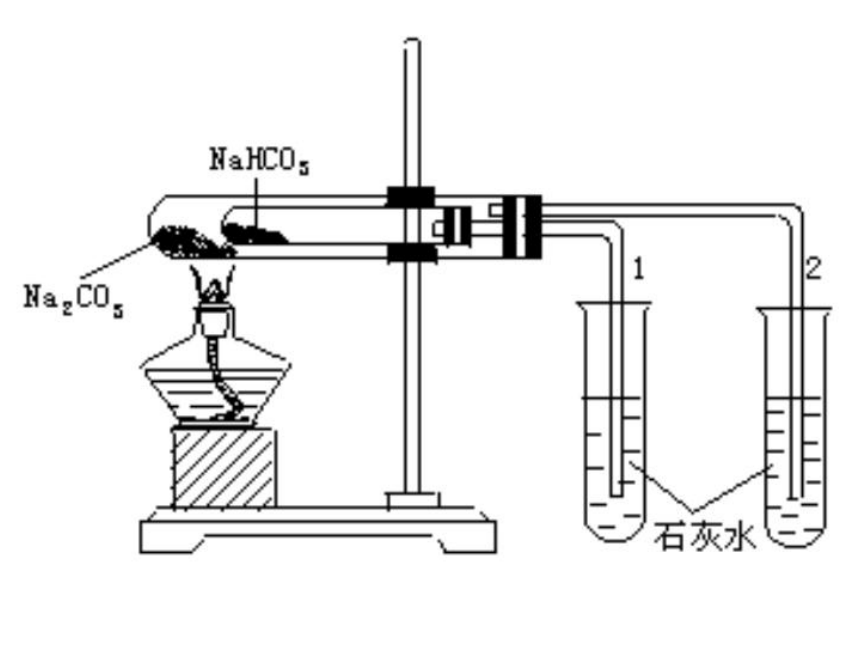
2、生成的NaHCO3的溶解度比Na2CO3的溶解度小。(2)Na2CO3和NaHCO3的热稳定性 Na2CO3稳定受热不分解 NaHCO3不稳定,受热可分解澄 清石灰水不变浑浊实验3-18①Na2CO3 ②澄 清石灰水变浑浊结论:
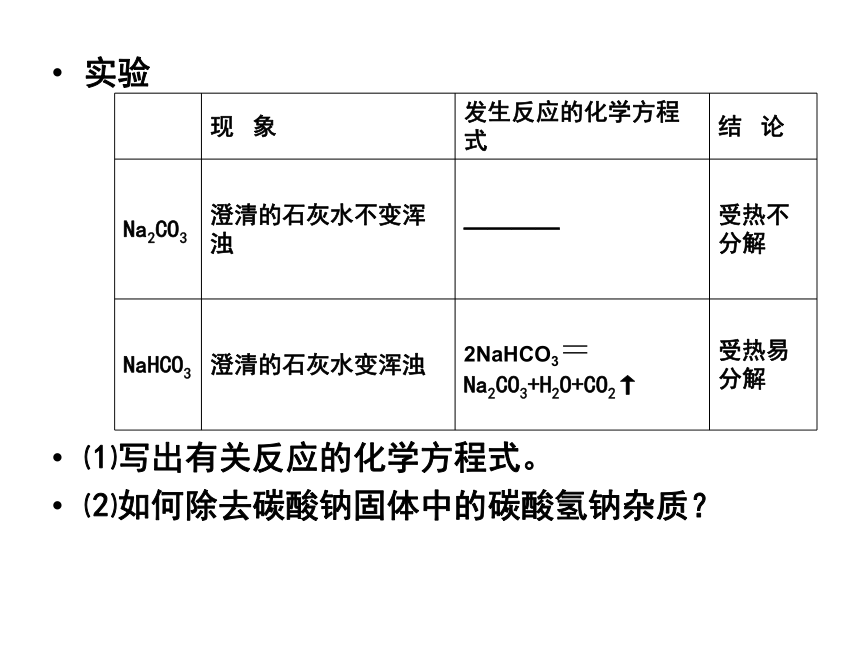
实验
⑴写出有关反应的化学方程式。
⑵如何除去碳酸钠固体中的碳酸氢钠杂质?
(3)Na2CO3和NaHCO3盐酸的反应刚开始滴入,没有明显现象,后来反应较剧烈,有气泡产生刚开始滴入,反应很剧烈,有气泡产生Na2CO3+HCl=NaHCO3+NaClCO32-+H+=HCO3-NaHCO3+HCl=NaCl+H2O+CO2↑HCO3-+H+=H2O+CO2↑CO32-+2H+=H2O+CO2↑Na2CO3+2HCl=2NaCl+H2O+CO2↑思考:把Na2CO3溶液和NaHCO3溶液分别滴入稀盐酸中,会有什么现象?为什么?(4)Na2CO3、NaHCO3
与某些盐的反应 Na2CO3+CaCl2=CaCO3 + 2NaCl NaHCO3+CaCl2 不反应 白色沉淀 NaHCO3+NaOH = Na2CO3+H2O
再加入NaOH溶液,有白色
沉淀生成 HCO3- + OH - = CO3 2- +H2O (5)Na2CO3、NaHCO3与某些碱的反应
HCO3- + OH - = CO3 2- +H2OCO3 2-与OH – 不反应Na2CO3、NaHCO3的相互转化 3、碳酸钠和碳酸氢钠的用处
碳酸钠:
用于玻璃、制皂、造纸、纺织等工业,还用来制造其它钠的化合物。
碳酸氢钠:是焙制糕点所用的发酵粉的主要成分,医疗上用来治疗胃酸过多。
讨论:将钠久置于空气中,最终将变成什么物质?写出一系列变化的化学方程式。总结Na2CO3NaHCO3小苏打纯碱 苏打易溶(比NaHCO3易溶)可溶较强较弱Na2CO3+2HCl=2NaCl+H2O+CO2↑NaHCO3+HCl=NaCl+H2O+CO2↑稳定,加热难分解不稳定,加热可分解热稳定性Na2CO3+HCl=NaHCO3+NaCl与酸反应与某些碱反应Na2CO3+ Ca(OH)2=CaCO3
+2NaOHNaHCO3+NaOH=Na2CO3+H2O区别Na2CO3和NaHCO3的方法:① 加热加热固体,产生能使澄清石灰水变浑浊的气体的是NaHCO3②滴入CaCl2或BaCl2溶液产生白色沉淀的是Na2CO3③逐滴滴入稀盐酸首先产生气体且反应较剧烈的是NaHO3Na2CO3+CaCl2=CaCO3↓+2NaCl怎样鉴别碳酸钠和碳酸氢钠 ⑴ 加热固体。产生能使石灰水变浑浊的无色气体
的是碳酸氢钠。2NaHCO3 = Na2CO3 + H2O + CO2△ ⑶ 在固体中加入相同浓度的盐酸,
反应剧烈的是碳酸氢钠。Na2CO3 + CaCl2 = 2NaCl + CaCO3 ⑵ 溶解,加入氯化钙溶液,产生沉淀的是碳酸钠。【思考】 1. Na2CO3和NaHCO3还有没有其他的性质?举例说明。2.能否实现的Na2CO3和NaHCO3相互转化?3.如何除去Na2CO3中的NaHCO3?又如何除去NaHCO3 中的Na2CO3?4.如何鉴别Na2CO3和NaHCO3两种溶液?思考思考与练习1、如何下列物质总的少量杂质(括号中为杂质)?
①Na2CO3(NaHCO3)固体
②NaHCO3(Na2CO3)2、同物质的量浓度同体积的Na2CO3和NaHCO3溶液分别跟过量稀盐酸反应,下列说法中正确的是( )
①NaHCO3消耗盐酸多 ②Na2CO3消耗盐酸多
③Na2CO3放出CO2多 ④NaHCO3放出CO2多
⑤Na2CO3放出CO2较快 ⑥NaHCO3放出CO2较快②⑥加热向溶液中通入过量CO2某干燥粉末可能由Na2O、Na2O2、Na2CO3、NaCl、NaHCO3、中的一种或几种组成。将该粉末与足量的盐酸反应有气体X逸出,X气体通过足量的NaOH溶液后体积缩小(同温同压下测定)。若将原来混合粉末在空气中用酒精灯加热,也有气体放出,且剩余固体质量大于原混合粉末的质量。试判断:
此粉末中一定有 ,可能有
Na2CO3NaHCO3
纯碱或苏打小苏打白色粉末白色细小粉末二.盐1.碳酸钠和碳酸氢钠 (1)Na2CO3和NaHCO3在水中的溶解性 晶体部分溶解溶液变浅红色 白色粉未,加水结块成晶体,放热 白色晶体,加水部分溶解,感受不到热量变化振荡长时间可溶解溶液变红色 加水先变成Na2CO3·10H2O晶体,比NaHCO3易溶,溶液的碱性比NaHCO3强
比Na2CO3难溶,溶液的碱性比Na2CO3弱初步结论 纯碱、苏打 小苏打思考:
通过滴加酚酞的对比实验,能说明一个什么问题?思考:1、在Na2CO3饱和溶液中通入CO2后有沉淀析出,
原因是什么?
[解析]
1、将CO2通入Na2CO3溶液中,发生如下反应:
Na2CO3+H2O+CO2=2NaHCO3
2、生成的NaHCO3的溶解度比Na2CO3的溶解度小。(2)Na2CO3和NaHCO3的热稳定性 Na2CO3稳定受热不分解 NaHCO3不稳定,受热可分解澄 清石灰水不变浑浊实验3-18①Na2CO3 ②澄 清石灰水变浑浊结论:
实验
⑴写出有关反应的化学方程式。
⑵如何除去碳酸钠固体中的碳酸氢钠杂质?
(3)Na2CO3和NaHCO3盐酸的反应刚开始滴入,没有明显现象,后来反应较剧烈,有气泡产生刚开始滴入,反应很剧烈,有气泡产生Na2CO3+HCl=NaHCO3+NaClCO32-+H+=HCO3-NaHCO3+HCl=NaCl+H2O+CO2↑HCO3-+H+=H2O+CO2↑CO32-+2H+=H2O+CO2↑Na2CO3+2HCl=2NaCl+H2O+CO2↑思考:把Na2CO3溶液和NaHCO3溶液分别滴入稀盐酸中,会有什么现象?为什么?(4)Na2CO3、NaHCO3
与某些盐的反应 Na2CO3+CaCl2=CaCO3 + 2NaCl NaHCO3+CaCl2 不反应 白色沉淀 NaHCO3+NaOH = Na2CO3+H2O
再加入NaOH溶液,有白色
沉淀生成 HCO3- + OH - = CO3 2- +H2O (5)Na2CO3、NaHCO3与某些碱的反应
HCO3- + OH - = CO3 2- +H2OCO3 2-与OH – 不反应Na2CO3、NaHCO3的相互转化 3、碳酸钠和碳酸氢钠的用处
碳酸钠:
用于玻璃、制皂、造纸、纺织等工业,还用来制造其它钠的化合物。
碳酸氢钠:是焙制糕点所用的发酵粉的主要成分,医疗上用来治疗胃酸过多。
讨论:将钠久置于空气中,最终将变成什么物质?写出一系列变化的化学方程式。总结Na2CO3NaHCO3小苏打纯碱 苏打易溶(比NaHCO3易溶)可溶较强较弱Na2CO3+2HCl=2NaCl+H2O+CO2↑NaHCO3+HCl=NaCl+H2O+CO2↑稳定,加热难分解不稳定,加热可分解热稳定性Na2CO3+HCl=NaHCO3+NaCl与酸反应与某些碱反应Na2CO3+ Ca(OH)2=CaCO3
+2NaOHNaHCO3+NaOH=Na2CO3+H2O区别Na2CO3和NaHCO3的方法:① 加热加热固体,产生能使澄清石灰水变浑浊的气体的是NaHCO3②滴入CaCl2或BaCl2溶液产生白色沉淀的是Na2CO3③逐滴滴入稀盐酸首先产生气体且反应较剧烈的是NaHO3Na2CO3+CaCl2=CaCO3↓+2NaCl怎样鉴别碳酸钠和碳酸氢钠 ⑴ 加热固体。产生能使石灰水变浑浊的无色气体
的是碳酸氢钠。2NaHCO3 = Na2CO3 + H2O + CO2△ ⑶ 在固体中加入相同浓度的盐酸,
反应剧烈的是碳酸氢钠。Na2CO3 + CaCl2 = 2NaCl + CaCO3 ⑵ 溶解,加入氯化钙溶液,产生沉淀的是碳酸钠。【思考】 1. Na2CO3和NaHCO3还有没有其他的性质?举例说明。2.能否实现的Na2CO3和NaHCO3相互转化?3.如何除去Na2CO3中的NaHCO3?又如何除去NaHCO3 中的Na2CO3?4.如何鉴别Na2CO3和NaHCO3两种溶液?思考思考与练习1、如何下列物质总的少量杂质(括号中为杂质)?
①Na2CO3(NaHCO3)固体
②NaHCO3(Na2CO3)2、同物质的量浓度同体积的Na2CO3和NaHCO3溶液分别跟过量稀盐酸反应,下列说法中正确的是( )
①NaHCO3消耗盐酸多 ②Na2CO3消耗盐酸多
③Na2CO3放出CO2多 ④NaHCO3放出CO2多
⑤Na2CO3放出CO2较快 ⑥NaHCO3放出CO2较快②⑥加热向溶液中通入过量CO2某干燥粉末可能由Na2O、Na2O2、Na2CO3、NaCl、NaHCO3、中的一种或几种组成。将该粉末与足量的盐酸反应有气体X逸出,X气体通过足量的NaOH溶液后体积缩小(同温同压下测定)。若将原来混合粉末在空气中用酒精灯加热,也有气体放出,且剩余固体质量大于原混合粉末的质量。试判断:
此粉末中一定有 ,可能有
