铁盐和亚铁盐
图片预览





文档简介
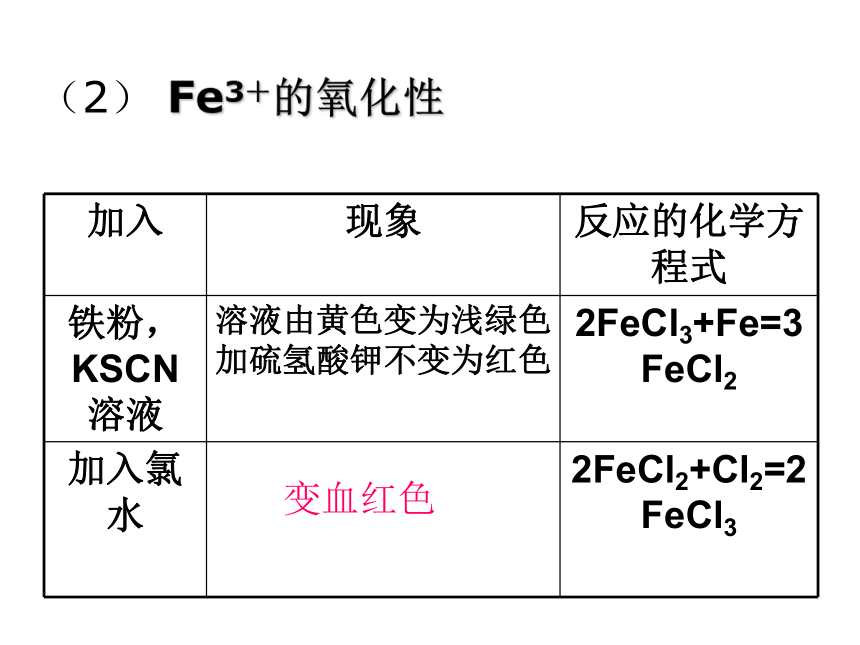
课件12张PPT。2.三价铁的氧化性变血红色无明显变化(1)Fe3+的检验(2) Fe3+的氧化性变血红色【思考】1.通过以上实验可以得出什么结论? Fe3+可以被还原成Fe2+, Fe2+ 也可以被氧化成Fe3+2.如何除去FeCl3溶液中少量的FeCl2,以及FeCl2溶液中少量的FeCl3溶液?现象:白色沉淀
灰绿色 红褐色
Fe2++2OH-=Fe(OH)2↓
4Fe(OH)2+O2+2H2O=
4Fe(OH)3Fe3+和Fe2+的检验现象:红褐色沉淀
Fe3++3OH-=Fe(OH)3↓现象:不变红色,若再通Cl2则变血红色 2Fe2++Cl2=2Fe3++2Cl-
Fe3++3SCN-=Fe(SCN)3现象:变血红色 Fe3++3SCN-
=Fe(SCN)3苹果汁是人们喜爱的饮料,但是现榨的苹果汁在空气中会慢慢的由浅绿色变为棕黄色,为什么呢?3、 Fe3+ 和Fe2+ 的转化O2 Fe2+ Fe3+ 如何判断FeCl2溶液中是否有部分Fe2+被氧化成Fe3+?实验:在2支试管里分别加入2mL FeCl2溶液和2mL FeCl3溶液,各加入1~2滴KSCN溶液。观察现象并记录,填写表格。无明显变化黄色溶液变成血红色(可用来检验Fe3+的存在) Fe2+ Fe3+ 还原剂:金属单质,如铁、铜、S2-、I-等
氧化剂:Cl2、H2O2、 O2 、 HNO3、
浓H2SO4 、 KMnO4 、 KClO3氧化剂还原剂1、 Fe2+和Fe3+的相互转化2、 铁盐(含Fe3+)的净水作用P52FeFe2+Fe3+123456弱氧化剂:H+、Cu2+、S、I2、Fe3+等 强氧化剂:Cl2、Br2、HNO3等Cl2、Br2、HNO3、O2等Zn、Fe、Cu、HI等Zn、H2、Al、C等 Zn、CO、Al等铁三角:1、Fe Fe2+弱氧化剂:H+、Cu2+、S、I2、Fe3+等 Fe+2H+=Fe2++H2↑, Fe+Cu2+=Fe2++CuFe+S==FeS, Fe+I2==FeI2, Fe+2Fe3+==3Fe2+?2、Fe Fe3+强氧化剂:Cl2、Br2、KMnO4、HNO3等2Fe+3Cl2==2FeCl3, 2Fe+3Br2==2FeBr3,
Fe+4HNO3(稀)==Fe(NO3)3+NO↑+2H2O
2Fe+6H2SO4(浓)==Fe2(SO4)3+3SO2↑+6H2O
5Fe+3MnO4-+24H+== 5Fe3++3Mn2++12H2O?3、Fe2+ Fe3+Cl2、Br2、KMnO4、HNO3、O2等 2Fe2+ +Cl2==2Fe3++2Cl-
2Fe2+ +Br2==2Fe3++2Br-
5Fe2+ +MnO4-+8H+==5Fe3++Mn2++4H2O
3Fe2++4H++NO3-==Fe3++NO↑+2H2O4、 Fe3+ Fe2+Zn、Fe、Cu、H2S、HI、SO22Fe3++Zn(不足)==2Fe2++Zn2+ 2Fe3++Cu==2Fe2++Cu2+
2Fe3++H2S==2Fe2++2H++S↓
2Fe3++2HI==2Fe2++2H++I2
2Fe3++SO2+2H2O==2Fe2++4H++SO42-5、Fe2+ FeZn、H2、Al、C、CO等 Fe2++Zn==Fe+Zn2+ FeO+H2====Fe+H2O
3FeO+2Al====3Fe+Al2O3
2 FeO+C====Fe+CO2↑高温高温高温6、Fe3+ FeZn、CO、Al等 2Fe3++3Zn(过量)===2Fe+3Zn2+
Fe2O3+3CO====2Fe+3CO2
Fe2O3+2Al====2Fe+Al2O3
高温高温
灰绿色 红褐色
Fe2++2OH-=Fe(OH)2↓
4Fe(OH)2+O2+2H2O=
4Fe(OH)3Fe3+和Fe2+的检验现象:红褐色沉淀
Fe3++3OH-=Fe(OH)3↓现象:不变红色,若再通Cl2则变血红色 2Fe2++Cl2=2Fe3++2Cl-
Fe3++3SCN-=Fe(SCN)3现象:变血红色 Fe3++3SCN-
=Fe(SCN)3苹果汁是人们喜爱的饮料,但是现榨的苹果汁在空气中会慢慢的由浅绿色变为棕黄色,为什么呢?3、 Fe3+ 和Fe2+ 的转化O2 Fe2+ Fe3+ 如何判断FeCl2溶液中是否有部分Fe2+被氧化成Fe3+?实验:在2支试管里分别加入2mL FeCl2溶液和2mL FeCl3溶液,各加入1~2滴KSCN溶液。观察现象并记录,填写表格。无明显变化黄色溶液变成血红色(可用来检验Fe3+的存在) Fe2+ Fe3+ 还原剂:金属单质,如铁、铜、S2-、I-等
氧化剂:Cl2、H2O2、 O2 、 HNO3、
浓H2SO4 、 KMnO4 、 KClO3氧化剂还原剂1、 Fe2+和Fe3+的相互转化2、 铁盐(含Fe3+)的净水作用P52FeFe2+Fe3+123456弱氧化剂:H+、Cu2+、S、I2、Fe3+等 强氧化剂:Cl2、Br2、HNO3等Cl2、Br2、HNO3、O2等Zn、Fe、Cu、HI等Zn、H2、Al、C等 Zn、CO、Al等铁三角:1、Fe Fe2+弱氧化剂:H+、Cu2+、S、I2、Fe3+等 Fe+2H+=Fe2++H2↑, Fe+Cu2+=Fe2++CuFe+S==FeS, Fe+I2==FeI2, Fe+2Fe3+==3Fe2+?2、Fe Fe3+强氧化剂:Cl2、Br2、KMnO4、HNO3等2Fe+3Cl2==2FeCl3, 2Fe+3Br2==2FeBr3,
Fe+4HNO3(稀)==Fe(NO3)3+NO↑+2H2O
2Fe+6H2SO4(浓)==Fe2(SO4)3+3SO2↑+6H2O
5Fe+3MnO4-+24H+== 5Fe3++3Mn2++12H2O?3、Fe2+ Fe3+Cl2、Br2、KMnO4、HNO3、O2等 2Fe2+ +Cl2==2Fe3++2Cl-
2Fe2+ +Br2==2Fe3++2Br-
5Fe2+ +MnO4-+8H+==5Fe3++Mn2++4H2O
3Fe2++4H++NO3-==Fe3++NO↑+2H2O4、 Fe3+ Fe2+Zn、Fe、Cu、H2S、HI、SO22Fe3++Zn(不足)==2Fe2++Zn2+ 2Fe3++Cu==2Fe2++Cu2+
2Fe3++H2S==2Fe2++2H++S↓
2Fe3++2HI==2Fe2++2H++I2
2Fe3++SO2+2H2O==2Fe2++4H++SO42-5、Fe2+ FeZn、H2、Al、C、CO等 Fe2++Zn==Fe+Zn2+ FeO+H2====Fe+H2O
3FeO+2Al====3Fe+Al2O3
2 FeO+C====Fe+CO2↑高温高温高温6、Fe3+ FeZn、CO、Al等 2Fe3++3Zn(过量)===2Fe+3Zn2+
Fe2O3+3CO====2Fe+3CO2
Fe2O3+2Al====2Fe+Al2O3
高温高温
