江苏省六合高级中学2008-2009学年度高二期终考试化学试题
文档属性
| 名称 | 江苏省六合高级中学2008-2009学年度高二期终考试化学试题 |
|
|
| 格式 | rar | ||
| 文件大小 | 75.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2009-02-03 00:00:00 | ||
图片预览


文档简介
江苏省六合高级中学2008/2009学年度期终考试
高二化学(必修)试题 2009.01.16
相对原子质量:H=1 C=12 N=14 O=16 Na=23 S=32 Cl=35.5
一、选择题(每小题只有一个正确选项)
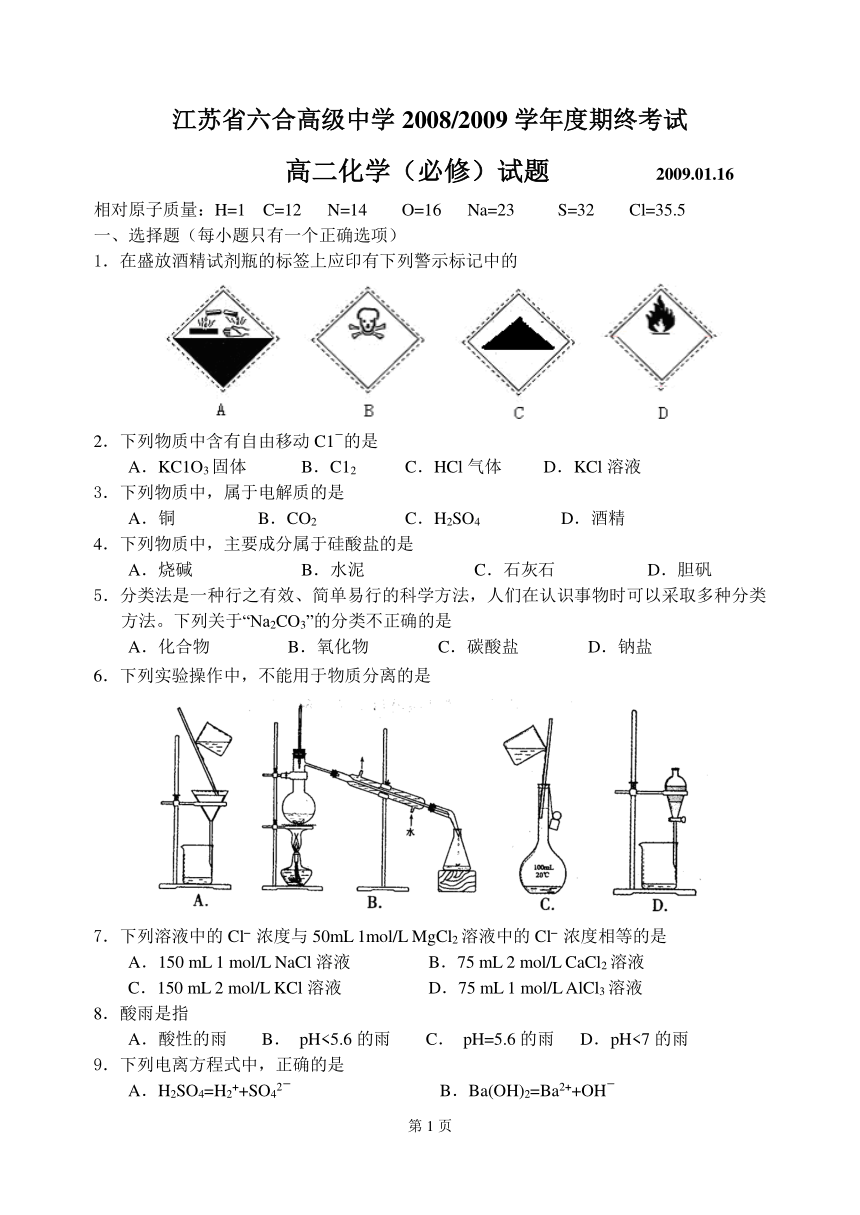
1.在盛放酒精试剂瓶的标签上应印有下列警示标记中的
2.下列物质中含有自由移动C1-的是
A.KC1O3固体 B.C12 C.HCl气体 D.KCl溶液
3.下列物质中,属于电解质的是
A.铜 B.CO2 ?? C.H2SO4 D.酒精
4.下列物质中,主要成分属于硅酸盐的是
A.烧碱 B.水泥 C.石灰石 D.胆矾
5.分类法是一种行之有效、简单易行的科学方法,人们在认识事物时可以采取多种分类方法。下列关于“Na2CO3”的分类不正确的是
A.化合物 B.氧化物 C.碳酸盐 D.钠盐
6.下列实验操作中,不能用于物质分离的是
7.下列溶液中的Cl( 浓度与50mL 1mol/L MgCl2溶液中的Cl( 浓度相等的是
A.150 mL 1 mol/L NaCl溶液 B.75 mL 2 mol/L CaCl2溶液
C.150 mL 2 mol/L KCl溶液 D.75 mL 1 mol/L AlCl3溶液
8.酸雨是指
A.酸性的雨 B. pH<5.6的雨 C. pH=5.6的雨 D.pH<7的雨
9.下列电离方程式中,正确的是
A.H2SO4=H2++SO42- B.Ba(OH)2=Ba2++OH-
C.NaNO3=Na++NO3- D.HClO=H++Cl-+O2-
10.下列食物中富含维生素C的是
A.食用油 B.蔗糖 C.西红柿 D.鸡蛋
11.下列产品所用的塑料,具有热固性的是
A.防水塑料手套 B.炒菜锅的手柄 C.雨衣 D.浴帽
12.对食物的酸、碱性判断正确的是
A.西瓜是酸性食物 B.猪肉、牛肉是碱性食物
C.大米、面包是碱性食物 D.巧克力、奶油是酸性食物
13.下列叙述正确的是
A.CH4的摩尔质量为16g B.3.01×1023个SO2分子的质量为32g
C.1 mol H2O的质量为18g/mol D.标准状况下,1 mol任何物质的体积约为22.4L
14.配制一定体积、一定物质的量浓度的溶液时,下列操作会使配得的溶液浓度偏大的是
A. 容量瓶未干燥
B. 溶液从烧杯转移到容量瓶中后没有洗涤烧杯
C.定容时观察液面俯视
D.定容时倒转容量瓶几次,发现凹液面最低点低于标线,再补几滴水到标线
15.下列反应属于氧化还原反应的是
A.H2SO4+2NaOH Na2SO4+2H2O
B.2NaHCO3 Na2CO3 + CO2↑ + H2O
C.NH3 + HCl NH4Cl
D.CuO + H2 Cu + H2O
16.钢铁发生吸氧腐蚀时,正极上发生的电极反应是:
A.2H+ + 2e- = H2↑ B.Fe – 2e- = Fe2+
C.2H2O + O2 + 4e- = 4OH- D.Fe – 3e- = Fe3+
17.下列离子在溶液中可以大量共存的一组是
A.H+ Na+ OH-? B.Na+ NO3- Cl-
C.K+ H+ HCO3- D.Ca2+ SO42- CO32-
18.下列化学方程式不能用离子方程式H+ + OH- == H2O表示的是
A.2NaOH +H2SO4 == Na2SO4 + 2H2O
B.Ba(OH)2 + 2HCl == BaCl2 + 2H2O
C.KOH + HCl == KCl + H2O
D.Cu(OH)2 + 2HNO3 == Cu(NO3)2 + 2H2O
19.下列食品添加剂与类别对应错误的是
A.调味剂——亚硝酸钠 B.防腐剂——苯甲酸钠
C.疏松剂——碳酸氢钠 D.着色剂——叶绿素
20.下列离子方程式书写正确的是
A.铁与稀硫酸反应: 2Fe + 6H+ = 2Fe3++3H2↑
B.氢氧化铜溶液与硫酸溶液的反应: Cu(OH)2 + 2H+ = Cu2++ 2H2O
C.碳酸钙与盐酸反应: CO32- +2H+ = H2O + CO2↑
D.硫酸铜溶液和氢氧化钡溶液: SO42- + Ba2+ = BaSO4↓
21.在反应3Cu+8HNO3 = 3Cu(NO3)2+ 2NO↑+4H2O中,氧化剂与还原剂物质的量之比是
A.3︰8 B.8︰3 C.2︰3 D.3︰2
22.量取100mL碘的饱和水溶液,倒入分液漏斗中,然后再注入4mL四氯化碳,用力振荡后静置,实验现象为
A.液体分层,上层为四氯化碳层且呈黄色 B.液体分层,上层为水层且呈紫色
C.液体分层,下层为四氯化碳层且呈紫色 D.液体分层,下层为水层且呈黄色
23.下列说法错误的是
A.钢板镀锌可以防止锈蚀
B.羊毛、蚕丝、棉花的主要成分都是纤维素
C.高纯石英玻璃可用来制造光导纤维
D.生铁和普通钢都是铁碳合金
请将选择题答案填入下列空格中
题号
1
2
3
4
5
6
7
8
9
10
11
12
答案
题号
13
14
15
16
17
18
19
20
21
22
23
答案
二、填空题
24.糖类、油脂、蛋白质都是人体必需的营养物质。
(1)油脂被摄入人体后,在酶的作用下水解为高级脂肪酸和_____________(写名称),进而被氧化生成二氧化碳和水并提供能量,或作为合成人体所需其他物质的原料。
(2)氨基酸是组成蛋白质的基本结构单元,其分子中一定含有的官能团是氨基(—NH2)和____________(写结构简式或名称)。人体中共有二十多种氨基酸,其中人体自身_______________(填“能”或“不能”)合成的氨基酸称为人体必需氨基酸。
(3)淀粉在淀粉酶的作用下最终水解为葡萄糖(C6H12O6),部分葡萄糖在体内被氧化生成二氧化碳和水。写出葡萄糖在体内被氧化的化学方程式:
________________________________________________。
25.取少量Fe2O3粉末(红棕色)加入适量盐酸,所发生反应的化学方程式:
。
反应后得到的FeCl3溶液呈棕黄色,用此溶液进行以下实验:
(1)取少量溶液置于试管中,滴入NaOH溶液,可观察到红褐色沉淀生成,反应的化学方程式为 ,此反应属于基本类型的 反应。
(2)在小烧杯中加入30mL蒸馏水,加热至沸腾后,向沸水中滴入2mL FeCl3溶液,继续加热至溶液呈 色,停止加热,即可制得Fe(OH)3胶体。
(3)取另一小烧杯加入30mL蒸馏水后,向烧杯中加入2mL FeCl3溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置暗处,分别用激光笔照射烧杯中的液体,可以看到 烧杯中的液体会产生丁达尔效应。这个实验可用来区别 。
26.实验室要配制0.5mol/L的NaOH溶液100mL,则:
(1)需要固体NaOH的质量是 ;
(2)用托盘天平称量NaOH固体时,必须把NaOH放在 仪器中称量;
(3)配制时还需要用到的仪器有 (填字母)
A.烧杯 B. 铁架台(带铁夹) C.100mL容量瓶
D. 50mL容量瓶 E.蒸馏烧瓶 F.胶头滴管 G.玻璃棒
(4)按实验先后顺序排列下列实验步骤 (填编号)
①将称量好的NaOH固体倒入烧杯中;
②往烧杯中倒入约20mL蒸馏水;
③将溶解并冷却后的NaOH溶液移入容量瓶;
④向容量瓶中加蒸馏水到液面离瓶颈刻度线下1~2cm;
⑤用适量蒸馏水洗涤烧杯和玻璃棒2~3次;
⑥将洗涤后的溶液也注入容量瓶中;
⑦盖好瓶塞,反复上下颠倒、摇匀;
⑧用胶头滴管滴加蒸馏水至液面与瓶颈刻度线相切。
27.已知在标准状况下,11.2L的HCl气体。回答下列问题:
(1)HCl的物质的量为多少?
(2)该气体用水全部吸收,并配制成2L的盐酸溶液,求HCl的物质的量浓度?
参考答案:
题号
1
2
3
4
5
6
7
8
9
10
11
12
答案
D
D
C
B
B
C
C
B
C
C
B
D
题号
13
14
15
16
17
18
19
20
21
22
23
答案
B
C
D
C
B
D
A
B
C
C
B
24、(1)甘油
(2)羧基 不能
(3)C6H12O6+6O2=6CO2+6H2O
25、Fe2O3+6HCl=2FeCl3+3H2O
FeCl3+3NaOH=Fe(OH)3+3NaCl
红褐
乙 胶体和溶液
26、(1)2g
(2) 玻璃
(3)A C F G
(4) 1 2 3 5 6 4 8 7
27、(1)0.5mol
(2)0.25mol/L
高二化学(必修)试题 2009.01.16
相对原子质量:H=1 C=12 N=14 O=16 Na=23 S=32 Cl=35.5
一、选择题(每小题只有一个正确选项)
1.在盛放酒精试剂瓶的标签上应印有下列警示标记中的
2.下列物质中含有自由移动C1-的是
A.KC1O3固体 B.C12 C.HCl气体 D.KCl溶液
3.下列物质中,属于电解质的是
A.铜 B.CO2 ?? C.H2SO4 D.酒精
4.下列物质中,主要成分属于硅酸盐的是
A.烧碱 B.水泥 C.石灰石 D.胆矾
5.分类法是一种行之有效、简单易行的科学方法,人们在认识事物时可以采取多种分类方法。下列关于“Na2CO3”的分类不正确的是
A.化合物 B.氧化物 C.碳酸盐 D.钠盐
6.下列实验操作中,不能用于物质分离的是
7.下列溶液中的Cl( 浓度与50mL 1mol/L MgCl2溶液中的Cl( 浓度相等的是
A.150 mL 1 mol/L NaCl溶液 B.75 mL 2 mol/L CaCl2溶液
C.150 mL 2 mol/L KCl溶液 D.75 mL 1 mol/L AlCl3溶液
8.酸雨是指
A.酸性的雨 B. pH<5.6的雨 C. pH=5.6的雨 D.pH<7的雨
9.下列电离方程式中,正确的是
A.H2SO4=H2++SO42- B.Ba(OH)2=Ba2++OH-
C.NaNO3=Na++NO3- D.HClO=H++Cl-+O2-
10.下列食物中富含维生素C的是
A.食用油 B.蔗糖 C.西红柿 D.鸡蛋
11.下列产品所用的塑料,具有热固性的是
A.防水塑料手套 B.炒菜锅的手柄 C.雨衣 D.浴帽
12.对食物的酸、碱性判断正确的是
A.西瓜是酸性食物 B.猪肉、牛肉是碱性食物
C.大米、面包是碱性食物 D.巧克力、奶油是酸性食物
13.下列叙述正确的是
A.CH4的摩尔质量为16g B.3.01×1023个SO2分子的质量为32g
C.1 mol H2O的质量为18g/mol D.标准状况下,1 mol任何物质的体积约为22.4L
14.配制一定体积、一定物质的量浓度的溶液时,下列操作会使配得的溶液浓度偏大的是
A. 容量瓶未干燥
B. 溶液从烧杯转移到容量瓶中后没有洗涤烧杯
C.定容时观察液面俯视
D.定容时倒转容量瓶几次,发现凹液面最低点低于标线,再补几滴水到标线
15.下列反应属于氧化还原反应的是
A.H2SO4+2NaOH Na2SO4+2H2O
B.2NaHCO3 Na2CO3 + CO2↑ + H2O
C.NH3 + HCl NH4Cl
D.CuO + H2 Cu + H2O
16.钢铁发生吸氧腐蚀时,正极上发生的电极反应是:
A.2H+ + 2e- = H2↑ B.Fe – 2e- = Fe2+
C.2H2O + O2 + 4e- = 4OH- D.Fe – 3e- = Fe3+
17.下列离子在溶液中可以大量共存的一组是
A.H+ Na+ OH-? B.Na+ NO3- Cl-
C.K+ H+ HCO3- D.Ca2+ SO42- CO32-
18.下列化学方程式不能用离子方程式H+ + OH- == H2O表示的是
A.2NaOH +H2SO4 == Na2SO4 + 2H2O
B.Ba(OH)2 + 2HCl == BaCl2 + 2H2O
C.KOH + HCl == KCl + H2O
D.Cu(OH)2 + 2HNO3 == Cu(NO3)2 + 2H2O
19.下列食品添加剂与类别对应错误的是
A.调味剂——亚硝酸钠 B.防腐剂——苯甲酸钠
C.疏松剂——碳酸氢钠 D.着色剂——叶绿素
20.下列离子方程式书写正确的是
A.铁与稀硫酸反应: 2Fe + 6H+ = 2Fe3++3H2↑
B.氢氧化铜溶液与硫酸溶液的反应: Cu(OH)2 + 2H+ = Cu2++ 2H2O
C.碳酸钙与盐酸反应: CO32- +2H+ = H2O + CO2↑
D.硫酸铜溶液和氢氧化钡溶液: SO42- + Ba2+ = BaSO4↓
21.在反应3Cu+8HNO3 = 3Cu(NO3)2+ 2NO↑+4H2O中,氧化剂与还原剂物质的量之比是
A.3︰8 B.8︰3 C.2︰3 D.3︰2
22.量取100mL碘的饱和水溶液,倒入分液漏斗中,然后再注入4mL四氯化碳,用力振荡后静置,实验现象为
A.液体分层,上层为四氯化碳层且呈黄色 B.液体分层,上层为水层且呈紫色
C.液体分层,下层为四氯化碳层且呈紫色 D.液体分层,下层为水层且呈黄色
23.下列说法错误的是
A.钢板镀锌可以防止锈蚀
B.羊毛、蚕丝、棉花的主要成分都是纤维素
C.高纯石英玻璃可用来制造光导纤维
D.生铁和普通钢都是铁碳合金
请将选择题答案填入下列空格中
题号
1
2
3
4
5
6
7
8
9
10
11
12
答案
题号
13
14
15
16
17
18
19
20
21
22
23
答案
二、填空题
24.糖类、油脂、蛋白质都是人体必需的营养物质。
(1)油脂被摄入人体后,在酶的作用下水解为高级脂肪酸和_____________(写名称),进而被氧化生成二氧化碳和水并提供能量,或作为合成人体所需其他物质的原料。
(2)氨基酸是组成蛋白质的基本结构单元,其分子中一定含有的官能团是氨基(—NH2)和____________(写结构简式或名称)。人体中共有二十多种氨基酸,其中人体自身_______________(填“能”或“不能”)合成的氨基酸称为人体必需氨基酸。
(3)淀粉在淀粉酶的作用下最终水解为葡萄糖(C6H12O6),部分葡萄糖在体内被氧化生成二氧化碳和水。写出葡萄糖在体内被氧化的化学方程式:
________________________________________________。
25.取少量Fe2O3粉末(红棕色)加入适量盐酸,所发生反应的化学方程式:
。
反应后得到的FeCl3溶液呈棕黄色,用此溶液进行以下实验:
(1)取少量溶液置于试管中,滴入NaOH溶液,可观察到红褐色沉淀生成,反应的化学方程式为 ,此反应属于基本类型的 反应。
(2)在小烧杯中加入30mL蒸馏水,加热至沸腾后,向沸水中滴入2mL FeCl3溶液,继续加热至溶液呈 色,停止加热,即可制得Fe(OH)3胶体。
(3)取另一小烧杯加入30mL蒸馏水后,向烧杯中加入2mL FeCl3溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置暗处,分别用激光笔照射烧杯中的液体,可以看到 烧杯中的液体会产生丁达尔效应。这个实验可用来区别 。
26.实验室要配制0.5mol/L的NaOH溶液100mL,则:
(1)需要固体NaOH的质量是 ;
(2)用托盘天平称量NaOH固体时,必须把NaOH放在 仪器中称量;
(3)配制时还需要用到的仪器有 (填字母)
A.烧杯 B. 铁架台(带铁夹) C.100mL容量瓶
D. 50mL容量瓶 E.蒸馏烧瓶 F.胶头滴管 G.玻璃棒
(4)按实验先后顺序排列下列实验步骤 (填编号)
①将称量好的NaOH固体倒入烧杯中;
②往烧杯中倒入约20mL蒸馏水;
③将溶解并冷却后的NaOH溶液移入容量瓶;
④向容量瓶中加蒸馏水到液面离瓶颈刻度线下1~2cm;
⑤用适量蒸馏水洗涤烧杯和玻璃棒2~3次;
⑥将洗涤后的溶液也注入容量瓶中;
⑦盖好瓶塞,反复上下颠倒、摇匀;
⑧用胶头滴管滴加蒸馏水至液面与瓶颈刻度线相切。
27.已知在标准状况下,11.2L的HCl气体。回答下列问题:
(1)HCl的物质的量为多少?
(2)该气体用水全部吸收,并配制成2L的盐酸溶液,求HCl的物质的量浓度?
参考答案:
题号
1
2
3
4
5
6
7
8
9
10
11
12
答案
D
D
C
B
B
C
C
B
C
C
B
D
题号
13
14
15
16
17
18
19
20
21
22
23
答案
B
C
D
C
B
D
A
B
C
C
B
24、(1)甘油
(2)羧基 不能
(3)C6H12O6+6O2=6CO2+6H2O
25、Fe2O3+6HCl=2FeCl3+3H2O
FeCl3+3NaOH=Fe(OH)3+3NaCl
红褐
乙 胶体和溶液
26、(1)2g
(2) 玻璃
(3)A C F G
(4) 1 2 3 5 6 4 8 7
27、(1)0.5mol
(2)0.25mol/L
同课章节目录
