胶体(浙江省绍兴市)
图片预览


文档简介
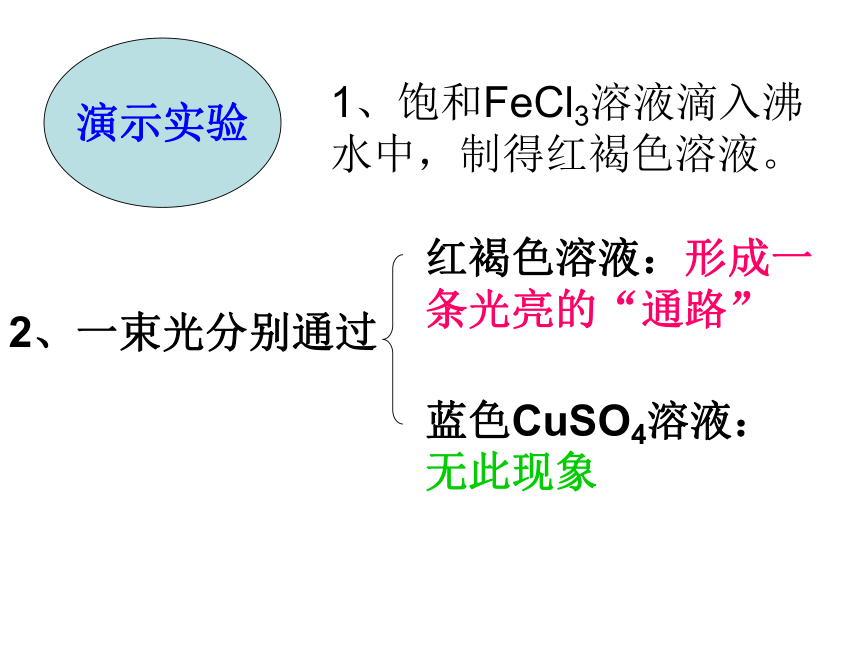
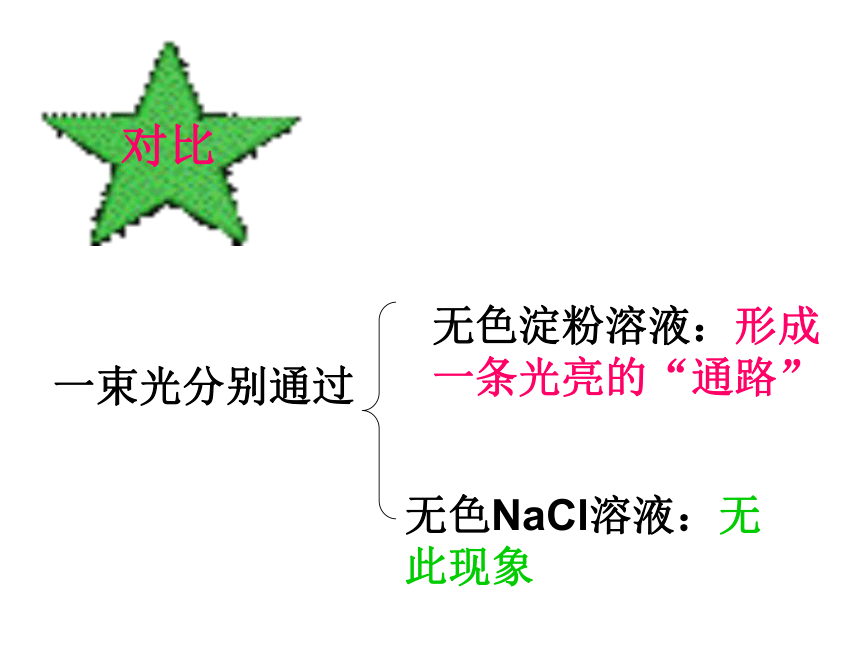
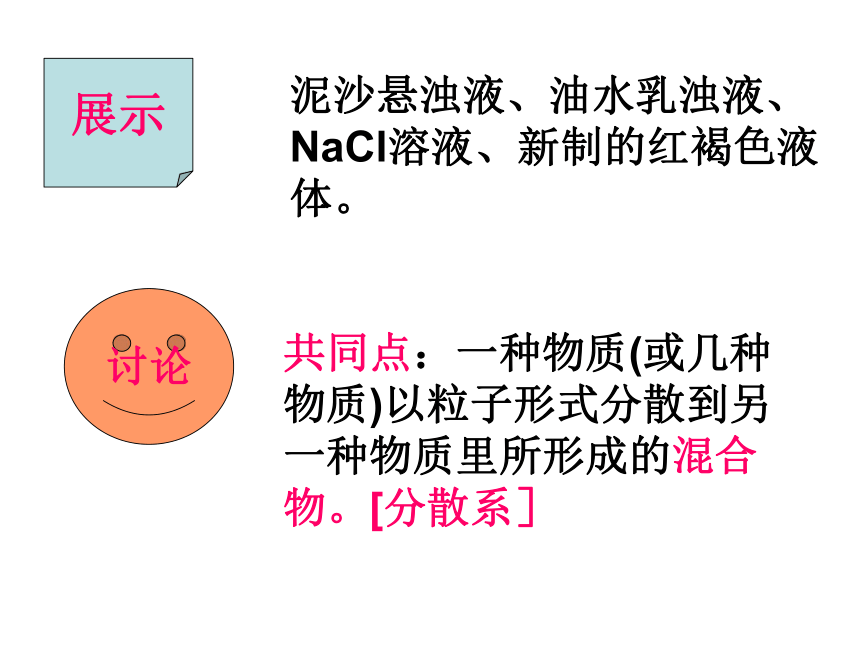
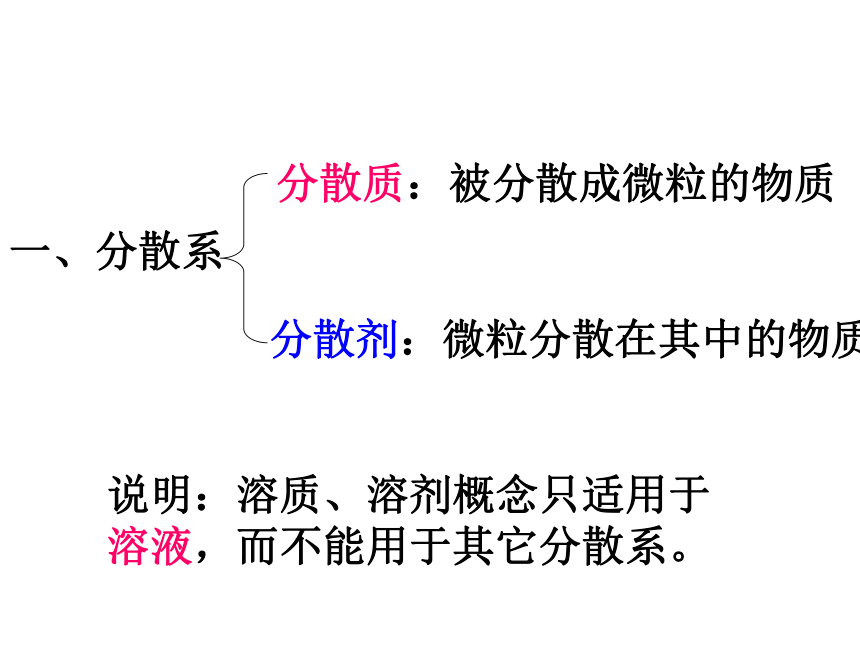
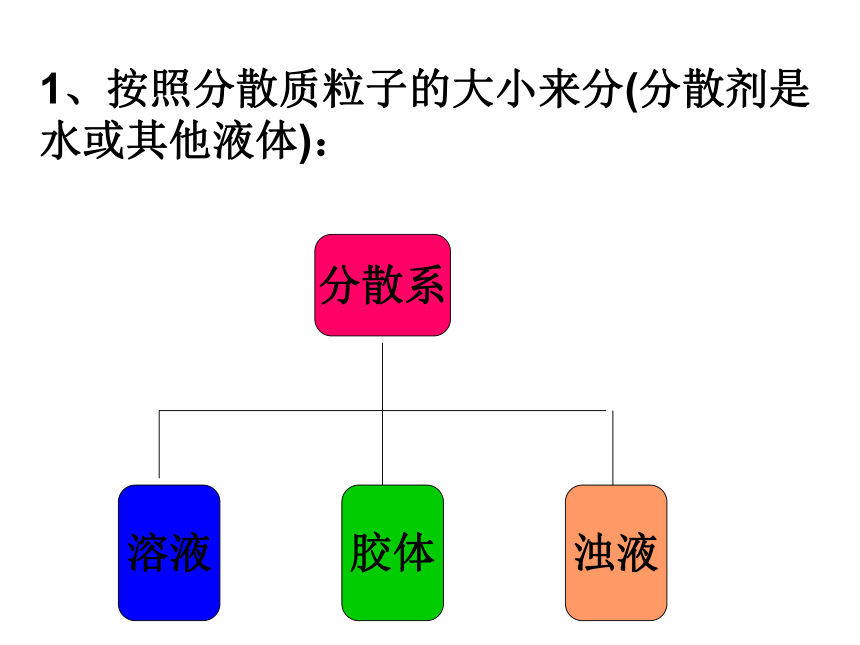
课件15张PPT。胶体演示实验1、饱和FeCl3溶液滴入沸水中,制得红褐色溶液。2、一束光分别通过红褐色溶液:形成一条光亮的“通路”蓝色CuSO4溶液:无此现象对比一束光分别通过无色淀粉溶液:形成一条光亮的“通路”无色NaCl溶液:无此现象 淀粉溶液及这种新制备的红褐色液体虽外观上均一、透明、与溶液一样,但在性质 上与溶液有区别,这种液体就是我们今天要学习的胶体。第一节 胶体 展示泥沙悬浊液、油水乳浊液、NaCl溶液、新制的红褐色液体。讨论共同点:一种物质(或几种物质)以粒子形式分散到另一种物质里所形成的混合物。[分散系]一、分散系分散质:被分散成微粒的物质分散剂:微粒分散在其中的物质说明:溶质、溶剂概念只适用于溶液,而不能用于其它分散系。1、按照分散质粒子的大小来分(分散剂是水或其他液体):分散系浊液胶体溶液2、按照分散质或分散剂所处的状态(气态、液态、固态),它们之间可以有9种组合方式。气液固固液气分散质分散剂2、胶体的定义:分散质粒子直径小于1nm的是溶液,大于100nm的是浊液。
分散质粒子直径在1nm~100nm之间的分散系叫胶体。按分散剂的不同,胶体可按下列方法分类。液溶胶:如Fe(OH)3胶体、淀粉胶体等。气溶胶:如雾、云、烟等。固溶胶:如有色玻璃等。
分散质粒子直径在1nm~100nm之间的分散系叫胶体。按分散剂的不同,胶体可按下列方法分类。液溶胶:如Fe(OH)3胶体、淀粉胶体等。气溶胶:如雾、云、烟等。固溶胶:如有色玻璃等。
