物质的分离和提纯(浙江省绍兴市)
图片预览








文档简介
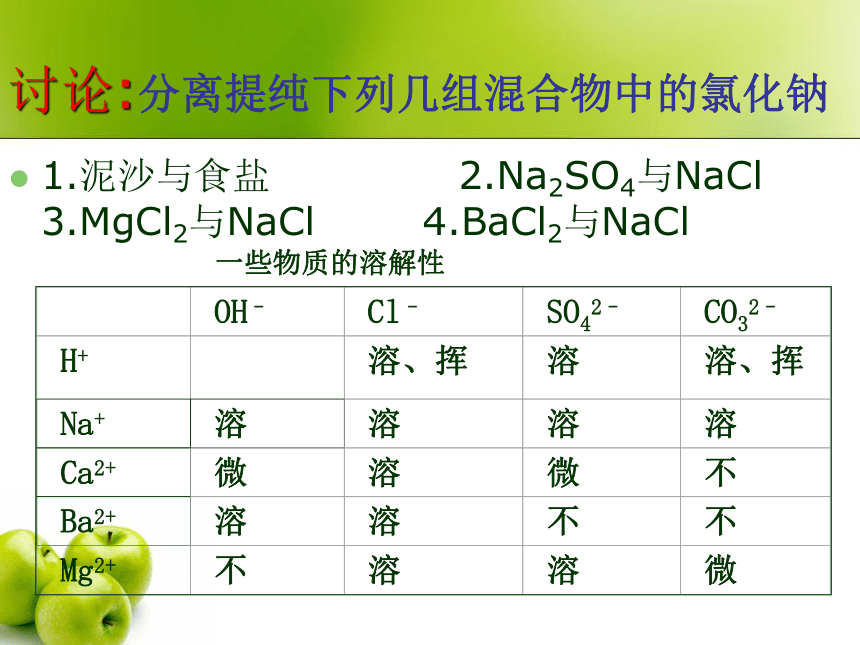
课件20张PPT。 讨论:分离提纯下列几组混合物中的氯化钠1.泥沙与食盐 2.Na2SO4与NaCl 3.MgCl2与NaCl 4.BaCl2与NaCl 一些物质的溶解性
交流与讨论已知氢氧化钠难溶于水,硫酸钡既难溶于水又难溶于酸,碳酸钡难溶于水,但可溶于盐酸.现有含硫酸钠.氯化镁和泥沙等杂质的粗食盐,请设计实验方案,由粗食盐提纯氯化钠(1)将粗盐溶解于水,过滤除去泥沙
(2)向所得滤液中加入稍过量的氯化钡溶液
(3)再加入稍过量的氢氧化钠和碳酸钠溶液
(4)过滤除去沉淀物
(5)在滤液中滴加稀盐酸至溶液显中性
(6)蒸发.结晶,得到精制的氯化钠晶体粗盐提纯方案二 操作原则“四原则”和“三必须”1“四原则”是:2“三必须”是:(1) 除杂试剂必须过量(2) 过量试剂必须除尽(因为过量试剂带入新的杂质)(3) 除杂途径必须选最佳氯化钾和硝酸钾混合物的分离方法1 将两者的混合物置于烧杯中,加少量100摄氏度热水,在加热的情况下不断少量加入热水并搅拌,直至混合物完全溶解
2 停止加热,冷却(可以用冰水水浴),当温度降至 30摄氏度时硝酸钾晶体析出。
3 过滤混合溶液得到较为纯净硝酸钾晶体 二 结晶1 原理: 利用溶剂对被提纯物质及杂质的溶解度不同,可以使被提纯物质从过饱和溶液中析出。而让杂质全部或大部分仍留在溶液中,从而达到提纯的目的。2 实验仪器:蒸发皿,酒精灯,玻璃棒,铁架台(铁圈),烧杯3 结晶方法:蒸发结晶冷却结晶蒸发结晶具体操作: 通过蒸发或气化,减少一部分溶剂使溶液达到饱和而析出晶体。适用物质: 此法主要用于溶解度随温度改变而变化不大的物质。(如氯化钠)冷却结晶具体操作: 通过降低温度,使溶液冷却达到饱和而析出晶体。重结晶指的是重复冷却结晶。适用物质: 此法主要用于溶解度随温度下降而明显减小的物质。(如硝酸钾)冷却结晶法: 若冷却时无晶体的析出,可用玻璃棒在容器内壁摩擦几下,或在溶液中投入几粒该晶体(俗称晶种),就会析出晶体。4 操作要点:蒸发结晶法:蒸发过程中要不断用玻璃棒搅拌蒸发皿内溶液不能超过其容量的2/3(1)生成沉淀法 例如NaCl溶液里混有少量的MgCl2杂质,可加入过量的NaOH溶液,使Mg2+离子转化为Mg(OH)2沉淀(但引入新的杂质OH-),过滤除去Mg(OH)2,然后加入适量盐酸,调节pH为中性。
(2)生成气体法 例如Na2SO4溶液中混有少量Na2CO3,为了不引入新的杂质并增加SO42-,可加入适量的稀H2SO4,将CO32-转化为CO2气体而除去。
(3)氧化还原法 例如在 FeCl3溶液里含有少量 FeCl2杂质,可通入适量的Cl2气将FeCl2氧化为FeCl3。若在 FeCl2溶液里含有少量 FeCl3,可加入适量的铁粉而将其除去。
(4)正盐和与酸式盐相互转化法 例如在Na2CO3固体中含有少量NaHCO3杂质,可将固体加热,使NaHCO3分解生成Na2CO3,而除去杂质。若在NaHCO3溶液中混有少量Na2CO3杂质,可向溶液里通入足量CO2,使Na2CO3转化为NaHCO3。对于无机物溶液常用下列方法进行分离和提纯三 蒸馏1 原理: 利用互溶的液体混合物中各组分的沸点不同,给液体混合物加热,使其中的某一组分变成蒸气再冷凝成液体,从而达到分离提纯的目的。蒸馏一般用于分离沸点相差较大的液体混合物。(例如蒸馏含有Fe3+的水提纯其中水份,蒸馏石油提纯不同沸点的有机组分) 2 实验仪器: 圆底烧瓶,水冷凝管,酒精灯,锥形瓶(接收器),牛角管,温度计,铁架台(铁圈、铁夹),石棉网等温度计水银球的顶端与支管下沿处于同一水平线蒸馏烧瓶中液体的量是烧瓶容量的1/3~1/2 在圆底烧瓶内放有沸石,防止爆沸冷凝管横放时头高尾
低保证冷凝液自然下
流,冷却水进水通入
与被冷凝蒸气流向相反给原底烧瓶加热要垫石棉网牛角管圆底烧瓶水冷凝管实验模拟4 思考:(1) 为什么冷却水通入方向与被冷凝蒸气流向相反为了使蒸馏出的蒸气与冷却水长时间充分接触,带走尽可能多的热量。四 萃取和分液1 原理:2 实验仪器:萃取:利用某溶质在互不相溶的溶剂中的溶解度不同,用一种溶剂把溶质从它与另一种溶剂组成的溶液中提取出来,在利用分液的原理和方法将它们分离开来。分液:把两种互不相溶的液体(且密度不同)分开的操作分液漏斗,铁架台(铁圈),烧杯3 操作要点:萃取:(1)选择的萃取剂,应对被提取物
有较大的溶解能力,而对杂质不溶
或微溶;跟原溶液的溶剂要互不相溶。(2)操作时先检验分液漏斗是否漏液。萃取溶液和萃取剂 总量不要超过漏斗容积的1/2。(4)静置后,当液体分成清晰的两层时分液。(3)振荡时,用右手掌压紧盖子,左手用
拇指、食指和中指握住活塞。把漏斗倒转过来振荡,如图。并不时旋开活塞,放出易挥发物质的蒸气。这样反复操作几次,当产生的气体很少时,再剧烈振荡几次,把漏斗放在漏斗架上静置。分液:静置到液体分成清晰的两层时开始分液。先把玻璃盖子取下,以便与大气相通。然后旋开活塞,使下层液体慢慢流入烧杯里,当下层液体恰好流尽时,迅速关上活塞。从漏斗口倒出上层液体。分液漏斗的液体量最多可达分液漏斗容量的2/3。 五 层析1 原理:2 实验仪器: 根据混合物中各物质被吸附性能的不同,将溶解在某溶剂中的混合物分离开来培养皿,吸附剂(如粉笔,层析纸等)3 应用举例:在距粉笔根部约2cm处滴一小滴红墨水,粉笔垂直竖立在盛有少量水的培养皿中(不能将粉笔上有红墨水的部分浸入水中) 用粉笔将红墨水中的红色物质分离开来
交流与讨论已知氢氧化钠难溶于水,硫酸钡既难溶于水又难溶于酸,碳酸钡难溶于水,但可溶于盐酸.现有含硫酸钠.氯化镁和泥沙等杂质的粗食盐,请设计实验方案,由粗食盐提纯氯化钠(1)将粗盐溶解于水,过滤除去泥沙
(2)向所得滤液中加入稍过量的氯化钡溶液
(3)再加入稍过量的氢氧化钠和碳酸钠溶液
(4)过滤除去沉淀物
(5)在滤液中滴加稀盐酸至溶液显中性
(6)蒸发.结晶,得到精制的氯化钠晶体粗盐提纯方案二 操作原则“四原则”和“三必须”1“四原则”是:2“三必须”是:(1) 除杂试剂必须过量(2) 过量试剂必须除尽(因为过量试剂带入新的杂质)(3) 除杂途径必须选最佳氯化钾和硝酸钾混合物的分离方法1 将两者的混合物置于烧杯中,加少量100摄氏度热水,在加热的情况下不断少量加入热水并搅拌,直至混合物完全溶解
2 停止加热,冷却(可以用冰水水浴),当温度降至 30摄氏度时硝酸钾晶体析出。
3 过滤混合溶液得到较为纯净硝酸钾晶体 二 结晶1 原理: 利用溶剂对被提纯物质及杂质的溶解度不同,可以使被提纯物质从过饱和溶液中析出。而让杂质全部或大部分仍留在溶液中,从而达到提纯的目的。2 实验仪器:蒸发皿,酒精灯,玻璃棒,铁架台(铁圈),烧杯3 结晶方法:蒸发结晶冷却结晶蒸发结晶具体操作: 通过蒸发或气化,减少一部分溶剂使溶液达到饱和而析出晶体。适用物质: 此法主要用于溶解度随温度改变而变化不大的物质。(如氯化钠)冷却结晶具体操作: 通过降低温度,使溶液冷却达到饱和而析出晶体。重结晶指的是重复冷却结晶。适用物质: 此法主要用于溶解度随温度下降而明显减小的物质。(如硝酸钾)冷却结晶法: 若冷却时无晶体的析出,可用玻璃棒在容器内壁摩擦几下,或在溶液中投入几粒该晶体(俗称晶种),就会析出晶体。4 操作要点:蒸发结晶法:蒸发过程中要不断用玻璃棒搅拌蒸发皿内溶液不能超过其容量的2/3(1)生成沉淀法 例如NaCl溶液里混有少量的MgCl2杂质,可加入过量的NaOH溶液,使Mg2+离子转化为Mg(OH)2沉淀(但引入新的杂质OH-),过滤除去Mg(OH)2,然后加入适量盐酸,调节pH为中性。
(2)生成气体法 例如Na2SO4溶液中混有少量Na2CO3,为了不引入新的杂质并增加SO42-,可加入适量的稀H2SO4,将CO32-转化为CO2气体而除去。
(3)氧化还原法 例如在 FeCl3溶液里含有少量 FeCl2杂质,可通入适量的Cl2气将FeCl2氧化为FeCl3。若在 FeCl2溶液里含有少量 FeCl3,可加入适量的铁粉而将其除去。
(4)正盐和与酸式盐相互转化法 例如在Na2CO3固体中含有少量NaHCO3杂质,可将固体加热,使NaHCO3分解生成Na2CO3,而除去杂质。若在NaHCO3溶液中混有少量Na2CO3杂质,可向溶液里通入足量CO2,使Na2CO3转化为NaHCO3。对于无机物溶液常用下列方法进行分离和提纯三 蒸馏1 原理: 利用互溶的液体混合物中各组分的沸点不同,给液体混合物加热,使其中的某一组分变成蒸气再冷凝成液体,从而达到分离提纯的目的。蒸馏一般用于分离沸点相差较大的液体混合物。(例如蒸馏含有Fe3+的水提纯其中水份,蒸馏石油提纯不同沸点的有机组分) 2 实验仪器: 圆底烧瓶,水冷凝管,酒精灯,锥形瓶(接收器),牛角管,温度计,铁架台(铁圈、铁夹),石棉网等温度计水银球的顶端与支管下沿处于同一水平线蒸馏烧瓶中液体的量是烧瓶容量的1/3~1/2 在圆底烧瓶内放有沸石,防止爆沸冷凝管横放时头高尾
低保证冷凝液自然下
流,冷却水进水通入
与被冷凝蒸气流向相反给原底烧瓶加热要垫石棉网牛角管圆底烧瓶水冷凝管实验模拟4 思考:(1) 为什么冷却水通入方向与被冷凝蒸气流向相反为了使蒸馏出的蒸气与冷却水长时间充分接触,带走尽可能多的热量。四 萃取和分液1 原理:2 实验仪器:萃取:利用某溶质在互不相溶的溶剂中的溶解度不同,用一种溶剂把溶质从它与另一种溶剂组成的溶液中提取出来,在利用分液的原理和方法将它们分离开来。分液:把两种互不相溶的液体(且密度不同)分开的操作分液漏斗,铁架台(铁圈),烧杯3 操作要点:萃取:(1)选择的萃取剂,应对被提取物
有较大的溶解能力,而对杂质不溶
或微溶;跟原溶液的溶剂要互不相溶。(2)操作时先检验分液漏斗是否漏液。萃取溶液和萃取剂 总量不要超过漏斗容积的1/2。(4)静置后,当液体分成清晰的两层时分液。(3)振荡时,用右手掌压紧盖子,左手用
拇指、食指和中指握住活塞。把漏斗倒转过来振荡,如图。并不时旋开活塞,放出易挥发物质的蒸气。这样反复操作几次,当产生的气体很少时,再剧烈振荡几次,把漏斗放在漏斗架上静置。分液:静置到液体分成清晰的两层时开始分液。先把玻璃盖子取下,以便与大气相通。然后旋开活塞,使下层液体慢慢流入烧杯里,当下层液体恰好流尽时,迅速关上活塞。从漏斗口倒出上层液体。分液漏斗的液体量最多可达分液漏斗容量的2/3。 五 层析1 原理:2 实验仪器: 根据混合物中各物质被吸附性能的不同,将溶解在某溶剂中的混合物分离开来培养皿,吸附剂(如粉笔,层析纸等)3 应用举例:在距粉笔根部约2cm处滴一小滴红墨水,粉笔垂直竖立在盛有少量水的培养皿中(不能将粉笔上有红墨水的部分浸入水中) 用粉笔将红墨水中的红色物质分离开来
