陕西省2009年高中学业水平考试模拟试题(三)
文档属性
| 名称 | 陕西省2009年高中学业水平考试模拟试题(三) |

|
|
| 格式 | zip | ||
| 文件大小 | 551.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2009-02-10 00:00:00 | ||
图片预览




文档简介
陕西省2009年高中学业水平考试模拟试题
化 学(三)
考生注意:
1.本试卷分第一部分(选择题)和第二部分(非选择题)两部分。满分100分,考试时间90分钟。
2.请将第一部分的答案填写在第二部分相应的答题栏内,交卷时只交第二部分。
可能用到的相对原子质量: H—1 C—12 N—14 O—16 Na—23 Al—27
S—32 Cl—35.5 Fe—56 Cu—64
第一部分(选择题 共50分)
一、选择题(本题包括10小题,每小题2分,计20分。每小题只有一个正确答案,多选、不选或错选均不给分)
1. 作为新世纪的年轻公民都应具有一定的化学科学素养,否则,在工作和生活中就可能闹笑话。下列有关媒体的报道与化学知识不相违背的是
A.这种人工皂不含任何化学物质
B.该科研人员发明了一种特殊催化剂,可以使水变为汽油
C.有关部门利用明矾对饮用水进行消毒杀菌,从而解决了灾民饮水难的问题
D.该科研机构发明了一种用植物秸秆生产乙醇的新工艺
2. 下列有关试剂的保存方法,错误的是
A. 少量的钠保存在煤油中
B. 浓硝酸保存在无色玻璃试剂瓶中
C. 氢氧化钠溶液保存在具橡皮塞的玻璃试剂瓶中
D. 新制的氯水通常保存在棕色玻璃试剂瓶中
3. 美国科学家用某有机分子和球形笼状分子C60制成了“纳米车”(如右下图所示),每辆“纳米车”是由一个有机分子和4个C60分子构成。“纳米车”可以用来运输单个的有机分子。下列说法正确的是
A.人们用肉眼可以清晰看到“纳米车”的运动
B.“纳米车”的诞生说明人类操纵分子的技术进入了一个新阶段
C.C60是一种新型的化合物
D.C60与金刚石互为同分异构体
4. “厨房化学”是指利用家庭生活用品来进行化学实验,从而对化学进行学习和探究的活动。下列实验在厨房中不能完成的是
A.检验鸡蛋壳中含有碳酸盐 B.检验蛋白质在加热条件下能发生变性
C.检验加碘食盐中不含碘单质 D.检验自来水中含有Cl—离子
5. 糖类、油脂、蛋白质为动物性和植物性食物中的基本营养物质。下列有关说法正确的是
A.蛋白质中只含C、H、O三种元素
B.油脂在人体中发生水解的产物是氨基酸
C.糖类的主要成分是高级脂肪酸甘油酯
D.糖类、油脂、蛋白质都能发生水解反应
6. 下列化学用语书写正确的是
A.氯原子的结构示意图:
B.作为相对原子质量测定标准的碳核素:C
C.氯化镁的电子式:
D.用电子式表示氯化氢分子的形成过程:
7. 根据我省气象中心报道,近年每到秋冬季,关中大部地区曾多次出现大雾天气,致使高速公路关闭,航班停飞。雾属于下列分散系中的
A.溶液 B.悬浊液 C.乳浊液 D.胶体
8. 北京2008奥运会金牌直径为70mm,厚6mm。某化学兴趣小组对金牌成分提出猜想:甲认为金牌是由纯金制造;乙认为金牌是由金银合金制成;丙认为金牌是由黄铜(铜锌合金)。为了验证他们的猜想,请你选择一种试剂来证明甲、乙、丙猜想的正误
A.硫酸铜溶液 B.盐酸 C.稀硝酸 D.硝酸银溶液
9. 下列描述中不正确的是 A.14N与15N具有相同的质子数 B.18O与17O具有相同的电子数
C.19 O与19F具有相同的中子数 D.40K与40Ca具有相同的质量数
10. 在2A(g)+B(g)3C(g)+4D(g)中,下列情况能够降低该反应速率的是
A.升高温度 B.减小压强 C.使用催化剂 D.增大A的浓度
二、选择题(本题包括10小题,每小题3分,计30分。每小题只有一个正确答案,多选、不选或错选均不给分)
11. 既能与盐酸反应又能与NaOH溶液反应的一组物质是
①Al ②Al2O3 ③Al(OH)3 ④NaHCO3
A. ②④ B. ①② C. ①②③ D. ①②③④
12. 元素X的单质及X与Y形成的化合物能按如下图所示的关系发生转化。则X为
A.Fe
B.Cu
C.S
D.C
13. 下列离子方程式中,错误的是
A.钠与水反应:Na+H2O=Na++OH-+H2↑
B.盐酸与氢氧化钾溶液反应:H++OH-=H2O
C.铁与稀硫酸反应:Fe+2H+=Fe2++H2↑
D.氯化钠溶液与硝酸银溶液反应:Ag++Cl-=AgCl↓
14. 下列有关环境保护的说法中错误的是
A、含氮、磷化合物的生活污水大量排放可使水体富营养化
B、各国工业大量排放二氧化硫是全球气候变暖的主要原因
C、劣质装修材料中的甲醛、苯、氡气等对人体有害
D、废旧电池中的汞、镉、铅等重金属盐对土壤和水源会造成污染
15. 巴豆酸的结构简式为CH3CH=CHCOOH ,现有①水;②溴的四氯化碳溶液;③乙醇;④纯碱溶液;⑤酸性KMnO4溶液,在一定条件下,能与巴豆酸反应的物质组合是
A.只有②④⑤ B.只有②③⑤ C.只有②③④⑤ D.①②③④⑤
16. 加成反应是有机化合物分子中双键上的碳原子与其他原子(或原子团)直接结合生成新的化合物分子的反应,下列过程与加成反应无关的是
A.苯与溴水混合振荡,水层颜色变浅
B.裂化汽油与溴水混合振荡,水层颜色变浅
C.乙烯与水在一定条件下反应制取乙醇
D.乙烯与氯化氢在一定条件下反应制取氯乙烷
17. 用右图表示的一些物质或概念间的从属关系中不正确的是
X Y Z
例 氧化物 化合物 纯净物
A 甲烷 烷烃 烃
B 胶体 分散系 混合物
C 电解质 离子化合物 化合物
D 碱性氧化物 金属氧化物 氧化物
18. 有A、B、C、D四块金属片,进行如下实验:①A、B用导线相连后,同时浸入稀硫酸中,A极为负极;②C、D用导线相连后,同时浸入稀硫酸中,电流由D→导线→C;③B、C相连后,同时浸入稀硫酸中,C极产生大量气泡;④B、D相连后,同时浸入稀硫酸中,D极产生大量气泡。据此,判断四种金属的活动性顺序是
A.A>B>C>D B.A>C>D>B
C.C>A>B>D D.B>D>C>A
19. 下列对硫酸的叙述正确的是
A.因浓硫酸具有强氧化性,故不可用它来干燥氢气
B.浓硫酸不活泼,可用铁铝容器存放
C.浓硫酸有强氧化性,稀硫酸不具有氧化性
D.浓硫酸具有腐蚀性,取用时要小心
20. 将钠、镁、铝各0.3mol分别放入 100mL 1mol/L盐酸中,同温同压下产生气体的体积比是
A、1:2:3 B、6:3:2 C、3:1:1 D、1:1:1
陕西省2009年高中学业水平考试模拟试题(卷)
化 学(三)
题 号 1 2 3 4 5 6 7 8 9 10
答 案
题 号 11 12 13 14 15 16 17 18 19 20
答 案
题 号 第一部分 第二部分 总 分
1—20 必答题 选答题
得 分
第二部分 (非选择题 共50分)
得 分 评卷人
三、必答题(本题包括5小题,计30分)
21. (6分)X、 Y、 Z三种短周期元素, X原子半径是所有元素中最小的,Y的最外层电子数比次外层多4个电子,Z的化合物进行焰色反应时火焰为黄色;又知Z、Y形成甲、乙两种固体化合物,乙中Z和Y的原子数比为1:1。则:
⑴X、Y、Z分别为:X__ ____、Y__ ____、Z__ ____;
⑵甲、乙化学式分别为______ ____;
⑶Z的原子结构示意图为________________________________。
22. (4分)乙醇是生活中常见的一种有机物,它的分子结构模型如右图所示:
(1)乙醇中的“-OH”原子团的名称是 ;
(2)一定条件下,乙醇能与乙酸反应生成一种具有香味的油状液体,该有机反应的类型是 反应;
(3)工业上可用乙烯与水反应来生成酒精,请写出该反应的化学方程式(不必写反应条件) 。
23. (7分)我国化工专家侯德榜发明的侯氏制碱法的化学原理是将二氧化碳通入氨水的氯化钠饱和溶液中,其化学反应方程式为:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl。
⑴在实验室中利用上述原理从反应所得溶液中分离出碳酸氢钠晶体,应选用下列装置中的 ,该装置使用的玻璃仪器有______________________________。
A B C D
⑵实验所得碳酸氢钠晶体中,可能含有的杂质离子有Cl—和NH4+,实验室鉴定Cl—所选用的试剂是 、 ,鉴定另一种杂质离子的方法是 。
⑶碳酸氢钠晶体受热分解可得到纯碱,其化学反应方程式为 ,请你设计一个简单的实验方案,判断碳酸氢钠晶体受热分解后所得固体中是否仍然含有碳酸氢钠: 。
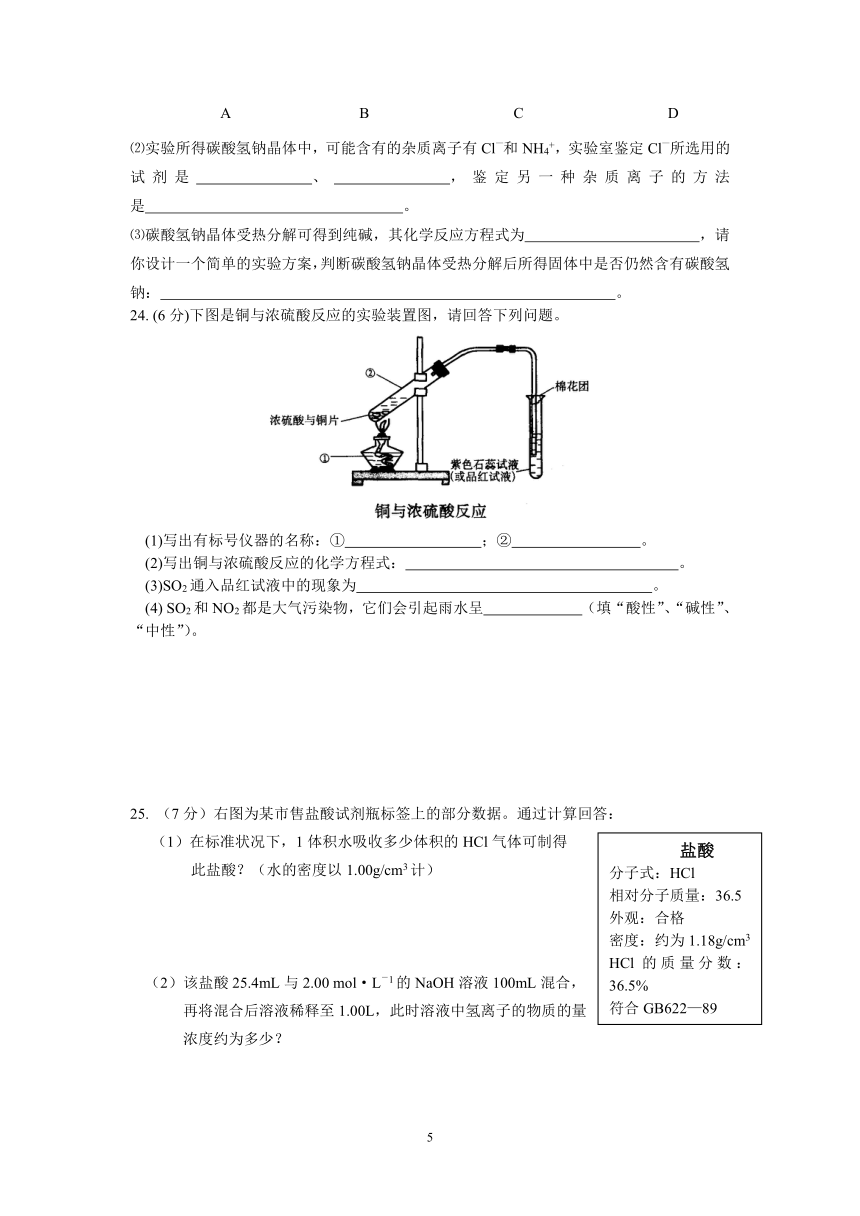
24. (6分)下图是铜与浓硫酸反应的实验装置图,请回答下列问题。
(1)写出有标号仪器的名称:① ;② 。
(2)写出铜与浓硫酸反应的化学方程式: 。
(3)SO2通入品红试液中的现象为 。
(4) SO2和NO2都是大气污染物,它们会引起雨水呈 (填“酸性”、“碱性”、“中性”)。
25. (7分)右图为某市售盐酸试剂瓶标签上的部分数据。通过计算回答:
(1)在标准状况下,1体积水吸收多少体积的HCl气体可制得
此盐酸?(水的密度以1.00g/cm3计)
(2)该盐酸25.4mL与2.00 mol·L-1的NaOH溶液100mL混合,
再将混合后溶液稀释至1.00L,此时溶液中氢离子的物质的量
浓度约为多少?
得 分 评卷人
四、选答题(本题分三个模块,每个模块包括3道小题,计20分。考生任选一个模块作答,不跨模块计分。)
化学与生活(选修模块)
26. (6分)(1)如下图所示,铁处于Ⅰ、Ⅱ、Ⅲ三种不同的环境中,铁被腐蚀的速率由大到小的顺序是(填序号) 。
(2)氯代烷是一种能破坏臭氧层的物质。在大气平流层中,氟氯代烷受紫外线的照射分解出氯原子,氯原子参与下列有关反应:
①C+O3→ClO+O2 ②O3O+O2 ③ClO→Cl+O2
上列反应的总反应式是 ,少量氟氯代烷能破坏大量臭氧的原因是 。
27. (8分)生活处处有化学,化学与生产、生活密切相关。请回答:
(1)经科学测定,人体平均含氧65%,含碳18%,含氢10%(以上均为质量分数),则三种元素中原子数目最多的是 (填元素符号)。
(2)为验证某易拉罐材质的主要成分是铁制还是铝制,如用物理方法验证,一般用 即可;如用化学方法验证,可使用的化学试剂为 。
(3)据报道,全世界每年因金属腐蚀造成的直接经济损失约达7000亿美元,我国因金属腐蚀造成的损失占国民生产总值(GNP)的4%。钢铁在潮湿的空气中发生电化学腐蚀时,负极的电极反应式为 。
(4)天然橡胶主要成分的结构简式是 。橡胶硫化的目的是使线型橡胶分子之间通过硫桥交联起来,形成 ,从而改善橡胶的性能。
28. (6分)阿司匹林的结构简式为 ,试根据阿司匹林的结构回答下列问题:
①阿司匹林看成酯类物质,口服后,在胃肠中酶的作用下,阿司匹林发生水解反应生成A
和B两种物质。其中A的结构简式为 ,则B的结构简式为 ;B中含有的官能团是 (填名称)
②上述水解产物A与氢氧化钠溶液反应的化学方程式为
化学反应原理(选修模块)
26. (共5分)
(1)1g碳与适量水蒸气反应生成CO和H2,需吸收10.94KJ热量,此反应的热化学方程式为
(2)已知CH4(g)+2O2(g)== CO2(g)+2H2O(l);ΔH=-Q1kJ·mol-1 ,
=2H2O(g);△H2=-Q2 kJ·,
=2H2O(l);△H2=-Q3 kJ·。
常温下,取体积比4∶1的甲烷和氢气的混合气体11.2L(标准状况下),经完全燃烧后恢复至室温,则放出的热量为 。
27. (7分)将气体A、B置于容积为2L的密闭容器,发生如下反应:
4A(g)+B(g)=2C(g)
反应进行到4S末,测得A为0.5mol,B为0.4mol,C为0.2mol,
(1)则vA= _____________ vB= _________________ vC= ______________
(2)反应前A有 ___ mol,反应前B有 _____ mol
28. (8分)如图所示是电解氯化钠溶液(含酚酞)的装置。有毒气体收集的装置省略没有画出,两电极均是惰性电极。
⑴a电极的名称 。
⑵电解过程中观察到的现象 。
⑶确定N出口的气体最简单的方法是 。
⑷电解的总反应离子方程式为 。
有机化学基础(选修模块)
26. (6分)某芳香族化合物的分子式为C7H8O,根据下列实验现象确定其结构简式:
(1)不能与金属钠反应,其结构简式的_____________ ______________。
(2)能与钠反应,但遇FeCl3不显色______________ __ __ __________。
(3)能与钠反应且遇FeCl3显紫色__________________ ____________。
27. (6分)现有6种有机物:①乙烯 ②苯 ③乙醇 ④乙醛 ⑤乙酸 ⑥乙酸乙酯。
按下列要求填写下列空格(填写序号):
(1)具有酸的通性的是 ;
(2)在一定条件下,能发生银镜反应的是 ;
(3)在一定条件下,能发生酯化反应的是 ;
(4)在一定条件下,既能使溴水褪色,又能使酸性高锰酸钾溶液褪色,还能发生加聚反应的是 ;
(5)在一定条件下,既可发生加成反应,又可发生取代反应的烃是 ;
(6)在一定条件下,能发生水解反应的是 。
28. (8分)现有A、B、C、D、E、F五种有机物,它们的转化关系如下图所示(图中部分反应条件及生成物没有全部写出)。已知:液体B能发生银镜反应,气体D的相对分子质量为28。
请回答下列问题:
⑴A、B、C的结构简式分别是 、 、 。
⑵C→A的反应物及反应条件是 。
⑶D→F反应的化学方程式是 。
⑷在一定的条件下,A与E反应可生成一种具有香味的物质。该反应的化学方程式
是 。
参考答案:
一、选择题(每小题2分,计20分)
1~5 DBBDD 6~10 CDCCB
二、选择题(每小题3分,计30分)
11~15DAABD 16~20 ACADC
三、必答题(本题包括5小题,计30分)
21.(6分)⑴ H、O、Na (各1分)
⑵ Na2O、Na2O2 (各1分) ⑶ 略 (1分)
22.(4分)(1)羟基 (2)取代(酯化) (3)CH2=CH2+ H2O→CH3CH2OH
23.(7分)⑴B 烧杯、漏斗、玻璃棒(2分)
⑵AgNO3溶液 稀HNO3 取少量固体与强碱溶液混合加热,生成的气体用湿润的红色石蕊试纸检验(3分)
⑶2NaHCO3Na2CO3+CO2↑+H2O 取所得固体,继续加热,将生成的气体通入澄清石灰水,若变浑浊,说明含有碳酸氢钠(2分)
24.(6分)⑴①酒精灯 ②试管
⑵Cu+2H2SO4==CuSO4+SO2↑+2H2O(加热条件)(2分)
⑶品红试液褪色
⑷酸性
25.(7分)(1) (VHCl / 22.4L · mol-1)×36.5g · mol-1
(VHCl / 22.4L · mol-1)×36.5g · mol-1 + 1000g
V(HCl )= 353 L 3分
(2)此盐酸的物质的量的浓度为
C(HCl) = = 11.8mol · L-1
2分
与NaOH溶液混合后溶液中的氢离子浓度为:
C(H+ )= ≈0.100 mol · L-1
2分
四、选答题(本题包括3小题,计20分)
化学与生活(选修模块)(共20分)
26.(6分)(1)I、Ⅲ、Ⅱ (I > Ⅲ > Ⅱ或Ⅱ < Ⅲ < I,其它写法不得分,写阿拉伯数字不得分)
(2分)
(2)2O3 3O2 (2分)
方程式书写正确得1分
条件答对(条件只能写“Cl”或“氯原子”,其它答案均不给分)得1分
(3)答案中出现“氯原子(Cl)是催化剂”或“氯原子(Cl)起催化作用”才能得分,如写中文字“氯”是催化剂,不给分。 (2分)
27.(8分)(1)H (2)磁铁是否能吸引 氢氧化钠溶液 (3)Fe-2e—=Fe2+ (2分)
(4) (2分) 网状结构
28.(6分)①CH3COOH (2分) 羧基 (2分)
② (2分)
+ 2NaOH → 2H2O +
化学反应原理(选修模块)(共20分)
26.(共5分)(1)C(S)+H2O(g) == CO(g) +H2(g) ΔH= +131.28 kJ·(2分)
(2)0.4Q1+0.05Q2(3分)
27.(5分)(1)(每空1分)0.05 mol/(L.S) , 0.0125 mol/(L.S) 0.025 mol/(L.S)
(2)(各2分)0.9 ,0.5
28.(8分每空2分) (1)阴极
(2)两极均有气泡产生;a极区溶液变成红色;b极液面上气体变为黄绿色;b极区溶液变为浅黄绿色。
(3)用湿润的淀粉碘化钾试纸检验,试纸变蓝则说明是Cl2。
有机化学基础(选修模块)(共20分)
26. (6分)
27. (6分)⑤;④;③⑤;①;②;⑥.
28. (9分)(1)CH3CH2OH CH3CHO CH3CH2Br(3分)
(2)NaOH的乙醇溶液,加热(2分)
(3) (1分)
(4) (2分)
X
XY2
XY3
置换
化合
化合
化合
X
Y
Z
盐酸
分子式:HCl
相对分子质量:36.5
外观:合格
密度:约为1.18g/cm3
HCl的质量分数:36.5%
符合GB622—89
COOH
OOCCH3
COOH
OH
= 36.5%
1000mL·L-1 ×1.18g · mL-1×36.5%
36.5g · mol-1
0.0254L×11.8mol · L-1 – 0.100L×2.00 mol · L-1
1.00L
Cl
COONa
ONa
COOH
OH
PAGE
1
化 学(三)
考生注意:
1.本试卷分第一部分(选择题)和第二部分(非选择题)两部分。满分100分,考试时间90分钟。
2.请将第一部分的答案填写在第二部分相应的答题栏内,交卷时只交第二部分。
可能用到的相对原子质量: H—1 C—12 N—14 O—16 Na—23 Al—27
S—32 Cl—35.5 Fe—56 Cu—64
第一部分(选择题 共50分)
一、选择题(本题包括10小题,每小题2分,计20分。每小题只有一个正确答案,多选、不选或错选均不给分)
1. 作为新世纪的年轻公民都应具有一定的化学科学素养,否则,在工作和生活中就可能闹笑话。下列有关媒体的报道与化学知识不相违背的是
A.这种人工皂不含任何化学物质
B.该科研人员发明了一种特殊催化剂,可以使水变为汽油
C.有关部门利用明矾对饮用水进行消毒杀菌,从而解决了灾民饮水难的问题
D.该科研机构发明了一种用植物秸秆生产乙醇的新工艺
2. 下列有关试剂的保存方法,错误的是
A. 少量的钠保存在煤油中
B. 浓硝酸保存在无色玻璃试剂瓶中
C. 氢氧化钠溶液保存在具橡皮塞的玻璃试剂瓶中
D. 新制的氯水通常保存在棕色玻璃试剂瓶中
3. 美国科学家用某有机分子和球形笼状分子C60制成了“纳米车”(如右下图所示),每辆“纳米车”是由一个有机分子和4个C60分子构成。“纳米车”可以用来运输单个的有机分子。下列说法正确的是
A.人们用肉眼可以清晰看到“纳米车”的运动
B.“纳米车”的诞生说明人类操纵分子的技术进入了一个新阶段
C.C60是一种新型的化合物
D.C60与金刚石互为同分异构体
4. “厨房化学”是指利用家庭生活用品来进行化学实验,从而对化学进行学习和探究的活动。下列实验在厨房中不能完成的是
A.检验鸡蛋壳中含有碳酸盐 B.检验蛋白质在加热条件下能发生变性
C.检验加碘食盐中不含碘单质 D.检验自来水中含有Cl—离子
5. 糖类、油脂、蛋白质为动物性和植物性食物中的基本营养物质。下列有关说法正确的是
A.蛋白质中只含C、H、O三种元素
B.油脂在人体中发生水解的产物是氨基酸
C.糖类的主要成分是高级脂肪酸甘油酯
D.糖类、油脂、蛋白质都能发生水解反应
6. 下列化学用语书写正确的是
A.氯原子的结构示意图:
B.作为相对原子质量测定标准的碳核素:C
C.氯化镁的电子式:
D.用电子式表示氯化氢分子的形成过程:
7. 根据我省气象中心报道,近年每到秋冬季,关中大部地区曾多次出现大雾天气,致使高速公路关闭,航班停飞。雾属于下列分散系中的
A.溶液 B.悬浊液 C.乳浊液 D.胶体
8. 北京2008奥运会金牌直径为70mm,厚6mm。某化学兴趣小组对金牌成分提出猜想:甲认为金牌是由纯金制造;乙认为金牌是由金银合金制成;丙认为金牌是由黄铜(铜锌合金)。为了验证他们的猜想,请你选择一种试剂来证明甲、乙、丙猜想的正误
A.硫酸铜溶液 B.盐酸 C.稀硝酸 D.硝酸银溶液
9. 下列描述中不正确的是 A.14N与15N具有相同的质子数 B.18O与17O具有相同的电子数
C.19 O与19F具有相同的中子数 D.40K与40Ca具有相同的质量数
10. 在2A(g)+B(g)3C(g)+4D(g)中,下列情况能够降低该反应速率的是
A.升高温度 B.减小压强 C.使用催化剂 D.增大A的浓度
二、选择题(本题包括10小题,每小题3分,计30分。每小题只有一个正确答案,多选、不选或错选均不给分)
11. 既能与盐酸反应又能与NaOH溶液反应的一组物质是
①Al ②Al2O3 ③Al(OH)3 ④NaHCO3
A. ②④ B. ①② C. ①②③ D. ①②③④
12. 元素X的单质及X与Y形成的化合物能按如下图所示的关系发生转化。则X为
A.Fe
B.Cu
C.S
D.C
13. 下列离子方程式中,错误的是
A.钠与水反应:Na+H2O=Na++OH-+H2↑
B.盐酸与氢氧化钾溶液反应:H++OH-=H2O
C.铁与稀硫酸反应:Fe+2H+=Fe2++H2↑
D.氯化钠溶液与硝酸银溶液反应:Ag++Cl-=AgCl↓
14. 下列有关环境保护的说法中错误的是
A、含氮、磷化合物的生活污水大量排放可使水体富营养化
B、各国工业大量排放二氧化硫是全球气候变暖的主要原因
C、劣质装修材料中的甲醛、苯、氡气等对人体有害
D、废旧电池中的汞、镉、铅等重金属盐对土壤和水源会造成污染
15. 巴豆酸的结构简式为CH3CH=CHCOOH ,现有①水;②溴的四氯化碳溶液;③乙醇;④纯碱溶液;⑤酸性KMnO4溶液,在一定条件下,能与巴豆酸反应的物质组合是
A.只有②④⑤ B.只有②③⑤ C.只有②③④⑤ D.①②③④⑤
16. 加成反应是有机化合物分子中双键上的碳原子与其他原子(或原子团)直接结合生成新的化合物分子的反应,下列过程与加成反应无关的是
A.苯与溴水混合振荡,水层颜色变浅
B.裂化汽油与溴水混合振荡,水层颜色变浅
C.乙烯与水在一定条件下反应制取乙醇
D.乙烯与氯化氢在一定条件下反应制取氯乙烷
17. 用右图表示的一些物质或概念间的从属关系中不正确的是
X Y Z
例 氧化物 化合物 纯净物
A 甲烷 烷烃 烃
B 胶体 分散系 混合物
C 电解质 离子化合物 化合物
D 碱性氧化物 金属氧化物 氧化物
18. 有A、B、C、D四块金属片,进行如下实验:①A、B用导线相连后,同时浸入稀硫酸中,A极为负极;②C、D用导线相连后,同时浸入稀硫酸中,电流由D→导线→C;③B、C相连后,同时浸入稀硫酸中,C极产生大量气泡;④B、D相连后,同时浸入稀硫酸中,D极产生大量气泡。据此,判断四种金属的活动性顺序是
A.A>B>C>D B.A>C>D>B
C.C>A>B>D D.B>D>C>A
19. 下列对硫酸的叙述正确的是
A.因浓硫酸具有强氧化性,故不可用它来干燥氢气
B.浓硫酸不活泼,可用铁铝容器存放
C.浓硫酸有强氧化性,稀硫酸不具有氧化性
D.浓硫酸具有腐蚀性,取用时要小心
20. 将钠、镁、铝各0.3mol分别放入 100mL 1mol/L盐酸中,同温同压下产生气体的体积比是
A、1:2:3 B、6:3:2 C、3:1:1 D、1:1:1
陕西省2009年高中学业水平考试模拟试题(卷)
化 学(三)
题 号 1 2 3 4 5 6 7 8 9 10
答 案
题 号 11 12 13 14 15 16 17 18 19 20
答 案
题 号 第一部分 第二部分 总 分
1—20 必答题 选答题
得 分
第二部分 (非选择题 共50分)
得 分 评卷人
三、必答题(本题包括5小题,计30分)
21. (6分)X、 Y、 Z三种短周期元素, X原子半径是所有元素中最小的,Y的最外层电子数比次外层多4个电子,Z的化合物进行焰色反应时火焰为黄色;又知Z、Y形成甲、乙两种固体化合物,乙中Z和Y的原子数比为1:1。则:
⑴X、Y、Z分别为:X__ ____、Y__ ____、Z__ ____;
⑵甲、乙化学式分别为______ ____;
⑶Z的原子结构示意图为________________________________。
22. (4分)乙醇是生活中常见的一种有机物,它的分子结构模型如右图所示:
(1)乙醇中的“-OH”原子团的名称是 ;
(2)一定条件下,乙醇能与乙酸反应生成一种具有香味的油状液体,该有机反应的类型是 反应;
(3)工业上可用乙烯与水反应来生成酒精,请写出该反应的化学方程式(不必写反应条件) 。
23. (7分)我国化工专家侯德榜发明的侯氏制碱法的化学原理是将二氧化碳通入氨水的氯化钠饱和溶液中,其化学反应方程式为:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl。
⑴在实验室中利用上述原理从反应所得溶液中分离出碳酸氢钠晶体,应选用下列装置中的 ,该装置使用的玻璃仪器有______________________________。
A B C D
⑵实验所得碳酸氢钠晶体中,可能含有的杂质离子有Cl—和NH4+,实验室鉴定Cl—所选用的试剂是 、 ,鉴定另一种杂质离子的方法是 。
⑶碳酸氢钠晶体受热分解可得到纯碱,其化学反应方程式为 ,请你设计一个简单的实验方案,判断碳酸氢钠晶体受热分解后所得固体中是否仍然含有碳酸氢钠: 。
24. (6分)下图是铜与浓硫酸反应的实验装置图,请回答下列问题。
(1)写出有标号仪器的名称:① ;② 。
(2)写出铜与浓硫酸反应的化学方程式: 。
(3)SO2通入品红试液中的现象为 。
(4) SO2和NO2都是大气污染物,它们会引起雨水呈 (填“酸性”、“碱性”、“中性”)。
25. (7分)右图为某市售盐酸试剂瓶标签上的部分数据。通过计算回答:
(1)在标准状况下,1体积水吸收多少体积的HCl气体可制得
此盐酸?(水的密度以1.00g/cm3计)
(2)该盐酸25.4mL与2.00 mol·L-1的NaOH溶液100mL混合,
再将混合后溶液稀释至1.00L,此时溶液中氢离子的物质的量
浓度约为多少?
得 分 评卷人
四、选答题(本题分三个模块,每个模块包括3道小题,计20分。考生任选一个模块作答,不跨模块计分。)
化学与生活(选修模块)
26. (6分)(1)如下图所示,铁处于Ⅰ、Ⅱ、Ⅲ三种不同的环境中,铁被腐蚀的速率由大到小的顺序是(填序号) 。
(2)氯代烷是一种能破坏臭氧层的物质。在大气平流层中,氟氯代烷受紫外线的照射分解出氯原子,氯原子参与下列有关反应:
①C+O3→ClO+O2 ②O3O+O2 ③ClO→Cl+O2
上列反应的总反应式是 ,少量氟氯代烷能破坏大量臭氧的原因是 。
27. (8分)生活处处有化学,化学与生产、生活密切相关。请回答:
(1)经科学测定,人体平均含氧65%,含碳18%,含氢10%(以上均为质量分数),则三种元素中原子数目最多的是 (填元素符号)。
(2)为验证某易拉罐材质的主要成分是铁制还是铝制,如用物理方法验证,一般用 即可;如用化学方法验证,可使用的化学试剂为 。
(3)据报道,全世界每年因金属腐蚀造成的直接经济损失约达7000亿美元,我国因金属腐蚀造成的损失占国民生产总值(GNP)的4%。钢铁在潮湿的空气中发生电化学腐蚀时,负极的电极反应式为 。
(4)天然橡胶主要成分的结构简式是 。橡胶硫化的目的是使线型橡胶分子之间通过硫桥交联起来,形成 ,从而改善橡胶的性能。
28. (6分)阿司匹林的结构简式为 ,试根据阿司匹林的结构回答下列问题:
①阿司匹林看成酯类物质,口服后,在胃肠中酶的作用下,阿司匹林发生水解反应生成A
和B两种物质。其中A的结构简式为 ,则B的结构简式为 ;B中含有的官能团是 (填名称)
②上述水解产物A与氢氧化钠溶液反应的化学方程式为
化学反应原理(选修模块)
26. (共5分)
(1)1g碳与适量水蒸气反应生成CO和H2,需吸收10.94KJ热量,此反应的热化学方程式为
(2)已知CH4(g)+2O2(g)== CO2(g)+2H2O(l);ΔH=-Q1kJ·mol-1 ,
=2H2O(g);△H2=-Q2 kJ·,
=2H2O(l);△H2=-Q3 kJ·。
常温下,取体积比4∶1的甲烷和氢气的混合气体11.2L(标准状况下),经完全燃烧后恢复至室温,则放出的热量为 。
27. (7分)将气体A、B置于容积为2L的密闭容器,发生如下反应:
4A(g)+B(g)=2C(g)
反应进行到4S末,测得A为0.5mol,B为0.4mol,C为0.2mol,
(1)则vA= _____________ vB= _________________ vC= ______________
(2)反应前A有 ___ mol,反应前B有 _____ mol
28. (8分)如图所示是电解氯化钠溶液(含酚酞)的装置。有毒气体收集的装置省略没有画出,两电极均是惰性电极。
⑴a电极的名称 。
⑵电解过程中观察到的现象 。
⑶确定N出口的气体最简单的方法是 。
⑷电解的总反应离子方程式为 。
有机化学基础(选修模块)
26. (6分)某芳香族化合物的分子式为C7H8O,根据下列实验现象确定其结构简式:
(1)不能与金属钠反应,其结构简式的_____________ ______________。
(2)能与钠反应,但遇FeCl3不显色______________ __ __ __________。
(3)能与钠反应且遇FeCl3显紫色__________________ ____________。
27. (6分)现有6种有机物:①乙烯 ②苯 ③乙醇 ④乙醛 ⑤乙酸 ⑥乙酸乙酯。
按下列要求填写下列空格(填写序号):
(1)具有酸的通性的是 ;
(2)在一定条件下,能发生银镜反应的是 ;
(3)在一定条件下,能发生酯化反应的是 ;
(4)在一定条件下,既能使溴水褪色,又能使酸性高锰酸钾溶液褪色,还能发生加聚反应的是 ;
(5)在一定条件下,既可发生加成反应,又可发生取代反应的烃是 ;
(6)在一定条件下,能发生水解反应的是 。
28. (8分)现有A、B、C、D、E、F五种有机物,它们的转化关系如下图所示(图中部分反应条件及生成物没有全部写出)。已知:液体B能发生银镜反应,气体D的相对分子质量为28。
请回答下列问题:
⑴A、B、C的结构简式分别是 、 、 。
⑵C→A的反应物及反应条件是 。
⑶D→F反应的化学方程式是 。
⑷在一定的条件下,A与E反应可生成一种具有香味的物质。该反应的化学方程式
是 。
参考答案:
一、选择题(每小题2分,计20分)
1~5 DBBDD 6~10 CDCCB
二、选择题(每小题3分,计30分)
11~15DAABD 16~20 ACADC
三、必答题(本题包括5小题,计30分)
21.(6分)⑴ H、O、Na (各1分)
⑵ Na2O、Na2O2 (各1分) ⑶ 略 (1分)
22.(4分)(1)羟基 (2)取代(酯化) (3)CH2=CH2+ H2O→CH3CH2OH
23.(7分)⑴B 烧杯、漏斗、玻璃棒(2分)
⑵AgNO3溶液 稀HNO3 取少量固体与强碱溶液混合加热,生成的气体用湿润的红色石蕊试纸检验(3分)
⑶2NaHCO3Na2CO3+CO2↑+H2O 取所得固体,继续加热,将生成的气体通入澄清石灰水,若变浑浊,说明含有碳酸氢钠(2分)
24.(6分)⑴①酒精灯 ②试管
⑵Cu+2H2SO4==CuSO4+SO2↑+2H2O(加热条件)(2分)
⑶品红试液褪色
⑷酸性
25.(7分)(1) (VHCl / 22.4L · mol-1)×36.5g · mol-1
(VHCl / 22.4L · mol-1)×36.5g · mol-1 + 1000g
V(HCl )= 353 L 3分
(2)此盐酸的物质的量的浓度为
C(HCl) = = 11.8mol · L-1
2分
与NaOH溶液混合后溶液中的氢离子浓度为:
C(H+ )= ≈0.100 mol · L-1
2分
四、选答题(本题包括3小题,计20分)
化学与生活(选修模块)(共20分)
26.(6分)(1)I、Ⅲ、Ⅱ (I > Ⅲ > Ⅱ或Ⅱ < Ⅲ < I,其它写法不得分,写阿拉伯数字不得分)
(2分)
(2)2O3 3O2 (2分)
方程式书写正确得1分
条件答对(条件只能写“Cl”或“氯原子”,其它答案均不给分)得1分
(3)答案中出现“氯原子(Cl)是催化剂”或“氯原子(Cl)起催化作用”才能得分,如写中文字“氯”是催化剂,不给分。 (2分)
27.(8分)(1)H (2)磁铁是否能吸引 氢氧化钠溶液 (3)Fe-2e—=Fe2+ (2分)
(4) (2分) 网状结构
28.(6分)①CH3COOH (2分) 羧基 (2分)
② (2分)
+ 2NaOH → 2H2O +
化学反应原理(选修模块)(共20分)
26.(共5分)(1)C(S)+H2O(g) == CO(g) +H2(g) ΔH= +131.28 kJ·(2分)
(2)0.4Q1+0.05Q2(3分)
27.(5分)(1)(每空1分)0.05 mol/(L.S) , 0.0125 mol/(L.S) 0.025 mol/(L.S)
(2)(各2分)0.9 ,0.5
28.(8分每空2分) (1)阴极
(2)两极均有气泡产生;a极区溶液变成红色;b极液面上气体变为黄绿色;b极区溶液变为浅黄绿色。
(3)用湿润的淀粉碘化钾试纸检验,试纸变蓝则说明是Cl2。
有机化学基础(选修模块)(共20分)
26. (6分)
27. (6分)⑤;④;③⑤;①;②;⑥.
28. (9分)(1)CH3CH2OH CH3CHO CH3CH2Br(3分)
(2)NaOH的乙醇溶液,加热(2分)
(3) (1分)
(4) (2分)
X
XY2
XY3
置换
化合
化合
化合
X
Y
Z
盐酸
分子式:HCl
相对分子质量:36.5
外观:合格
密度:约为1.18g/cm3
HCl的质量分数:36.5%
符合GB622—89
COOH
OOCCH3
COOH
OH
= 36.5%
1000mL·L-1 ×1.18g · mL-1×36.5%
36.5g · mol-1
0.0254L×11.8mol · L-1 – 0.100L×2.00 mol · L-1
1.00L
Cl
COONa
ONa
COOH
OH
PAGE
1
同课章节目录
