高二化学乙醛
图片预览





文档简介
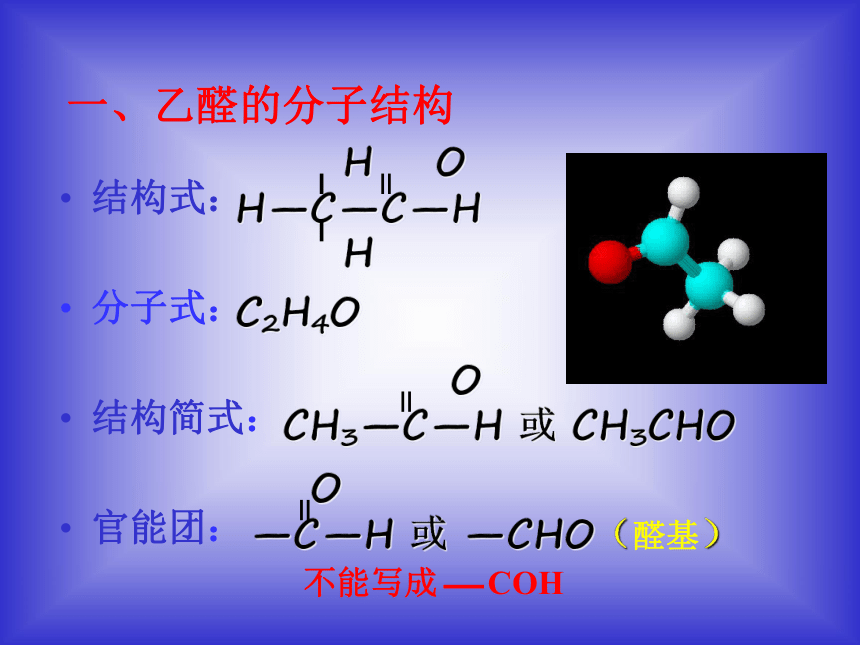
课件19张PPT。 第二节 乙醛江西省泰和四中 胡荣椿一、乙醛的分子结构结构式:
分子式:
结构简式:
官能团:C2H4O二、乙醛的物理性质1、无色、有刺激性气味的液体;
2、密度比水小,沸点是20.8℃;
3、易挥发,易燃烧;
4、能跟水、乙醇、氯仿等互溶。
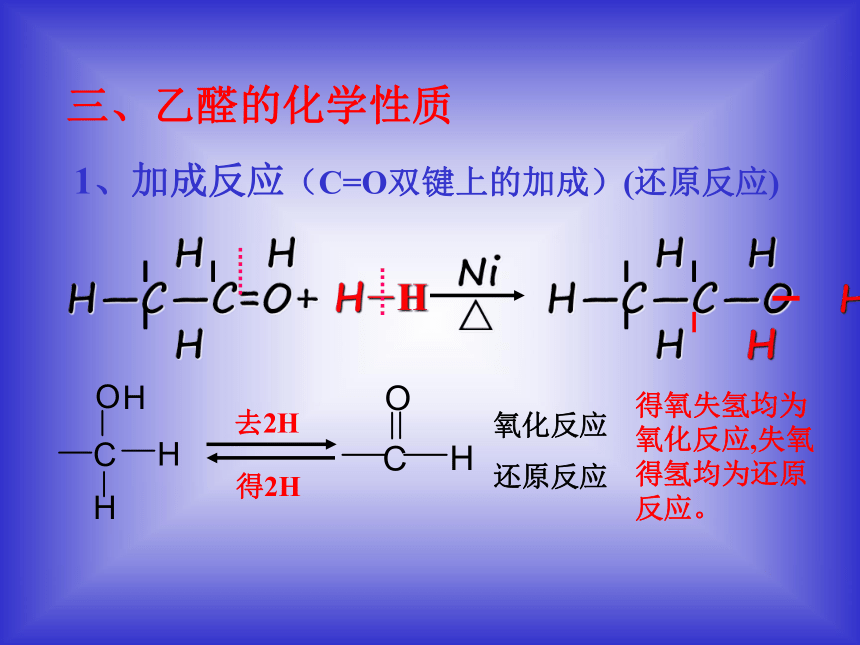
三、乙醛的化学性质1、加成反应(C=O双键上的加成)(还原反应)+ H-H去2H氧化反应得2H
还原反应
得氧失氢均为氧化反应,失氧得氢均为还原反应。a 催化氧化
乙醇乙醛乙酸工业制乙酸2、乙醛的氧化反应b 燃烧
c 被弱氧化剂氧化①与银氨溶液反应—银镜反应
沉淀恰好
完全溶解银氨溶液试管内壁上附有一层光亮如镜的金属银AgNO3溶液 + 稀氨水生成白色沉淀Ag++NH3·H2O=AgOH+NH4+
AgOH+2NH3·H2O=[Ag(NH3)2]++OH-+2H2O 银镜反应
(一水二银三氨醋酸铵)
银镜反应注意事项(1)试管内壁必须洁净;
(2)60℃水浴加热,不能用酒精灯直接加热;
(3)加热时不可振荡和摇动试管;
(4)须用新配制的银氨溶液,氨水不能过量(防此生成易爆炸的物质);
(5)乙醛用量不可太多;
(6)实验后,银镜用HNO3浸泡,再用水洗。
(7)此反应的用途:
①、检验醛基的存在
②、工业上利用这个反应,把银均匀地镀在玻璃上制镜或者保温瓶胆
试管内有红色沉淀产生CuSO4 + 2NaOH = Cu(OH)2↓ + Na2SO4此反应可以检验醛基存在注意:a 氢氧化铜必须新制;
b 直接加热至沸腾② 和新制的Cu(OH)2反应NaOH溶液+少量CuSO4 溶液蓝色
沉淀新制的
氢氧化铜弱氧化剂可将醛基氧化,强氧化剂是否可将醛基氧化?请议一议:乙醛能否使酸性高锰酸钾溶液褪色?能否使
溴水褪色?练习一一个学生做乙醛的还原性实验时,取1mol/L CuSO4溶液和0.5mol/L NaOH溶液各1ml,在一支洁将的试管内混合后,向其中又加入5ml 40%的乙醛,结果无红色沉淀出现。实验失败原因可能是( )
A、未充分加热 B、加入乙醛太少
C、加入溶液的量不够
D、加入CuSO4溶液的量不够 A、C练习二乙醛性质的小节:2、氧化反应a 燃烧b 催化氧化c 被弱氧化剂氧化
(银氨溶液、新制的Cu(OH)2)d 使酸性高锰酸钾溶液、溴水褪色乙酸四、乙醛的制备(1)乙醇氧化法:(2)乙炔水化法:
(3)乙烯氧化法:五、乙醛的用途 乙醛主要用于制取乙酸、丁醇、乙酸乙酯等,是有机合成的重要原料。六、醛类1、定义:由烃基和醛基构成的化合物。2、通式:R-CHO(饱和一元醛为:CnH2nO)(1)物理性质3、性质一般有刺激性气味,易溶于有机溶剂;在水中的溶解度随碳原子数的递增而减小。(2)化学性质醛类具有和乙醛类似的化学性质:加成反应氧化反应燃烧催化氧化被弱氧化剂氧化CO2、H2O银镜反应Cu(OH)2羧酸能使高锰酸钾、溴水褪色七、甲醛 HCHO(也叫蚁醛,分子结构最简单的醛) 无色、有刺激性气味的气体,易溶于水(35%~40%的甲醛水溶液叫做福尔马林)。2、甲醛的化学性质与乙醛相似3、用途:浸制标本,制药,香料,燃料。1、物理性质3、下列物质能发生银镜反应的是( )练习三B、DD作业P149一、二、三
分子式:
结构简式:
官能团:C2H4O二、乙醛的物理性质1、无色、有刺激性气味的液体;
2、密度比水小,沸点是20.8℃;
3、易挥发,易燃烧;
4、能跟水、乙醇、氯仿等互溶。
三、乙醛的化学性质1、加成反应(C=O双键上的加成)(还原反应)+ H-H去2H氧化反应得2H
还原反应
得氧失氢均为氧化反应,失氧得氢均为还原反应。a 催化氧化
乙醇乙醛乙酸工业制乙酸2、乙醛的氧化反应b 燃烧
c 被弱氧化剂氧化①与银氨溶液反应—银镜反应
沉淀恰好
完全溶解银氨溶液试管内壁上附有一层光亮如镜的金属银AgNO3溶液 + 稀氨水生成白色沉淀Ag++NH3·H2O=AgOH+NH4+
AgOH+2NH3·H2O=[Ag(NH3)2]++OH-+2H2O 银镜反应
(一水二银三氨醋酸铵)
银镜反应注意事项(1)试管内壁必须洁净;
(2)60℃水浴加热,不能用酒精灯直接加热;
(3)加热时不可振荡和摇动试管;
(4)须用新配制的银氨溶液,氨水不能过量(防此生成易爆炸的物质);
(5)乙醛用量不可太多;
(6)实验后,银镜用HNO3浸泡,再用水洗。
(7)此反应的用途:
①、检验醛基的存在
②、工业上利用这个反应,把银均匀地镀在玻璃上制镜或者保温瓶胆
试管内有红色沉淀产生CuSO4 + 2NaOH = Cu(OH)2↓ + Na2SO4此反应可以检验醛基存在注意:a 氢氧化铜必须新制;
b 直接加热至沸腾② 和新制的Cu(OH)2反应NaOH溶液+少量CuSO4 溶液蓝色
沉淀新制的
氢氧化铜弱氧化剂可将醛基氧化,强氧化剂是否可将醛基氧化?请议一议:乙醛能否使酸性高锰酸钾溶液褪色?能否使
溴水褪色?练习一一个学生做乙醛的还原性实验时,取1mol/L CuSO4溶液和0.5mol/L NaOH溶液各1ml,在一支洁将的试管内混合后,向其中又加入5ml 40%的乙醛,结果无红色沉淀出现。实验失败原因可能是( )
A、未充分加热 B、加入乙醛太少
C、加入溶液的量不够
D、加入CuSO4溶液的量不够 A、C练习二乙醛性质的小节:2、氧化反应a 燃烧b 催化氧化c 被弱氧化剂氧化
(银氨溶液、新制的Cu(OH)2)d 使酸性高锰酸钾溶液、溴水褪色乙酸四、乙醛的制备(1)乙醇氧化法:(2)乙炔水化法:
(3)乙烯氧化法:五、乙醛的用途 乙醛主要用于制取乙酸、丁醇、乙酸乙酯等,是有机合成的重要原料。六、醛类1、定义:由烃基和醛基构成的化合物。2、通式:R-CHO(饱和一元醛为:CnH2nO)(1)物理性质3、性质一般有刺激性气味,易溶于有机溶剂;在水中的溶解度随碳原子数的递增而减小。(2)化学性质醛类具有和乙醛类似的化学性质:加成反应氧化反应燃烧催化氧化被弱氧化剂氧化CO2、H2O银镜反应Cu(OH)2羧酸能使高锰酸钾、溴水褪色七、甲醛 HCHO(也叫蚁醛,分子结构最简单的醛) 无色、有刺激性气味的气体,易溶于水(35%~40%的甲醛水溶液叫做福尔马林)。2、甲醛的化学性质与乙醛相似3、用途:浸制标本,制药,香料,燃料。1、物理性质3、下列物质能发生银镜反应的是( )练习三B、DD作业P149一、二、三
同课章节目录
