化学能转化为电能(浙江省温州市)
图片预览




文档简介
课件18张PPT。化学能与电能转化火电站工作原理示意图观察思考讨论
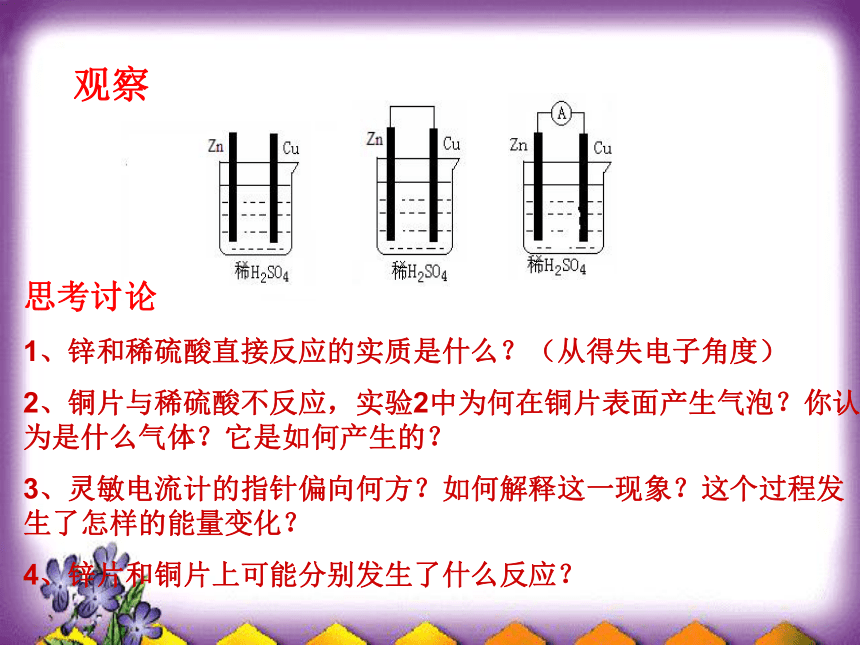
1、锌和稀硫酸直接反应的实质是什么?(从得失电子角度)
2、铜片与稀硫酸不反应,实验2中为何在铜片表面产生气泡?你认为是什么气体?它是如何产生的?
3、灵敏电流计的指针偏向何方?如何解释这一现象?这个过程发生了怎样的能量变化?
4、锌片和铜片上可能分别发生了什么反应?
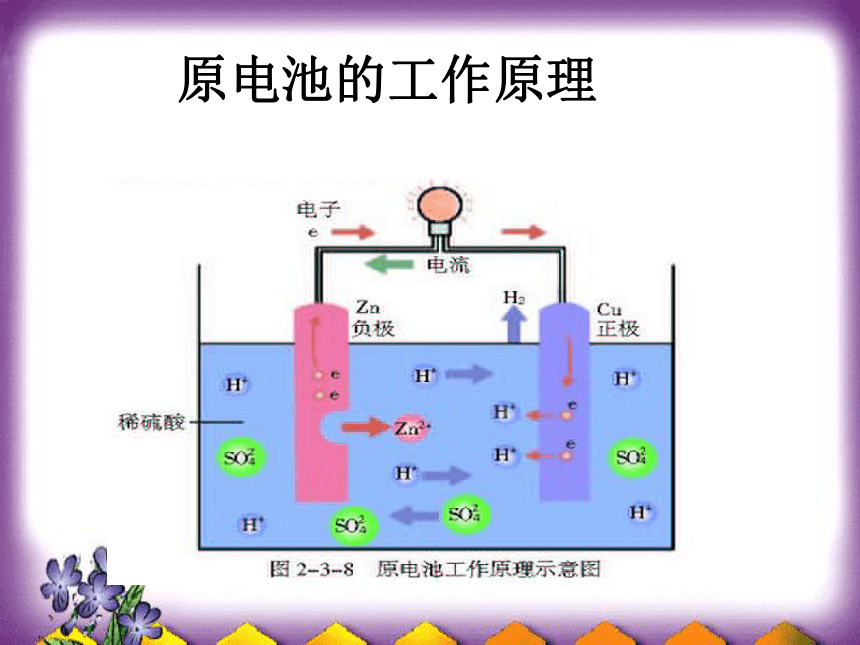
原电池的工作原理失得Zn-2e-= Zn2+2H++ 2e-= H2↑负极正极Zn+ 2H+ = Zn2+ + H2↑有气体产生Zn片溶解练习.有a、b、c、d四种金属浸入稀硫酸中,
将a与b用导线相连,b为正极;
将c、d相连,电流由d到c;
将a、c相连时, c极上产生大量的气泡;
将b、d相连时, b上有大量的气泡。
据此判断它们的活动性由强到弱的顺序是
A.a、b、c、d B.a、c、d、b
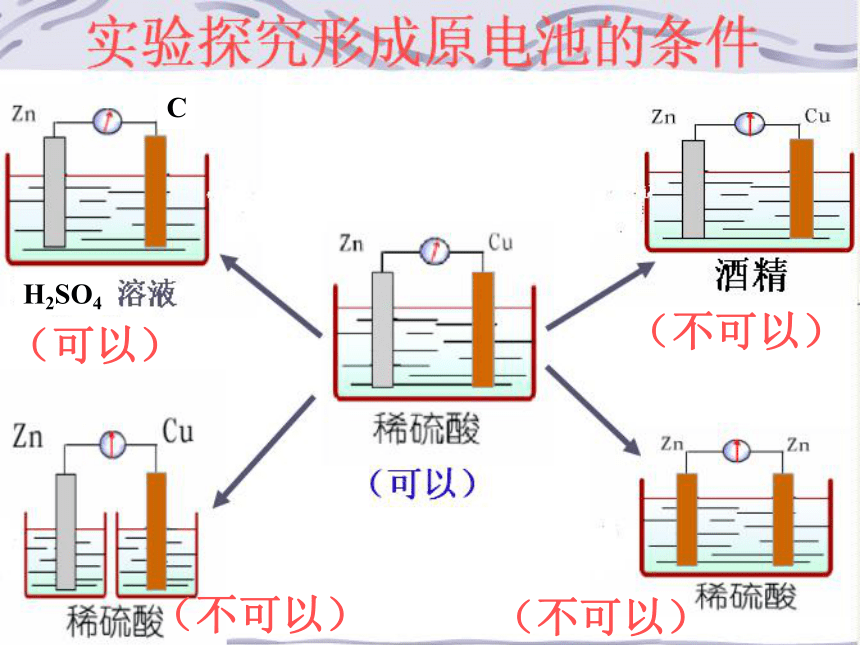
C.c、a、b、d D.b、d、c、aCH2SO4(不可以)(不可以)(可以)(不可以)原电池的构成条件 1、电极:两种活泼性不同的金属(或一
种金属和另一种非金属导体)构成电极。
2、溶液:两电极同时插入电解质溶液。
3、导线:两电极用导线相连,形成闭合
回路。
4、能自发进行的氧化还原反应。
(通常为原电池负极与电解质溶液之间的
氧化还原反应)思 考 题请根据反应
Fe + Cu2+ = Fe 2++ Cu
设计原电池,你有哪些可行方案?
原电池设计思路:1.确定正负极反应2.选择相应电极3.选择电解质溶液4.导线连通成闭合回路思 考 题家用炒菜铁锅用水清洗放置后,出现红棕色的锈斑,在此变化过程中不发生的化学反应是
A、4Fe(OH)2+2H2O+O2=4Fe(OH)3↓
B、2Fe+2H2O+O2=2Fe(OH)2↓
C、2H2O+O2+4e=4OH-
D、Fe-3e=Fe3+思 考 题以下现象与电化学理论无关的是
A、黄铜(铜锌合金)制作的铜锣不易生铜锈
B、生铁比软件铁芯(几乎是纯铁)容易生锈
C、纯锌与稀硫酸反应时,滴少量硫酸铜溶液
后速率加快
D、银质奖牌久置后表面变暗 请同学们根据原电池的原理,指出下列原电池的正极与负极分别是什么?写出电极反应式和总反应方程式。 相同条件下,纯锌粒和粗锌粒与同浓度的稀硫酸反应的速率一样吗?为什么?假如要求你设计实验来证明你的观点,你的实验方案是怎样的?证据和结论又是什么?原电池分析电极反应式的书写总反应方程式的书写化学电池的反应本质:氧化还原反应原电池电极名称的确定方法①根据电极材料的性质确定。通常是活泼金属是负极,不活泼金属、碳棒、化合物是正极。②根据电极反应的本身确定。失电子的反应→氧化反应→负极
得电子的反应→还原反应→正极二、发展中的电源氢氧燃料电池
1、锌和稀硫酸直接反应的实质是什么?(从得失电子角度)
2、铜片与稀硫酸不反应,实验2中为何在铜片表面产生气泡?你认为是什么气体?它是如何产生的?
3、灵敏电流计的指针偏向何方?如何解释这一现象?这个过程发生了怎样的能量变化?
4、锌片和铜片上可能分别发生了什么反应?
原电池的工作原理失得Zn-2e-= Zn2+2H++ 2e-= H2↑负极正极Zn+ 2H+ = Zn2+ + H2↑有气体产生Zn片溶解练习.有a、b、c、d四种金属浸入稀硫酸中,
将a与b用导线相连,b为正极;
将c、d相连,电流由d到c;
将a、c相连时, c极上产生大量的气泡;
将b、d相连时, b上有大量的气泡。
据此判断它们的活动性由强到弱的顺序是
A.a、b、c、d B.a、c、d、b
C.c、a、b、d D.b、d、c、aCH2SO4(不可以)(不可以)(可以)(不可以)原电池的构成条件 1、电极:两种活泼性不同的金属(或一
种金属和另一种非金属导体)构成电极。
2、溶液:两电极同时插入电解质溶液。
3、导线:两电极用导线相连,形成闭合
回路。
4、能自发进行的氧化还原反应。
(通常为原电池负极与电解质溶液之间的
氧化还原反应)思 考 题请根据反应
Fe + Cu2+ = Fe 2++ Cu
设计原电池,你有哪些可行方案?
原电池设计思路:1.确定正负极反应2.选择相应电极3.选择电解质溶液4.导线连通成闭合回路思 考 题家用炒菜铁锅用水清洗放置后,出现红棕色的锈斑,在此变化过程中不发生的化学反应是
A、4Fe(OH)2+2H2O+O2=4Fe(OH)3↓
B、2Fe+2H2O+O2=2Fe(OH)2↓
C、2H2O+O2+4e=4OH-
D、Fe-3e=Fe3+思 考 题以下现象与电化学理论无关的是
A、黄铜(铜锌合金)制作的铜锣不易生铜锈
B、生铁比软件铁芯(几乎是纯铁)容易生锈
C、纯锌与稀硫酸反应时,滴少量硫酸铜溶液
后速率加快
D、银质奖牌久置后表面变暗 请同学们根据原电池的原理,指出下列原电池的正极与负极分别是什么?写出电极反应式和总反应方程式。 相同条件下,纯锌粒和粗锌粒与同浓度的稀硫酸反应的速率一样吗?为什么?假如要求你设计实验来证明你的观点,你的实验方案是怎样的?证据和结论又是什么?原电池分析电极反应式的书写总反应方程式的书写化学电池的反应本质:氧化还原反应原电池电极名称的确定方法①根据电极材料的性质确定。通常是活泼金属是负极,不活泼金属、碳棒、化合物是正极。②根据电极反应的本身确定。失电子的反应→氧化反应→负极
得电子的反应→还原反应→正极二、发展中的电源氢氧燃料电池
