(特别免费资料)四川省南山中学08-09学年高二第一次月考(化学)
文档属性
| 名称 | (特别免费资料)四川省南山中学08-09学年高二第一次月考(化学) |

|
|
| 格式 | rar | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 其它版本 | ||
| 科目 | 化学 | ||
| 更新时间 | 2009-04-04 00:00:00 | ||
图片预览



文档简介
南山中学08-09学年高二第一次月考
化学试题
可能用到的相对原子质量:H— 1 N— 14 O— 16 C— 12 Cl— 35.5
第Ⅰ卷(选择题,共55分)
一、选择题(本题包括20小题,每小题2分,共40分,每小题只一个选项符合题意。)
1.工业上生产乙烯最主要的途径是 ( )
A.乙炔加氢 B.乙醇与浓硫酸混合脱水 C.石油裂解 D.煤炭干馏
2. 下列说法错误的是 ( )
A.石油中含有C5~C11的烷烃,可以通过石油的分馏得到汽油
B.含C18以上烷烃的重油经过催化裂化可以得到汽油
C.煤是由有机物和无机物组成的复杂的混合物
D.煤中含有苯和甲苯,可以用先干馏后分馏的方法把它们分离出来
3.为了减少大气污染,许多城市推广使用汽车清洁燃料。目前使用的清洁燃料主要有两类,一类是压缩天然气(CNG),另一类是液化石油气(LPG)。这两类燃料的主要成分都是( )
A.碳水化合物 B.碳氢化合物 C.氢气 D.醇类
4.下列变化属于物理变化的是 ( )
A.煤的干馏 B.石油的减压分馏
C.重油的裂化 D.石油的裂解
5.1—溴丙烷和2—溴丙烷分别与NaOH的乙醇溶液共热的反应中,两反应
A.产物相同,反应类型相同 B.产物不同,反应类型不同
C.碳氢键断裂的位置相同 D.碳溴键断裂的位置相同
6.某有机物结构简式如图。下列关于该有机物叙述错误的是 ( )
A.它是由碳、氢、氧、氮四种元素组成
B.它的分子式是C16H10N2O2
C.它是有机离子化合物
D.它是不饱和的有机物
7.只用一种试剂区别甲苯、已烯、四氯化碳、碘化钾、亚硫酸、乙醇、苯酚七种无色液体,可选用的试剂是 ( )
A.性高锰酸钾 B.溴水 C.碘水 D.硝酸银溶液
8.分子式为C5H7Cl的有机物,其结构不可能是 ( )
A.只含有1个双键的直链有机物 B.含2个双键的直链有机物
C.含1个双键的环状有机物 D.含一个三键的直链有机物
9.从烷烃(CnH2n+2),烯烃(CnH2n),二烯烃(CnH2n-2)的通式分析,得出碳氢原子的个数与分子中所含双键有一定关系,某种烃的分子式为CxHy,其中所含双键数目为: ( )
A.y/2 B.(y-x)/2 C.(y+2-x)/2 D.(2x+2-y)/2
10.分子式为C5H12O的有机物,它的同分异构体中,经氧化可生成醛的有 ( )
A.4种 B.3种 C.2种 D.5种
11.在实验室进行下列实验时,不需要使用温度计的是 ( )
A.制备乙烯气体 B.石油分馏 C.制备硝基苯 D.制备溴苯
12.下列电子式书写错误的是 ( )
13.下列各组分子中的各个原子,或者处于同一平面,或者在一条直线上的是: ( )
A.C6H6,C2H4,CO2 B.CO2,HCl,HC≡CCH3
C.C6H6,HCl,CH4 D.C2H6、HCl、C2H2
14.有A、B两种烃,含碳的质量分数相同,关于A和B叙述中正确的是 ( )
A.二者一定是同分异构体 B.二者最简式相同
C.二者不可能是同系物 D.各1mol的A和B分别燃烧生成CO2的质量一定相等
15.丁香油酚是一种液体,它的结构简式是:
推断它不应具有的化学性质是 ( )
A.可与溴发生加成反应 B.与NaHCO3反应放出CO2
C.遇氯化铁溶液呈紫色 D.能使酸性KMnO4溶液褪色
16.CaC2和ZnC2、Al4C3、Mg2C3、Li2C2等都同属离子型碳化物,请通过对CaC2制C2H2的反应进行思考,从中得到必要的启示,判断反应物与水反应产物正确的是 ( )
A.ZnC2水 解生成乙烷(C2H6) B.Al4C3水解生成丙炔(C3H4)
C.Mg2C3水解生成丙炔(C3H4) D.Li2C2水解生成乙烯(C2H4)
17.除去酒精中少量水而得到无水乙醇,所采用的正确操作是 ( )
A.将混合物加入熟石灰加热蒸馏 B.将混合物反复蒸馏
C.将混合物加入生石灰加热蒸馏 D.加浓硫酸蒸馏
18.下列为制取溴苯实验的有关现象的解释和叙述,其中正确的是: ( )
A.溴苯和苯的混合物可以用水萃取分离
B.溴苯比水轻,因此溴苯浮在水面上
C.实验室制取溴苯时,长导管的作用是只作为冷凝器
D.实验室制取的溴苯为褐色的液体,是由于溶解了溴而造成的
19.下列说法不正确的是 ( )
A.分子为C3H8与C6H14的两种有机物一定互为同系物
B.具有相同通式的有机物不一定互为同系物
C.两个相邻同系物的分子量数值一定相差14
D.分子组成相差一个或几个CH2原子团的化合物必定互为同系物
20.下列化合物沸点比较错误的是 ( )
A.丙烷>乙烷>甲烷 B.正戊烷>异戊烷>新戊烷
C.邻二甲苯>间二甲苯>对二甲苯 D.1—氯戊烷<1—氯丙烷
二、选择题(本题包括15小题,每小题3分,共45分,每小题有一个或两个选项符合题意。)
21.在120℃时,某混合烃和过量O2在一密闭容器中完全反应,测知反应前后的压强没有变化,则该混合烃可能是 ( )
A.CH4和C2H4 B.C2H2和C2H6
C.C2H4和C2H6 D.C3H4和C3H6
22. 乙醇分子中各化学键如图所示,对乙醇在各种反应中应断裂的键说明不正确的是( )
A.和金属钠作用时,键①断裂
B.和浓硫酸共热至170 ℃时,键②和④断裂
C.和浓硫酸共热至140 ℃时,键②断裂
D.在铜催化下和氧气反应时,键①和③断裂
23.某一元醇A发生消去反应,可同时生成互为同分异构体的两物质B和C。已知B的结构为CH2=C(CH3)CH2CH3,则A和C的结构简式应分别为 ( )
24. 某气态化合物X含C、H、O三种元素,现己知下列条件:①X中C的质量分数;②X中H的质量分数;③X在标准状况下的体积;④X对H2的相对密度;⑤X的质量。欲确定X的分子式,所需的最少条件是 ( )
A.①②④ B.②③④ C.①③⑤ D.①②
25.一定量醇等分成两份,取一份充分燃烧,可生成0.2molCO2,另一份与足量钠作用放出0.1 mol H2,则该醇不可能是 ( )
A.甲醇 B .乙二醇 C.异丙醇 C.甘油
第Ⅱ卷(非选择题,共45分)
三、填空题(每空2分,共16分)
26.(4分)分别完全燃烧等物质的量的C2H6、C2H4、C2H2需要氧气最多的是____________生成水最多的是___________。
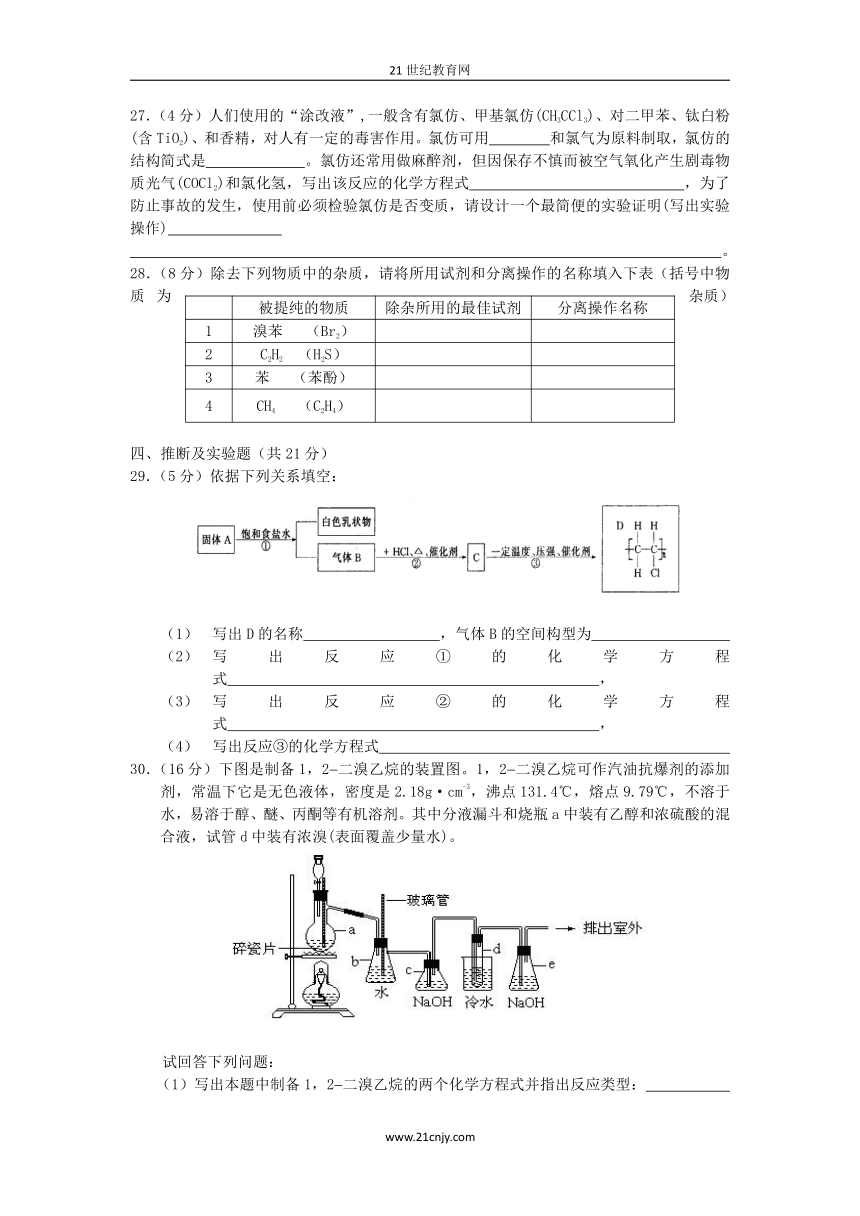
27.(4分)人们使用的“涂改液”,一般含有氯仿、甲基氯仿(CH3CCl3)、对二甲苯、钛白粉(含TiO2)、和香精,对人有一定的毒害作用。氯仿可用 和氯气为原料制取,氯仿的结构简式是 。氯仿还常用做麻醉剂,但因保存不慎而被空气氧化产生剧毒物质光气(COCl2)和氯化氢,写出该反应的化学方程式 ,为了防止事故的发生,使用前必须检验氯仿是否变质,请设计一个最简便的实验证明(写出实验操作)
。
被提纯的物质
除杂所用的最佳试剂
分离操作名称
1
溴苯 (Br2)
2
C2H2 (H2S)
3
苯 (苯酚)
4
CH4 (C2H4)
28.(8分)除去下列物质中的杂质,请将所用试剂和分离操作的名称填入下表(括号中物质为杂质)
四、推断及实验题(共21分)
29.(5分)依据下列关系填空:
写出D的名称 ,气体B的空间构型为
写出反应①的化学方程式 ,
写出反应②的化学方程式 ,
写出反应③的化学方程式
30.(16分)下图是制备1,2(二溴乙烷的装置图。1,2(二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度是2.18g·cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有浓溴(表面覆盖少量水)。
试回答下列问题:
(1)写出本题中制备1,2(二溴乙烷的两个化学方程式并指出反应类型:
(2)①a瓶中在温度高于170℃时,液体慢慢变黑同时有SO2、CO2气体产生,试写出生成SO2、CO2的化学反应方程式: 。
(3)写出容器c中NaOH溶液的作用 。
(4)容器e中的NaOH溶液的作用是: ,
其离子反应的方程式为:
(5)安全瓶b可以防倒吸,并可以检查实验进行时试管d中是否发生堵塞。请写出发生堵塞时瓶b中的现象:
五、计算题(共8分)(解题步骤合理均给分)
31.0.05mol某烃完全燃烧,生成二氧化碳气体5.6 L(标准状况下)和5.4g水。
(1)通过计算写出该烃的分子式。
(2)若该烃的一氯代物只有一种结构,写出该烃的结构简式,并用系统命名法命名。
化学(第Ⅱ卷)答题卷
题号
三
四
五
第Ⅱ卷总分
得分
26. , 。
27. , ,
,
。
1
2
3
4
28.
29.(1) ,
(2)
(3)
(4)
30.⑴ ,反应类型: 。
,反应类型: 。
⑵ 。
⑶
⑷ , 。
⑸ .
31.
南山中学高二第一次月考参考答案
1.C 2. D 3.B 4.B 5.A 6.C 7.B 8.A 9.D 10.A 11.D 12.B 13.A 14.B 15.B 16.C 17.C 18.D 19.D 20.D 21.A B 22. B C 23.B 24.A 25. C
三、填空题(每空2分,共16分)
26.(每空2分共4分) C2H6 、 C2H6
27.(每空1分共4分) CH4, ClHCl3 ; 2ClHCl3 + O2 = 2 COCl2+ 2HCl ;
取少量样品于试管中,加入AgNO3溶液,若有白色沉淀产生,再加入稀硝酸沉淀不溶解,则证明氯仿变质了,否则没变质。
1
NaOH溶液
分液
2
CuSO4或 NaOH溶液
洗气
3
NaOH溶液
分液
4
溴水
洗气
28.(每空1分共8分)
四、(共21分)29.(每空1分共5分)
30.(16分)
31.(8分解:设该烃的化学式为CxHy
5.6L/22.4L·mol-1=0.25mol 5.4g/18g mol-1=0.3mol
CxHy+(X+Y/4)O2 XCO2 + Y/2H2O
1mol Xmol Y/2mol
0.05mol 0.25mol 0.3mol
X=5 mol Y=12 mol
∴分子式为C5H12
(2)
w.w.w.k.s.5.u.c.o.m
化学试题
可能用到的相对原子质量:H— 1 N— 14 O— 16 C— 12 Cl— 35.5
第Ⅰ卷(选择题,共55分)
一、选择题(本题包括20小题,每小题2分,共40分,每小题只一个选项符合题意。)
1.工业上生产乙烯最主要的途径是 ( )
A.乙炔加氢 B.乙醇与浓硫酸混合脱水 C.石油裂解 D.煤炭干馏
2. 下列说法错误的是 ( )
A.石油中含有C5~C11的烷烃,可以通过石油的分馏得到汽油
B.含C18以上烷烃的重油经过催化裂化可以得到汽油
C.煤是由有机物和无机物组成的复杂的混合物
D.煤中含有苯和甲苯,可以用先干馏后分馏的方法把它们分离出来
3.为了减少大气污染,许多城市推广使用汽车清洁燃料。目前使用的清洁燃料主要有两类,一类是压缩天然气(CNG),另一类是液化石油气(LPG)。这两类燃料的主要成分都是( )
A.碳水化合物 B.碳氢化合物 C.氢气 D.醇类
4.下列变化属于物理变化的是 ( )
A.煤的干馏 B.石油的减压分馏
C.重油的裂化 D.石油的裂解
5.1—溴丙烷和2—溴丙烷分别与NaOH的乙醇溶液共热的反应中,两反应
A.产物相同,反应类型相同 B.产物不同,反应类型不同
C.碳氢键断裂的位置相同 D.碳溴键断裂的位置相同
6.某有机物结构简式如图。下列关于该有机物叙述错误的是 ( )
A.它是由碳、氢、氧、氮四种元素组成
B.它的分子式是C16H10N2O2
C.它是有机离子化合物
D.它是不饱和的有机物
7.只用一种试剂区别甲苯、已烯、四氯化碳、碘化钾、亚硫酸、乙醇、苯酚七种无色液体,可选用的试剂是 ( )
A.性高锰酸钾 B.溴水 C.碘水 D.硝酸银溶液
8.分子式为C5H7Cl的有机物,其结构不可能是 ( )
A.只含有1个双键的直链有机物 B.含2个双键的直链有机物
C.含1个双键的环状有机物 D.含一个三键的直链有机物
9.从烷烃(CnH2n+2),烯烃(CnH2n),二烯烃(CnH2n-2)的通式分析,得出碳氢原子的个数与分子中所含双键有一定关系,某种烃的分子式为CxHy,其中所含双键数目为: ( )
A.y/2 B.(y-x)/2 C.(y+2-x)/2 D.(2x+2-y)/2
10.分子式为C5H12O的有机物,它的同分异构体中,经氧化可生成醛的有 ( )
A.4种 B.3种 C.2种 D.5种
11.在实验室进行下列实验时,不需要使用温度计的是 ( )
A.制备乙烯气体 B.石油分馏 C.制备硝基苯 D.制备溴苯
12.下列电子式书写错误的是 ( )
13.下列各组分子中的各个原子,或者处于同一平面,或者在一条直线上的是: ( )
A.C6H6,C2H4,CO2 B.CO2,HCl,HC≡CCH3
C.C6H6,HCl,CH4 D.C2H6、HCl、C2H2
14.有A、B两种烃,含碳的质量分数相同,关于A和B叙述中正确的是 ( )
A.二者一定是同分异构体 B.二者最简式相同
C.二者不可能是同系物 D.各1mol的A和B分别燃烧生成CO2的质量一定相等
15.丁香油酚是一种液体,它的结构简式是:
推断它不应具有的化学性质是 ( )
A.可与溴发生加成反应 B.与NaHCO3反应放出CO2
C.遇氯化铁溶液呈紫色 D.能使酸性KMnO4溶液褪色
16.CaC2和ZnC2、Al4C3、Mg2C3、Li2C2等都同属离子型碳化物,请通过对CaC2制C2H2的反应进行思考,从中得到必要的启示,判断反应物与水反应产物正确的是 ( )
A.ZnC2水 解生成乙烷(C2H6) B.Al4C3水解生成丙炔(C3H4)
C.Mg2C3水解生成丙炔(C3H4) D.Li2C2水解生成乙烯(C2H4)
17.除去酒精中少量水而得到无水乙醇,所采用的正确操作是 ( )
A.将混合物加入熟石灰加热蒸馏 B.将混合物反复蒸馏
C.将混合物加入生石灰加热蒸馏 D.加浓硫酸蒸馏
18.下列为制取溴苯实验的有关现象的解释和叙述,其中正确的是: ( )
A.溴苯和苯的混合物可以用水萃取分离
B.溴苯比水轻,因此溴苯浮在水面上
C.实验室制取溴苯时,长导管的作用是只作为冷凝器
D.实验室制取的溴苯为褐色的液体,是由于溶解了溴而造成的
19.下列说法不正确的是 ( )
A.分子为C3H8与C6H14的两种有机物一定互为同系物
B.具有相同通式的有机物不一定互为同系物
C.两个相邻同系物的分子量数值一定相差14
D.分子组成相差一个或几个CH2原子团的化合物必定互为同系物
20.下列化合物沸点比较错误的是 ( )
A.丙烷>乙烷>甲烷 B.正戊烷>异戊烷>新戊烷
C.邻二甲苯>间二甲苯>对二甲苯 D.1—氯戊烷<1—氯丙烷
二、选择题(本题包括15小题,每小题3分,共45分,每小题有一个或两个选项符合题意。)
21.在120℃时,某混合烃和过量O2在一密闭容器中完全反应,测知反应前后的压强没有变化,则该混合烃可能是 ( )
A.CH4和C2H4 B.C2H2和C2H6
C.C2H4和C2H6 D.C3H4和C3H6
22. 乙醇分子中各化学键如图所示,对乙醇在各种反应中应断裂的键说明不正确的是( )
A.和金属钠作用时,键①断裂
B.和浓硫酸共热至170 ℃时,键②和④断裂
C.和浓硫酸共热至140 ℃时,键②断裂
D.在铜催化下和氧气反应时,键①和③断裂
23.某一元醇A发生消去反应,可同时生成互为同分异构体的两物质B和C。已知B的结构为CH2=C(CH3)CH2CH3,则A和C的结构简式应分别为 ( )
24. 某气态化合物X含C、H、O三种元素,现己知下列条件:①X中C的质量分数;②X中H的质量分数;③X在标准状况下的体积;④X对H2的相对密度;⑤X的质量。欲确定X的分子式,所需的最少条件是 ( )
A.①②④ B.②③④ C.①③⑤ D.①②
25.一定量醇等分成两份,取一份充分燃烧,可生成0.2molCO2,另一份与足量钠作用放出0.1 mol H2,则该醇不可能是 ( )
A.甲醇 B .乙二醇 C.异丙醇 C.甘油
第Ⅱ卷(非选择题,共45分)
三、填空题(每空2分,共16分)
26.(4分)分别完全燃烧等物质的量的C2H6、C2H4、C2H2需要氧气最多的是____________生成水最多的是___________。
27.(4分)人们使用的“涂改液”,一般含有氯仿、甲基氯仿(CH3CCl3)、对二甲苯、钛白粉(含TiO2)、和香精,对人有一定的毒害作用。氯仿可用 和氯气为原料制取,氯仿的结构简式是 。氯仿还常用做麻醉剂,但因保存不慎而被空气氧化产生剧毒物质光气(COCl2)和氯化氢,写出该反应的化学方程式 ,为了防止事故的发生,使用前必须检验氯仿是否变质,请设计一个最简便的实验证明(写出实验操作)
。
被提纯的物质
除杂所用的最佳试剂
分离操作名称
1
溴苯 (Br2)
2
C2H2 (H2S)
3
苯 (苯酚)
4
CH4 (C2H4)
28.(8分)除去下列物质中的杂质,请将所用试剂和分离操作的名称填入下表(括号中物质为杂质)
四、推断及实验题(共21分)
29.(5分)依据下列关系填空:
写出D的名称 ,气体B的空间构型为
写出反应①的化学方程式 ,
写出反应②的化学方程式 ,
写出反应③的化学方程式
30.(16分)下图是制备1,2(二溴乙烷的装置图。1,2(二溴乙烷可作汽油抗爆剂的添加剂,常温下它是无色液体,密度是2.18g·cm-3,沸点131.4℃,熔点9.79℃,不溶于水,易溶于醇、醚、丙酮等有机溶剂。其中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有浓溴(表面覆盖少量水)。
试回答下列问题:
(1)写出本题中制备1,2(二溴乙烷的两个化学方程式并指出反应类型:
(2)①a瓶中在温度高于170℃时,液体慢慢变黑同时有SO2、CO2气体产生,试写出生成SO2、CO2的化学反应方程式: 。
(3)写出容器c中NaOH溶液的作用 。
(4)容器e中的NaOH溶液的作用是: ,
其离子反应的方程式为:
(5)安全瓶b可以防倒吸,并可以检查实验进行时试管d中是否发生堵塞。请写出发生堵塞时瓶b中的现象:
五、计算题(共8分)(解题步骤合理均给分)
31.0.05mol某烃完全燃烧,生成二氧化碳气体5.6 L(标准状况下)和5.4g水。
(1)通过计算写出该烃的分子式。
(2)若该烃的一氯代物只有一种结构,写出该烃的结构简式,并用系统命名法命名。
化学(第Ⅱ卷)答题卷
题号
三
四
五
第Ⅱ卷总分
得分
26. , 。
27. , ,
,
。
1
2
3
4
28.
29.(1) ,
(2)
(3)
(4)
30.⑴ ,反应类型: 。
,反应类型: 。
⑵ 。
⑶
⑷ , 。
⑸ .
31.
南山中学高二第一次月考参考答案
1.C 2. D 3.B 4.B 5.A 6.C 7.B 8.A 9.D 10.A 11.D 12.B 13.A 14.B 15.B 16.C 17.C 18.D 19.D 20.D 21.A B 22. B C 23.B 24.A 25. C
三、填空题(每空2分,共16分)
26.(每空2分共4分) C2H6 、 C2H6
27.(每空1分共4分) CH4, ClHCl3 ; 2ClHCl3 + O2 = 2 COCl2+ 2HCl ;
取少量样品于试管中,加入AgNO3溶液,若有白色沉淀产生,再加入稀硝酸沉淀不溶解,则证明氯仿变质了,否则没变质。
1
NaOH溶液
分液
2
CuSO4或 NaOH溶液
洗气
3
NaOH溶液
分液
4
溴水
洗气
28.(每空1分共8分)
四、(共21分)29.(每空1分共5分)
30.(16分)
31.(8分解:设该烃的化学式为CxHy
5.6L/22.4L·mol-1=0.25mol 5.4g/18g mol-1=0.3mol
CxHy+(X+Y/4)O2 XCO2 + Y/2H2O
1mol Xmol Y/2mol
0.05mol 0.25mol 0.3mol
X=5 mol Y=12 mol
∴分子式为C5H12
(2)
w.w.w.k.s.5.u.c.o.m
同课章节目录
